第八单元 金属和金属材料 课题3 金属资源的利用和保护 同步练习(带解析)
文档属性
| 名称 | 第八单元 金属和金属材料 课题3 金属资源的利用和保护 同步练习(带解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 470.7KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-02-14 00:00:00 | ||
图片预览


文档简介
课题3 金属资源的利用和保护 同步练习
(带解析)
一、选择题
1.铁生锈主要条件是( )
A.仅需水 B.仅需氧气 C.水或氧气 D.水和氧气
2.下列说法正确的是 ( )
A.在钢铁表面镀铬能防止钢铁生锈
B.浓盐酸露置于空气中质量会增大
C.棉纤维在空气燃烧时产生烧焦羽毛的气味
D.二氧化碳是造成酸雨的主要物质
3.逻辑推理是科学学习常用的思维方法。下列推理正确的是( )
A.由于水比冰的比热容大,所以冷却食品时0℃的水比0℃的冰效果好
B.铁在潮湿的空气中容易被锈蚀,所以金属在潮湿的空气中都容易被锈蚀
C.真空罩内的空气越稀薄,在外面听到的铃声越小,所以“真空不能传声”
D.置换反应生成单质和化合物,所以有单质和化合物生成的反应一定是置换反应
4.铁是一种应用广泛的金属。下列有关铁的叙述正确的是( )
A.铁是地壳中含量最多的金属
B.工业上用二氧化碳冶炼钢铁
C.用铁可以回收硝酸银废液中的银
D.铁丝在氧气中燃烧生成氧化铁
5.下列有关资源的叙述正确的是( )
A.保护金属资源唯一的途径是防止金属的腐蚀
B.大气资源中含量最少的物质是稀有气体
C.人类可以利用的淡水量不到总水量的1%
D.金属资源都以化合物形式存在
6.下列物品需采取防锈措施的是( )
A.铁制防盗网 B.不锈钢菜刀 C.铝合金窗 D.金戒指
7.为了防止钢铁制品生锈,可采取的措施是( )
①涂油 ②刷油漆 ③保持干燥 ④镀上其他金属 ⑤烤蓝 ⑥包塑料布.
A.①②③⑥ B.③④⑤⑥ C.②③④⑤ D.①②③④⑤
8.铁在潮湿的空气里会发生锈蚀,证明氧气一定参加了反应,必须要做的实验是( )
A.(1)(2) B.(1)(3) C.(2)(3) D.(1)(2)(3)
二、填空题
9.据报道,金属材料因锈蚀而报废相当于世界年产量的1/3左右。铁生锈的条件是_____________________________;根据铁锈蚀的条件,写出一种防止铁制品锈蚀的具体方法是 (合理均可)。21教育网
10.(1)用铁制成铁锅,这利用了铁的_______(填字母序号)。
A.导电性 B.导热性 C.明亮的金属光泽
(2)用水洗完的铁锅要用抹布擦干可以防止生锈,其理由是_______。
11.金属在生产生活中有着非常广泛的应用。
(1)在酱油中加入铁强化剂,是我国为解决________(填“甲状腺肿大”“贫血”或“骨质疏松”)而实施的项目。21cnjy.com
(2)常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉。请将下列脱氧中的主要反应的化学方程式补充完整:4Fe(OH)2+O2+2________===4Fe(OH)3;此反应的基本类型是________。www.21-cn-jy.com
(3)实验室开放日,同学们在验证铜、铁、锌、银四种金属的活动性顺序时。小明发现四种金属中有一种金属的盐溶液与其他三种金属单质都能发生反应,请你写出其中一个反应的化学方程式 。 2·1·c·n·j·y
(4)目前世界上每年因腐蚀而报废的金属设备和材料相当于年产量的20%~40%。请举出一种保护金属资源的方法:______________________________________。
12.(1)在春秋战国时期,我国就开始生产和使用铁器,钢的质量也达到较高水平。古代,人们把烧红的生铁放在铁砧上反复锤打,最终使生铁转化为钢,用化学方程式表示原理 。21·世纪*教育网
(2)工业上用一氧化碳和赤铁矿炼铁的化学方程式是_______________________。
(3)新型材料纳米铁粉具有广泛的用途,它比普通铁粉更易与氧气反应,其制备的主要流程如下图所示。
纳米级铁粉遇氧气无需加热就能燃烧,生成物的化学式为 。
高温反应器中发生反应的化学方程式为 。反应前需向反应器中通入氮气,目的是 。www-2-1-cnjy-com
【中考大练兵】
13.光亮的铁钉在下列几种情况下,最不容易生锈的是( )
A B C D
14.“对比法”是实验探究中常用的一种科学方法,分析以下铁钉生锈实验的设计,得出的结论不正确的是( )2-1-c-n-j-y
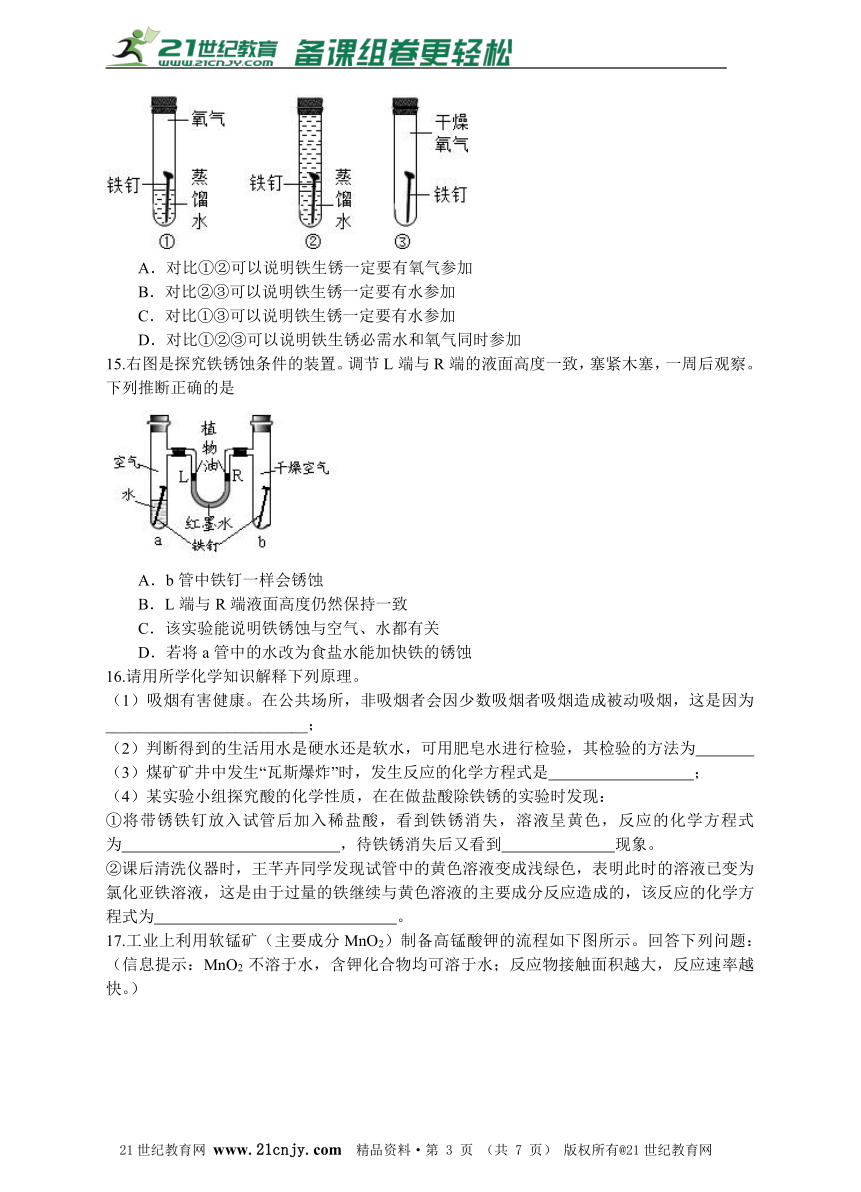
A.对比①②可以说明铁生锈一定要有氧气参加
B.对比②③可以说明铁生锈一定要有水参加
C.对比①③可以说明铁生锈一定要有水参加
D.对比①②③可以说明铁生锈必需水和氧气同时参加
15.右图是探究铁锈蚀条件的装置。调节L端与R端的液面高度一致,塞紧木塞,一周后观察。下列推断正确的是 【出处:21教育名师】
A.b管中铁钉一样会锈蚀
B.L端与R端液面高度仍然保持一致
C.该实验能说明铁锈蚀与空气、水都有关
D.若将a管中的水改为食盐水能加快铁的锈蚀
16.请用所学化学知识解释下列原理。
(1)吸烟有害健康。在公共场所,非吸烟者会因少数吸烟者吸烟造成被动吸烟,这是因为_________________________;【来源:21·世纪·教育·网】
(2)判断得到的生活用水是硬水还是软水,可用肥皂水进行检验,其检验的方法为
(3)煤矿矿井中发生“瓦斯爆炸”时,发生反应的化学方程式是 ;
(4)某实验小组探究酸的化学性质,在在做盐酸除铁锈的实验时发现:
①将带锈铁钉放入试管后加入稀盐酸,看到铁锈消失,溶液呈黄色,反应的化学方程式为 ,待铁锈消失后又看到 现象。
②课后清洗仪器时,王芊卉同学发现试管中的黄色溶液变成浅绿色,表明此时的溶液已变为氯化亚铁溶液,这是由于过量的铁继续与黄色溶液的主要成分反应造成的,该反应的化学方程式为 。【版权所有:21教育】
17.工业上利用软锰矿(主要成分MnO2)制备高锰酸钾的流程如下图所示。回答下列问题:(信息提示:MnO2 不溶于水,含钾化合物均可溶于水;反应物接触面积越大,反应速率越快。)
(1)将软锰矿粉碎的目的是_____________________。
(2)流程中通入的气体X是___________(填标号)
A.N2 B.CO2 C.H2
(3)操作Y的名称叫 ,用到的玻璃仪器有烧杯和 、 。
(4)上述流程中可循环利用的物质有 和_______。
18.(1)用下图所示实验探究铁生锈的条件(每支试管中均放有完全相同的洁净铁片):
①甲同学认为,试管A发生的现象就能够说明铁的锈蚀是铁与空气中的氧气、水蒸气共同作用的结果。乙同学不同意他的观点,认为必须全面观察试管_____________(选填试管编号)发生的现象,并经过科学严谨的推理,才能得出上述结论。
②试管D和E实验的目的是进一步探究铁在_____________________的环境中是否更容易锈蚀。
③为防止金属锈蚀,除了采用覆盖保护膜等措施以外,还可以制成合金。这是因为合金与纯金属相比,其组成和内部组织结构发生变化,从而引起__________________的变化。
(2)某同学向分别盛有等质量的铁粉和锌粒的试管中,倒入等质量、等溶质质量分数的稀硫酸,以“金属表面产生气泡的快慢”为标准来判断两种金属的活动性强弱。有的同学认为这种方案不够合理,理由是___________________________________________。
(3)将一定质量的铁粉放入硝酸铜、硝酸锌的混合溶液中,充分反应后过滤,所得固体中一定含有的物质是_______________________________,且反应后溶液质量比反应前___________(选填“增大”、 “减小”或“不变” )。21*cnjy*com
参考答案及解析
1.D
【解析】铁生锈主要条件是水和氧气。故选D.
2.A
【解析】浓盐酸有挥发性,置于空气中质量会减少,B错误;棉纤维的组成元素是碳、氢、氧,燃烧没有气味,C错误;二氧化碳是造成温室效应的主要物质,D错误。
3.C
【解析】虽然水比冰的比热容大,但在冷却食品时0℃的冰需要先熔化成水,吸收热量,所以冰的冷却效果好,A错误;铁在与水和氧气同时接触时易生锈,并不意味着其他的金属在潮湿的空气中都已被锈蚀,比如金,B错误;置换反应是单质与化合物反应生成另外的单质7.D21·cn·jy·com
【解析】钢铁制品在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果,使铁制品与氧气和水隔绝可以防止生锈.①涂油、②刷油漆、④镀上其他金属、⑤烤蓝、⑥包塑料布,能使铁制品与氧气和水隔绝,可以防止钢铁制品生锈.③保持干燥,可以防止钢铁制品生锈.故①②③④⑤.故选:D.21*cnjy*com
8.A
【解析】铁在潮湿的空气里会发生锈蚀,是由于与空气中的氧气和水接触,所以要探究铁生锈的条件,一定要设置对比试验,所以证明氧气一定参加了反应,必须要做的实验是(1)(2),实验(1)有氧气铁生锈,试验(2)没有与氧气接触不生锈,故选A
9.水和氧气(空气);涂油(刷漆等)
【解析】铁生锈的条件是水和氧气(空气);;根据铁锈蚀的条件,写出一种防止铁制品锈蚀的具体方法是涂油(刷漆等)。
10.(1)B(2)防止铁和水接触
【解析】用铁制成铁锅,这利用了铁的导热性。用水洗完的铁锅要用抹布擦干可以防止生锈,其理由是防止铁和水接触。
11.(1)贫血
(2)H2O 化合
(3)Fe + 2AgNO3==Fe(NO3)2 +2Ag
(4)在铁制品表面刷油漆,防止铁制品锈蚀
【解析】(1)缺铁会患缺铁性贫血
(2)反应前后各种原子的个数相等,反应后有4Fe、12H、12O而反应前只有4Fe、8H、10O,前后共差4H、2O,则一个分子中有2H、O,故填H2O 两种或两种以上的物质发生化学反应生成另外一种物质的反应是化合反应21世纪教育网版权所有
(3)铜、铁、锌、银四种金属中有一种金属的盐溶液与其他三种金属单质都能发生反应,则该盐溶液是银盐溶液,常见的银盐溶液是AgNO3溶液
(4)铁生锈是铁与空气中的氧气、水发生一系列反应生成铁锈,使铁与空气隔绝就可以防止铁生锈
12.(1)C + O2 点燃 CO2
(2)3CO+ Fe2O3 高温 2Fe + 3CO2
(3)Fe3O4 FeCl2 + H2高温 2HCl+Fe;赶走装置内的空气,防止生成的铁粉氧化。
【解析】(1)生铁转化为钢,用化学方程式表示原理为;C + O2 点燃 CO2
(2)工业上用一氧化碳和赤铁矿炼铁的化学方程式是3CO+ Fe2O3 高温 2Fe + 3CO2;
15.D
【解析】b管中铁钉不会锈蚀,缺少水分;L端与R端液面高度仍然不能保持一致,因为左端铁定会生锈,消耗其中的氧气,会出现L端高于R端;该实验能说明铁锈蚀与水都有关。故选D.【来源:21cnj*y.co*m】
16.(1)分子在不停地运动
(2)取水样加肥皂水,振荡,有沉淀或浮渣出现的为硬水,有泡沫出现的为软水
(3)CH4+2O2点燃2H2O+CO2
(4)Fe2O3+6HCl=2FeCl3+3H2O 气体生成 2FeCl3+Fe=3FeCl221教育名师原创作品
【解析】吸烟有害健康。在公共场所,非吸烟者会因少数吸烟者吸烟造成被动吸烟,这是因为)分子在不停地运动;判断得到的生活用水是硬水还是软水,可用肥皂水进行检验,其检验的方法为取水样加肥皂水,振荡,有沉淀或浮渣出现的为硬水,有泡沫出现的为软水。煤矿矿井中发生“瓦斯爆炸”时,发生反应的化学方程式是CH4+2O2点燃2H2O+CO2;[某实验小组探究酸的化学性质,在在做盐酸除铁锈的实验时发现:①将带锈铁钉放入试管后加入稀盐酸,看到铁锈消失,溶液呈黄色,反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O,待铁锈消失后又看到有气泡产生的现象。课后清洗仪器时,王芊卉同学发现试管中的黄色溶液变成浅绿色,表明此时的溶液已变为氯化亚铁溶液,这是由于过量的铁继续与黄色溶液的主要成分反应造成的,该反应的化学方程式为2FeCl3+Fe=3FeCl2。
17.(1)增大反应物的接触面积,提高反应速率。
(2)B
(3)过滤漏斗玻璃棒
(4)MnO2和KOH
【解析】将软锰矿粉碎的目的是增大反应物的接触面积,提高反应速率。流程中通入的气体X是CO2,因为根据质量守恒定律可以知道发生化学变化的时候元素的质量不会发生改变,(2)铁粉和锌粒的状态不相同,与酸反应的接触面积不同,反应速率也不同,所以这种方案不够合理
(3)铁粉能将硝酸铜中的铜置换出来,而与硝酸锌不发生反应,则充分反应后的固体中一定含有铜,反应后溶液由硝酸铜变为硝酸亚铁,溶液质量减小。
(带解析)
一、选择题
1.铁生锈主要条件是( )
A.仅需水 B.仅需氧气 C.水或氧气 D.水和氧气
2.下列说法正确的是 ( )
A.在钢铁表面镀铬能防止钢铁生锈
B.浓盐酸露置于空气中质量会增大
C.棉纤维在空气燃烧时产生烧焦羽毛的气味
D.二氧化碳是造成酸雨的主要物质
3.逻辑推理是科学学习常用的思维方法。下列推理正确的是( )
A.由于水比冰的比热容大,所以冷却食品时0℃的水比0℃的冰效果好
B.铁在潮湿的空气中容易被锈蚀,所以金属在潮湿的空气中都容易被锈蚀
C.真空罩内的空气越稀薄,在外面听到的铃声越小,所以“真空不能传声”
D.置换反应生成单质和化合物,所以有单质和化合物生成的反应一定是置换反应
4.铁是一种应用广泛的金属。下列有关铁的叙述正确的是( )
A.铁是地壳中含量最多的金属
B.工业上用二氧化碳冶炼钢铁
C.用铁可以回收硝酸银废液中的银
D.铁丝在氧气中燃烧生成氧化铁
5.下列有关资源的叙述正确的是( )
A.保护金属资源唯一的途径是防止金属的腐蚀
B.大气资源中含量最少的物质是稀有气体
C.人类可以利用的淡水量不到总水量的1%
D.金属资源都以化合物形式存在
6.下列物品需采取防锈措施的是( )
A.铁制防盗网 B.不锈钢菜刀 C.铝合金窗 D.金戒指
7.为了防止钢铁制品生锈,可采取的措施是( )
①涂油 ②刷油漆 ③保持干燥 ④镀上其他金属 ⑤烤蓝 ⑥包塑料布.
A.①②③⑥ B.③④⑤⑥ C.②③④⑤ D.①②③④⑤
8.铁在潮湿的空气里会发生锈蚀,证明氧气一定参加了反应,必须要做的实验是( )
A.(1)(2) B.(1)(3) C.(2)(3) D.(1)(2)(3)
二、填空题
9.据报道,金属材料因锈蚀而报废相当于世界年产量的1/3左右。铁生锈的条件是_____________________________;根据铁锈蚀的条件,写出一种防止铁制品锈蚀的具体方法是 (合理均可)。21教育网
10.(1)用铁制成铁锅,这利用了铁的_______(填字母序号)。
A.导电性 B.导热性 C.明亮的金属光泽
(2)用水洗完的铁锅要用抹布擦干可以防止生锈,其理由是_______。
11.金属在生产生活中有着非常广泛的应用。
(1)在酱油中加入铁强化剂,是我国为解决________(填“甲状腺肿大”“贫血”或“骨质疏松”)而实施的项目。21cnjy.com
(2)常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉。请将下列脱氧中的主要反应的化学方程式补充完整:4Fe(OH)2+O2+2________===4Fe(OH)3;此反应的基本类型是________。www.21-cn-jy.com
(3)实验室开放日,同学们在验证铜、铁、锌、银四种金属的活动性顺序时。小明发现四种金属中有一种金属的盐溶液与其他三种金属单质都能发生反应,请你写出其中一个反应的化学方程式 。 2·1·c·n·j·y
(4)目前世界上每年因腐蚀而报废的金属设备和材料相当于年产量的20%~40%。请举出一种保护金属资源的方法:______________________________________。
12.(1)在春秋战国时期,我国就开始生产和使用铁器,钢的质量也达到较高水平。古代,人们把烧红的生铁放在铁砧上反复锤打,最终使生铁转化为钢,用化学方程式表示原理 。21·世纪*教育网
(2)工业上用一氧化碳和赤铁矿炼铁的化学方程式是_______________________。
(3)新型材料纳米铁粉具有广泛的用途,它比普通铁粉更易与氧气反应,其制备的主要流程如下图所示。
纳米级铁粉遇氧气无需加热就能燃烧,生成物的化学式为 。
高温反应器中发生反应的化学方程式为 。反应前需向反应器中通入氮气,目的是 。www-2-1-cnjy-com
【中考大练兵】
13.光亮的铁钉在下列几种情况下,最不容易生锈的是( )
A B C D
14.“对比法”是实验探究中常用的一种科学方法,分析以下铁钉生锈实验的设计,得出的结论不正确的是( )2-1-c-n-j-y
A.对比①②可以说明铁生锈一定要有氧气参加
B.对比②③可以说明铁生锈一定要有水参加
C.对比①③可以说明铁生锈一定要有水参加
D.对比①②③可以说明铁生锈必需水和氧气同时参加
15.右图是探究铁锈蚀条件的装置。调节L端与R端的液面高度一致,塞紧木塞,一周后观察。下列推断正确的是 【出处:21教育名师】
A.b管中铁钉一样会锈蚀
B.L端与R端液面高度仍然保持一致
C.该实验能说明铁锈蚀与空气、水都有关
D.若将a管中的水改为食盐水能加快铁的锈蚀
16.请用所学化学知识解释下列原理。
(1)吸烟有害健康。在公共场所,非吸烟者会因少数吸烟者吸烟造成被动吸烟,这是因为_________________________;【来源:21·世纪·教育·网】
(2)判断得到的生活用水是硬水还是软水,可用肥皂水进行检验,其检验的方法为
(3)煤矿矿井中发生“瓦斯爆炸”时,发生反应的化学方程式是 ;
(4)某实验小组探究酸的化学性质,在在做盐酸除铁锈的实验时发现:
①将带锈铁钉放入试管后加入稀盐酸,看到铁锈消失,溶液呈黄色,反应的化学方程式为 ,待铁锈消失后又看到 现象。
②课后清洗仪器时,王芊卉同学发现试管中的黄色溶液变成浅绿色,表明此时的溶液已变为氯化亚铁溶液,这是由于过量的铁继续与黄色溶液的主要成分反应造成的,该反应的化学方程式为 。【版权所有:21教育】
17.工业上利用软锰矿(主要成分MnO2)制备高锰酸钾的流程如下图所示。回答下列问题:(信息提示:MnO2 不溶于水,含钾化合物均可溶于水;反应物接触面积越大,反应速率越快。)
(1)将软锰矿粉碎的目的是_____________________。
(2)流程中通入的气体X是___________(填标号)
A.N2 B.CO2 C.H2
(3)操作Y的名称叫 ,用到的玻璃仪器有烧杯和 、 。
(4)上述流程中可循环利用的物质有 和_______。
18.(1)用下图所示实验探究铁生锈的条件(每支试管中均放有完全相同的洁净铁片):
①甲同学认为,试管A发生的现象就能够说明铁的锈蚀是铁与空气中的氧气、水蒸气共同作用的结果。乙同学不同意他的观点,认为必须全面观察试管_____________(选填试管编号)发生的现象,并经过科学严谨的推理,才能得出上述结论。
②试管D和E实验的目的是进一步探究铁在_____________________的环境中是否更容易锈蚀。
③为防止金属锈蚀,除了采用覆盖保护膜等措施以外,还可以制成合金。这是因为合金与纯金属相比,其组成和内部组织结构发生变化,从而引起__________________的变化。
(2)某同学向分别盛有等质量的铁粉和锌粒的试管中,倒入等质量、等溶质质量分数的稀硫酸,以“金属表面产生气泡的快慢”为标准来判断两种金属的活动性强弱。有的同学认为这种方案不够合理,理由是___________________________________________。
(3)将一定质量的铁粉放入硝酸铜、硝酸锌的混合溶液中,充分反应后过滤,所得固体中一定含有的物质是_______________________________,且反应后溶液质量比反应前___________(选填“增大”、 “减小”或“不变” )。21*cnjy*com
参考答案及解析
1.D
【解析】铁生锈主要条件是水和氧气。故选D.
2.A
【解析】浓盐酸有挥发性,置于空气中质量会减少,B错误;棉纤维的组成元素是碳、氢、氧,燃烧没有气味,C错误;二氧化碳是造成温室效应的主要物质,D错误。
3.C
【解析】虽然水比冰的比热容大,但在冷却食品时0℃的冰需要先熔化成水,吸收热量,所以冰的冷却效果好,A错误;铁在与水和氧气同时接触时易生锈,并不意味着其他的金属在潮湿的空气中都已被锈蚀,比如金,B错误;置换反应是单质与化合物反应生成另外的单质7.D21·cn·jy·com
【解析】钢铁制品在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果,使铁制品与氧气和水隔绝可以防止生锈.①涂油、②刷油漆、④镀上其他金属、⑤烤蓝、⑥包塑料布,能使铁制品与氧气和水隔绝,可以防止钢铁制品生锈.③保持干燥,可以防止钢铁制品生锈.故①②③④⑤.故选:D.21*cnjy*com
8.A
【解析】铁在潮湿的空气里会发生锈蚀,是由于与空气中的氧气和水接触,所以要探究铁生锈的条件,一定要设置对比试验,所以证明氧气一定参加了反应,必须要做的实验是(1)(2),实验(1)有氧气铁生锈,试验(2)没有与氧气接触不生锈,故选A
9.水和氧气(空气);涂油(刷漆等)
【解析】铁生锈的条件是水和氧气(空气);;根据铁锈蚀的条件,写出一种防止铁制品锈蚀的具体方法是涂油(刷漆等)。
10.(1)B(2)防止铁和水接触
【解析】用铁制成铁锅,这利用了铁的导热性。用水洗完的铁锅要用抹布擦干可以防止生锈,其理由是防止铁和水接触。
11.(1)贫血
(2)H2O 化合
(3)Fe + 2AgNO3==Fe(NO3)2 +2Ag
(4)在铁制品表面刷油漆,防止铁制品锈蚀
【解析】(1)缺铁会患缺铁性贫血
(2)反应前后各种原子的个数相等,反应后有4Fe、12H、12O而反应前只有4Fe、8H、10O,前后共差4H、2O,则一个分子中有2H、O,故填H2O 两种或两种以上的物质发生化学反应生成另外一种物质的反应是化合反应21世纪教育网版权所有
(3)铜、铁、锌、银四种金属中有一种金属的盐溶液与其他三种金属单质都能发生反应,则该盐溶液是银盐溶液,常见的银盐溶液是AgNO3溶液
(4)铁生锈是铁与空气中的氧气、水发生一系列反应生成铁锈,使铁与空气隔绝就可以防止铁生锈
12.(1)C + O2 点燃 CO2
(2)3CO+ Fe2O3 高温 2Fe + 3CO2
(3)Fe3O4 FeCl2 + H2高温 2HCl+Fe;赶走装置内的空气,防止生成的铁粉氧化。
【解析】(1)生铁转化为钢,用化学方程式表示原理为;C + O2 点燃 CO2
(2)工业上用一氧化碳和赤铁矿炼铁的化学方程式是3CO+ Fe2O3 高温 2Fe + 3CO2;
15.D
【解析】b管中铁钉不会锈蚀,缺少水分;L端与R端液面高度仍然不能保持一致,因为左端铁定会生锈,消耗其中的氧气,会出现L端高于R端;该实验能说明铁锈蚀与水都有关。故选D.【来源:21cnj*y.co*m】
16.(1)分子在不停地运动
(2)取水样加肥皂水,振荡,有沉淀或浮渣出现的为硬水,有泡沫出现的为软水
(3)CH4+2O2点燃2H2O+CO2
(4)Fe2O3+6HCl=2FeCl3+3H2O 气体生成 2FeCl3+Fe=3FeCl221教育名师原创作品
【解析】吸烟有害健康。在公共场所,非吸烟者会因少数吸烟者吸烟造成被动吸烟,这是因为)分子在不停地运动;判断得到的生活用水是硬水还是软水,可用肥皂水进行检验,其检验的方法为取水样加肥皂水,振荡,有沉淀或浮渣出现的为硬水,有泡沫出现的为软水。煤矿矿井中发生“瓦斯爆炸”时,发生反应的化学方程式是CH4+2O2点燃2H2O+CO2;[某实验小组探究酸的化学性质,在在做盐酸除铁锈的实验时发现:①将带锈铁钉放入试管后加入稀盐酸,看到铁锈消失,溶液呈黄色,反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O,待铁锈消失后又看到有气泡产生的现象。课后清洗仪器时,王芊卉同学发现试管中的黄色溶液变成浅绿色,表明此时的溶液已变为氯化亚铁溶液,这是由于过量的铁继续与黄色溶液的主要成分反应造成的,该反应的化学方程式为2FeCl3+Fe=3FeCl2。
17.(1)增大反应物的接触面积,提高反应速率。
(2)B
(3)过滤漏斗玻璃棒
(4)MnO2和KOH
【解析】将软锰矿粉碎的目的是增大反应物的接触面积,提高反应速率。流程中通入的气体X是CO2,因为根据质量守恒定律可以知道发生化学变化的时候元素的质量不会发生改变,(2)铁粉和锌粒的状态不相同,与酸反应的接触面积不同,反应速率也不同,所以这种方案不够合理
(3)铁粉能将硝酸铜中的铜置换出来,而与硝酸锌不发生反应,则充分反应后的固体中一定含有铜,反应后溶液由硝酸铜变为硝酸亚铁,溶液质量减小。
同课章节目录
