化学反应中的热量【课件】
图片预览





文档简介
课件12张PPT。化学反应中的热量变化学习目标1. 认识化学反应伴随能量变化,了解吸热反应和放热反应。2. 了解热化学方程式的书写。 2013年6月“神十”凯旋而归为中国梦注入了科技正能量。自主学习1阅读课本p34,请结合图2-3和生活常识,举例说明化学反应中伴随着能量变化,并指出其中能量转化的方式。试管外壁
发热镁与盐酸反应
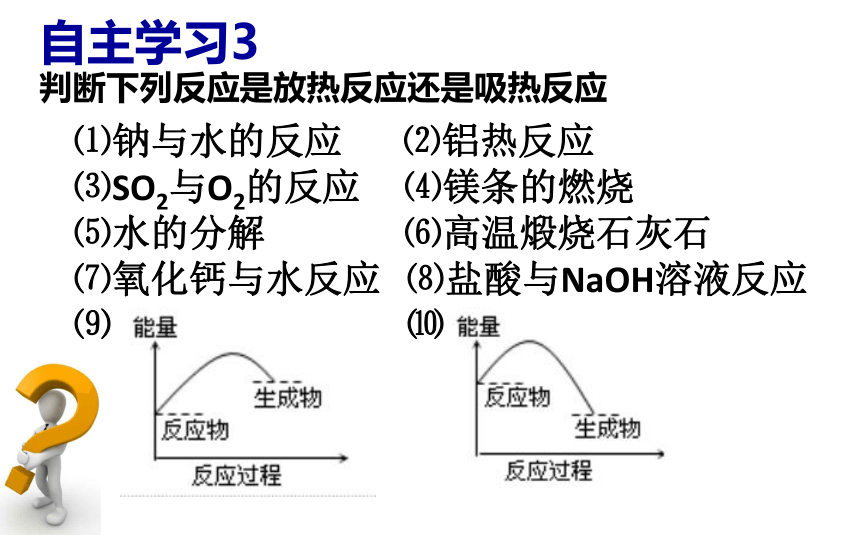
有热量放出温度降低氢氧化钡固体与氯化铵固体反应需要吸收热量合作探究2 感受化学反应中的能量变化 判断下列反应是放热反应还是吸热反应自主学习3⑴钠与水的反应 ⑵铝热反应
⑶SO2与O2的反应 ⑷镁条的燃烧
⑸水的分解 ⑹高温煅烧石灰石
⑺氧化钙与水反应 ⑻盐酸与NaOH溶液反应⑼ ⑽自主学习4阅读课本p35找出热化学方程式的特征及意义并完成牛刀小试1.沼气是一种能源,它的主要成分是CH4。已知0.5molCH4完全燃烧生成CO2和液态水时放出445kJ的热量。则下列热化学方程式正确的是( )
A.2CH4(g)+4O2(g)=2CO2(g)+4H2O(l)
△H =+890kJ/mol
B.CH4(g)+2O2(g)=CO2(g)+2H2O(g)
△H =-890kJ/mol
C.CH4(g)+2O2(g)=CO2(g)+2H2O(l)
△H =-890kJ
D.1/2CH4(g)+O2(g)=CO2(g)+H2O(l)
△H =-445kJ/molD牛刀小试在一定温度下,1molCO与1mol水蒸气在催化剂作用下完全反应,生成CO2气体和H2,放出41kJ的热量。请写出该反应的热化学方程式。CO(g)+H2O(g)= CO2 (g)+H2(g) ΔH=-41kJ/mol
1下列说法正确的是( )
A.需要加热才能发生的反应一定是吸热反应
B.凡是有能量变化的过程都是化学变化
C.反应物和生成物所具有的总能量的相对大小决定了放热还是吸热
D.反应放出热量,则ΔH>0;反应吸收热量,则ΔH<0。当堂检测C2神舟十号飞船的运载火箭上发动机使用四氧化二氮和偏二甲肼作燃料。下列热化学方程式书写正确的是( )
A.C2H8N2+2N2O4=2CO2+4H2O+3N2
△H =-2250kJ/mol
B.C2H8N2(l)+2N2O4(l)=2CO2(g)+4H2O(g)+3N2(g) △H =+2250kJ/mol
C.C2H8N2(l)+2N2O4(l)=2CO2(g)+4H2O(g)+3N2(g) △H =-2250kJ/mol
D.C2H8N2(l)+2N2O4(l)=2CO2(g)+4H2O(g)+3N2(g) △H =-2250kJ
C33.1molCu(s)与适量O2(g)发生反应,生成CuO(s),放出157kJ热量,写出该反应的热化学方程式。Cu(s)+1/2O2 (g)= CuO (s) ΔH=-157kJ/mol
发热镁与盐酸反应
有热量放出温度降低氢氧化钡固体与氯化铵固体反应需要吸收热量合作探究2 感受化学反应中的能量变化 判断下列反应是放热反应还是吸热反应自主学习3⑴钠与水的反应 ⑵铝热反应
⑶SO2与O2的反应 ⑷镁条的燃烧
⑸水的分解 ⑹高温煅烧石灰石
⑺氧化钙与水反应 ⑻盐酸与NaOH溶液反应⑼ ⑽自主学习4阅读课本p35找出热化学方程式的特征及意义并完成牛刀小试1.沼气是一种能源,它的主要成分是CH4。已知0.5molCH4完全燃烧生成CO2和液态水时放出445kJ的热量。则下列热化学方程式正确的是( )
A.2CH4(g)+4O2(g)=2CO2(g)+4H2O(l)
△H =+890kJ/mol
B.CH4(g)+2O2(g)=CO2(g)+2H2O(g)
△H =-890kJ/mol
C.CH4(g)+2O2(g)=CO2(g)+2H2O(l)
△H =-890kJ
D.1/2CH4(g)+O2(g)=CO2(g)+H2O(l)
△H =-445kJ/molD牛刀小试在一定温度下,1molCO与1mol水蒸气在催化剂作用下完全反应,生成CO2气体和H2,放出41kJ的热量。请写出该反应的热化学方程式。CO(g)+H2O(g)= CO2 (g)+H2(g) ΔH=-41kJ/mol
1下列说法正确的是( )
A.需要加热才能发生的反应一定是吸热反应
B.凡是有能量变化的过程都是化学变化
C.反应物和生成物所具有的总能量的相对大小决定了放热还是吸热
D.反应放出热量,则ΔH>0;反应吸收热量,则ΔH<0。当堂检测C2神舟十号飞船的运载火箭上发动机使用四氧化二氮和偏二甲肼作燃料。下列热化学方程式书写正确的是( )
A.C2H8N2+2N2O4=2CO2+4H2O+3N2
△H =-2250kJ/mol
B.C2H8N2(l)+2N2O4(l)=2CO2(g)+4H2O(g)+3N2(g) △H =+2250kJ/mol
C.C2H8N2(l)+2N2O4(l)=2CO2(g)+4H2O(g)+3N2(g) △H =-2250kJ/mol
D.C2H8N2(l)+2N2O4(l)=2CO2(g)+4H2O(g)+3N2(g) △H =-2250kJ
C33.1molCu(s)与适量O2(g)发生反应,生成CuO(s),放出157kJ热量,写出该反应的热化学方程式。Cu(s)+1/2O2 (g)= CuO (s) ΔH=-157kJ/mol
