课题2 酸和碱的中和反应 同步练习(带解析)
文档属性
| 名称 | 课题2 酸和碱的中和反应 同步练习(带解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 565.6KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-02-24 00:00:00 | ||
图片预览



文档简介
课题2 酸和碱的中和反应 同步练习(带解析)
一、选择题
1、肥皂水呈弱碱性,则肥皂水的pH可能是( )
A.9.5? B.7.0? C.5.6? D.1.2
2、酸与碱中和生成盐和水,现将20g20%的NaOH溶液与20g20%的H2SO4溶液充分反应后滴入紫色石蕊试液,混合物呈现( )
A.蓝色 B.紫色 C.红色 D.无色
3、下列关于中和反应的说法,正确的是( )???????????????????????
A.纯碱和稀盐酸混合后发生中和反应??????????????????????????????
B.有盐和水生成的反应一定是中和反应????????????????????????????
C.工厂废水中含有的硫酸可以用氨水中和??????????????????????????
D.中和反应的发生必须借助酸碱指示剂进行判断????????????????????????
4、下列实际应用中,利用中和反应原理的是( )
①用氢氧化钠溶液洗去石油产品中的残余硫酸;②用稀硫酸除铁锈;③用熟石灰改良酸性土壤;④用碳酸氢钠治疗胃酸过多.21世纪教育网版权所有
A.①③ B.③④ C.①②④?? D.①③④
5、逻辑推理是一种重要的化学思维方法,以下推理合理的是( )
A.因为酸性的溶液能使石蕊变红,所以酸溶液一定能使石蕊变红
B.因为酸和碱中和反应生成盐和水,所以生成盐和水一定是中和反应
C.因为金属能和酸反应产生氢气,所以能和酸产生气体的一定是金属
D.因为H2O和H2O2的组成元素相同,所以它们的化学性质相同
6、向滴有酚酞的NaOH溶液中,逐渐滴入稀盐酸至过量,下面叙述正确的是( )
A.溶液由红色变为无色,PH逐渐增大
B.溶液由无色变为红色,PH逐渐减小
C.溶液由红色变为无色,PH逐渐减小
D.溶液颜色不变,PH逐渐增大
7、如图为喷墨打印机工作原理示意图,溶解在打印墨水(pH:7.5﹣9.0)中的染料,从喷嘴喷到打印纸(pH:4.5﹣6.5)上,变为不溶于水的固体.下列说法正确的是( )
A.打印墨水偏酸性?? B.打印墨水呈中性
C.打印纸偏酸性 D.打印纸偏碱性
8、如图是稀HCl和NaOH溶液反应的pH变化曲线,以下说法正确的是( )
A.该反应是稀HCl滴入NaOH溶液中
B.ag是指加入氢氧化钠固体质量
C.A点溶液的溶质为HCl和NaCl
D.检验B点溶液的溶质先滴加足量的AgNO3,静置后再滴入少量Ba(NO3)2
二、填空题
9、用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示,当加入熟石灰mg时,溶液中的溶质为 .2·1·c·n·j·y
10、化学就在我们身边,它与我们的生活息息相关.请从A熟石灰、B苏打、C一氧化碳、D氮气、E浓硫酸、F盐酸这六种物质中,选择适当的物质用序号填空.
(1)能与酸发生中和反应的物质是 ;?
(2)常用于工业除锈的试剂是 ;
(3)有毒的物质是 ;?
(4)我国著名化学家侯德榜发明的联合制碱法中的“碱”是指 .
11、请根据下表回答有关问题.??????????????????????????????????????? 21·cn·jy·com
序号?????
①??????????
②?????????????
③?????????????
④
物质?????
醋酸????????
高锰酸钾???????
熟石灰?????????
纯碱
化学式???
CH3COOH?????
KMnO4??????????
Ca(OH)2??????
Na2CO3
(1)槟榔芋皮上含有一种碱性的物质﹣﹣皂角素,皮肤沾上它会奇痒难忍.可选用上表中哪种物质来涂抹止痒 (填序号).??????????????????????????????????????????????????????
(2)利用上表中的物质作为反应物,写出制取氢氧化钠的化学方程式 .??????????
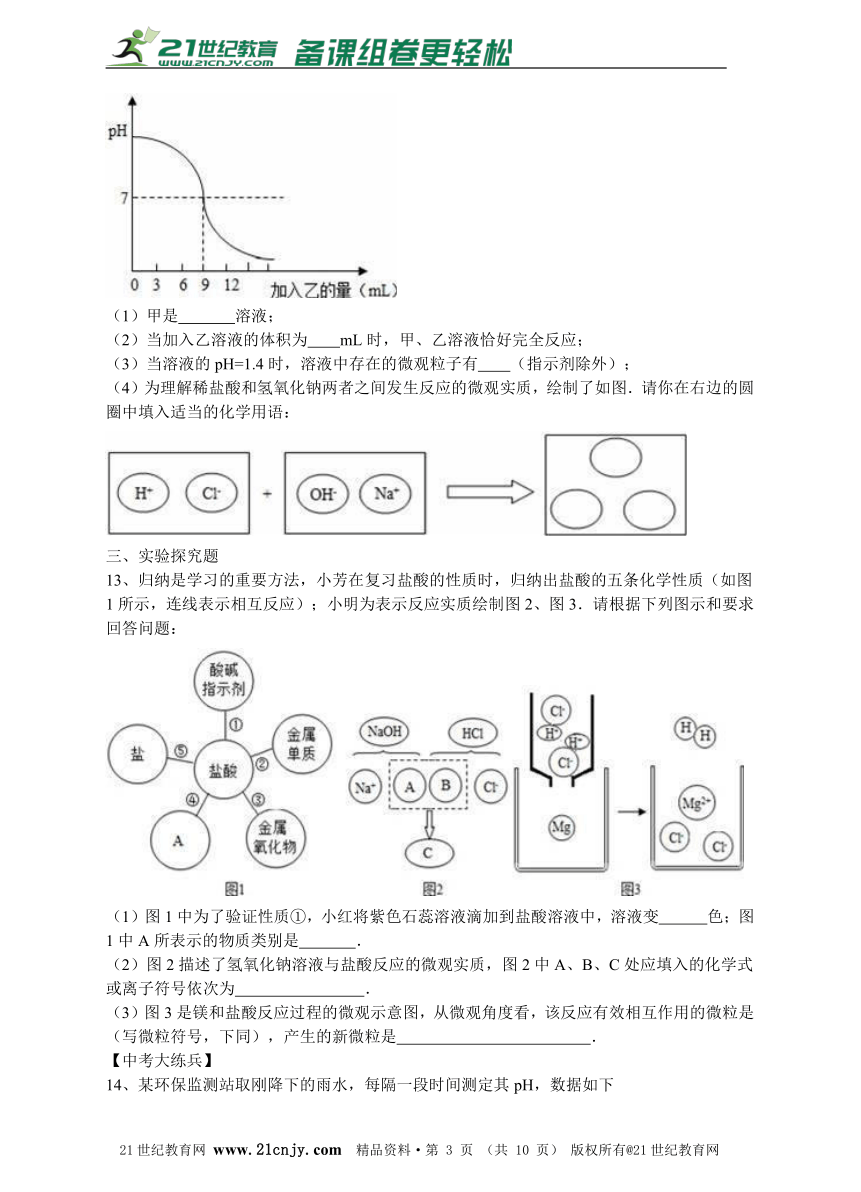
12、如图表示的是向盛有l0mL稀的甲溶液(其中滴有少量紫色石蕊试剂)中,加入乙溶液(相同浓度)后,溶液pH的变化曲线.已知甲、乙分别是盐酸溶液和氢氧化钠溶液中的一种.请分析曲线回答问题:21教育网
(1)甲是 溶液;
(2)当加入乙溶液的体积为 mL时,甲、乙溶液恰好完全反应;
(3)当溶液的pH=1.4时,溶液中存在的微观粒子有 (指示剂除外);
(4)为理解稀盐酸和氢氧化钠两者之间发生反应的微观实质,绘制了如图.请你在右边的圆圈中填入适当的化学用语:
三、实验探究题
13、归纳是学习的重要方法,小芳在复习盐酸的性质时,归纳出盐酸的五条化学性质(如图1所示,连线表示相互反应);小明为表示反应实质绘制图2、图3.请根据下列图示和要求回答问题:【来源:21·世纪·教育·网】
(1)图1中为了验证性质①,小红将紫色石蕊溶液滴加到盐酸溶液中,溶液变 色;图1中A所表示的物质类别是 .21·世纪*教育网
(2)图2描述了氢氧化钠溶液与盐酸反应的微观实质,图2中A、B、C处应填入的化学式或离子符号依次为 .2-1-c-n-j-y
(3)图3是镁和盐酸反应过程的微观示意图,从微观角度看,该反应有效相互作用的微粒是 (写微粒符号,下同),产生的新微粒是 .
【中考大练兵】
14、某环保监测站取刚降下的雨水,每隔一段时间测定其pH,数据如下
测定时间∕分钟
0
1
2
4
5
pH
4.8
4.6
4.5
4.5
4.5
下列有关说法不正确的是( )
A.雨水酸性逐渐减弱
B.雨水的酸性一段时间后趋于稳定
C.酸雨会腐蚀机械设备和建筑物
D.硫和氮的氧化物是形成酸雨的主要因素
15、下列图象能正确反映对应实验操作中量的关系是( )
A.一定量稀硫酸加水稀释
B.一定量氯化铜和盐酸的混合溶液中逐渐加入稀硫酸
C.等质量的镁粉和铁粉中分别缓慢加入稀硫酸
D.等质量的高锰酸钾和氯酸钾加热制氧气
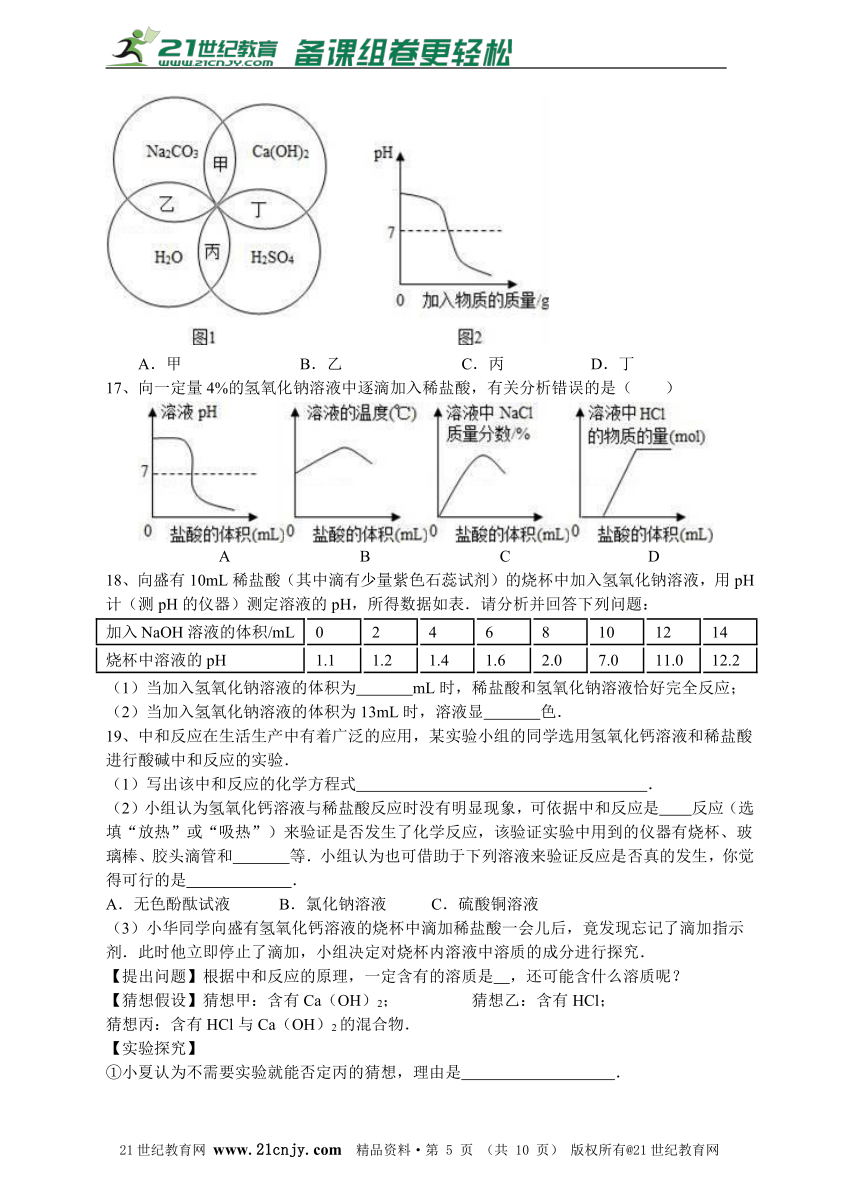
16、图1中甲、乙、丙、丁表示相邻两物质相互混合过程中溶液酸碱度的变化,其中可能得图2所示变化关系的是( )www.21-cn-jy.com
A.甲?? B.乙?? C.丙?? D.丁
17、向一定量4%的氢氧化钠溶液中逐滴加入稀盐酸,有关分析错误的是( )
A B C D
18、向盛有10mL稀盐酸(其中滴有少量紫色石蕊试剂)的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如表.请分析并回答下列问题:
加入NaOH溶液的体积/mL
0
2
4
6
8
10
12
14
烧杯中溶液的pH
1.1
1.2
1.4
1.6
2.0
7.0
11.0
12.2
(1)当加入氢氧化钠溶液的体积为 mL时,稀盐酸和氢氧化钠溶液恰好完全反应;
(2)当加入氢氧化钠溶液的体积为13mL时,溶液显 色.
19、中和反应在生活生产中有着广泛的应用,某实验小组的同学选用氢氧化钙溶液和稀盐酸进行酸碱中和反应的实验.【出处:21教育名师】
(1)写出该中和反应的化学方程式 .
(2)小组认为氢氧化钙溶液与稀盐酸反应时没有明显现象,可依据中和反应是 反应(选填“放热”或“吸热”)来验证是否发生了化学反应,该验证实验中用到的仪器有烧杯、玻璃棒、胶头滴管和 等.小组认为也可借助于下列溶液来验证反应是否真的发生,你觉得可行的是 .【版权所有:21教育】
A.无色酚酞试液?????????? B.氯化钠溶液????????? C.硫酸铜溶液
(3)小华同学向盛有氢氧化钙溶液的烧杯中滴加稀盐酸一会儿后,竟发现忘记了滴加指示剂.此时他立即停止了滴加,小组决定对烧杯内溶液中溶质的成分进行探究.
【提出问题】根据中和反应的原理,一定含有的溶质是 ,还可能含什么溶质呢?
【猜想假设】猜想甲:含有Ca(OH)2;???????????????? 猜想乙:含有HCl;
猜想丙:含有HCl与Ca(OH)2的混合物.
【实验探究】
①小夏认为不需要实验就能否定丙的猜想,理由是 .
②小腾向反应后的溶液中滴加几滴无色酚酞试液并振荡,观察到酚酞试液不变色.于是他排除了猜想甲,你认为他排除的原因是 .21*cnjy*com
③小飞只用一种溶液完成了对猜想乙的验证,请你帮他完成实验表格:
实验操作
预测现象
结论
取少量反应后的溶液于烧杯中,并向其中滴加足量的 溶液.
且溶液中出现沉淀
猜想乙正确
【反思拓展】
中和反应的微观实质就是酸中的氢离子和碱中的氢氧根离子结合生成了水,即:氢离子+氢氧根离子═水,将该表达式用化学符号表示为 .
参考答案及解析
1、A
【解答】A、pH=9.5,大于7,显弱碱性.
B、pH=7,显中性.
A、纯碱(是盐不是碱)和稀盐酸反应,反应物不是酸和碱,且生成物也不仅仅是盐和水,还生成了二氧化碳.错误. ???????????????????????????????????????? 21cnjy.com
B、生成盐和水的反应未必是中和反应,因为反应物可以是非金属氧化物和碱反应(如CO2+2NaOH=Na2CO3+H2O),也可以是金属氧化物与酸反应(如CuO+2HCl=CuCl2+H2O.错误.????????????????????? www-2-1-cnjy-com
C、氨水是碱,可以用来中和含有硫酸的废水(这个方案不是最佳的,因为成本以及运输等都不合适,氨水是液体,且现在使用氨水的情况很少,还是使用熟石灰或者生石灰的较多).正确.??????? 【来源:21cnj*y.co*m】
D、中和反应的发生不一定需要借助酸碱指示剂来进行判断,如氢氧化铜、氢氧化铁和氢氧化铝等难溶性且有颜色的碱和酸反应就不需要借助指示剂来判断反应的进行与否,而是看难溶性碱是否溶解于酸.错误.???????????
4、A
【解答】①氢氧化钠与硫酸的反应是酸和碱的反应,属于中和反应;
②用硫酸除铁锈,铁锈的主要成分为氧化铁,硫酸与氧化铁反应,不属于中和反应;
③用熟石灰改良酸性土壤,是酸和碱的反应,属于中和反应;
④碳酸氢钠治疗胃酸过多,碳酸氢钠是盐不是碱,不属于中和反应.
5、A
【解答】A、为酸性的溶液能使石蕊变红,所以酸溶液一定能使石蕊变红,故正确;
B、生成盐和水的反应不一定是中和反应,例如氧化铜和盐酸反应能生成盐氯化铜和水,不属于中和反应.故错误;21教育名师原创作品
C、与盐酸反应放出气体的物质不一定是金属,例如碳酸盐与稀盐酸反应能生成二氧化碳.故错误;
D、水(H2O)和过氧化氢(H2O2)的元素组成相同,但分子结构不同,一个过氧化氢分子比一个水分子多一个氧原子,所以化学性质不同,故错误.
6、C
【解答】酚酞遇碱变红遇酸不变色,故在反应过程中溶液会先有红色,至恰好反应到过量时溶液会变成无色,PH会由大于7到等于7再到小于7.
7、C
(2)盐酸能与金属氧化物反应生成盐和水,常用于金属去锈,故选F;
(3)一氧化碳是有毒的物质,故选C;
(4)苏打是碳酸钠的俗称,是德榜发明的联合制碱法中的“碱”,故选B;
11、(1)①;???????????????????????????????????????????????????
(2)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
【解答】(1)槟榔芋皮上含有一种碱性的物质﹣﹣皂角素,沾上它会使皮肤奇痒难忍;因为皂角素显碱性,所以应该选用显酸性的物质来与它反应,①②③④这三种物质中只有①显酸性,而②显中性,③④显碱性.???????????
(2)碳酸钠溶液与氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,可用于制取氢氧化钠,反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.????????????????????????????????????????
12、(1)NaOH;
(2)9;
(3)H+、Cl﹣、Na+;
(4)H2O,Na+,Cl﹣.
【解答】(1)开始时溶液的pH大于7,故甲是氢氧化钠溶液,故填:氢氧化钠;
(2)据图可知,当加入的盐酸的量为9mL时,溶液的pH等于7,此时二者恰好完全反应,故填:9;
(3)氢氧化钠能和盐酸反应生成氯化钠和水,pH=1.4时,盐酸过量,故溶液中的溶质是氯化氢和氯化钠,溶液中存在的微观粒子有:H+、Cl﹣、Na+;21*cnjy*com
(4)酸碱反应的实质是酸中的氢离子和碱中的氢氧根离子结合生成水分子,而金属钠离子和酸根离子氯离子仍然是以自由移动的离子存在,故填:H2O,Na+,Cl﹣.
13、(1)红,碱;
(2)OH﹣、H+、H2O;
(3)Mg、H+,H2、Mg2+
【解答】(1)将紫色石蕊试液滴加到盐酸溶液中,溶液变红色;图1中A所表示的物质类别是碱;
(2)图2中A、B、C处应填入的化学式或离子符号依次为OH﹣、H+、H2O;
(3)图3是镁和盐酸反应过程的微观示意图,从微观角度看,该反应有效相互作用的微粒是Mg、H+,产生的新微粒是H2、Mg2+.
B.酸碱中和反应会放出热量,故随着稀盐酸的加入,溶液的温度升高,当恰好完全中和时,溶液温度最高,继续滴加稀盐酸,溶液的温度就会降低,所以图象正确;
C.没有滴加稀盐酸时,溶液中氯化钠的质量分数为零,随着加入稀盐酸生成的氯化钠越来越多,溶液中氯化钠的质量分数越来越大,当二者完全中和时,溶液中氯化钠的质量分数达到最大值且不再增加,再滴加稀盐酸,溶液的质量增大,氯化钠的质量不变,溶液中氯化钠的质量分数减小,故图象正确;
D.当加入的稀盐酸与氢氧化钠发生反应时,HCl的物质的量为零,当二者恰好完全反应时,继续滴加稀盐酸,HCl的物质的量增加,且随着稀盐酸加入的量的增多,而不断增大,故图象错误.
18、10; 蓝.
【解答】解:(1)pH=7时,氢氧化钠和稀盐酸恰好完全反应.故填:10;
(2)当加入氢氧化钠溶液13毫升时,溶液显碱性.能使石蕊试液变蓝.故填;蓝.
19、(1)Ca(OH)2+2HCl═CaCl2+2H2O;
(2)放热;温度计;AC;
(3)【提出问题】氯化钙;
【实验探究】
①氢氧化钙和盐酸反应生成氯化钙和水,二者不共存;
②氢氧化钙溶液呈碱性,使酚酞试液变红,现不变红,故溶质不可能含氢氧化钙;
③
实验操作
预测现象
结论
取少量反应后的溶液于烧杯中,并向其中滴加足量的碳酸钠溶液.
先有气泡产生且溶液中出现沉淀
猜想乙正确
【反思拓展】H++OH﹣=H2O.
【解答】(1)氢氧化钙和盐酸发生中和反应生成氯化钙和水,故答案为:Ca(OH)2+2HCl③氯化钙溶液可以和碳酸钠溶液反应生成沉淀,和稀盐酸反应生成二氧化碳气体,所以可以将碳酸钠溶液滴入反应后的溶液中,若观察到有气泡冒出,当没有气泡冒出时,则说明溶液中含有氯化氢和氯化钙;
【反思拓展】中和反应的微观实质就是酸中的氢离子和碱中的氢氧根离子结合生成了水,即:氢离子+氢氧根离子=水,将该表达式用化学符号表示为:
H++OH﹣=H2O.
一、选择题
1、肥皂水呈弱碱性,则肥皂水的pH可能是( )
A.9.5? B.7.0? C.5.6? D.1.2
2、酸与碱中和生成盐和水,现将20g20%的NaOH溶液与20g20%的H2SO4溶液充分反应后滴入紫色石蕊试液,混合物呈现( )
A.蓝色 B.紫色 C.红色 D.无色
3、下列关于中和反应的说法,正确的是( )???????????????????????
A.纯碱和稀盐酸混合后发生中和反应??????????????????????????????
B.有盐和水生成的反应一定是中和反应????????????????????????????
C.工厂废水中含有的硫酸可以用氨水中和??????????????????????????
D.中和反应的发生必须借助酸碱指示剂进行判断????????????????????????
4、下列实际应用中,利用中和反应原理的是( )
①用氢氧化钠溶液洗去石油产品中的残余硫酸;②用稀硫酸除铁锈;③用熟石灰改良酸性土壤;④用碳酸氢钠治疗胃酸过多.21世纪教育网版权所有
A.①③ B.③④ C.①②④?? D.①③④
5、逻辑推理是一种重要的化学思维方法,以下推理合理的是( )
A.因为酸性的溶液能使石蕊变红,所以酸溶液一定能使石蕊变红
B.因为酸和碱中和反应生成盐和水,所以生成盐和水一定是中和反应
C.因为金属能和酸反应产生氢气,所以能和酸产生气体的一定是金属
D.因为H2O和H2O2的组成元素相同,所以它们的化学性质相同
6、向滴有酚酞的NaOH溶液中,逐渐滴入稀盐酸至过量,下面叙述正确的是( )
A.溶液由红色变为无色,PH逐渐增大
B.溶液由无色变为红色,PH逐渐减小
C.溶液由红色变为无色,PH逐渐减小
D.溶液颜色不变,PH逐渐增大
7、如图为喷墨打印机工作原理示意图,溶解在打印墨水(pH:7.5﹣9.0)中的染料,从喷嘴喷到打印纸(pH:4.5﹣6.5)上,变为不溶于水的固体.下列说法正确的是( )
A.打印墨水偏酸性?? B.打印墨水呈中性
C.打印纸偏酸性 D.打印纸偏碱性
8、如图是稀HCl和NaOH溶液反应的pH变化曲线,以下说法正确的是( )
A.该反应是稀HCl滴入NaOH溶液中
B.ag是指加入氢氧化钠固体质量
C.A点溶液的溶质为HCl和NaCl
D.检验B点溶液的溶质先滴加足量的AgNO3,静置后再滴入少量Ba(NO3)2
二、填空题
9、用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示,当加入熟石灰mg时,溶液中的溶质为 .2·1·c·n·j·y
10、化学就在我们身边,它与我们的生活息息相关.请从A熟石灰、B苏打、C一氧化碳、D氮气、E浓硫酸、F盐酸这六种物质中,选择适当的物质用序号填空.
(1)能与酸发生中和反应的物质是 ;?
(2)常用于工业除锈的试剂是 ;
(3)有毒的物质是 ;?
(4)我国著名化学家侯德榜发明的联合制碱法中的“碱”是指 .
11、请根据下表回答有关问题.??????????????????????????????????????? 21·cn·jy·com
序号?????
①??????????
②?????????????
③?????????????
④
物质?????
醋酸????????
高锰酸钾???????
熟石灰?????????
纯碱
化学式???
CH3COOH?????
KMnO4??????????
Ca(OH)2??????
Na2CO3
(1)槟榔芋皮上含有一种碱性的物质﹣﹣皂角素,皮肤沾上它会奇痒难忍.可选用上表中哪种物质来涂抹止痒 (填序号).??????????????????????????????????????????????????????
(2)利用上表中的物质作为反应物,写出制取氢氧化钠的化学方程式 .??????????
12、如图表示的是向盛有l0mL稀的甲溶液(其中滴有少量紫色石蕊试剂)中,加入乙溶液(相同浓度)后,溶液pH的变化曲线.已知甲、乙分别是盐酸溶液和氢氧化钠溶液中的一种.请分析曲线回答问题:21教育网
(1)甲是 溶液;
(2)当加入乙溶液的体积为 mL时,甲、乙溶液恰好完全反应;
(3)当溶液的pH=1.4时,溶液中存在的微观粒子有 (指示剂除外);
(4)为理解稀盐酸和氢氧化钠两者之间发生反应的微观实质,绘制了如图.请你在右边的圆圈中填入适当的化学用语:
三、实验探究题
13、归纳是学习的重要方法,小芳在复习盐酸的性质时,归纳出盐酸的五条化学性质(如图1所示,连线表示相互反应);小明为表示反应实质绘制图2、图3.请根据下列图示和要求回答问题:【来源:21·世纪·教育·网】
(1)图1中为了验证性质①,小红将紫色石蕊溶液滴加到盐酸溶液中,溶液变 色;图1中A所表示的物质类别是 .21·世纪*教育网
(2)图2描述了氢氧化钠溶液与盐酸反应的微观实质,图2中A、B、C处应填入的化学式或离子符号依次为 .2-1-c-n-j-y
(3)图3是镁和盐酸反应过程的微观示意图,从微观角度看,该反应有效相互作用的微粒是 (写微粒符号,下同),产生的新微粒是 .
【中考大练兵】
14、某环保监测站取刚降下的雨水,每隔一段时间测定其pH,数据如下
测定时间∕分钟
0
1
2
4
5
pH
4.8
4.6
4.5
4.5
4.5
下列有关说法不正确的是( )
A.雨水酸性逐渐减弱
B.雨水的酸性一段时间后趋于稳定
C.酸雨会腐蚀机械设备和建筑物
D.硫和氮的氧化物是形成酸雨的主要因素
15、下列图象能正确反映对应实验操作中量的关系是( )
A.一定量稀硫酸加水稀释
B.一定量氯化铜和盐酸的混合溶液中逐渐加入稀硫酸
C.等质量的镁粉和铁粉中分别缓慢加入稀硫酸
D.等质量的高锰酸钾和氯酸钾加热制氧气
16、图1中甲、乙、丙、丁表示相邻两物质相互混合过程中溶液酸碱度的变化,其中可能得图2所示变化关系的是( )www.21-cn-jy.com
A.甲?? B.乙?? C.丙?? D.丁
17、向一定量4%的氢氧化钠溶液中逐滴加入稀盐酸,有关分析错误的是( )
A B C D
18、向盛有10mL稀盐酸(其中滴有少量紫色石蕊试剂)的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如表.请分析并回答下列问题:
加入NaOH溶液的体积/mL
0
2
4
6
8
10
12
14
烧杯中溶液的pH
1.1
1.2
1.4
1.6
2.0
7.0
11.0
12.2
(1)当加入氢氧化钠溶液的体积为 mL时,稀盐酸和氢氧化钠溶液恰好完全反应;
(2)当加入氢氧化钠溶液的体积为13mL时,溶液显 色.
19、中和反应在生活生产中有着广泛的应用,某实验小组的同学选用氢氧化钙溶液和稀盐酸进行酸碱中和反应的实验.【出处:21教育名师】
(1)写出该中和反应的化学方程式 .
(2)小组认为氢氧化钙溶液与稀盐酸反应时没有明显现象,可依据中和反应是 反应(选填“放热”或“吸热”)来验证是否发生了化学反应,该验证实验中用到的仪器有烧杯、玻璃棒、胶头滴管和 等.小组认为也可借助于下列溶液来验证反应是否真的发生,你觉得可行的是 .【版权所有:21教育】
A.无色酚酞试液?????????? B.氯化钠溶液????????? C.硫酸铜溶液
(3)小华同学向盛有氢氧化钙溶液的烧杯中滴加稀盐酸一会儿后,竟发现忘记了滴加指示剂.此时他立即停止了滴加,小组决定对烧杯内溶液中溶质的成分进行探究.
【提出问题】根据中和反应的原理,一定含有的溶质是 ,还可能含什么溶质呢?
【猜想假设】猜想甲:含有Ca(OH)2;???????????????? 猜想乙:含有HCl;
猜想丙:含有HCl与Ca(OH)2的混合物.
【实验探究】
①小夏认为不需要实验就能否定丙的猜想,理由是 .
②小腾向反应后的溶液中滴加几滴无色酚酞试液并振荡,观察到酚酞试液不变色.于是他排除了猜想甲,你认为他排除的原因是 .21*cnjy*com
③小飞只用一种溶液完成了对猜想乙的验证,请你帮他完成实验表格:
实验操作
预测现象
结论
取少量反应后的溶液于烧杯中,并向其中滴加足量的 溶液.
且溶液中出现沉淀
猜想乙正确
【反思拓展】
中和反应的微观实质就是酸中的氢离子和碱中的氢氧根离子结合生成了水,即:氢离子+氢氧根离子═水,将该表达式用化学符号表示为 .
参考答案及解析
1、A
【解答】A、pH=9.5,大于7,显弱碱性.
B、pH=7,显中性.
A、纯碱(是盐不是碱)和稀盐酸反应,反应物不是酸和碱,且生成物也不仅仅是盐和水,还生成了二氧化碳.错误. ???????????????????????????????????????? 21cnjy.com
B、生成盐和水的反应未必是中和反应,因为反应物可以是非金属氧化物和碱反应(如CO2+2NaOH=Na2CO3+H2O),也可以是金属氧化物与酸反应(如CuO+2HCl=CuCl2+H2O.错误.????????????????????? www-2-1-cnjy-com
C、氨水是碱,可以用来中和含有硫酸的废水(这个方案不是最佳的,因为成本以及运输等都不合适,氨水是液体,且现在使用氨水的情况很少,还是使用熟石灰或者生石灰的较多).正确.??????? 【来源:21cnj*y.co*m】
D、中和反应的发生不一定需要借助酸碱指示剂来进行判断,如氢氧化铜、氢氧化铁和氢氧化铝等难溶性且有颜色的碱和酸反应就不需要借助指示剂来判断反应的进行与否,而是看难溶性碱是否溶解于酸.错误.???????????
4、A
【解答】①氢氧化钠与硫酸的反应是酸和碱的反应,属于中和反应;
②用硫酸除铁锈,铁锈的主要成分为氧化铁,硫酸与氧化铁反应,不属于中和反应;
③用熟石灰改良酸性土壤,是酸和碱的反应,属于中和反应;
④碳酸氢钠治疗胃酸过多,碳酸氢钠是盐不是碱,不属于中和反应.
5、A
【解答】A、为酸性的溶液能使石蕊变红,所以酸溶液一定能使石蕊变红,故正确;
B、生成盐和水的反应不一定是中和反应,例如氧化铜和盐酸反应能生成盐氯化铜和水,不属于中和反应.故错误;21教育名师原创作品
C、与盐酸反应放出气体的物质不一定是金属,例如碳酸盐与稀盐酸反应能生成二氧化碳.故错误;
D、水(H2O)和过氧化氢(H2O2)的元素组成相同,但分子结构不同,一个过氧化氢分子比一个水分子多一个氧原子,所以化学性质不同,故错误.
6、C
【解答】酚酞遇碱变红遇酸不变色,故在反应过程中溶液会先有红色,至恰好反应到过量时溶液会变成无色,PH会由大于7到等于7再到小于7.
7、C
(2)盐酸能与金属氧化物反应生成盐和水,常用于金属去锈,故选F;
(3)一氧化碳是有毒的物质,故选C;
(4)苏打是碳酸钠的俗称,是德榜发明的联合制碱法中的“碱”,故选B;
11、(1)①;???????????????????????????????????????????????????
(2)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
【解答】(1)槟榔芋皮上含有一种碱性的物质﹣﹣皂角素,沾上它会使皮肤奇痒难忍;因为皂角素显碱性,所以应该选用显酸性的物质来与它反应,①②③④这三种物质中只有①显酸性,而②显中性,③④显碱性.???????????
(2)碳酸钠溶液与氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,可用于制取氢氧化钠,反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.????????????????????????????????????????
12、(1)NaOH;
(2)9;
(3)H+、Cl﹣、Na+;
(4)H2O,Na+,Cl﹣.
【解答】(1)开始时溶液的pH大于7,故甲是氢氧化钠溶液,故填:氢氧化钠;
(2)据图可知,当加入的盐酸的量为9mL时,溶液的pH等于7,此时二者恰好完全反应,故填:9;
(3)氢氧化钠能和盐酸反应生成氯化钠和水,pH=1.4时,盐酸过量,故溶液中的溶质是氯化氢和氯化钠,溶液中存在的微观粒子有:H+、Cl﹣、Na+;21*cnjy*com
(4)酸碱反应的实质是酸中的氢离子和碱中的氢氧根离子结合生成水分子,而金属钠离子和酸根离子氯离子仍然是以自由移动的离子存在,故填:H2O,Na+,Cl﹣.
13、(1)红,碱;
(2)OH﹣、H+、H2O;
(3)Mg、H+,H2、Mg2+
【解答】(1)将紫色石蕊试液滴加到盐酸溶液中,溶液变红色;图1中A所表示的物质类别是碱;
(2)图2中A、B、C处应填入的化学式或离子符号依次为OH﹣、H+、H2O;
(3)图3是镁和盐酸反应过程的微观示意图,从微观角度看,该反应有效相互作用的微粒是Mg、H+,产生的新微粒是H2、Mg2+.
B.酸碱中和反应会放出热量,故随着稀盐酸的加入,溶液的温度升高,当恰好完全中和时,溶液温度最高,继续滴加稀盐酸,溶液的温度就会降低,所以图象正确;
C.没有滴加稀盐酸时,溶液中氯化钠的质量分数为零,随着加入稀盐酸生成的氯化钠越来越多,溶液中氯化钠的质量分数越来越大,当二者完全中和时,溶液中氯化钠的质量分数达到最大值且不再增加,再滴加稀盐酸,溶液的质量增大,氯化钠的质量不变,溶液中氯化钠的质量分数减小,故图象正确;
D.当加入的稀盐酸与氢氧化钠发生反应时,HCl的物质的量为零,当二者恰好完全反应时,继续滴加稀盐酸,HCl的物质的量增加,且随着稀盐酸加入的量的增多,而不断增大,故图象错误.
18、10; 蓝.
【解答】解:(1)pH=7时,氢氧化钠和稀盐酸恰好完全反应.故填:10;
(2)当加入氢氧化钠溶液13毫升时,溶液显碱性.能使石蕊试液变蓝.故填;蓝.
19、(1)Ca(OH)2+2HCl═CaCl2+2H2O;
(2)放热;温度计;AC;
(3)【提出问题】氯化钙;
【实验探究】
①氢氧化钙和盐酸反应生成氯化钙和水,二者不共存;
②氢氧化钙溶液呈碱性,使酚酞试液变红,现不变红,故溶质不可能含氢氧化钙;
③
实验操作
预测现象
结论
取少量反应后的溶液于烧杯中,并向其中滴加足量的碳酸钠溶液.
先有气泡产生且溶液中出现沉淀
猜想乙正确
【反思拓展】H++OH﹣=H2O.
【解答】(1)氢氧化钙和盐酸发生中和反应生成氯化钙和水,故答案为:Ca(OH)2+2HCl③氯化钙溶液可以和碳酸钠溶液反应生成沉淀,和稀盐酸反应生成二氧化碳气体,所以可以将碳酸钠溶液滴入反应后的溶液中,若观察到有气泡冒出,当没有气泡冒出时,则说明溶液中含有氯化氢和氯化钙;
【反思拓展】中和反应的微观实质就是酸中的氢离子和碱中的氢氧根离子结合生成了水,即:氢离子+氢氧根离子=水,将该表达式用化学符号表示为:
H++OH﹣=H2O.
同课章节目录
