物质的量浓度2
图片预览







文档简介
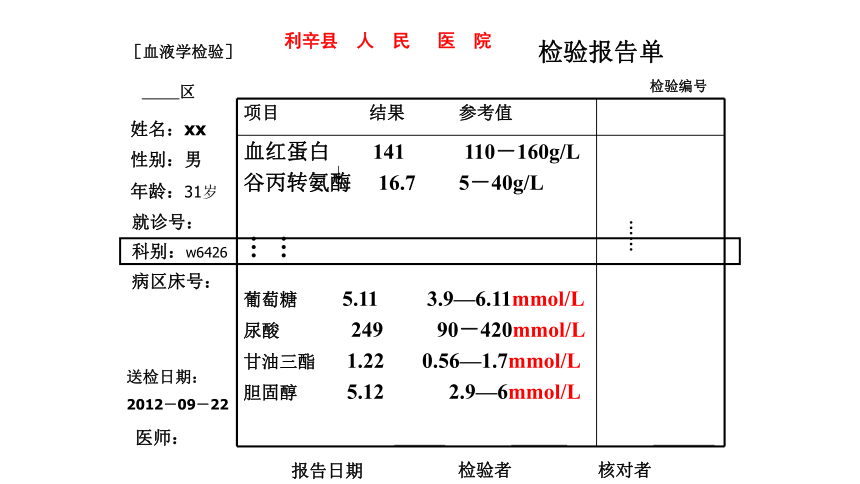
课件20张PPT。思考回忆? 我们知道溶液有稀溶液和浓溶液之分那么如何定量的表示溶液的浓稀程度呢?质量分数讨论:在使用溶质的质量分数溶液的时候,有什么不方便的地方? [来源:学*科*网]1、要准确称量溶液的质量;2、物质之间反应的直接效果是微粒之间的 反应, 物质的量的关系要比质量的关系简单的多。利辛县 人 民 医 院
检验报告单检验编号[血液学检验] 区姓名:xx性别:男
年龄:31岁 就诊号:科别:w6426病区床号:送检日期:
2012-09-22医师:报告日期 检验者核对者…………物质的量浓度学习目标
1.知道什么是物质的量浓度
2.会计算溶液中各物质的物质的量浓度
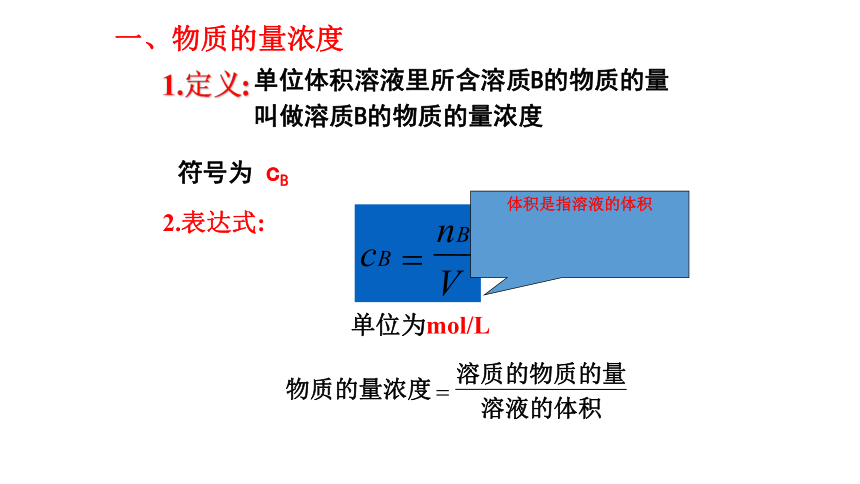
3.会根据物质的量浓度,计算一定体积中溶质的物质的量1.定义:单位体积溶液里所含溶质B的物质的量
叫做溶质B的物质的量浓度
符号为 cB单位为mol/L 2.表达式:一、物质的量浓度体积是指溶液的体积想一想2 mol/L NaCl溶液所表示的含义是什么?每升溶液中含有2mol NaCl或
每升溶液中含有117g NaCl例题1、将4gNaOH溶于水配成2L溶液,其物质的量浓度为多少?n(NaOH)= m(NaOH)M(NaOH)=4g40g/mol=0.1molc(NaOH)=n(NaOH)V(aq)=2L0.1mol=0.05mol/L解:答:40克氢氧化钠溶于水配成2L溶液,物质的量浓度为0.05mol/L学以致用:这些题目你会做了吗?1.用58.5gNaCl配成2L溶液,其物质的量浓度________mol/L2.标准状况下,22.4LHCl配成0.5L盐酸,其物质的量浓度________mol/L 3. 25gCuSO4.5H2O溶与水配成500ml溶液,其物质的量浓度________mol/L 0.520.2注意:带结晶水的物质溶于水溶质是去掉结晶水的物质公式变形应用例2. 物质的量浓度为2mol/L的硫酸溶液250mL,含硫酸的物质的量为_________mol含硫酸的质量为_________ g
0.5解:注意:知道公式中任意两个的量可求出剩余一个的量496. 已知某硫酸钠溶液的物质的量浓度为2mol/L,该溶液中含硫酸钠的物质的量为3moL,则该溶液的体积为_____L1.5学以致用:这些题目你会做了吗?解:问题与讨论讨论1:将342克C12H22O11(蔗糖)溶解在1L水中,所得
溶液中溶质的物质的量浓度是否为1mol/L?讨论2:从1L1mol/L的C12H22O11溶液中取出100ml,取出
的C12H22O11溶液的物质的量浓度是多少?结论:同一溶液,无论取多少体积,溶质的物质的
量浓度相同,但溶质的物质的量不同。结论:溶液的体积不等于溶剂的体积,且不同物质(尤其是状态不同的物质)的体积是没有加和性的。3.注意:(1)在一定物质的量浓度溶液中取出任意体积的溶液,其物质的量浓度不变,但所含溶质的物质的量或质量因体积的不同而不同(2)溶质可以是单质、化合物,也可以是离子或其他特定组合。氨气溶于水一般认为溶质为氨气分子。(3)单一溶质的溶液中,离子的浓度之比等于其化学式中离子个数之比。填空1、1 mol/L MgCl2 溶液,Mg2+ 的物质的量浓度为 mol/L, Cl- 的物质的量浓度为 mol/L 。1 2、0.5 mol/L H2SO4 溶液,H+ 的物质的量浓度为 mol/L, SO42- 的物质的量浓度为 mol/L 。3、0.1 mol/L Al2(SO4)3 溶液,Al3+ 的物质的量浓度为
mol/L,SO42- 的物质的量浓度为 mol/L 。2 1 0. 5 0. 2 0. 3 下列各溶液中,Na+ 浓度最大的是 ( )
(A)4L 0. 5 mol/L NaCl 溶液
(B)1L 0. 3 mol/L Na2SO4 溶液
(C) 0. 8L 0. 4 mol/L NaOH 溶液
(D) 2L 0. 15 mol/L Na3PO4 溶液
C (Na+) = 0. 5 mol/L×1 = 0. 5 mol/L C (Na+) = 0. 3 mol/L×2 = 0. 6 mol/L C (Na+) = 0. 4 mol/L×1 = 0. 4 mol/L C (Na+) = 0. 15 mol/L×3 = 0. 45 mol/LB比较质量分数与物质的量浓度溶质的质量分数定义表达式实例用溶质质量占溶液质量的比表示的浓度以单位体积里所含溶质B的物质的量来表示溶液组成的物理量,叫做溶质B的物质的量浓度某溶液浓度10%指…某溶液中溶质的物质的量浓度10mol/L…物质的量浓度知识网络:粒子个数N 物质的量n 质量m
气体体积V 物质的量浓度CB ×Vm ÷Vm ×NA ÷NA ×M ÷M ×V液 ÷V液 当堂练习:1.下列溶液中,与100ml0.5mol/LNaCl溶液所含的Cl--物质的量浓度相同的是( )
A.100ml0.5mol/LMgCl2溶液
B.200ml0.25mol/LCaCl2溶液
C.50ml1.0mol/LNaCl溶液
D.25ml0.5mol/LHCl溶液
2.NA为阿伏加德罗常数,下列对0.3mol/L硫酸钾溶液的说法中,正确的是( )
A.1L溶液中含有0.3NA个K+
B.1L溶液中含有0.9NA个离子
C.2L溶液中K+浓度是1.2mol/L
D.2L溶液中含有0.6NA个离子BDB3.关于0.2 mol/L的NaOH溶液,下列说法不正确的是 ( )
A.100 mL该溶液中含0.8 g NaOH
B.200 mL该溶液与100 mL 0.2 mol/L的硫酸溶液反应形成中性溶液
C.100 mL该溶液中约含0.02 mol×6.02×23mol-1个Na+
D.配制含1 L水的该溶液,需NaOH的质量为8 gD解 根据溶液稀释定律有:c(浓溶液)·V(浓溶液)=c(稀溶液)·V(稀溶液)即有:0.1L×18mol·L-1=2L×c[H2SO4(aq)]解得: c[H2SO4(aq)] = 0.9mol·L-1答:稀释后所得稀硫酸的物质的量浓度为0.9mol·L-1例、向100ml18mol/L的硫酸加水稀释至2L,所得稀硫酸的物质的量浓度为多少?
检验报告单检验编号[血液学检验] 区姓名:xx性别:男
年龄:31岁 就诊号:科别:w6426病区床号:送检日期:
2012-09-22医师:报告日期 检验者核对者…………物质的量浓度学习目标
1.知道什么是物质的量浓度
2.会计算溶液中各物质的物质的量浓度
3.会根据物质的量浓度,计算一定体积中溶质的物质的量1.定义:单位体积溶液里所含溶质B的物质的量
叫做溶质B的物质的量浓度
符号为 cB单位为mol/L 2.表达式:一、物质的量浓度体积是指溶液的体积想一想2 mol/L NaCl溶液所表示的含义是什么?每升溶液中含有2mol NaCl或
每升溶液中含有117g NaCl例题1、将4gNaOH溶于水配成2L溶液,其物质的量浓度为多少?n(NaOH)= m(NaOH)M(NaOH)=4g40g/mol=0.1molc(NaOH)=n(NaOH)V(aq)=2L0.1mol=0.05mol/L解:答:40克氢氧化钠溶于水配成2L溶液,物质的量浓度为0.05mol/L学以致用:这些题目你会做了吗?1.用58.5gNaCl配成2L溶液,其物质的量浓度________mol/L2.标准状况下,22.4LHCl配成0.5L盐酸,其物质的量浓度________mol/L 3. 25gCuSO4.5H2O溶与水配成500ml溶液,其物质的量浓度________mol/L 0.520.2注意:带结晶水的物质溶于水溶质是去掉结晶水的物质公式变形应用例2. 物质的量浓度为2mol/L的硫酸溶液250mL,含硫酸的物质的量为_________mol含硫酸的质量为_________ g
0.5解:注意:知道公式中任意两个的量可求出剩余一个的量496. 已知某硫酸钠溶液的物质的量浓度为2mol/L,该溶液中含硫酸钠的物质的量为3moL,则该溶液的体积为_____L1.5学以致用:这些题目你会做了吗?解:问题与讨论讨论1:将342克C12H22O11(蔗糖)溶解在1L水中,所得
溶液中溶质的物质的量浓度是否为1mol/L?讨论2:从1L1mol/L的C12H22O11溶液中取出100ml,取出
的C12H22O11溶液的物质的量浓度是多少?结论:同一溶液,无论取多少体积,溶质的物质的
量浓度相同,但溶质的物质的量不同。结论:溶液的体积不等于溶剂的体积,且不同物质(尤其是状态不同的物质)的体积是没有加和性的。3.注意:(1)在一定物质的量浓度溶液中取出任意体积的溶液,其物质的量浓度不变,但所含溶质的物质的量或质量因体积的不同而不同(2)溶质可以是单质、化合物,也可以是离子或其他特定组合。氨气溶于水一般认为溶质为氨气分子。(3)单一溶质的溶液中,离子的浓度之比等于其化学式中离子个数之比。填空1、1 mol/L MgCl2 溶液,Mg2+ 的物质的量浓度为 mol/L, Cl- 的物质的量浓度为 mol/L 。1 2、0.5 mol/L H2SO4 溶液,H+ 的物质的量浓度为 mol/L, SO42- 的物质的量浓度为 mol/L 。3、0.1 mol/L Al2(SO4)3 溶液,Al3+ 的物质的量浓度为
mol/L,SO42- 的物质的量浓度为 mol/L 。2 1 0. 5 0. 2 0. 3 下列各溶液中,Na+ 浓度最大的是 ( )
(A)4L 0. 5 mol/L NaCl 溶液
(B)1L 0. 3 mol/L Na2SO4 溶液
(C) 0. 8L 0. 4 mol/L NaOH 溶液
(D) 2L 0. 15 mol/L Na3PO4 溶液
C (Na+) = 0. 5 mol/L×1 = 0. 5 mol/L C (Na+) = 0. 3 mol/L×2 = 0. 6 mol/L C (Na+) = 0. 4 mol/L×1 = 0. 4 mol/L C (Na+) = 0. 15 mol/L×3 = 0. 45 mol/LB比较质量分数与物质的量浓度溶质的质量分数定义表达式实例用溶质质量占溶液质量的比表示的浓度以单位体积里所含溶质B的物质的量来表示溶液组成的物理量,叫做溶质B的物质的量浓度某溶液浓度10%指…某溶液中溶质的物质的量浓度10mol/L…物质的量浓度知识网络:粒子个数N 物质的量n 质量m
气体体积V 物质的量浓度CB ×Vm ÷Vm ×NA ÷NA ×M ÷M ×V液 ÷V液 当堂练习:1.下列溶液中,与100ml0.5mol/LNaCl溶液所含的Cl--物质的量浓度相同的是( )
A.100ml0.5mol/LMgCl2溶液
B.200ml0.25mol/LCaCl2溶液
C.50ml1.0mol/LNaCl溶液
D.25ml0.5mol/LHCl溶液
2.NA为阿伏加德罗常数,下列对0.3mol/L硫酸钾溶液的说法中,正确的是( )
A.1L溶液中含有0.3NA个K+
B.1L溶液中含有0.9NA个离子
C.2L溶液中K+浓度是1.2mol/L
D.2L溶液中含有0.6NA个离子BDB3.关于0.2 mol/L的NaOH溶液,下列说法不正确的是 ( )
A.100 mL该溶液中含0.8 g NaOH
B.200 mL该溶液与100 mL 0.2 mol/L的硫酸溶液反应形成中性溶液
C.100 mL该溶液中约含0.02 mol×6.02×23mol-1个Na+
D.配制含1 L水的该溶液,需NaOH的质量为8 gD解 根据溶液稀释定律有:c(浓溶液)·V(浓溶液)=c(稀溶液)·V(稀溶液)即有:0.1L×18mol·L-1=2L×c[H2SO4(aq)]解得: c[H2SO4(aq)] = 0.9mol·L-1答:稀释后所得稀硫酸的物质的量浓度为0.9mol·L-1例、向100ml18mol/L的硫酸加水稀释至2L,所得稀硫酸的物质的量浓度为多少?
