江苏省盐城市2016-2017学年高二学业水平模拟(一)化学试题
文档属性
| 名称 | 江苏省盐城市2016-2017学年高二学业水平模拟(一)化学试题 |

|
|
| 格式 | zip | ||
| 文件大小 | 948.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-03-22 00:00:00 | ||
图片预览



文档简介
盐城市高二学业水平模拟测试
2017届高二学业水平测试模拟卷(一)
化学本试卷可能用到的相对原子质量:H—1 N—l4 O—16 S—32 Cl—35.5 Cu—64 I—127
一、
单项选择题:在每题的4个选项中,只有1个选项是符合要求的(本部分23题,每题3分,共69分)。
1.
《中国能源矿产地质调查报告》显示我国天然气水合物超千亿吨油当量。天然气主要成分为( )
A.
H2
B.
CO
C.
CH4
D.
C2H4
2.
我国首飞的长征七号运载火箭采用液氧和煤油作为推进剂。煤油属于( )
A.
纯净物
B.
混合物
C.
氧化物
D.
单质
3.
最近我国“人造太阳”研究获重大进展。核聚变中下列质子数小于中子数的原子是( )
A.
H
B.
H
C.
He
D.
H
4.
下列过程属于物理变化的是( )
A.
油脂酸败
B.
石油裂解
C.
钢铁生锈
D.
干冰升华
5.
下列物质中既含有离子键又含有共价键的是( )
A.
NH4Cl
B.
NaCI
C.
H2O
D.
Cl2
6.
里约奥运会游泳池误多加H2O2导致水体变绿,发生反应H2O2+Cl2===2HCl+O2。该反应属
于( )
A.
化合反应
B.
分解反应
C.
置换反应
D.
复分解反应
7.
在含有大量Fe3+、H+、SO的溶液中,还可能大量共存的离子是( )
A.
Ba2+
B.
OH-
C.
I-
D.
NH
8.
既可用排水法又可用向上排空气法收集的气体是( )
A.
NO
B.
O2
C.
NH3
D.
NO2
9.
下列过程中吸收热量的是( )
A.
焦炭制水煤气
B.
浓硫酸的稀释C.
酸碱中和反应
D.
镁条溶于盐酸
10.
下列有关物质用途的说法不正确的是( )
A.
聚氯乙烯可用于制食品袋
B.
液NH3可用作制冷剂
C.
SiO2可用于制造光导纤维
D.
漂白粉可用于杀菌消毒
11.
下列有关乙醇的说法正确的是( )
A.
能与H2O发生加成反应
B.
能使石蕊试液变红
C.
与CH3OCH3互为同分异构体
D.
是食醋的主要成分
12.
下列化学用语表示正确的是( )
A.
HF的电子式:H+[?F?,?
?]-
B.
S2-结构示意图:
C.
异丁烷的结构筒式:CH3CH2CH2CH3
D.
硝酸钙的电离方程式:Ca(NO3)2===Ca2++(NO3)
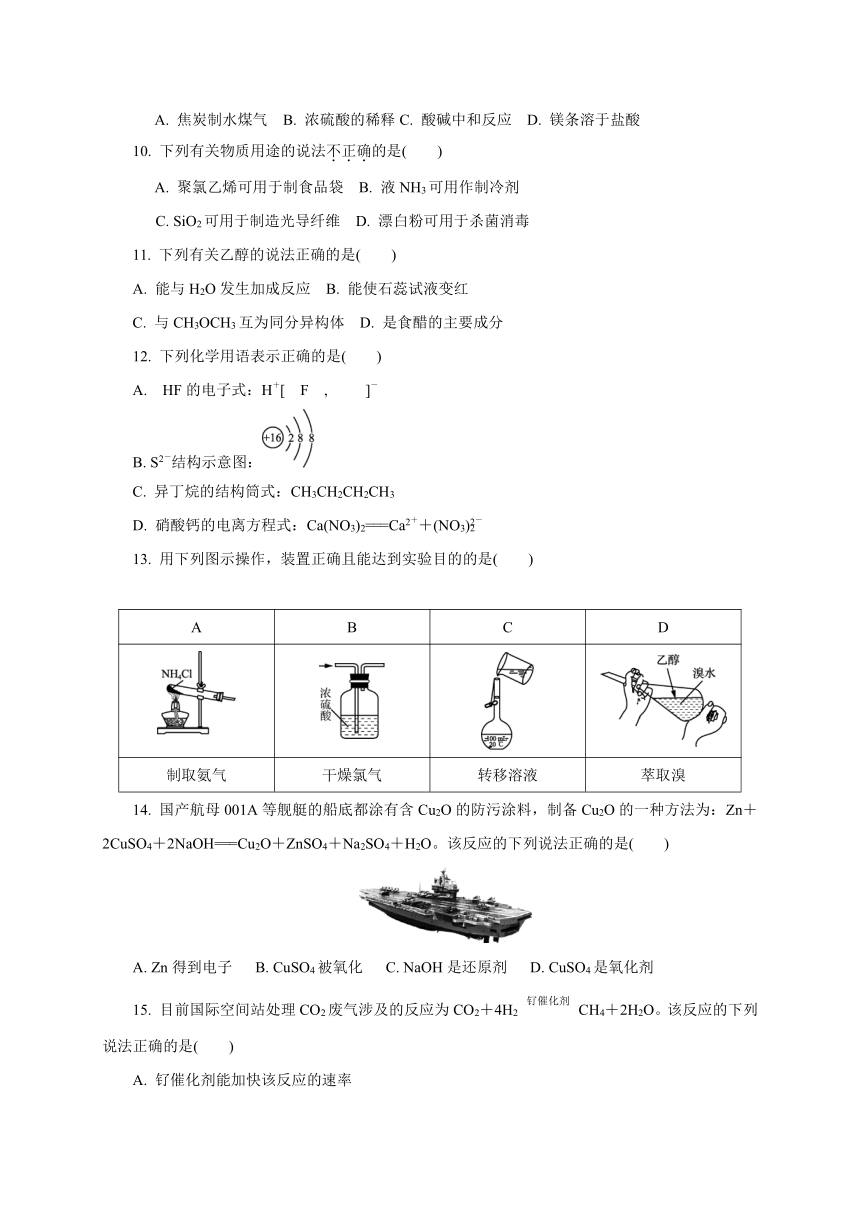
13.
用下列图示操作,装置正确且能达到实验目的的是( )
A
B
C
D
制取氨气
干燥氯气
转移溶液
萃取溴
14.
国产航母001A等舰艇的船底都涂有含Cu2O的防污涂料,制备Cu2O的一种方法为:Zn+2CuSO4+2NaOH===Cu2O+ZnSO4+Na2SO4+H2O。该反应的下列说法正确的是( )
A.
Zn得到电子
B.
CuSO4被氧化
C.
NaOH是还原剂
D.
CuSO4是氧化剂
15.
目前国际空间站处理CO2废气涉及的反应为CO2+4H2CH4+2H2O。该反应的下列说法正确的是( )
A.
钌催化剂能加快该反应的速率
B.
升高温度能减慢该反应的速率
C.
达到平衡时,CO2能100%转化为CH4
D.
达到平衡时,反应速率:v(正)=v(逆)=0
16.
下列化学方程式书写正确的是( )
A.
nCH2===CH2?CH2—CH2?
B.
CH2===CH2+Br2―→CH3CHBr2
C.
+HNO3
O2N+H2O
D.
CH3COOH+CH3CH2OHCH3COOCH3CH2+H2O
17.
下列反应的离子方程式书写正确的是( )
A.
锌与CH3COOH溶液反应:Zn+2H+===Zn2++H2↑
B.
氢氧化铝与稀硝酸反应:H++OH-===H2O
C.
CuCl2溶液与铁粉反应:3Cu2++2Fe===3Cu+2Fe3+
D.
MgCl2溶液与氨水反应:Mg2++2NH3·H2O===Mg(OH)2↓+2NH
18.
美国NASA曾开发一种铁—空气二次电池。该电池放电时,其原理如下图所示,电池反应为:2Fe+O2+2H2O===2Fe(OH)2。
有关该电池放电时的说法正确的是( )
a极质量不变
B.
b极为电池负极
C.
电子由a极经负载流向b极
D.
由电能转变为化学能
19.
用蘸有浓氨水的棉棒检漏输氯管道的原理为:
3Cl2+8NH3??N2+6NH4Cl。该反应的下列说法正确的是( )
A.
35.5
g氯气所含的分子数为6.02×1023
B.
常温常压下,22.4
L氨气所含原子总数为4×6.02×1023
C.
反应每生成1
mol
N2转移电子数约为6×6.02×
1023
D.
1
mol·L-1
NH4Cl溶液中,含有Cl-数约为6.02×1023
20.
下列有关二氧化硫的说法正确的是( )
A.
密度比空气小
B.
是无色无味的气体
C.
SO2能使溴水褪色,说明SO2具有漂白性
D.
某生产硫酸厂区紫罗兰花变成白色,说明其周围空气中可能含较高浓度SO2
21.
下列实验方法能达到实验目的的是( )
A.
用湿润的红色石蕊试纸检验氨气
B.
用长颈漏斗分离碘的四氯化碳溶液和水溶液
C.
用焰色反应鉴别NaCl和Na2SO4两种无色晶体
D.
用KSCN溶液鉴别FeCl3溶液和Fe(NO3)3溶液
22.
X、Y、Z、W是原子序数依次增大的短周期主族元素。Y与W同主族,Z所在的族序数等于周期数,X、Y最外层电子数之和为7;X、Z原子的电子数总和与Y、W原子的电子数总和之比为7:12。下列说法正确的是( )
A.
原子半径:r(X)B.
Y的简单气态氢化物的热稳定性比W的弱
C.
由X、Y组成的物质与由Y、W组成的物质化合,可能发生氧化还原反应
D.
常温下,Z的单质一定易溶于由X、Y、W三种元素组成的化合物的溶液
23.
将一定量的由Cu和Cu2O组成的混合粉末加入到125
mL
2.6
mol·L-1的硝酸中,固体恰好完全溶解,得蓝色溶液X并收集到V
mL(标准状况)的纯净无色气体Y。下列结论正确的是( )
A.
X中有两种溶质
B.
Y通入纯水中得到酸性溶液
C.
原混合粉末的总质量小于7.8
g
D.
当V=1
680时,原混合粉末中Cu和Cu2O的物质的量之比为8∶1
二、
非选择题(本部分3题,共31分)
24.
(15分)本题为选做题。包括A、B两题。选学《化学与生活》模块的考生答A题,选学《有机化学基础》模块的考生答B题,每位考生只可选做l题。若两题都作答,则以A题计分。
A.
《化学与生活》
(1)
(3分)在“天宫二号”上蚕宝宝的“太空屋”形似胶囊(如图),两端的半球体由航天铝合金打造,中间部分采用透明有机玻璃,蚕宝宝由聚氨酯海绵包裹着。
①蚕丝的主要成份为________(填字母)。
a.
多糖 b.
蛋白质 c.
油脂
②有机玻璃和聚氨酯海绵均属于________(填字母)。
a.
金属材料
b.
无机非金属材料
c.
有机高分子材料
③钛铝合金是常见的航天铝合金,下列不属于钛铝合金性质的是________(填字母)。
a.
高密度
b.
高强度
c.
高韧性
品名:果肉果冻
配料表:水、白砂糖、桔子
果肉(≥15%)、魔芋粉。
食品添加剂:卡拉胶、黄原
胶、柠檬酸、氯化钾、桔子
香精、甜密素、柠檬黄、诱
惑红、山梨酸钾(2)
(5分)某品牌果冻标签如右图所示。回答下列问题:
①食品添加剂中,属于无机盐的是________(填化学式)。
②属于着色剂的是诱惑红和________;属于防腐剂的是________。
③配料表中白砂糖的成分是蔗糖,请写出蔗糖在人体内水解的化学方程式____________________________。
(3)
(7分)化学与科学技术、生产生活及环境保护等密切相关。
①2016年12月我省启动了保卫碧水蓝天的“263”行动,减少煤炭消费总量,减少雾霾天气的发生。形成硫酸型酸雨的主要气体是________;严格整治畜禽养殖场污染,主要是为减少________和P等元素及化学需氧量对水体的污染。
②目前正在推广用尿素水解液来消除柴油汽车尾气中的氮氧化物。写出尿素水解液中的NH3与NO在催化剂作用下,反应生成无污染物质的化学方程式_____________________________________。
③阿司匹林作为一种药物,主要具有________作用;Mg2Si3O8·nH2O(三硅酸镁)具有治疗胃酸过多的作用,写出其与胃酸反应生成SiO2·H2O等物质的化学方程式__________________________________。
B.
《有机化学基础》
(1)
(3分)有机物的组成、结构与性质密切相关。
①室内装修产生的主要污染气体有:苯、甲醛及DMF(富马酸二甲酯)等,其中属于烃的是________(填字母)。
a.
苯 b.
甲醛 c.
DMF
②下列分子中所有原子可以处于同一平面中的是________(填字母)。
a.
乙烷
b.
溴乙烷
c.
苯乙烯
③提纯含有少量苯酚的甲苯,适宜的试剂是________(填字母)。
a.
溴水
b.
KMnO4酸性溶液
c.
NaOH溶液
(2)
(5分)紫薯中的鞣花酸(结构如右图)具有防癌和抗癌作用。
①鞣花酸分子中含氧官能团的名称为________。
②鞣花酸的分子式为________。
③1
mol鞣花酸最多可与________mol
NaOH发生反应。
(3)
(7分)以A为原料可制备C(丹皮酚)和D(树脂),其合成路线如下:
①A在空气中会缓慢变成粉红色,其原因是________。
②A→B的反应类型为____________;A生成D的反应中,试剂X(烃的含氧衍生物)为________(写结构简式)。
③只含有两个取代基的芳香化合物E是C的同分异构体,E既能与FeCl3溶液发生显色反应又能发生银镜反应和水解反应,则E可能的结构简式有________种(不考虑立体结构),其中核磁共振氢谱有6组峰,且面积比为1∶2∶2∶2∶2∶1的是____________________(写结构简式)。
25.
(6分)有关物质的转化关系如下图所示(部分物质已略去)。A、C都是常见的金属氧化物,B是常见的强酸,D是最常见的无色液体,E、F、H都是常见的气体,且E、F都可用于漂白,H是空气中主要成分之一,I、J都是由三种相同元素(短周期元素)组成的盐。
请回答下列问题:
(1)
D的化学式为____________。
(2)
G的电子式为____________。
(3)
写出反应①的化学方程式________________________。
(4)
写出反应②的离子方程式________________________。
26.
(10分)KIO3是一种无色易溶于水的晶体,医药上可作防治地方甲状腺肿的药剂,目前碘酸钾被广泛应用于食盐加碘。一种由含碘废水制取碘酸钾的工艺如下:
(1)
检验“含碘废水”中含有的单质I2,常用的试剂是________。
(2)
进行“过滤1”时,需同时对CuI沉淀进行洗涤。在洗涤过滤滤液中可通过滴加________盐溶液来检验其是否已洗涤干净。
(3)
“滤渣2”的成分为____________(填化学式)。
(4)
“制KI”时,发生反应的化学方程式为____________。
(5)
江苏食用加碘盐新标准是每千克食盐中碘元素含量为25毫克(波动范围为18~33
mg/kg)。测定食盐试样中碘元素含量的步骤如下:称取4.000
g市售食盐加入锥形瓶中,依次加入适量的水、稍过量KI及稀硫酸;充分反应后,再加入12.00
mL
6.000×10-4
mol·L-1
Na2S2O3溶液,与生成的碘恰好完全反应。有关反应原理为:
KIO3+5KI+3H2SO4===3K2SO4+3I2+3H2O; I2+2S2O===2I-+S4O。
①计算该食盐试样中碘元素的含量(单位mg/kg,写出计算过程)。
②该食盐试样是否符合江苏食用加碘盐新标准并说明判断依据
2017届高二学业水平测试模拟卷(一)(盐城市)
化学参考答案
一、
单项选择题:共69分。
1.
C 2.
B 3.
B 4.
D 5.
A 6.
C 7.
D 8.
B 9.
A 10.
A 11.
C 12.
B 13.
B 14.
D 15.
A 16.
A 17.
D 18.
C 19.
C 20.
D 21.
A 22.
C 23.
D
二、
非选择题:共31分。
24.
(15分)
A.
化学与生活
(1)
①b(1分) ②c(1分) ③a(1分)
(2)
①氯化钾(KCl)(1分) ②柠蒙黄(1分) 山梨酸钾(1分)
③C12H22O11+H2OC6H12O6+C6H12O6(2分)
蔗糖
葡萄糖
果糖
(3)
①SO2(1分) N(氮)(1分)
②6NO+4NH35N2+6H2O(2分)
③解热镇痛(1分)
Mg2Si3O8·nH2O+4HCl===2MgCl2+3SiO2·H2O+(n-1)H2O(2分)
B.
有机化学基础
(1)
①a(1分) ②c(1分) ③c(1分)
(2)
①酯基和(酚)羟基(共2分) ②C14H6O8(1分) ③8(2分)
(3)
①A易被空气中的氧气氧化(1分)
②取代反应(1分) HCHO(1分)
③6(2分) HCOOCH2CH2OH(2分)
25.
(6分)
(1)
H2O(1分)
(2)
Na+[?O?,??H]-(1分)
(3)
MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O(2分)
(4)
Cl2+SO+H2O===SO+2Cl-+2H+(2分)
26.
(10分)
(1)
淀粉溶液(1分)
(2)
BaCl2[或Ba(NO3)2](1分)
(3)
Cu(或Cu和Fe)(1分)
(4)
K2CO3+FeI2===FeCO3↓+2KI(1分)
(5)
①KIO3~6Na2S2O3
n(I)=n(KIO3)=n(Na2S2O3)=×6.000×10-4
mol·L-1×12.00
mL×10-3
L·mL-1
=1.200×10-6
mol(2分)
m(I)=1.200×10-6
mol×127
g·mol-1×103
mg·g-1=0.152
4
mg(2分)
碘含量为:=38.10
mg/kg(1分)
②不符合新标准。因为38.10
mg/kg不在18~33
mg/kg范围内(1分)
2017届高二学业水平测试模拟卷(一)
化学本试卷可能用到的相对原子质量:H—1 N—l4 O—16 S—32 Cl—35.5 Cu—64 I—127
一、
单项选择题:在每题的4个选项中,只有1个选项是符合要求的(本部分23题,每题3分,共69分)。
1.
《中国能源矿产地质调查报告》显示我国天然气水合物超千亿吨油当量。天然气主要成分为( )
A.
H2
B.
CO
C.
CH4
D.
C2H4
2.
我国首飞的长征七号运载火箭采用液氧和煤油作为推进剂。煤油属于( )
A.
纯净物
B.
混合物
C.
氧化物
D.
单质
3.
最近我国“人造太阳”研究获重大进展。核聚变中下列质子数小于中子数的原子是( )
A.
H
B.
H
C.
He
D.
H
4.
下列过程属于物理变化的是( )
A.
油脂酸败
B.
石油裂解
C.
钢铁生锈
D.
干冰升华
5.
下列物质中既含有离子键又含有共价键的是( )
A.
NH4Cl
B.
NaCI
C.
H2O
D.
Cl2
6.
里约奥运会游泳池误多加H2O2导致水体变绿,发生反应H2O2+Cl2===2HCl+O2。该反应属
于( )
A.
化合反应
B.
分解反应
C.
置换反应
D.
复分解反应
7.
在含有大量Fe3+、H+、SO的溶液中,还可能大量共存的离子是( )
A.
Ba2+
B.
OH-
C.
I-
D.
NH
8.
既可用排水法又可用向上排空气法收集的气体是( )
A.
NO
B.
O2
C.
NH3
D.
NO2
9.
下列过程中吸收热量的是( )
A.
焦炭制水煤气
B.
浓硫酸的稀释C.
酸碱中和反应
D.
镁条溶于盐酸
10.
下列有关物质用途的说法不正确的是( )
A.
聚氯乙烯可用于制食品袋
B.
液NH3可用作制冷剂
C.
SiO2可用于制造光导纤维
D.
漂白粉可用于杀菌消毒
11.
下列有关乙醇的说法正确的是( )
A.
能与H2O发生加成反应
B.
能使石蕊试液变红
C.
与CH3OCH3互为同分异构体
D.
是食醋的主要成分
12.
下列化学用语表示正确的是( )
A.
HF的电子式:H+[?F?,?
?]-
B.
S2-结构示意图:
C.
异丁烷的结构筒式:CH3CH2CH2CH3
D.
硝酸钙的电离方程式:Ca(NO3)2===Ca2++(NO3)
13.
用下列图示操作,装置正确且能达到实验目的的是( )
A
B
C
D
制取氨气
干燥氯气
转移溶液
萃取溴
14.
国产航母001A等舰艇的船底都涂有含Cu2O的防污涂料,制备Cu2O的一种方法为:Zn+2CuSO4+2NaOH===Cu2O+ZnSO4+Na2SO4+H2O。该反应的下列说法正确的是( )
A.
Zn得到电子
B.
CuSO4被氧化
C.
NaOH是还原剂
D.
CuSO4是氧化剂
15.
目前国际空间站处理CO2废气涉及的反应为CO2+4H2CH4+2H2O。该反应的下列说法正确的是( )
A.
钌催化剂能加快该反应的速率
B.
升高温度能减慢该反应的速率
C.
达到平衡时,CO2能100%转化为CH4
D.
达到平衡时,反应速率:v(正)=v(逆)=0
16.
下列化学方程式书写正确的是( )
A.
nCH2===CH2?CH2—CH2?
B.
CH2===CH2+Br2―→CH3CHBr2
C.
+HNO3
O2N+H2O
D.
CH3COOH+CH3CH2OHCH3COOCH3CH2+H2O
17.
下列反应的离子方程式书写正确的是( )
A.
锌与CH3COOH溶液反应:Zn+2H+===Zn2++H2↑
B.
氢氧化铝与稀硝酸反应:H++OH-===H2O
C.
CuCl2溶液与铁粉反应:3Cu2++2Fe===3Cu+2Fe3+
D.
MgCl2溶液与氨水反应:Mg2++2NH3·H2O===Mg(OH)2↓+2NH
18.
美国NASA曾开发一种铁—空气二次电池。该电池放电时,其原理如下图所示,电池反应为:2Fe+O2+2H2O===2Fe(OH)2。
有关该电池放电时的说法正确的是( )
a极质量不变
B.
b极为电池负极
C.
电子由a极经负载流向b极
D.
由电能转变为化学能
19.
用蘸有浓氨水的棉棒检漏输氯管道的原理为:
3Cl2+8NH3??N2+6NH4Cl。该反应的下列说法正确的是( )
A.
35.5
g氯气所含的分子数为6.02×1023
B.
常温常压下,22.4
L氨气所含原子总数为4×6.02×1023
C.
反应每生成1
mol
N2转移电子数约为6×6.02×
1023
D.
1
mol·L-1
NH4Cl溶液中,含有Cl-数约为6.02×1023
20.
下列有关二氧化硫的说法正确的是( )
A.
密度比空气小
B.
是无色无味的气体
C.
SO2能使溴水褪色,说明SO2具有漂白性
D.
某生产硫酸厂区紫罗兰花变成白色,说明其周围空气中可能含较高浓度SO2
21.
下列实验方法能达到实验目的的是( )
A.
用湿润的红色石蕊试纸检验氨气
B.
用长颈漏斗分离碘的四氯化碳溶液和水溶液
C.
用焰色反应鉴别NaCl和Na2SO4两种无色晶体
D.
用KSCN溶液鉴别FeCl3溶液和Fe(NO3)3溶液
22.
X、Y、Z、W是原子序数依次增大的短周期主族元素。Y与W同主族,Z所在的族序数等于周期数,X、Y最外层电子数之和为7;X、Z原子的电子数总和与Y、W原子的电子数总和之比为7:12。下列说法正确的是( )
A.
原子半径:r(X)
Y的简单气态氢化物的热稳定性比W的弱
C.
由X、Y组成的物质与由Y、W组成的物质化合,可能发生氧化还原反应
D.
常温下,Z的单质一定易溶于由X、Y、W三种元素组成的化合物的溶液
23.
将一定量的由Cu和Cu2O组成的混合粉末加入到125
mL
2.6
mol·L-1的硝酸中,固体恰好完全溶解,得蓝色溶液X并收集到V
mL(标准状况)的纯净无色气体Y。下列结论正确的是( )
A.
X中有两种溶质
B.
Y通入纯水中得到酸性溶液
C.
原混合粉末的总质量小于7.8
g
D.
当V=1
680时,原混合粉末中Cu和Cu2O的物质的量之比为8∶1
二、
非选择题(本部分3题,共31分)
24.
(15分)本题为选做题。包括A、B两题。选学《化学与生活》模块的考生答A题,选学《有机化学基础》模块的考生答B题,每位考生只可选做l题。若两题都作答,则以A题计分。
A.
《化学与生活》
(1)
(3分)在“天宫二号”上蚕宝宝的“太空屋”形似胶囊(如图),两端的半球体由航天铝合金打造,中间部分采用透明有机玻璃,蚕宝宝由聚氨酯海绵包裹着。
①蚕丝的主要成份为________(填字母)。
a.
多糖 b.
蛋白质 c.
油脂
②有机玻璃和聚氨酯海绵均属于________(填字母)。
a.
金属材料
b.
无机非金属材料
c.
有机高分子材料
③钛铝合金是常见的航天铝合金,下列不属于钛铝合金性质的是________(填字母)。
a.
高密度
b.
高强度
c.
高韧性
品名:果肉果冻
配料表:水、白砂糖、桔子
果肉(≥15%)、魔芋粉。
食品添加剂:卡拉胶、黄原
胶、柠檬酸、氯化钾、桔子
香精、甜密素、柠檬黄、诱
惑红、山梨酸钾(2)
(5分)某品牌果冻标签如右图所示。回答下列问题:
①食品添加剂中,属于无机盐的是________(填化学式)。
②属于着色剂的是诱惑红和________;属于防腐剂的是________。
③配料表中白砂糖的成分是蔗糖,请写出蔗糖在人体内水解的化学方程式____________________________。
(3)
(7分)化学与科学技术、生产生活及环境保护等密切相关。
①2016年12月我省启动了保卫碧水蓝天的“263”行动,减少煤炭消费总量,减少雾霾天气的发生。形成硫酸型酸雨的主要气体是________;严格整治畜禽养殖场污染,主要是为减少________和P等元素及化学需氧量对水体的污染。
②目前正在推广用尿素水解液来消除柴油汽车尾气中的氮氧化物。写出尿素水解液中的NH3与NO在催化剂作用下,反应生成无污染物质的化学方程式_____________________________________。
③阿司匹林作为一种药物,主要具有________作用;Mg2Si3O8·nH2O(三硅酸镁)具有治疗胃酸过多的作用,写出其与胃酸反应生成SiO2·H2O等物质的化学方程式__________________________________。
B.
《有机化学基础》
(1)
(3分)有机物的组成、结构与性质密切相关。
①室内装修产生的主要污染气体有:苯、甲醛及DMF(富马酸二甲酯)等,其中属于烃的是________(填字母)。
a.
苯 b.
甲醛 c.
DMF
②下列分子中所有原子可以处于同一平面中的是________(填字母)。
a.
乙烷
b.
溴乙烷
c.
苯乙烯
③提纯含有少量苯酚的甲苯,适宜的试剂是________(填字母)。
a.
溴水
b.
KMnO4酸性溶液
c.
NaOH溶液
(2)
(5分)紫薯中的鞣花酸(结构如右图)具有防癌和抗癌作用。
①鞣花酸分子中含氧官能团的名称为________。
②鞣花酸的分子式为________。
③1
mol鞣花酸最多可与________mol
NaOH发生反应。
(3)
(7分)以A为原料可制备C(丹皮酚)和D(树脂),其合成路线如下:
①A在空气中会缓慢变成粉红色,其原因是________。
②A→B的反应类型为____________;A生成D的反应中,试剂X(烃的含氧衍生物)为________(写结构简式)。
③只含有两个取代基的芳香化合物E是C的同分异构体,E既能与FeCl3溶液发生显色反应又能发生银镜反应和水解反应,则E可能的结构简式有________种(不考虑立体结构),其中核磁共振氢谱有6组峰,且面积比为1∶2∶2∶2∶2∶1的是____________________(写结构简式)。
25.
(6分)有关物质的转化关系如下图所示(部分物质已略去)。A、C都是常见的金属氧化物,B是常见的强酸,D是最常见的无色液体,E、F、H都是常见的气体,且E、F都可用于漂白,H是空气中主要成分之一,I、J都是由三种相同元素(短周期元素)组成的盐。
请回答下列问题:
(1)
D的化学式为____________。
(2)
G的电子式为____________。
(3)
写出反应①的化学方程式________________________。
(4)
写出反应②的离子方程式________________________。
26.
(10分)KIO3是一种无色易溶于水的晶体,医药上可作防治地方甲状腺肿的药剂,目前碘酸钾被广泛应用于食盐加碘。一种由含碘废水制取碘酸钾的工艺如下:
(1)
检验“含碘废水”中含有的单质I2,常用的试剂是________。
(2)
进行“过滤1”时,需同时对CuI沉淀进行洗涤。在洗涤过滤滤液中可通过滴加________盐溶液来检验其是否已洗涤干净。
(3)
“滤渣2”的成分为____________(填化学式)。
(4)
“制KI”时,发生反应的化学方程式为____________。
(5)
江苏食用加碘盐新标准是每千克食盐中碘元素含量为25毫克(波动范围为18~33
mg/kg)。测定食盐试样中碘元素含量的步骤如下:称取4.000
g市售食盐加入锥形瓶中,依次加入适量的水、稍过量KI及稀硫酸;充分反应后,再加入12.00
mL
6.000×10-4
mol·L-1
Na2S2O3溶液,与生成的碘恰好完全反应。有关反应原理为:
KIO3+5KI+3H2SO4===3K2SO4+3I2+3H2O; I2+2S2O===2I-+S4O。
①计算该食盐试样中碘元素的含量(单位mg/kg,写出计算过程)。
②该食盐试样是否符合江苏食用加碘盐新标准并说明判断依据
2017届高二学业水平测试模拟卷(一)(盐城市)
化学参考答案
一、
单项选择题:共69分。
1.
C 2.
B 3.
B 4.
D 5.
A 6.
C 7.
D 8.
B 9.
A 10.
A 11.
C 12.
B 13.
B 14.
D 15.
A 16.
A 17.
D 18.
C 19.
C 20.
D 21.
A 22.
C 23.
D
二、
非选择题:共31分。
24.
(15分)
A.
化学与生活
(1)
①b(1分) ②c(1分) ③a(1分)
(2)
①氯化钾(KCl)(1分) ②柠蒙黄(1分) 山梨酸钾(1分)
③C12H22O11+H2OC6H12O6+C6H12O6(2分)
蔗糖
葡萄糖
果糖
(3)
①SO2(1分) N(氮)(1分)
②6NO+4NH35N2+6H2O(2分)
③解热镇痛(1分)
Mg2Si3O8·nH2O+4HCl===2MgCl2+3SiO2·H2O+(n-1)H2O(2分)
B.
有机化学基础
(1)
①a(1分) ②c(1分) ③c(1分)
(2)
①酯基和(酚)羟基(共2分) ②C14H6O8(1分) ③8(2分)
(3)
①A易被空气中的氧气氧化(1分)
②取代反应(1分) HCHO(1分)
③6(2分) HCOOCH2CH2OH(2分)
25.
(6分)
(1)
H2O(1分)
(2)
Na+[?O?,??H]-(1分)
(3)
MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O(2分)
(4)
Cl2+SO+H2O===SO+2Cl-+2H+(2分)
26.
(10分)
(1)
淀粉溶液(1分)
(2)
BaCl2[或Ba(NO3)2](1分)
(3)
Cu(或Cu和Fe)(1分)
(4)
K2CO3+FeI2===FeCO3↓+2KI(1分)
(5)
①KIO3~6Na2S2O3
n(I)=n(KIO3)=n(Na2S2O3)=×6.000×10-4
mol·L-1×12.00
mL×10-3
L·mL-1
=1.200×10-6
mol(2分)
m(I)=1.200×10-6
mol×127
g·mol-1×103
mg·g-1=0.152
4
mg(2分)
碘含量为:=38.10
mg/kg(1分)
②不符合新标准。因为38.10
mg/kg不在18~33
mg/kg范围内(1分)
同课章节目录
