《从实验走进化学》单元检测 同步练习
文档属性
| 名称 | 《从实验走进化学》单元检测 同步练习 |

|
|
| 格式 | zip | ||
| 文件大小 | 532.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-04-07 00:00:00 | ||
图片预览

文档简介
课题1
从实验走进化学
单元检测
同步练习
(时间:90分钟 满分:100分)
第Ⅰ卷(选择题,共45分)
选择题
(本题包括15小题,每小题3分,共45分,每小题只有一个选项符合题意)
1.下列做法中不符合“绿色化学”思想的是
( )
A.以水性涂料代替油性涂料
B.以无磷洗涤剂代替含磷洗涤剂
C.实验后的有毒有害物质应分类收集,统一处理
D.在通风橱中制取氯气时不用NaOH溶液吸收尾气
2.下列做法正确的是
( )
A.将浓硝酸保存在无色玻璃瓶中
B.用镊子取出白磷置于水中进行切割
C.把氯酸钾制氧气后的残渣倒入垃圾桶
D.氢气还原氧化铜实验先加热再通氢气
3.关于绿色化学的叙述错误的是
( )
A.采用无毒无害的原料,生产有利环保、人体健康、安全的产品
B.在无毒、无害的条件下反应,减少废物向环境排放
C.充分利用能源、资源,提高原子利用率、使原料的原子都成为产品
D.充分利用绿色原料进行化工生产,产出绿颜色产品
4.一定条件下,电解较稀的硫酸,其还原产
( http: / / www.21cnjy.com )物为双氧水,该原理可用于制取双氧水,其电解的化学方程式为3H2O+3O2===O3+3H2O2。下列有关说法正确的是
( )
A.电解池的阳极生成双氧水,阴极生成臭氧
B.电解池中硫酸溶液的pH保持不变
C.产生臭氧的电极反应式为3H2O-6e-===O3+6H+
D.产生双氧水的电极反应式为2H2O-2e-===H2O2+2H+
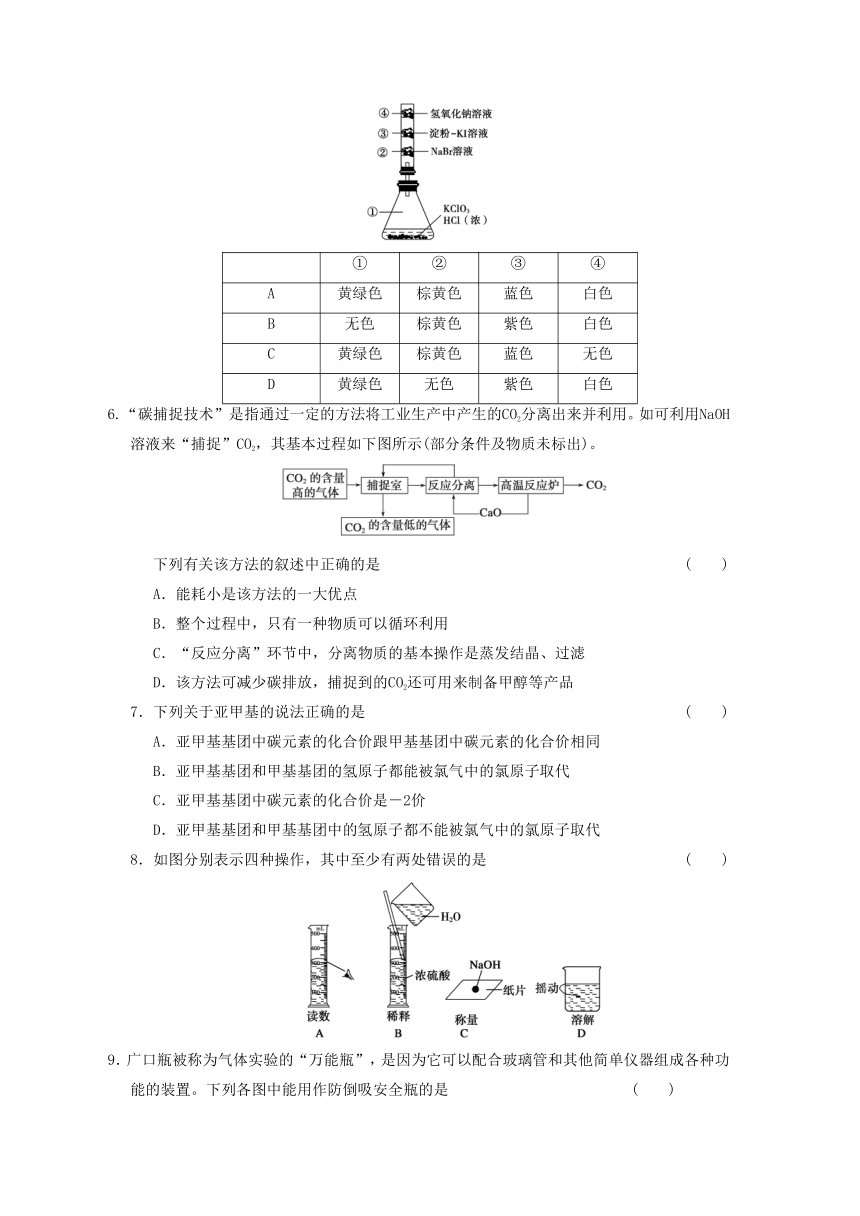
5.已知常温下氯酸钾与浓盐酸反应放出氯气,
( http: / / www.21cnjy.com )现按下图进行卤素的性质实验。玻璃管内装有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部分颜色描述正确的是
( )
①
②
③
④
A
黄绿色
棕黄色
蓝色
白色
B
无色
棕黄色
紫色
白色
C
黄绿色
棕黄色
蓝色
无色
D
黄绿色
无色
紫色
白色
6.“碳捕捉技术”是指通过一定的方法将工业
( http: / / www.21cnjy.com )生产中产生的CO2分离出来并利用。如可利用NaOH溶液来“捕捉”CO2,其基本过程如下图所示(部分条件及物质未标出)。
下列有关该方法的叙述中正确的是
( )
A.能耗小是该方法的一大优点
B.整个过程中,只有一种物质可以循环利用
C.“反应分离”环节中,分离物质的基本操作是蒸发结晶、过滤
D.该方法可减少碳排放,捕捉到的CO2还可用来制备甲醇等产品
7.下列关于亚甲基的说法正确的是
( )
A.亚甲基基团中碳元素的化合价跟甲基基团中碳元素的化合价相同
B.亚甲基基团和甲基基团的氢原子都能被氯气中的氯原子取代
C.亚甲基基团中碳元素的化合价是-2价
D.亚甲基基团和甲基基团中的氢原子都不能被氯气中的氯原子取代
8.如图分别表示四种操作,其中至少有两处错误的是
( )
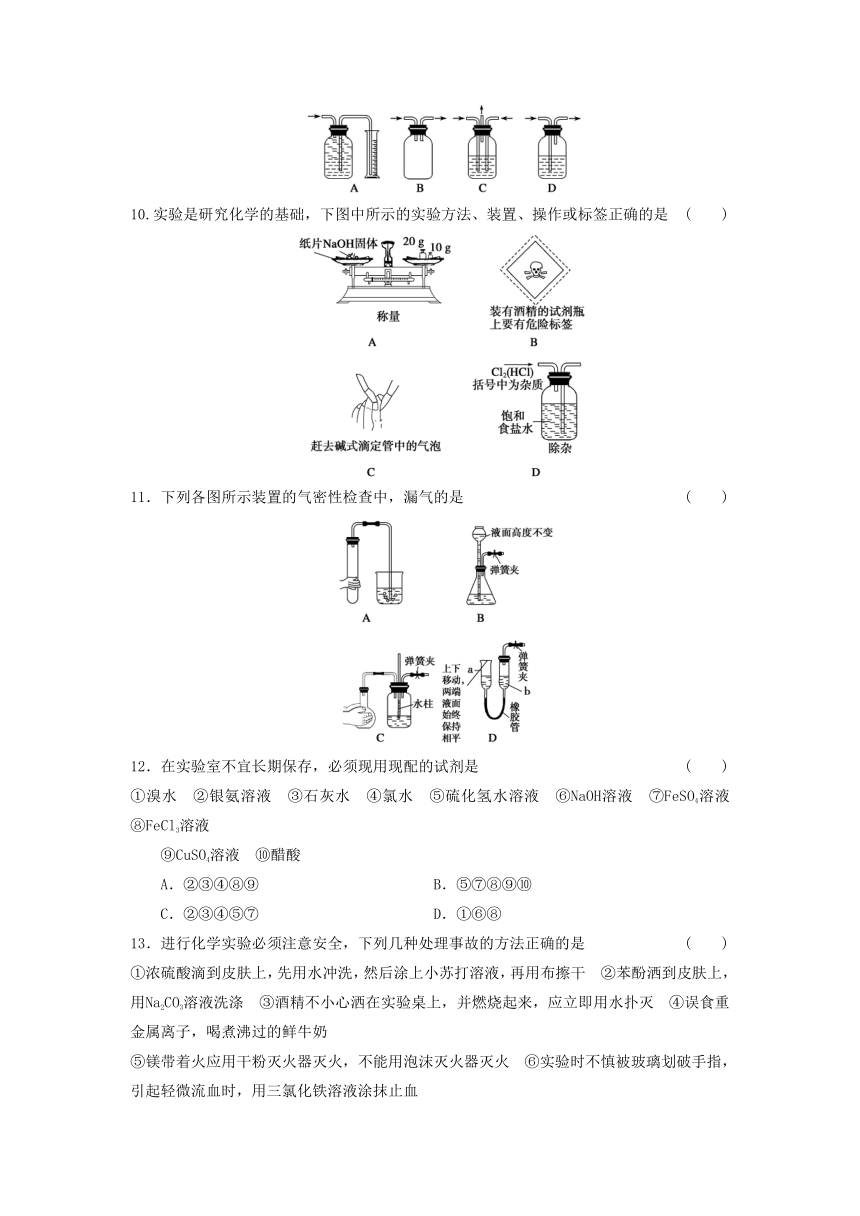
9.广口瓶被称为气体实验的
( http: / / www.21cnjy.com )“万能瓶”,是因为它可以配合玻璃管和其他简单仪器组成各种功能的装置。下列各图中能用作防倒吸安全瓶的是
( )
10.实验是研究化学的基础,下图中所示的实验方法、装置、操作或标签正确的是
( )
11.下列各图所示装置的气密性检查中,漏气的是
( )
12.在实验室不宜长期保存,必须现用现配的试剂是
( )
①溴水 ②银氨溶液 ③石灰水 ④氯水 ⑤硫化氢水溶液 ⑥NaOH溶液 ⑦FeSO4溶液 ⑧FeCl3溶液
⑨CuSO4溶液 ⑩醋酸
A.②③④⑧⑨
B.⑤⑦⑧⑨⑩
C.②③④⑤⑦
D.①⑥⑧
13.进行化学实验必须注意安全,下列几种处理事故的方法正确的是
( )
①浓硫酸滴到皮肤上,先用水冲洗,然后涂
( http: / / www.21cnjy.com )上小苏打溶液,再用布擦干 ②苯酚洒到皮肤上,用Na2CO3溶液洗涤 ③酒精不小心洒在实验桌上,并燃烧起来,应立即用水扑灭 ④误食重金属离子,喝煮沸过的鲜牛奶
⑤镁带着火应用干粉灭火器灭火,不能用泡沫灭火器灭火 ⑥实验时不慎被玻璃划破手指,引起轻微流血时,用三氯化铁溶液涂抹止血
A.全部正确
B.只有②③④⑤正确
C.只有⑥正确
D.全部错误
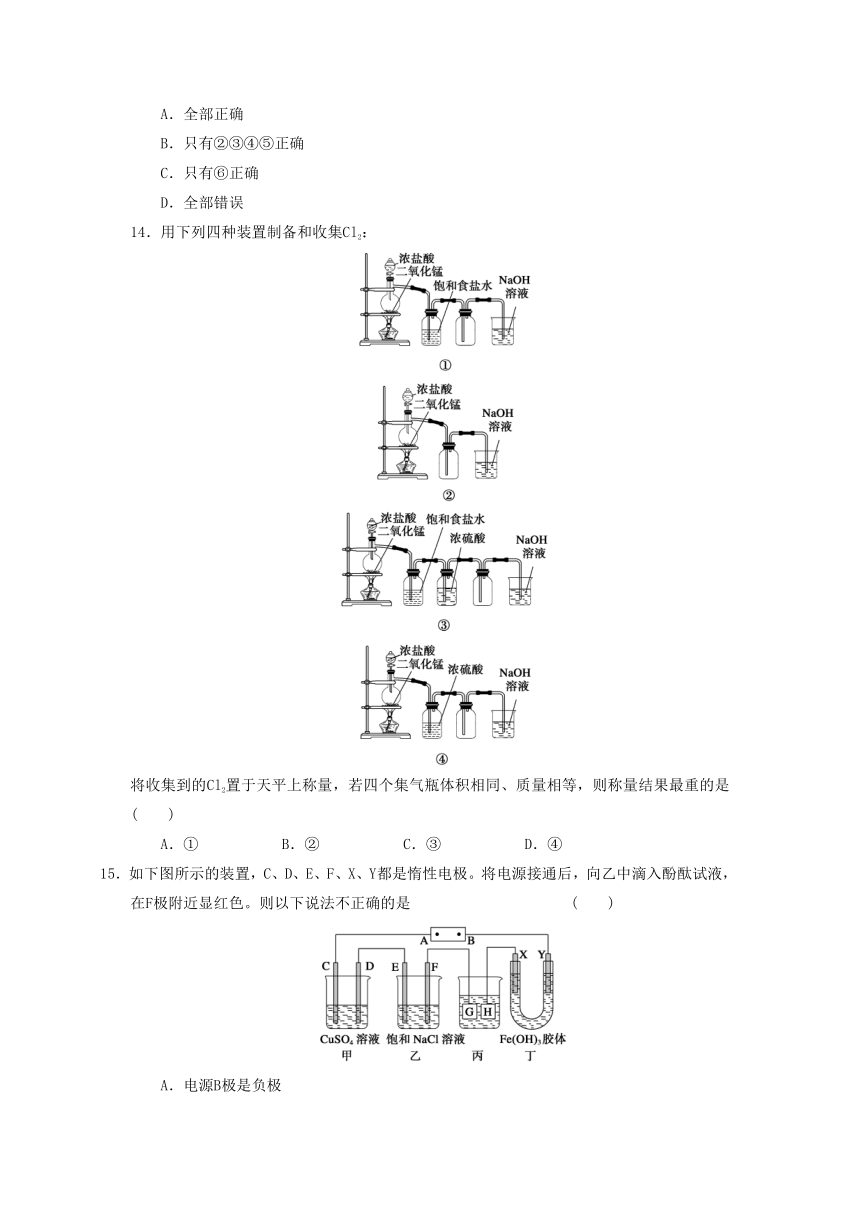
14.用下列四种装置制备和收集Cl2:
将收集到的Cl2置于天平上称量,若
( http: / / www.21cnjy.com )四个集气瓶体积相同、质量相等,则称量结果最重的是
( )
A.①
B.②
C.③
D.④
15.如下图所示的装置,C、D、E
( http: / / www.21cnjy.com )、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。则以下说法不正确的是
( )
A.电源B极是负极
B.甲、乙装置的C、D、E、F电极均有单质生成,其物质的量之比为1∶2∶2∶2
C.欲用丙装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液
D.装置丁中Y极附近红褐色变深,说明氢氧化铁胶粒带正电荷
非选择题
(本题包括5小题,共55分)
16.(8分)请根据下列实验要求填空:
(1)分离饱和食盐水和泥沙的混合物,分离方法为____________,所用的玻璃仪器有
________________________________________________________________________。
(2)从碘水里提取并得到固体碘,应先进行________操作,再进行________操作。
(3)指出在使用下列仪器(已经洗涤干净)或用品时的第一步操作:
①石蕊试纸(检验气体):
_____________________________________________________
__________________________________________________________________________。
②容量瓶:
_______________________________________________________________
________________________________________________________________________。
③滴定管:________________________________________________________________
________________________________________________________________________。
④集气瓶(收集氯化氢):____________________________________________________
________________________________________________________________________。
17.(8分)电浮选凝聚法是工业上采用的一种污水处理方法。如图是电
解污水实验装置示意图。接通直流电源一段时间后,在A电极附近
有深色沉淀物沉积下来,A、B电极附近都有气泡产生。试填空。
(1)图中的A为________极。做B电极材料的物质X的名称是
____________________。
(2)深色沉淀具有____________性,可以将水中的污物沉积下来。
(3)若污水导电性不良时,可以加入适量盐溶液,试写出其中一种溶质的化学式
______________。
18.(12分)(1)某化工厂排出
( http: / / www.21cnjy.com )的废水中含有Cl2和H2SO4,为了除去此废水中的游离氯,并使废水变为中性,供使用的试剂有Na2CO3溶液和Na2SO3溶液。试回答:
①应先向废水中加入________溶液,离子方程式为_____________________________
________________________________________________________________________。
②然后向废水中加入________溶液,离子方程式为_____________________________
________________________________________________________________________。
(2)某河道两旁有甲、乙两厂。它们排放的工业废水中,共含K+、Ag+、Fe3+、Cl-、
OH-、NO六种离子。甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是
________、________、________。乙厂的废水中含有另外三种离子。如果加一定量
________(选填:活性炭、硫酸亚铁、铁粉),可以回收其中的金属________(填写金属元
素符号)。
另一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的___________(填
写离子符号)转化为沉淀。经过滤后的废水主要含________,可用来浇灌农田。
19.(13分)某课外活动小组用如图所
( http: / / www.21cnjy.com )示的实验装置探究氯气与氨气之间的反应。其中A、F
为氯气和氨气的发生装置,D为纯净、干燥的氯气与氨气反应的装置。
请回答下列问题:
(1)
实验室用二氧化锰和浓盐酸反应制取氯气,写出该反应的化学方程式____________
__________________________________________________________________________。
(2)洗气瓶B的作用是_______________________________________________________
C、E都是干燥装置,其中E中干燥管内所装的试剂是________。
(3)反应开始后装置D中出现浓厚的白烟并在容器内壁凝结,活动小组拟继续通过实验鉴定该固体的成分。请你协助他们完成该实验探究。
步骤①:取固体样品加少量水溶解,分装于
( http: / / www.21cnjy.com )两支试管中。向其中一支试管中加入浓NaOH溶液,加热,将湿润的红色石蕊试纸放在试管口附近,红色石蕊试纸变蓝,证明该固体中含有__________________;
步骤②:___________________________________________________________________
__________________________________________________________________________。
(4)从绿色化学的角度考虑该装置中有一明显不合理之处,请你提出改进的意见。
20.(14分)根据下图所示装置和操作,回答下列有关问题。
(1)按图Ⅰ所示装置,用两种不同的操作分别进行实验,观察B管中的现象。
①操作1:先夹紧止水夹a,再使A管开始反应,实验中观察到B管中的现象是
________________________________________________________________________
________________________________________________________________________。
②操作2:打开止水夹a,使A管反应一段时间后再夹紧止水夹a,实验中观察到B管
中的现象是_________________________________________________________________
__________________________________________________________________________。
③请说明造成两种操作现象不同的原因(如两种现象相同,此小题不用回答):
________________________________________________________________________
________________________________________________________________________。
(2)
上述装置实验结束后,取A管内反应所得的溶液,隔绝空气小心蒸干后,再高温煅
烧(有关装置和操作均已略去),最后留下红
( http: / / www.21cnjy.com )色固体,将分解时产生的气体按图Ⅱ所示装置依次通过洗气装置,结果试管甲内出现白色沉淀,试管乙内品红溶液红色褪去,回答:
①
用方程式表示试管甲产生白色沉淀的原因___________________________________
__________________________________________________________________________。
②
根据实验现象写出A管内溶液蒸干后,在高温煅烧分解时所发生的化学反应方程式
__________________________________________________________________________
__________________________________________________________________________。
③图Ⅱ中丙装置的作用是____________________________________________________。
实验结束时,在装置丙中观察到的现象是______________________________________
__________________________________________________________________________。
答案
1.D 2.B 3.D
4.C 5.A 6.D 7.B 8.B 9.B
10.C 11.D 12.C 13.C 14.C 15.C
16.(1)过滤 烧杯、漏斗、玻璃棒
(2)萃取分液 蒸馏
(3)①把试纸用蒸馏水湿润 ②检查容量瓶是否漏水 ③用待装液润洗滴定管2~3次(也可以写:检查滴定管是否漏水) ④干燥集气瓶
17.(1)阳 炭或石墨或铝等(合理即可)
(2)吸附
(3)Na2SO4、K2SO4等(合理即可)
18.(1)①Na2SO3 Cl2+SO+H2O===SO+2Cl-+2H+
②Na2CO3 CO+2H+===H2O+CO2↑
(2)OH- Cl- K+ 铁粉 Ag Ag+、Cl-、Fe3+、OH- KNO3
19.(1)4HCl(浓)+MnO2MnCl2+Cl2↑+2H2O
(2)除去Cl2中的HCl 碱石灰
(3)步骤①:NH
步骤②:向另一支试管中加入硝酸酸化的硝酸银溶液,若产生白色沉淀,说明溶液中含有Cl-
(4)将D装置的竖直导管口套一个气囊收集尾气,以防尾气污染环境。
20.(1)①液面升高且生成白色沉淀,且迅速变为灰绿色,最后变为红褐色
②液面上升,有白色沉淀生成,且保持较长时间不变色
③操作2中产生的H2将系统内空气赶尽,避免了Fe(OH)2的氧化
(2)①SO3+H2O+BaCl2===BaSO4↓+2HCl ②2FeSO4Fe2O3+SO3↑+SO2↑
③吸收剩余的SO2气体 导管内倒吸一段液柱
从实验走进化学
单元检测
同步练习
(时间:90分钟 满分:100分)
第Ⅰ卷(选择题,共45分)
选择题
(本题包括15小题,每小题3分,共45分,每小题只有一个选项符合题意)
1.下列做法中不符合“绿色化学”思想的是
( )
A.以水性涂料代替油性涂料
B.以无磷洗涤剂代替含磷洗涤剂
C.实验后的有毒有害物质应分类收集,统一处理
D.在通风橱中制取氯气时不用NaOH溶液吸收尾气
2.下列做法正确的是
( )
A.将浓硝酸保存在无色玻璃瓶中
B.用镊子取出白磷置于水中进行切割
C.把氯酸钾制氧气后的残渣倒入垃圾桶
D.氢气还原氧化铜实验先加热再通氢气
3.关于绿色化学的叙述错误的是
( )
A.采用无毒无害的原料,生产有利环保、人体健康、安全的产品
B.在无毒、无害的条件下反应,减少废物向环境排放
C.充分利用能源、资源,提高原子利用率、使原料的原子都成为产品
D.充分利用绿色原料进行化工生产,产出绿颜色产品
4.一定条件下,电解较稀的硫酸,其还原产
( http: / / www.21cnjy.com )物为双氧水,该原理可用于制取双氧水,其电解的化学方程式为3H2O+3O2===O3+3H2O2。下列有关说法正确的是
( )
A.电解池的阳极生成双氧水,阴极生成臭氧
B.电解池中硫酸溶液的pH保持不变
C.产生臭氧的电极反应式为3H2O-6e-===O3+6H+
D.产生双氧水的电极反应式为2H2O-2e-===H2O2+2H+
5.已知常温下氯酸钾与浓盐酸反应放出氯气,
( http: / / www.21cnjy.com )现按下图进行卤素的性质实验。玻璃管内装有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部分颜色描述正确的是
( )
①
②
③
④
A
黄绿色
棕黄色
蓝色
白色
B
无色
棕黄色
紫色
白色
C
黄绿色
棕黄色
蓝色
无色
D
黄绿色
无色
紫色
白色
6.“碳捕捉技术”是指通过一定的方法将工业
( http: / / www.21cnjy.com )生产中产生的CO2分离出来并利用。如可利用NaOH溶液来“捕捉”CO2,其基本过程如下图所示(部分条件及物质未标出)。
下列有关该方法的叙述中正确的是
( )
A.能耗小是该方法的一大优点
B.整个过程中,只有一种物质可以循环利用
C.“反应分离”环节中,分离物质的基本操作是蒸发结晶、过滤
D.该方法可减少碳排放,捕捉到的CO2还可用来制备甲醇等产品
7.下列关于亚甲基的说法正确的是
( )
A.亚甲基基团中碳元素的化合价跟甲基基团中碳元素的化合价相同
B.亚甲基基团和甲基基团的氢原子都能被氯气中的氯原子取代
C.亚甲基基团中碳元素的化合价是-2价
D.亚甲基基团和甲基基团中的氢原子都不能被氯气中的氯原子取代
8.如图分别表示四种操作,其中至少有两处错误的是
( )
9.广口瓶被称为气体实验的
( http: / / www.21cnjy.com )“万能瓶”,是因为它可以配合玻璃管和其他简单仪器组成各种功能的装置。下列各图中能用作防倒吸安全瓶的是
( )
10.实验是研究化学的基础,下图中所示的实验方法、装置、操作或标签正确的是
( )
11.下列各图所示装置的气密性检查中,漏气的是
( )
12.在实验室不宜长期保存,必须现用现配的试剂是
( )
①溴水 ②银氨溶液 ③石灰水 ④氯水 ⑤硫化氢水溶液 ⑥NaOH溶液 ⑦FeSO4溶液 ⑧FeCl3溶液
⑨CuSO4溶液 ⑩醋酸
A.②③④⑧⑨
B.⑤⑦⑧⑨⑩
C.②③④⑤⑦
D.①⑥⑧
13.进行化学实验必须注意安全,下列几种处理事故的方法正确的是
( )
①浓硫酸滴到皮肤上,先用水冲洗,然后涂
( http: / / www.21cnjy.com )上小苏打溶液,再用布擦干 ②苯酚洒到皮肤上,用Na2CO3溶液洗涤 ③酒精不小心洒在实验桌上,并燃烧起来,应立即用水扑灭 ④误食重金属离子,喝煮沸过的鲜牛奶
⑤镁带着火应用干粉灭火器灭火,不能用泡沫灭火器灭火 ⑥实验时不慎被玻璃划破手指,引起轻微流血时,用三氯化铁溶液涂抹止血
A.全部正确
B.只有②③④⑤正确
C.只有⑥正确
D.全部错误
14.用下列四种装置制备和收集Cl2:
将收集到的Cl2置于天平上称量,若
( http: / / www.21cnjy.com )四个集气瓶体积相同、质量相等,则称量结果最重的是
( )
A.①
B.②
C.③
D.④
15.如下图所示的装置,C、D、E
( http: / / www.21cnjy.com )、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。则以下说法不正确的是
( )
A.电源B极是负极
B.甲、乙装置的C、D、E、F电极均有单质生成,其物质的量之比为1∶2∶2∶2
C.欲用丙装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液
D.装置丁中Y极附近红褐色变深,说明氢氧化铁胶粒带正电荷
非选择题
(本题包括5小题,共55分)
16.(8分)请根据下列实验要求填空:
(1)分离饱和食盐水和泥沙的混合物,分离方法为____________,所用的玻璃仪器有
________________________________________________________________________。
(2)从碘水里提取并得到固体碘,应先进行________操作,再进行________操作。
(3)指出在使用下列仪器(已经洗涤干净)或用品时的第一步操作:
①石蕊试纸(检验气体):
_____________________________________________________
__________________________________________________________________________。
②容量瓶:
_______________________________________________________________
________________________________________________________________________。
③滴定管:________________________________________________________________
________________________________________________________________________。
④集气瓶(收集氯化氢):____________________________________________________
________________________________________________________________________。
17.(8分)电浮选凝聚法是工业上采用的一种污水处理方法。如图是电
解污水实验装置示意图。接通直流电源一段时间后,在A电极附近
有深色沉淀物沉积下来,A、B电极附近都有气泡产生。试填空。
(1)图中的A为________极。做B电极材料的物质X的名称是
____________________。
(2)深色沉淀具有____________性,可以将水中的污物沉积下来。
(3)若污水导电性不良时,可以加入适量盐溶液,试写出其中一种溶质的化学式
______________。
18.(12分)(1)某化工厂排出
( http: / / www.21cnjy.com )的废水中含有Cl2和H2SO4,为了除去此废水中的游离氯,并使废水变为中性,供使用的试剂有Na2CO3溶液和Na2SO3溶液。试回答:
①应先向废水中加入________溶液,离子方程式为_____________________________
________________________________________________________________________。
②然后向废水中加入________溶液,离子方程式为_____________________________
________________________________________________________________________。
(2)某河道两旁有甲、乙两厂。它们排放的工业废水中,共含K+、Ag+、Fe3+、Cl-、
OH-、NO六种离子。甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是
________、________、________。乙厂的废水中含有另外三种离子。如果加一定量
________(选填:活性炭、硫酸亚铁、铁粉),可以回收其中的金属________(填写金属元
素符号)。
另一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的___________(填
写离子符号)转化为沉淀。经过滤后的废水主要含________,可用来浇灌农田。
19.(13分)某课外活动小组用如图所
( http: / / www.21cnjy.com )示的实验装置探究氯气与氨气之间的反应。其中A、F
为氯气和氨气的发生装置,D为纯净、干燥的氯气与氨气反应的装置。
请回答下列问题:
(1)
实验室用二氧化锰和浓盐酸反应制取氯气,写出该反应的化学方程式____________
__________________________________________________________________________。
(2)洗气瓶B的作用是_______________________________________________________
C、E都是干燥装置,其中E中干燥管内所装的试剂是________。
(3)反应开始后装置D中出现浓厚的白烟并在容器内壁凝结,活动小组拟继续通过实验鉴定该固体的成分。请你协助他们完成该实验探究。
步骤①:取固体样品加少量水溶解,分装于
( http: / / www.21cnjy.com )两支试管中。向其中一支试管中加入浓NaOH溶液,加热,将湿润的红色石蕊试纸放在试管口附近,红色石蕊试纸变蓝,证明该固体中含有__________________;
步骤②:___________________________________________________________________
__________________________________________________________________________。
(4)从绿色化学的角度考虑该装置中有一明显不合理之处,请你提出改进的意见。
20.(14分)根据下图所示装置和操作,回答下列有关问题。
(1)按图Ⅰ所示装置,用两种不同的操作分别进行实验,观察B管中的现象。
①操作1:先夹紧止水夹a,再使A管开始反应,实验中观察到B管中的现象是
________________________________________________________________________
________________________________________________________________________。
②操作2:打开止水夹a,使A管反应一段时间后再夹紧止水夹a,实验中观察到B管
中的现象是_________________________________________________________________
__________________________________________________________________________。
③请说明造成两种操作现象不同的原因(如两种现象相同,此小题不用回答):
________________________________________________________________________
________________________________________________________________________。
(2)
上述装置实验结束后,取A管内反应所得的溶液,隔绝空气小心蒸干后,再高温煅
烧(有关装置和操作均已略去),最后留下红
( http: / / www.21cnjy.com )色固体,将分解时产生的气体按图Ⅱ所示装置依次通过洗气装置,结果试管甲内出现白色沉淀,试管乙内品红溶液红色褪去,回答:
①
用方程式表示试管甲产生白色沉淀的原因___________________________________
__________________________________________________________________________。
②
根据实验现象写出A管内溶液蒸干后,在高温煅烧分解时所发生的化学反应方程式
__________________________________________________________________________
__________________________________________________________________________。
③图Ⅱ中丙装置的作用是____________________________________________________。
实验结束时,在装置丙中观察到的现象是______________________________________
__________________________________________________________________________。
答案
1.D 2.B 3.D
4.C 5.A 6.D 7.B 8.B 9.B
10.C 11.D 12.C 13.C 14.C 15.C
16.(1)过滤 烧杯、漏斗、玻璃棒
(2)萃取分液 蒸馏
(3)①把试纸用蒸馏水湿润 ②检查容量瓶是否漏水 ③用待装液润洗滴定管2~3次(也可以写:检查滴定管是否漏水) ④干燥集气瓶
17.(1)阳 炭或石墨或铝等(合理即可)
(2)吸附
(3)Na2SO4、K2SO4等(合理即可)
18.(1)①Na2SO3 Cl2+SO+H2O===SO+2Cl-+2H+
②Na2CO3 CO+2H+===H2O+CO2↑
(2)OH- Cl- K+ 铁粉 Ag Ag+、Cl-、Fe3+、OH- KNO3
19.(1)4HCl(浓)+MnO2MnCl2+Cl2↑+2H2O
(2)除去Cl2中的HCl 碱石灰
(3)步骤①:NH
步骤②:向另一支试管中加入硝酸酸化的硝酸银溶液,若产生白色沉淀,说明溶液中含有Cl-
(4)将D装置的竖直导管口套一个气囊收集尾气,以防尾气污染环境。
20.(1)①液面升高且生成白色沉淀,且迅速变为灰绿色,最后变为红褐色
②液面上升,有白色沉淀生成,且保持较长时间不变色
③操作2中产生的H2将系统内空气赶尽,避免了Fe(OH)2的氧化
(2)①SO3+H2O+BaCl2===BaSO4↓+2HCl ②2FeSO4Fe2O3+SO3↑+SO2↑
③吸收剩余的SO2气体 导管内倒吸一段液柱
同课章节目录
- 第一单元 从实验走进化学
- 课题一 实验化学起步
- 实验1-1 蓝瓶子实验
- 课题二 化学实验的绿色追求
- 实验1-2 氯气的生成及其性质的微型实验
- 实验1-3 污水处理--电浮选凝聚法
- 第二单元 物质的获取
- 课题一 物质的分离和提纯
- 实验2-1 纸上层析分离甲基橙和酚酞
- 实验2-2 海水的蒸馏
- 实验2-3 从海带中提取碘
- 课题二 物质的制备
- 实验2-4 硫酸亚铁铵的制备
- 实验2-5 乙酸乙酯的制备及反应条件探究
- 实验2-6 氢氧化铝的制备
- 第三单元 物质的检测
- 课题一 物质的检验
- 实验3-1 几种无机离子的检验
- 实验3-2 几种有机物的检验
- 实验3-3 植物体中某些元素的检验
- 课题二 物质含量的测定
- 实验3-4 酸碱滴定曲线的测绘
- 实验3-5 比色法测定抗贫血药物中铁的含量
- 实验3-6 食醋中总酸量的测定
- 第四单元 研究型实验
- 课题一 物质性质的研究
- 实验4-1 纯净物与混合物性质的比较
- 实验4-2 金属镁、铝、锌化学性质的探究
- 课题二 身边化学问题的探究
- 实验4-3 含氯消毒液性质、作用的探究
- 实验4-4 饮料的研究
