《从实验走进化学》专项训练 同步练习
文档属性
| 名称 | 《从实验走进化学》专项训练 同步练习 |
|
|
| 格式 | zip | ||
| 文件大小 | 379.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-04-07 00:00:00 | ||
图片预览



文档简介
课题1
从实验走进化学
专项训练
同步练习
一、化学实验基本操作
1.下列仪器:①烧杯、②烧瓶、③试管、④
( http: / / www.21cnjy.com )锥形瓶、⑤表面皿、⑥坩埚。其中属于玻璃仪器且可用于加热的有
( )
A.②③
B.①②③④
C.①②③④⑤
D.①②③④⑤⑥
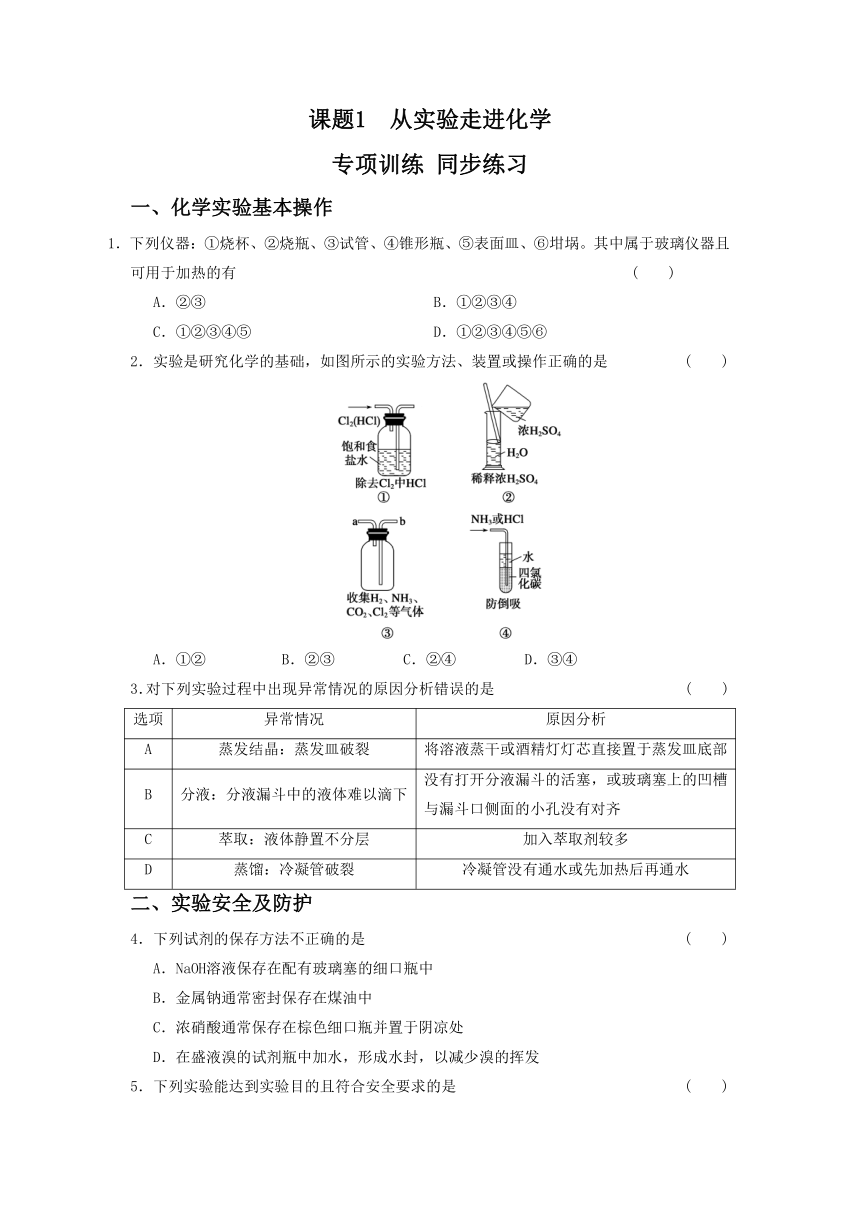
2.实验是研究化学的基础,如图所示的实验方法、装置或操作正确的是
( )
A.①②
B.②③
C.②④
D.③④
3.对下列实验过程中出现异常情况的原因分析错误的是
( )
选项
异常情况
原因分析
A
蒸发结晶:蒸发皿破裂
将溶液蒸干或酒精灯灯芯直接置于蒸发皿底部
B
分液:分液漏斗中的液体难以滴下
没有打开分液漏斗的活塞,或玻璃塞上的凹槽与漏斗口侧面的小孔没有对齐
C
萃取:液体静置不分层
加入萃取剂较多
D
蒸馏:冷凝管破裂
冷凝管没有通水或先加热后再通水
二、实验安全及防护
4.下列试剂的保存方法不正确的是
( )
A.NaOH溶液保存在配有玻璃塞的细口瓶中
B.金属钠通常密封保存在煤油中
C.浓硝酸通常保存在棕色细口瓶并置于阴凉处
D.在盛液溴的试剂瓶中加水,形成水封,以减少溴的挥发
5.下列实验能达到实验目的且符合安全要求的是
( )
三、实验成功的关键
6.演示铁在纯氧中燃烧实验时,将铁丝绕成螺旋状,其主要目的是
( )
A.提高铁丝利用率
B.提高反应温度
C.增大反应的接触面积
D.使瓶底氧气充分利用
7.下列说法正确的是
( )
A.亚甲基蓝和亚甲基白在碱性条件下都不能稳定存在
B.亚甲基蓝变为亚甲基白后,通常不能再复原为亚甲基蓝
C.亚甲基白变为亚甲基蓝后,通常不能再复原为亚甲基白
D.亚甲基白不稳定,容易被氧气氧化
四、实验化学的绿色化追求
8.下列实验或叙述不符合绿色理念的是
( )
A.实验室用H2O2代替KClO3制取O2
B.用稀HNO3代替浓HNO3与Cu反应制取Cu(NO3)2
C.工业上用H2O2代替NaClO3作氧化剂氧化Fe2+
D.用KClO3代替MnO2在盖有表面皿的点滴板上制取Cl2并做Cl2与KBr、KI、FeSO4、NaOH等溶液反应的实验
9.在“绿色化学工艺”中,理想状态是反应物
( http: / / www.21cnjy.com )中的原子全部转化为欲制得的产物,即原子利用率为100%。在用CH3C≡CH合成CH2===C(CH3)COOCH3(二者物质的量比为1∶1)的过程中,欲使原子利用率达到最高,还需要的其他反应物有
( )
A.CO和CH3OH
B.CO2和H2O
C.H2和CO2
D.CH3OH和H2
五、化学实验的微型化
10.如图所示,在注射器中加入少量Na2SO3晶体,并吸入少量的浓硫酸(以不接触纸条为准)。
则下列有关说法正确的是
( )
A.蓝色石蕊试纸先变红后褪色
B.蘸有KMnO4溶液的滤纸褪色,证明了SO2的漂白性
C.品红试纸褪色,证明了SO2的漂白性
D.蘸有酚酞和NaOH溶液的滤纸褪色,证明了SO2的漂白性
11.向足量的氯化亚铁溶液中加入少量(1~2滴)液溴,振荡后溶液变为黄色。
Ⅰ.(1)甲同学认为是Br2单质溶于水,溶液才变成黄色;乙认为是Fe2+被氧化成Fe3+,使溶液变成黄色。
(2)请根据提供的试剂作出判断:
A.酸性高锰酸钾溶液
B.氢氧化钠溶液
C.四氯化碳
D.硫氰化钾溶液
两个同学的观点正确的是________(填“甲”或“乙”),并用两种方法(原理不同)进行实验,写出选用的试剂编号及实验中观察到的现象:
选用试剂
实验现象
第一种方法
第二种方法
(3)若选用淀粉 碘化钾溶液判断哪位同学的
( http: / / www.21cnjy.com )推断是否可行?若可行,本问不需要回答,若不可行,请说明原因。____________________________________________________
__________________________________________________________________________。
Ⅱ.若要把溶解于水中的Br2单质分离出来,所需要的主要玻璃仪器是________,该操作的名称是__________。
六、综合应用题
12.下图是验证氯酸钾和浓盐酸反应的装置,乙、丙是师生对实验改进后的装置[已知:
KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O]:
(1)
和装置甲相比,装置乙的优点是____________________________________________
__________________________________________________________________________。
(2)
和装置B相比,装置D制备氯气的优点是____________________________________
__________________________________________________________________________。
(3)为了进一步验证氯气和水的反应,某学生设计了装置丙。如何控制弹簧夹才能使氯气充满集气瓶F?
(4)当气体充满集气瓶F后,欲使装置E中的水进入集气瓶F应如何操作?
13.电解原理在化学工业中有着广泛的应用。如图所示为一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答下列问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式是____________________________________________。
在X极附近观察到的现象是__________________________________________________。
②Y极上的电极反应式是____________________________________________________,
检验该电极反应产物的方法是________________________________________________。
(2)如果用电解的方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是__________,电极反应式是__________________________________。
②Y电极的材料是__________,电极反应式是__________________________________。
(说明:杂质发生的电极反应不必写出)
14.甲、乙两同学进行课外实验,各
( http: / / www.21cnjy.com )取250
mL无色透明饮料瓶一个,依次加入4
g氢氧化钠、4
g葡萄糖、半瓶水、3滴0.2%的亚甲基蓝溶液旋上瓶塞振荡,溶液呈蓝色,静置后溶液变为无色。甲再次振荡,又呈蓝色,静置后又变为无色,多次反复可重现上述现象。而乙在蓝色消失后,向瓶内加满水旋上瓶塞,振荡却不再出现蓝色,乙认为是物质浓度不同引起的。甲设计并完成了一个实验,否定了乙的说法。
你认为甲实验的操作和现象是________________________________________________。
振荡后出现的蓝色主要与________有关(填写化学式,下同);蓝色消失又与___________有关。
答案
1.B 2.D 3.C 4.A 5.B
6.C 7.D 8.B 9.A 10.C
11.Ⅰ.(2)乙 从左到右,从上到下:C 有机层(下层)无色 D 溶液变为血红色
(3)不可行;因为Br2和Fe3+都能把I-氧化成I2
Ⅱ.分液漏斗 萃取、分液
12.(1)有吸收氯气的装置C,防止污染环境
(2)有起液封作用的小试管,防止氯气从长颈漏斗中逸出
(3)关闭b,打开a、c。
(4)先关闭a、c,后打开b,再用手捂热集气瓶F(或其他合理答案)。
13.(1)①2H++2e-===H2↑ 有气泡冒出,溶液变红
②2Cl--2e-===Cl2↑
把湿润的淀粉 碘化钾试纸放在Y电极附近,试纸变成蓝色
(2)①纯铜 Cu2++2e-===Cu ②粗铜 Cu-2e-===Cu2+
14.将乙瓶中溶液倒掉一半(一部分)后振荡即可出现蓝色(或乙瓶中通入氧气或空气,即可出现蓝色) O2 C6H12O6(或葡萄糖)
从实验走进化学
专项训练
同步练习
一、化学实验基本操作
1.下列仪器:①烧杯、②烧瓶、③试管、④
( http: / / www.21cnjy.com )锥形瓶、⑤表面皿、⑥坩埚。其中属于玻璃仪器且可用于加热的有
( )
A.②③
B.①②③④
C.①②③④⑤
D.①②③④⑤⑥
2.实验是研究化学的基础,如图所示的实验方法、装置或操作正确的是
( )
A.①②
B.②③
C.②④
D.③④
3.对下列实验过程中出现异常情况的原因分析错误的是
( )
选项
异常情况
原因分析
A
蒸发结晶:蒸发皿破裂
将溶液蒸干或酒精灯灯芯直接置于蒸发皿底部
B
分液:分液漏斗中的液体难以滴下
没有打开分液漏斗的活塞,或玻璃塞上的凹槽与漏斗口侧面的小孔没有对齐
C
萃取:液体静置不分层
加入萃取剂较多
D
蒸馏:冷凝管破裂
冷凝管没有通水或先加热后再通水
二、实验安全及防护
4.下列试剂的保存方法不正确的是
( )
A.NaOH溶液保存在配有玻璃塞的细口瓶中
B.金属钠通常密封保存在煤油中
C.浓硝酸通常保存在棕色细口瓶并置于阴凉处
D.在盛液溴的试剂瓶中加水,形成水封,以减少溴的挥发
5.下列实验能达到实验目的且符合安全要求的是
( )
三、实验成功的关键
6.演示铁在纯氧中燃烧实验时,将铁丝绕成螺旋状,其主要目的是
( )
A.提高铁丝利用率
B.提高反应温度
C.增大反应的接触面积
D.使瓶底氧气充分利用
7.下列说法正确的是
( )
A.亚甲基蓝和亚甲基白在碱性条件下都不能稳定存在
B.亚甲基蓝变为亚甲基白后,通常不能再复原为亚甲基蓝
C.亚甲基白变为亚甲基蓝后,通常不能再复原为亚甲基白
D.亚甲基白不稳定,容易被氧气氧化
四、实验化学的绿色化追求
8.下列实验或叙述不符合绿色理念的是
( )
A.实验室用H2O2代替KClO3制取O2
B.用稀HNO3代替浓HNO3与Cu反应制取Cu(NO3)2
C.工业上用H2O2代替NaClO3作氧化剂氧化Fe2+
D.用KClO3代替MnO2在盖有表面皿的点滴板上制取Cl2并做Cl2与KBr、KI、FeSO4、NaOH等溶液反应的实验
9.在“绿色化学工艺”中,理想状态是反应物
( http: / / www.21cnjy.com )中的原子全部转化为欲制得的产物,即原子利用率为100%。在用CH3C≡CH合成CH2===C(CH3)COOCH3(二者物质的量比为1∶1)的过程中,欲使原子利用率达到最高,还需要的其他反应物有
( )
A.CO和CH3OH
B.CO2和H2O
C.H2和CO2
D.CH3OH和H2
五、化学实验的微型化
10.如图所示,在注射器中加入少量Na2SO3晶体,并吸入少量的浓硫酸(以不接触纸条为准)。
则下列有关说法正确的是
( )
A.蓝色石蕊试纸先变红后褪色
B.蘸有KMnO4溶液的滤纸褪色,证明了SO2的漂白性
C.品红试纸褪色,证明了SO2的漂白性
D.蘸有酚酞和NaOH溶液的滤纸褪色,证明了SO2的漂白性
11.向足量的氯化亚铁溶液中加入少量(1~2滴)液溴,振荡后溶液变为黄色。
Ⅰ.(1)甲同学认为是Br2单质溶于水,溶液才变成黄色;乙认为是Fe2+被氧化成Fe3+,使溶液变成黄色。
(2)请根据提供的试剂作出判断:
A.酸性高锰酸钾溶液
B.氢氧化钠溶液
C.四氯化碳
D.硫氰化钾溶液
两个同学的观点正确的是________(填“甲”或“乙”),并用两种方法(原理不同)进行实验,写出选用的试剂编号及实验中观察到的现象:
选用试剂
实验现象
第一种方法
第二种方法
(3)若选用淀粉 碘化钾溶液判断哪位同学的
( http: / / www.21cnjy.com )推断是否可行?若可行,本问不需要回答,若不可行,请说明原因。____________________________________________________
__________________________________________________________________________。
Ⅱ.若要把溶解于水中的Br2单质分离出来,所需要的主要玻璃仪器是________,该操作的名称是__________。
六、综合应用题
12.下图是验证氯酸钾和浓盐酸反应的装置,乙、丙是师生对实验改进后的装置[已知:
KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O]:
(1)
和装置甲相比,装置乙的优点是____________________________________________
__________________________________________________________________________。
(2)
和装置B相比,装置D制备氯气的优点是____________________________________
__________________________________________________________________________。
(3)为了进一步验证氯气和水的反应,某学生设计了装置丙。如何控制弹簧夹才能使氯气充满集气瓶F?
(4)当气体充满集气瓶F后,欲使装置E中的水进入集气瓶F应如何操作?
13.电解原理在化学工业中有着广泛的应用。如图所示为一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答下列问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式是____________________________________________。
在X极附近观察到的现象是__________________________________________________。
②Y极上的电极反应式是____________________________________________________,
检验该电极反应产物的方法是________________________________________________。
(2)如果用电解的方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是__________,电极反应式是__________________________________。
②Y电极的材料是__________,电极反应式是__________________________________。
(说明:杂质发生的电极反应不必写出)
14.甲、乙两同学进行课外实验,各
( http: / / www.21cnjy.com )取250
mL无色透明饮料瓶一个,依次加入4
g氢氧化钠、4
g葡萄糖、半瓶水、3滴0.2%的亚甲基蓝溶液旋上瓶塞振荡,溶液呈蓝色,静置后溶液变为无色。甲再次振荡,又呈蓝色,静置后又变为无色,多次反复可重现上述现象。而乙在蓝色消失后,向瓶内加满水旋上瓶塞,振荡却不再出现蓝色,乙认为是物质浓度不同引起的。甲设计并完成了一个实验,否定了乙的说法。
你认为甲实验的操作和现象是________________________________________________。
振荡后出现的蓝色主要与________有关(填写化学式,下同);蓝色消失又与___________有关。
答案
1.B 2.D 3.C 4.A 5.B
6.C 7.D 8.B 9.A 10.C
11.Ⅰ.(2)乙 从左到右,从上到下:C 有机层(下层)无色 D 溶液变为血红色
(3)不可行;因为Br2和Fe3+都能把I-氧化成I2
Ⅱ.分液漏斗 萃取、分液
12.(1)有吸收氯气的装置C,防止污染环境
(2)有起液封作用的小试管,防止氯气从长颈漏斗中逸出
(3)关闭b,打开a、c。
(4)先关闭a、c,后打开b,再用手捂热集气瓶F(或其他合理答案)。
13.(1)①2H++2e-===H2↑ 有气泡冒出,溶液变红
②2Cl--2e-===Cl2↑
把湿润的淀粉 碘化钾试纸放在Y电极附近,试纸变成蓝色
(2)①纯铜 Cu2++2e-===Cu ②粗铜 Cu-2e-===Cu2+
14.将乙瓶中溶液倒掉一半(一部分)后振荡即可出现蓝色(或乙瓶中通入氧气或空气,即可出现蓝色) O2 C6H12O6(或葡萄糖)
同课章节目录
- 第一单元 从实验走进化学
- 课题一 实验化学起步
- 实验1-1 蓝瓶子实验
- 课题二 化学实验的绿色追求
- 实验1-2 氯气的生成及其性质的微型实验
- 实验1-3 污水处理--电浮选凝聚法
- 第二单元 物质的获取
- 课题一 物质的分离和提纯
- 实验2-1 纸上层析分离甲基橙和酚酞
- 实验2-2 海水的蒸馏
- 实验2-3 从海带中提取碘
- 课题二 物质的制备
- 实验2-4 硫酸亚铁铵的制备
- 实验2-5 乙酸乙酯的制备及反应条件探究
- 实验2-6 氢氧化铝的制备
- 第三单元 物质的检测
- 课题一 物质的检验
- 实验3-1 几种无机离子的检验
- 实验3-2 几种有机物的检验
- 实验3-3 植物体中某些元素的检验
- 课题二 物质含量的测定
- 实验3-4 酸碱滴定曲线的测绘
- 实验3-5 比色法测定抗贫血药物中铁的含量
- 实验3-6 食醋中总酸量的测定
- 第四单元 研究型实验
- 课题一 物质性质的研究
- 实验4-1 纯净物与混合物性质的比较
- 实验4-2 金属镁、铝、锌化学性质的探究
- 课题二 身边化学问题的探究
- 实验4-3 含氯消毒液性质、作用的探究
- 实验4-4 饮料的研究
