《硫酸亚铁铵的制备》课件
图片预览






文档简介
课件18张PPT。硫 酸 亚 铁 铵 的 制备实验原理:亚铁盐在空气中易被氧化,但形成复盐硫酸亚铁铵FeSO4·(NH4)2SO4·6H2O后可稳定存在。
FeSO4 + (NH4)2SO4 + 6H2O =
FeSO4·(NH4)2SO4·6H2O
而硫酸亚铁可由铁屑和稀硫酸反应制得。
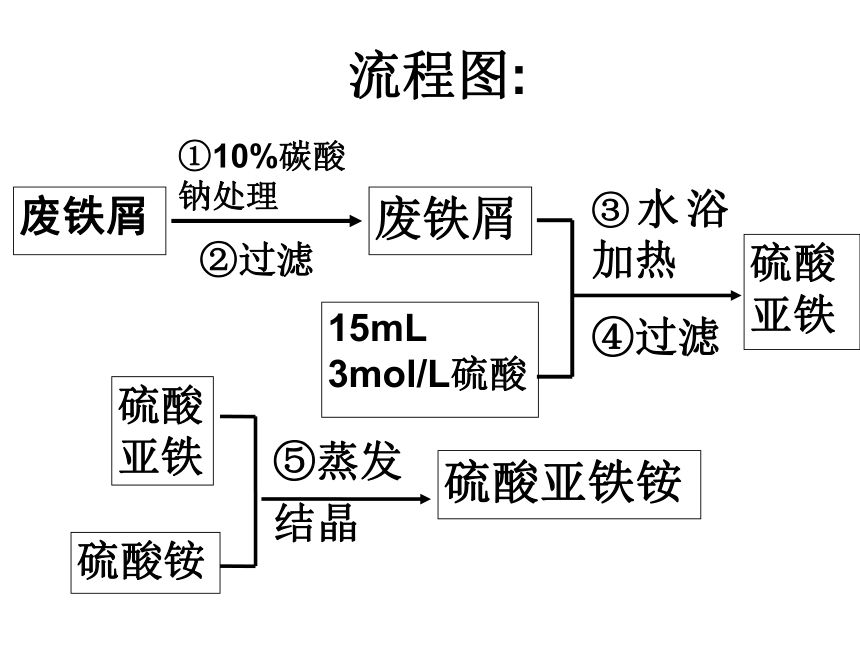
Fe + H2SO4 = FeSO4 + H2↑流程图:废铁屑废铁屑①10%碳酸
钠处理②过滤15mL
3mol/L硫酸硫酸
亚铁④过滤③水浴加热硫酸
亚铁硫酸铵⑤蒸发
结晶硫酸亚铁铵计算产率:
计算得理论产量应为为19.6g。实际称得产品约12.2g 。产率约为62% 。不过因为产品是用滤纸压干,会混有水份,实际产率应更低些。实验体会:
1. 制备硫酸亚铁时要保持铁过量,水浴加热。
2. 硫酸亚铁铵的制备:加入硫酸铵后,应使其充分溶解后再往下进行。这样有利于保证产品的纯度。蒸发时要缓缓加热,以防局部过热。
3. 实验过程中应保持足够的酸度。如果溶液的酸性减弱,则亚铁盐(或铁盐)中Fe2+与水作用的程度将会增大。在制备(NH4)2SO4·FeSO4·6H2O过程中,为了使Fe2+ 不与水作用,溶液需要保持足够的酸度。
FeSO4 + (NH4)2SO4 + 6H2O =
FeSO4·(NH4)2SO4·6H2O
而硫酸亚铁可由铁屑和稀硫酸反应制得。
Fe + H2SO4 = FeSO4 + H2↑流程图:废铁屑废铁屑①10%碳酸
钠处理②过滤15mL
3mol/L硫酸硫酸
亚铁④过滤③水浴加热硫酸
亚铁硫酸铵⑤蒸发
结晶硫酸亚铁铵计算产率:
计算得理论产量应为为19.6g。实际称得产品约12.2g 。产率约为62% 。不过因为产品是用滤纸压干,会混有水份,实际产率应更低些。实验体会:
1. 制备硫酸亚铁时要保持铁过量,水浴加热。
2. 硫酸亚铁铵的制备:加入硫酸铵后,应使其充分溶解后再往下进行。这样有利于保证产品的纯度。蒸发时要缓缓加热,以防局部过热。
3. 实验过程中应保持足够的酸度。如果溶液的酸性减弱,则亚铁盐(或铁盐)中Fe2+与水作用的程度将会增大。在制备(NH4)2SO4·FeSO4·6H2O过程中,为了使Fe2+ 不与水作用,溶液需要保持足够的酸度。
同课章节目录
- 专题一 物质的分离与提纯
- 课题1 海带中碘元素的分离及检验
- 拓展课题1-1 茶叶中某些元素的鉴定
- 课题2 用纸层析法分离铁离子和铜离子
- 拓展课题1-2 菠菜的叶绿体中色素的提取和分离
- 拓展课题1-3 用粉笔进行层析分离
- 课题3 硝酸钾晶体的制备
- 拓展课题1-4 粗盐提纯
- 专题二 物质性质的研究
- 课题1 铝及其化合物的性质
- 拓展课题2-1 铝热反应
- 课题2 乙醇和苯酚的性质
- 拓展课题2-2 苯酚与甲醛的反应
- 专题三 物质的检验与鉴别
- 课题1 牙膏和火柴中某些成分的检验
- 拓展课题3-1 新装修居室内空气中甲醛浓度的检测
- 拓展课题3-2 汽车尾气成分的检验
- 课题2 亚硝酸钠和食盐的鉴别
- 拓展课题3-3 真假碘盐的鉴别
- 专题四 化学反应条件的控制
- 课题1 硫代硫酸钠与酸反应速率的影响因素
- 拓展课题4-1 “蓝瓶子”实验
- 课题2 催化剂对过氧化氢分解反应速率的影响
- 拓展课题4-2 过氧化氢酶的催化作用
- 拓展课题4-3 蔗糖的燃烧
- 课题3 反应条件对化学平衡的影响
- 拓展课题4-4 淀粉与碘显色现象的探究
- 拓展课题4-5 压强对化学平衡的影响
- 专题五 电化学问题研究
- 课题1 原电池
- 拓展课题5-1 干电池模拟实验
- 课题2 电解与电镀
- 拓展课题5-2 阿伏加德罗常数的测定
- 专题六 物质的定量分析
- 课题1 食醋总酸含量的测定
- 拓展课题6-1 配制并标定氢氧化钠溶液
- 课题2 镀锌铁皮锌镀层厚度的测定
- 拓展课题6-2 水果中维生素C含量的测定
- 专题七 物质的制备与合成
- 课题1 硫酸亚铁铵的制备
- 拓展课题7-1 用制氢废液制备硫酸锌晶体
- 课题2 阿司匹林的合成
- 拓展课题7-2 对氨基苯磺酸的合成
