高二化学人教版选修6第二单元 课题二 物质的制备 第1课时练习(含解析)
文档属性
| 名称 | 高二化学人教版选修6第二单元 课题二 物质的制备 第1课时练习(含解析) |
|
|
| 格式 | zip | ||
| 文件大小 | 4.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-04-26 00:00:00 | ||
图片预览


文档简介
自我小测
1.在实验室里用铁屑、氧化铜、稀硫酸为原料制备铜,有下列两种途径:(1)FeH2Cu
(2)CuOCuSO4Cu
若用这两种方法制得等量的铜,下列说法符合实际情况的是( )。
A.消耗氧化铜的质量相同
B.消耗铁的质量相同
C.消耗稀硫酸的质量相同
D.生成硫酸亚铁的质量相同
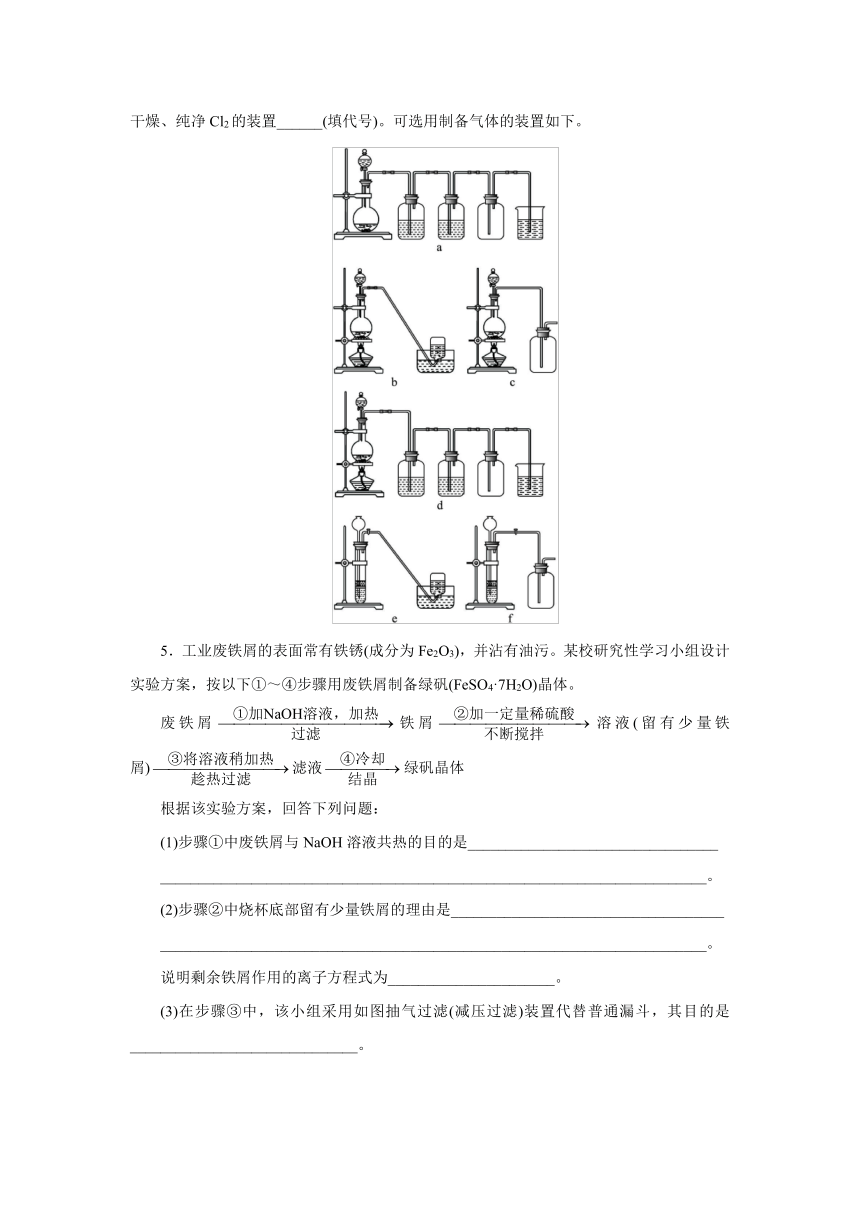
2.用下列装置制取并收集NO2气体,其中最合理的是( )。
3.如图装置可以用来发生、洗涤、干燥、收集(不考虑尾气处理)气体。该装置可用于( )。
A.锌和盐酸反应生成氢气
B.二氧化锰和浓盐酸反应生成氯气
C.碳酸钙和盐酸反应生成二氧化碳
D.氯化钠和浓硫酸反应生成氯化氢
4.实验室制备H2和Cl2通常采用下列反应:
Zn+H2SO4===ZnSO4+H2↑
MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O
据此,从下列所给仪器装置中选择制备并收集H2的装置______(填代号)和制备并收集干燥、纯净Cl2的装置______(填代号)。可选用制备气体的装置如下。
5.工业废铁屑的表面常有铁锈(成分为Fe2O3),并沾有油污。某校研究性学习小组设计实验方案,按以下①~④步骤用废铁屑制备绿矾(FeSO4·7H2O)晶体。
废铁屑铁屑溶液(留有少量铁屑)滤液绿矾晶体
根据该实验方案,回答下列问题:
(1)步骤①中废铁屑与NaOH溶液共热的目的是_________________________________
________________________________________________________________________。
(2)步骤②中烧杯底部留有少量铁屑的理由是____________________________________
________________________________________________________________________。
说明剩余铁屑作用的离子方程式为______________________。
(3)在步骤③中,该小组采用如图抽气过滤(减压过滤)装置代替普通漏斗,其目的是______________________________。
(4)检查步骤③的滤液中没有Fe3+的方法是__________________。
6.一水硫酸四氨合铜(Ⅱ)的化学式为[Cu(NH3)4]SO4·H2O,是一种重要的染料及农药中间体。某学习小组在实验室以氧化铜为主要原料合成该物质,设计的合成路线为:
相关信息如下:
①[Cu(NH3)4]SO4·H2O在溶液中存在以下电离(解离)过程:[Cu(NH3)4]SO4·H2O===[Cu(NH3)4]2+++H2O
[Cu(NH3)4]2+Cu2++4NH3
②(NH4)2SO4在水中可溶,在乙醇中难溶。
③[Cu(NH3)4]SO4·H2O在乙醇—水混合溶剂中的溶解度随乙醇体积分数的变化曲线如下图所示:
请根据以上信息回答下列问题:
(1)方案1的实验步骤为:
a.加热蒸发
b.冷却结晶
c.抽滤
d.洗涤
e.干燥①步骤c的抽滤装置如下图所示,该装置中的错误之处是______________;抽滤完毕或中途需停止抽滤时,应先______________,然后__________________________________。
②该方案存在明显缺陷,因为得到的产物晶体中往往含有______杂质,产生该杂质可能的原因是________________________。
(2)方案2的实验步骤为:
a.向溶液C中加入适量______,b.______,c.洗涤,d.干燥。
①请在上述空格内填写合适的试剂或操作名称。
②下列选项中,最适合作为步骤c的洗涤液是______。
A.乙醇B.蒸馏水
C.乙醇和水的混合液
D.饱和硫酸钠溶液
③步骤d不宜采用加热干燥的方法,可能的原因是_____________________________。
参考答案
1.答案:A 解析:用H2还原CuO时,需要先通入H2排出系统中的空气,反应完毕后也要使Cu在H2气流中冷却,故B、C、D错误。
2.答案:C 解析:铜与浓硝酸反应的产物是NO2,其密度比空气的密度大。因此利用排空气法收集NO2气体时,导气管应长进短出,这样才能将装置中的空气排尽,只有C项符合。
3.答案:A 解析:A中用水吸收H2中混有的HCl气体,然后用向下排气法收集H2是可行的;B中因Cl2的密度大于空气的密度,应用向上排气法收集,且制Cl2反应需要加热;C中CO2不可用向下排气法收集;D中NaCl与浓硫酸反应制HCl需加热,HCl极易溶于水,且密度比空气的密度大,故应用向上排气法收集且不能用水净化。4.答案:e d
解析:考虑所给反应物质的状态与气体的性质选用气体发生和收集的装置。制备氢气不需加热,且锌粒为固体颗粒;氢气难溶于水,其密度比空气的小,因此只有e正确。制备氯气需要加热,氯气可溶于水,且氯气中混有氯化氢和水蒸气,故需选用d装置。
5.答案:(1)除去铁屑表面的油污
(2)防止Fe2+被氧化 2Fe3++Fe===3Fe2+
(3)使吸滤瓶内的压强减小,提高过滤的速度,减少滤液与空气的接触,避免Fe2+被氧化等
(4)取少许滤液,加入KSCN溶液,无血红色出现
解析:制备FeSO4·7H2O晶体,关键是要避免Fe2+被空气氧化,利用抽气过滤,可提高过滤速度,趁热过滤还可以防止FeSO4结晶。
6.答案:(1)①布氏漏斗的颈口斜面未朝向抽滤瓶的支管口
断开连接安全瓶与抽气装置间的橡皮管
关闭抽气装置中的水龙头
②Cu(OH)2或Cu2(OH)2SO4
加热蒸发过程中NH3挥发,使反应[Cu(NH3)4]2+Cu2++4NH3平衡往右移动,且Cu2+发生水解
(2)①乙醇 抽滤(或减压过滤、吸滤)
②C ③加热易使[Cu(NH3)4]SO4·H2O分解(失H2O,失NH3)
解析:(1)①停止抽滤时为防止水倒吸应先断开抽滤瓶和安全瓶,然后关闭水龙头。②根据平衡移动原理和Cu2+的水解知识,可知该杂质为Cu(OH)2[或Cu2(OH)2SO4]。(2)由信息可知(NH4)2SO4在水中可溶,在乙醇中难溶,而一水硫酸四氨合铜(Ⅱ)在乙醇和水的混合溶剂中溶解度随乙醇体积分数增大而减小,故可在溶液C中加入适量乙醇使[Cu(NH3)4]SO4·H2O析出,使(NH4)2SO4仍留在溶液中。洗涤晶体时为除去晶体表面吸附的杂质离子又不减少产物,可用乙醇和水的混合液作洗涤液。
1.在实验室里用铁屑、氧化铜、稀硫酸为原料制备铜,有下列两种途径:(1)FeH2Cu
(2)CuOCuSO4Cu
若用这两种方法制得等量的铜,下列说法符合实际情况的是( )。
A.消耗氧化铜的质量相同
B.消耗铁的质量相同
C.消耗稀硫酸的质量相同
D.生成硫酸亚铁的质量相同
2.用下列装置制取并收集NO2气体,其中最合理的是( )。
3.如图装置可以用来发生、洗涤、干燥、收集(不考虑尾气处理)气体。该装置可用于( )。
A.锌和盐酸反应生成氢气
B.二氧化锰和浓盐酸反应生成氯气
C.碳酸钙和盐酸反应生成二氧化碳
D.氯化钠和浓硫酸反应生成氯化氢
4.实验室制备H2和Cl2通常采用下列反应:
Zn+H2SO4===ZnSO4+H2↑
MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O
据此,从下列所给仪器装置中选择制备并收集H2的装置______(填代号)和制备并收集干燥、纯净Cl2的装置______(填代号)。可选用制备气体的装置如下。
5.工业废铁屑的表面常有铁锈(成分为Fe2O3),并沾有油污。某校研究性学习小组设计实验方案,按以下①~④步骤用废铁屑制备绿矾(FeSO4·7H2O)晶体。
废铁屑铁屑溶液(留有少量铁屑)滤液绿矾晶体
根据该实验方案,回答下列问题:
(1)步骤①中废铁屑与NaOH溶液共热的目的是_________________________________
________________________________________________________________________。
(2)步骤②中烧杯底部留有少量铁屑的理由是____________________________________
________________________________________________________________________。
说明剩余铁屑作用的离子方程式为______________________。
(3)在步骤③中,该小组采用如图抽气过滤(减压过滤)装置代替普通漏斗,其目的是______________________________。
(4)检查步骤③的滤液中没有Fe3+的方法是__________________。
6.一水硫酸四氨合铜(Ⅱ)的化学式为[Cu(NH3)4]SO4·H2O,是一种重要的染料及农药中间体。某学习小组在实验室以氧化铜为主要原料合成该物质,设计的合成路线为:
相关信息如下:
①[Cu(NH3)4]SO4·H2O在溶液中存在以下电离(解离)过程:[Cu(NH3)4]SO4·H2O===[Cu(NH3)4]2+++H2O
[Cu(NH3)4]2+Cu2++4NH3
②(NH4)2SO4在水中可溶,在乙醇中难溶。
③[Cu(NH3)4]SO4·H2O在乙醇—水混合溶剂中的溶解度随乙醇体积分数的变化曲线如下图所示:
请根据以上信息回答下列问题:
(1)方案1的实验步骤为:
a.加热蒸发
b.冷却结晶
c.抽滤
d.洗涤
e.干燥①步骤c的抽滤装置如下图所示,该装置中的错误之处是______________;抽滤完毕或中途需停止抽滤时,应先______________,然后__________________________________。
②该方案存在明显缺陷,因为得到的产物晶体中往往含有______杂质,产生该杂质可能的原因是________________________。
(2)方案2的实验步骤为:
a.向溶液C中加入适量______,b.______,c.洗涤,d.干燥。
①请在上述空格内填写合适的试剂或操作名称。
②下列选项中,最适合作为步骤c的洗涤液是______。
A.乙醇B.蒸馏水
C.乙醇和水的混合液
D.饱和硫酸钠溶液
③步骤d不宜采用加热干燥的方法,可能的原因是_____________________________。
参考答案
1.答案:A 解析:用H2还原CuO时,需要先通入H2排出系统中的空气,反应完毕后也要使Cu在H2气流中冷却,故B、C、D错误。
2.答案:C 解析:铜与浓硝酸反应的产物是NO2,其密度比空气的密度大。因此利用排空气法收集NO2气体时,导气管应长进短出,这样才能将装置中的空气排尽,只有C项符合。
3.答案:A 解析:A中用水吸收H2中混有的HCl气体,然后用向下排气法收集H2是可行的;B中因Cl2的密度大于空气的密度,应用向上排气法收集,且制Cl2反应需要加热;C中CO2不可用向下排气法收集;D中NaCl与浓硫酸反应制HCl需加热,HCl极易溶于水,且密度比空气的密度大,故应用向上排气法收集且不能用水净化。4.答案:e d
解析:考虑所给反应物质的状态与气体的性质选用气体发生和收集的装置。制备氢气不需加热,且锌粒为固体颗粒;氢气难溶于水,其密度比空气的小,因此只有e正确。制备氯气需要加热,氯气可溶于水,且氯气中混有氯化氢和水蒸气,故需选用d装置。
5.答案:(1)除去铁屑表面的油污
(2)防止Fe2+被氧化 2Fe3++Fe===3Fe2+
(3)使吸滤瓶内的压强减小,提高过滤的速度,减少滤液与空气的接触,避免Fe2+被氧化等
(4)取少许滤液,加入KSCN溶液,无血红色出现
解析:制备FeSO4·7H2O晶体,关键是要避免Fe2+被空气氧化,利用抽气过滤,可提高过滤速度,趁热过滤还可以防止FeSO4结晶。
6.答案:(1)①布氏漏斗的颈口斜面未朝向抽滤瓶的支管口
断开连接安全瓶与抽气装置间的橡皮管
关闭抽气装置中的水龙头
②Cu(OH)2或Cu2(OH)2SO4
加热蒸发过程中NH3挥发,使反应[Cu(NH3)4]2+Cu2++4NH3平衡往右移动,且Cu2+发生水解
(2)①乙醇 抽滤(或减压过滤、吸滤)
②C ③加热易使[Cu(NH3)4]SO4·H2O分解(失H2O,失NH3)
解析:(1)①停止抽滤时为防止水倒吸应先断开抽滤瓶和安全瓶,然后关闭水龙头。②根据平衡移动原理和Cu2+的水解知识,可知该杂质为Cu(OH)2[或Cu2(OH)2SO4]。(2)由信息可知(NH4)2SO4在水中可溶,在乙醇中难溶,而一水硫酸四氨合铜(Ⅱ)在乙醇和水的混合溶剂中溶解度随乙醇体积分数增大而减小,故可在溶液C中加入适量乙醇使[Cu(NH3)4]SO4·H2O析出,使(NH4)2SO4仍留在溶液中。洗涤晶体时为除去晶体表面吸附的杂质离子又不减少产物,可用乙醇和水的混合液作洗涤液。
同课章节目录
- 第一单元 从实验走进化学
- 课题一 实验化学起步
- 实验1-1 蓝瓶子实验
- 课题二 化学实验的绿色追求
- 实验1-2 氯气的生成及其性质的微型实验
- 实验1-3 污水处理--电浮选凝聚法
- 第二单元 物质的获取
- 课题一 物质的分离和提纯
- 实验2-1 纸上层析分离甲基橙和酚酞
- 实验2-2 海水的蒸馏
- 实验2-3 从海带中提取碘
- 课题二 物质的制备
- 实验2-4 硫酸亚铁铵的制备
- 实验2-5 乙酸乙酯的制备及反应条件探究
- 实验2-6 氢氧化铝的制备
- 第三单元 物质的检测
- 课题一 物质的检验
- 实验3-1 几种无机离子的检验
- 实验3-2 几种有机物的检验
- 实验3-3 植物体中某些元素的检验
- 课题二 物质含量的测定
- 实验3-4 酸碱滴定曲线的测绘
- 实验3-5 比色法测定抗贫血药物中铁的含量
- 实验3-6 食醋中总酸量的测定
- 第四单元 研究型实验
- 课题一 物质性质的研究
- 实验4-1 纯净物与混合物性质的比较
- 实验4-2 金属镁、铝、锌化学性质的探究
- 课题二 身边化学问题的探究
- 实验4-3 含氯消毒液性质、作用的探究
- 实验4-4 饮料的研究
