高二化学人教版选修6第二单元 课题二 物质的制备 第2课时 练习题(含解析)
文档属性
| 名称 | 高二化学人教版选修6第二单元 课题二 物质的制备 第2课时 练习题(含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-04-26 00:00:00 | ||
图片预览


文档简介
自我小测
1.不能用水浴加热的实验是( )。
A.苯的硝化反应
B.银镜反应
C.制酚醛树脂
D.由乙醇制乙烯
2.下列实验方案合理的是( )。
制取乙酸乙酯的简易装置
A.配制50
g质量分数为5%NaCl溶液:将45
mL水加入到盛有5
g
NaCl的烧杯中,搅拌溶解
B.制备乙酸乙酯:用如上图所示的实验装置
C.鉴定:向溶液中加入盐酸酸化的氯化钡溶液
D.鉴别环己烯和苯:将溴的四氯化碳溶液分别滴加到少量环己烯和苯中
3.1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125
℃,反应装置如下图。下列对该实验的描述错误的是( )。
A.不能用水浴加热
B.长玻璃管起冷凝回流作用
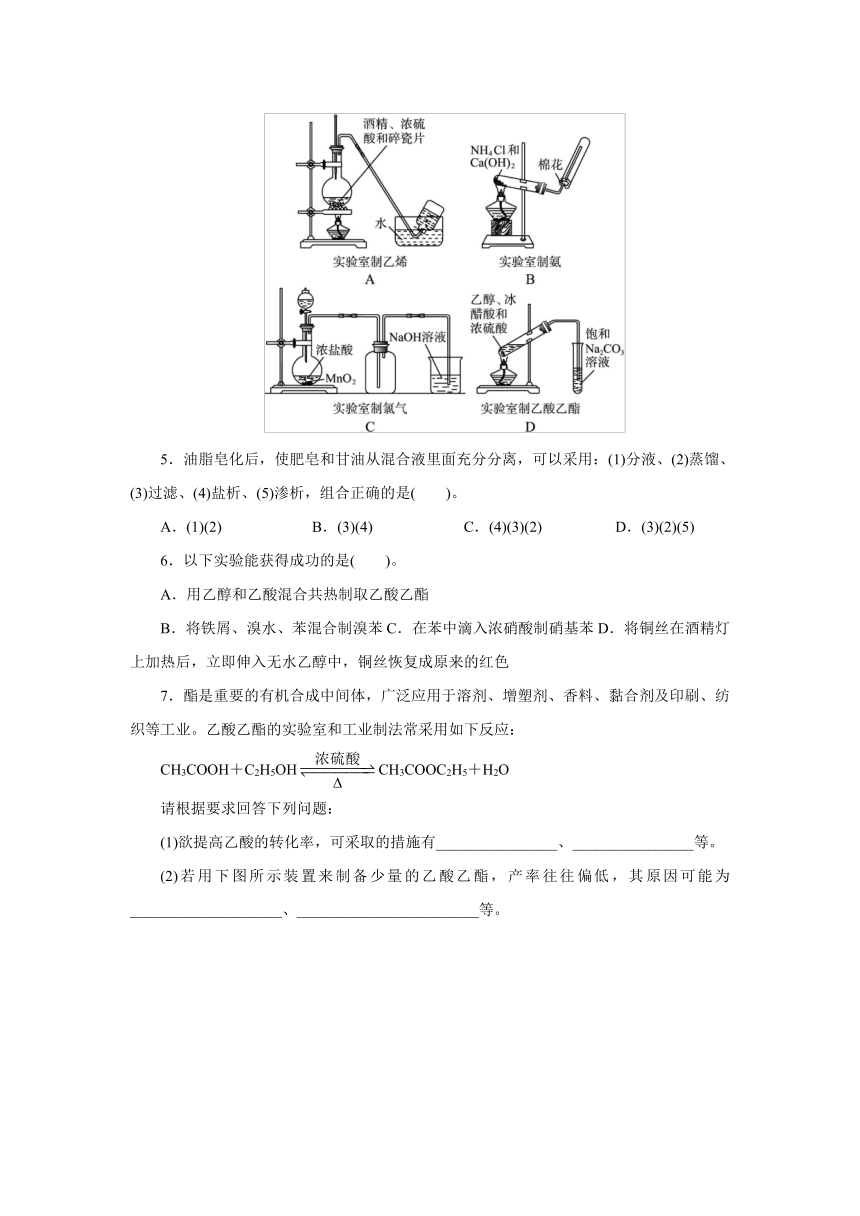
C.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤D.加入过量乙酸可以提高1-丁醇的转化率4.下列实验装置图正确的是( )。
5.油脂皂化后,使肥皂和甘油从混合液里面充分分离,可以采用:(1)分液、(2)蒸馏、(3)过滤、(4)盐析、(5)渗析,组合正确的是( )。
A.(1)(2)
B.(3)(4)
C.(4)(3)(2)
D.(3)(2)(5)
6.以下实验能获得成功的是( )。
A.用乙醇和乙酸混合共热制取乙酸乙酯
B.将铁屑、溴水、苯混合制溴苯C.在苯中滴入浓硝酸制硝基苯D.将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色
7.酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、黏合剂及印刷、纺织等工业。乙酸乙酯的实验室和工业制法常采用如下反应:
CH3COOH+C2H5OHCH3COOC2H5+H2O
请根据要求回答下列问题:
(1)欲提高乙酸的转化率,可采取的措施有________________、________________等。
(2)若用下图所示装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为____________________、________________________等。
(3)此反应以浓硫酸为催化剂,可能会造成________、________等问题。
(4)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可作此反应的催化剂,且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)。
同一反应时间
反应温度/℃
转化率(%)
选择性(%)
40
77.8
100
60
92.3
100
80
92.6
100
120
94.5
98.7
同一反应温度
反应时间/h
转化率(%)
选择性(%)
2
80.2
100
3
87.8
100
4
92.3
100
6
93.0
100
选择性100%表示反应生成的产物是乙酸乙酯和水
①根据表中数据,下列________(填字母)为该反应的最佳条件。
A.120
℃,4
h
B.80
℃,2
h
C.60
℃,4
h
D.40
℃,3
h
②当反应温度达到120
℃时,反应选择性降低的原因可能为________________。
8.某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯。
已知:
密度/(g·cm-3)
熔点/℃
沸点/℃
溶解性
环己醇
0.96
25
161
能溶于水
环己烯
0.81
-103
83
难溶于水
将12.5
mL环己醇加入试管A中,再加入1
mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
(1)A中碎瓷片的作用是________,导管B除了导气外还具有的作用是________。
(2)试管C置于冰水浴中的目的是____________________________。
(3)环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在______层(填“上”或“下”),分液后用________(填入编号)洗涤。
a.KMnO4溶液
b.稀硫酸
c.Na2CO3溶液
(4)再将环己烯进行蒸馏,可得环己烯精品。蒸馏时要加入生石灰,目的是____________________。
9.实验室用乙酸和正丁醇制备乙酸正丁酯。有关物质的物理性质如下表。请回答有关问题。
化合物
密度/(g·cm-3)
沸点/℃
溶解度/100
g水
正丁醇
0.810
118.0
9
冰醋酸
1.049
118.1
任意比互溶
乙酸正丁酯
0.882
126.1
0.7
Ⅰ.乙酸正丁酯粗产品的制备。
在干燥的50
mL圆底烧瓶中,装入沸石,加入11.5
mL正丁醇和9.4
mL冰醋酸,再加3~4滴浓硫酸。然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热使其反应。
(1)本实验过程中可能产生多种有机副产物,写出其中两种的结构简式:________、________。
(2)实验中为了提高乙酸正丁酯的产率,采取的措施是__________________________、__________________________。
Ⅱ.乙酸正丁酯精品的制备。
(1)将乙酸正丁酯粗产品用如下的操作进行精制:①水洗 ②蒸馏 ③用无水MgSO4干燥 ④用10%碳酸钠洗涤
正确的操作步骤是________(填字母)。
A.①②③④
B.③①④②
C.①④①③②
D.④①③②③
(2)将酯层采用如下图所示装置蒸馏。
①写出上图中仪器A的名称________。冷却水从________口进入(填字母)。
②蒸馏收集乙酸正丁酯产品时,应将温度控制在________左右。
参考答案
1.答案:D 解析:乙醇制乙烯的实验需170
℃,而水浴加热最高为100
℃。苯的硝化反应用50~60
℃水浴加热,银镜反应用热水浴加热,制酚醛树脂用沸水浴加热。
2.
答案:D 解析:将45
mL水加入到盛有5
g
NaCl的烧杯中,搅拌溶解,所配制的50
g溶液的质量分数为10%;制备乙酸乙酯的实验中缺少催化剂浓硫酸;向溶液中加入盐酸酸化的氯化钡溶液鉴定,无法排除Ag+的干扰;将溴的四氯化碳溶液分别滴加到少量环己烯和苯中,环己烯使溴的四氯化碳溶液褪色而苯不能,可以鉴别环己烯和苯。
3.答案:C 解析:因为反应温度为
115~125
℃,所以无法使用水浴加热,A对。反应物都具有挥发性,所以长玻璃管有冷凝回流的作用,B对。提纯时不能加氢氧化钠溶液,以防乙酸丁酯发生水解反应,C错。1-丁醇和乙酸的酯化反应是可逆反应,加入过量乙酸,可促进反应正向进行,提高1-丁醇转化率,D对。
4.
答案:B 解析:A选项,实验室制备乙烯控制乙醇的温度是关键,温度计的水银球必须置于反应混合液的液面以下;C选项,实验室制备氯气是在加热条件下反应的,由于反应在加热条件下进行,盐酸的挥发性导致一部分氯化氢气体随着氯气挥发出来,同时伴有少量的水蒸气产生,所以在收集装置前应该连有两个洗气瓶,一个装有饱和食盐水除去氯气中的氯化氢气体,一个装有浓硫酸除去氯气中的水蒸气,而该装置中没有热源和除杂装置;D选项,随着乙酸乙酯挥发出来的有乙醇和乙酸,其中乙醇极易溶于水,而乙酸又能和碳酸钠溶液反应,导管插入液面以下会产生倒吸。
5.答案:C 解析:为了使皂化后的反应液中肥皂的成分(C17H35COONa)析出,加食盐以降低其溶解度——盐析,析出的固体经过滤得到硬脂酸钠,剩余的液体中含有甘油,由于甘油易溶于水,故采用蒸馏的方法分离。
6.
答案:D 解析:A制取乙酸乙酯,应将乙醇和乙酸、浓硫酸三者混合加热;B应注意溴苯是在Fe作催化剂下,由液溴和苯混合制得的;C在苯中滴入浓硝酸和浓硫酸的混合酸后水浴加热才能制得硝基苯;铜丝在酒精灯上加热后生成CuO,CuO可把乙醇氧化为乙醛,D正确。
7.答案:(1)增大乙醇的浓度 移去生成物
(2)原料来不及反应就被蒸出 温度过高,发生了副反应 冷凝效果不好,部分产物挥发(任填两种)
(3)产生大量的酸性废液(或造成环境污染) 部分原料炭化 催化剂重复使用困难 催化效果不理想(任填两种)
(4)①C ②乙醇脱水生成乙醚
解析:(1)增大反应物的浓度,减小生成物的浓度都能促进平衡向正反应方向移动。(2)因为反应物沸点低很易蒸出,温度过高后浓硫酸会使乙醇脱水炭化而发生副反应,装置冷凝效果不好,部分产品挥发等。(3)浓硫酸有吸水性同时也有脱水性。(4)要注意认真审题,对比表中数据,不难得出答案。
8.答案:(1)防暴沸 冷凝
(2)防止环己烯挥发
(3)上层 c
(4)与水反应,利于环己烯的蒸出
解析:(1)在化学实验中,加入碎瓷片的作用是防止溶液暴沸;导管B比较长,能增加与空气的接触面积,其作用是导气和将生成的气体物质冷凝回流。(2)因为产物环己烯的沸点只有83
℃,易挥发,将其置于冰水浴中的目的是防止环己烯的挥发,减少其损失。(3)环己烯难溶于水,且密度比水小,加入饱和食盐水后,溶液分层,环己烯在上层;环己烯中含有碳碳双键,可以被KMnO4溶液氧化,稀硫酸不能除去杂质,反而能引入新的酸性杂质,只有Na2CO3溶液,既不与环己烯反应,又能除去酸性物质。(4)加入生石灰后,生石灰可以与水反应,这样,再加热时就不会有水挥发出来造成产品不纯。9.答案:Ⅰ.(1)CH3CH2CH2CH2OCH2CH2CH2CH3、CH2===CHCH2CH3
(2)用分水器及时移走反应生成的水,减小生成物的浓度 使用过量醋酸,提高正丁醇的转化率
Ⅱ.(1)C (2)①冷凝管
g ②126.1
℃
解析:Ⅰ.(1)正丁醇在浓硫酸的作用下发生分子内或分子间的脱水等副反应,分别生成1丁烯或丁醚等;(2)实验中要提高乙酸正丁酯的产率,即使酯化反应平衡向右移动,采取的措施:一是增大另一种反应物乙酸的浓度(用量);二是减小生成物的浓度。乙酸乙酯的制取,由于乙酸乙酯的沸点低于水,采取将乙酸乙酯蒸出的措施,但本题中乙酸正丁酯的沸点比水的高,因此采用分水器及时移走反应生成的水的措施。Ⅱ.(1)乙酸正丁酯粗产品中含有的杂质:乙酸、正丁醇、水、丁醚等,分析题目给出的四种操作:①水洗、②蒸馏、③用无水MgSO4干燥、④用10%碳酸钠洗涤,结合操作的难易、顺序和必要性,如干燥要放在水洗或10%碳酸钠洗涤之后,蒸馏操作复杂,一般放在最后等,可知正确的操作步骤是①④①③②,即C选项正确。
1.不能用水浴加热的实验是( )。
A.苯的硝化反应
B.银镜反应
C.制酚醛树脂
D.由乙醇制乙烯
2.下列实验方案合理的是( )。
制取乙酸乙酯的简易装置
A.配制50
g质量分数为5%NaCl溶液:将45
mL水加入到盛有5
g
NaCl的烧杯中,搅拌溶解
B.制备乙酸乙酯:用如上图所示的实验装置
C.鉴定:向溶液中加入盐酸酸化的氯化钡溶液
D.鉴别环己烯和苯:将溴的四氯化碳溶液分别滴加到少量环己烯和苯中
3.1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125
℃,反应装置如下图。下列对该实验的描述错误的是( )。
A.不能用水浴加热
B.长玻璃管起冷凝回流作用
C.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤D.加入过量乙酸可以提高1-丁醇的转化率4.下列实验装置图正确的是( )。
5.油脂皂化后,使肥皂和甘油从混合液里面充分分离,可以采用:(1)分液、(2)蒸馏、(3)过滤、(4)盐析、(5)渗析,组合正确的是( )。
A.(1)(2)
B.(3)(4)
C.(4)(3)(2)
D.(3)(2)(5)
6.以下实验能获得成功的是( )。
A.用乙醇和乙酸混合共热制取乙酸乙酯
B.将铁屑、溴水、苯混合制溴苯C.在苯中滴入浓硝酸制硝基苯D.将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色
7.酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、黏合剂及印刷、纺织等工业。乙酸乙酯的实验室和工业制法常采用如下反应:
CH3COOH+C2H5OHCH3COOC2H5+H2O
请根据要求回答下列问题:
(1)欲提高乙酸的转化率,可采取的措施有________________、________________等。
(2)若用下图所示装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为____________________、________________________等。
(3)此反应以浓硫酸为催化剂,可能会造成________、________等问题。
(4)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可作此反应的催化剂,且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)。
同一反应时间
反应温度/℃
转化率(%)
选择性(%)
40
77.8
100
60
92.3
100
80
92.6
100
120
94.5
98.7
同一反应温度
反应时间/h
转化率(%)
选择性(%)
2
80.2
100
3
87.8
100
4
92.3
100
6
93.0
100
选择性100%表示反应生成的产物是乙酸乙酯和水
①根据表中数据,下列________(填字母)为该反应的最佳条件。
A.120
℃,4
h
B.80
℃,2
h
C.60
℃,4
h
D.40
℃,3
h
②当反应温度达到120
℃时,反应选择性降低的原因可能为________________。
8.某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯。
已知:
密度/(g·cm-3)
熔点/℃
沸点/℃
溶解性
环己醇
0.96
25
161
能溶于水
环己烯
0.81
-103
83
难溶于水
将12.5
mL环己醇加入试管A中,再加入1
mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
(1)A中碎瓷片的作用是________,导管B除了导气外还具有的作用是________。
(2)试管C置于冰水浴中的目的是____________________________。
(3)环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在______层(填“上”或“下”),分液后用________(填入编号)洗涤。
a.KMnO4溶液
b.稀硫酸
c.Na2CO3溶液
(4)再将环己烯进行蒸馏,可得环己烯精品。蒸馏时要加入生石灰,目的是____________________。
9.实验室用乙酸和正丁醇制备乙酸正丁酯。有关物质的物理性质如下表。请回答有关问题。
化合物
密度/(g·cm-3)
沸点/℃
溶解度/100
g水
正丁醇
0.810
118.0
9
冰醋酸
1.049
118.1
任意比互溶
乙酸正丁酯
0.882
126.1
0.7
Ⅰ.乙酸正丁酯粗产品的制备。
在干燥的50
mL圆底烧瓶中,装入沸石,加入11.5
mL正丁醇和9.4
mL冰醋酸,再加3~4滴浓硫酸。然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热使其反应。
(1)本实验过程中可能产生多种有机副产物,写出其中两种的结构简式:________、________。
(2)实验中为了提高乙酸正丁酯的产率,采取的措施是__________________________、__________________________。
Ⅱ.乙酸正丁酯精品的制备。
(1)将乙酸正丁酯粗产品用如下的操作进行精制:①水洗 ②蒸馏 ③用无水MgSO4干燥 ④用10%碳酸钠洗涤
正确的操作步骤是________(填字母)。
A.①②③④
B.③①④②
C.①④①③②
D.④①③②③
(2)将酯层采用如下图所示装置蒸馏。
①写出上图中仪器A的名称________。冷却水从________口进入(填字母)。
②蒸馏收集乙酸正丁酯产品时,应将温度控制在________左右。
参考答案
1.答案:D 解析:乙醇制乙烯的实验需170
℃,而水浴加热最高为100
℃。苯的硝化反应用50~60
℃水浴加热,银镜反应用热水浴加热,制酚醛树脂用沸水浴加热。
2.
答案:D 解析:将45
mL水加入到盛有5
g
NaCl的烧杯中,搅拌溶解,所配制的50
g溶液的质量分数为10%;制备乙酸乙酯的实验中缺少催化剂浓硫酸;向溶液中加入盐酸酸化的氯化钡溶液鉴定,无法排除Ag+的干扰;将溴的四氯化碳溶液分别滴加到少量环己烯和苯中,环己烯使溴的四氯化碳溶液褪色而苯不能,可以鉴别环己烯和苯。
3.答案:C 解析:因为反应温度为
115~125
℃,所以无法使用水浴加热,A对。反应物都具有挥发性,所以长玻璃管有冷凝回流的作用,B对。提纯时不能加氢氧化钠溶液,以防乙酸丁酯发生水解反应,C错。1-丁醇和乙酸的酯化反应是可逆反应,加入过量乙酸,可促进反应正向进行,提高1-丁醇转化率,D对。
4.
答案:B 解析:A选项,实验室制备乙烯控制乙醇的温度是关键,温度计的水银球必须置于反应混合液的液面以下;C选项,实验室制备氯气是在加热条件下反应的,由于反应在加热条件下进行,盐酸的挥发性导致一部分氯化氢气体随着氯气挥发出来,同时伴有少量的水蒸气产生,所以在收集装置前应该连有两个洗气瓶,一个装有饱和食盐水除去氯气中的氯化氢气体,一个装有浓硫酸除去氯气中的水蒸气,而该装置中没有热源和除杂装置;D选项,随着乙酸乙酯挥发出来的有乙醇和乙酸,其中乙醇极易溶于水,而乙酸又能和碳酸钠溶液反应,导管插入液面以下会产生倒吸。
5.答案:C 解析:为了使皂化后的反应液中肥皂的成分(C17H35COONa)析出,加食盐以降低其溶解度——盐析,析出的固体经过滤得到硬脂酸钠,剩余的液体中含有甘油,由于甘油易溶于水,故采用蒸馏的方法分离。
6.
答案:D 解析:A制取乙酸乙酯,应将乙醇和乙酸、浓硫酸三者混合加热;B应注意溴苯是在Fe作催化剂下,由液溴和苯混合制得的;C在苯中滴入浓硝酸和浓硫酸的混合酸后水浴加热才能制得硝基苯;铜丝在酒精灯上加热后生成CuO,CuO可把乙醇氧化为乙醛,D正确。
7.答案:(1)增大乙醇的浓度 移去生成物
(2)原料来不及反应就被蒸出 温度过高,发生了副反应 冷凝效果不好,部分产物挥发(任填两种)
(3)产生大量的酸性废液(或造成环境污染) 部分原料炭化 催化剂重复使用困难 催化效果不理想(任填两种)
(4)①C ②乙醇脱水生成乙醚
解析:(1)增大反应物的浓度,减小生成物的浓度都能促进平衡向正反应方向移动。(2)因为反应物沸点低很易蒸出,温度过高后浓硫酸会使乙醇脱水炭化而发生副反应,装置冷凝效果不好,部分产品挥发等。(3)浓硫酸有吸水性同时也有脱水性。(4)要注意认真审题,对比表中数据,不难得出答案。
8.答案:(1)防暴沸 冷凝
(2)防止环己烯挥发
(3)上层 c
(4)与水反应,利于环己烯的蒸出
解析:(1)在化学实验中,加入碎瓷片的作用是防止溶液暴沸;导管B比较长,能增加与空气的接触面积,其作用是导气和将生成的气体物质冷凝回流。(2)因为产物环己烯的沸点只有83
℃,易挥发,将其置于冰水浴中的目的是防止环己烯的挥发,减少其损失。(3)环己烯难溶于水,且密度比水小,加入饱和食盐水后,溶液分层,环己烯在上层;环己烯中含有碳碳双键,可以被KMnO4溶液氧化,稀硫酸不能除去杂质,反而能引入新的酸性杂质,只有Na2CO3溶液,既不与环己烯反应,又能除去酸性物质。(4)加入生石灰后,生石灰可以与水反应,这样,再加热时就不会有水挥发出来造成产品不纯。9.答案:Ⅰ.(1)CH3CH2CH2CH2OCH2CH2CH2CH3、CH2===CHCH2CH3
(2)用分水器及时移走反应生成的水,减小生成物的浓度 使用过量醋酸,提高正丁醇的转化率
Ⅱ.(1)C (2)①冷凝管
g ②126.1
℃
解析:Ⅰ.(1)正丁醇在浓硫酸的作用下发生分子内或分子间的脱水等副反应,分别生成1丁烯或丁醚等;(2)实验中要提高乙酸正丁酯的产率,即使酯化反应平衡向右移动,采取的措施:一是增大另一种反应物乙酸的浓度(用量);二是减小生成物的浓度。乙酸乙酯的制取,由于乙酸乙酯的沸点低于水,采取将乙酸乙酯蒸出的措施,但本题中乙酸正丁酯的沸点比水的高,因此采用分水器及时移走反应生成的水的措施。Ⅱ.(1)乙酸正丁酯粗产品中含有的杂质:乙酸、正丁醇、水、丁醚等,分析题目给出的四种操作:①水洗、②蒸馏、③用无水MgSO4干燥、④用10%碳酸钠洗涤,结合操作的难易、顺序和必要性,如干燥要放在水洗或10%碳酸钠洗涤之后,蒸馏操作复杂,一般放在最后等,可知正确的操作步骤是①④①③②,即C选项正确。
同课章节目录
- 第一单元 从实验走进化学
- 课题一 实验化学起步
- 实验1-1 蓝瓶子实验
- 课题二 化学实验的绿色追求
- 实验1-2 氯气的生成及其性质的微型实验
- 实验1-3 污水处理--电浮选凝聚法
- 第二单元 物质的获取
- 课题一 物质的分离和提纯
- 实验2-1 纸上层析分离甲基橙和酚酞
- 实验2-2 海水的蒸馏
- 实验2-3 从海带中提取碘
- 课题二 物质的制备
- 实验2-4 硫酸亚铁铵的制备
- 实验2-5 乙酸乙酯的制备及反应条件探究
- 实验2-6 氢氧化铝的制备
- 第三单元 物质的检测
- 课题一 物质的检验
- 实验3-1 几种无机离子的检验
- 实验3-2 几种有机物的检验
- 实验3-3 植物体中某些元素的检验
- 课题二 物质含量的测定
- 实验3-4 酸碱滴定曲线的测绘
- 实验3-5 比色法测定抗贫血药物中铁的含量
- 实验3-6 食醋中总酸量的测定
- 第四单元 研究型实验
- 课题一 物质性质的研究
- 实验4-1 纯净物与混合物性质的比较
- 实验4-2 金属镁、铝、锌化学性质的探究
- 课题二 身边化学问题的探究
- 实验4-3 含氯消毒液性质、作用的探究
- 实验4-4 饮料的研究
