陕西省黄陵中学高新部2016-2017学年高一下学期期中考试化学试题 Word版含答案
文档属性
| 名称 | 陕西省黄陵中学高新部2016-2017学年高一下学期期中考试化学试题 Word版含答案 |  | |
| 格式 | zip | ||
| 文件大小 | 346.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-05-05 08:48:28 | ||
图片预览



文档简介
黄陵中学高新部2016-2017学年度第二学期期中考试
高一化学试题
一、选择题(本题包括18个小题,每小题只有一个选项符合题意,每小题3分,共54分)
1.下列叙述不正确的是( )
A.根据一次能源和二次能源的划分,氢气为二次能源
B.电能是现代社会中应用最广泛、使用最方便、污染最小的一种二次能源
C.火力发电是将燃料中的化学能直接转变为电能的过程
D.在火力发电过程中,化学能转化为热能的过程实际上是氧化还原反应发生的过程,伴随着能量的变化
2.对于锌、铜和稀硫酸组成的原电池(如右图),下列有关说法不正确的是
( )
( http: / / www.21cnjy.com )
A.Zn是负极
B.Cu是正极
C.负极上发生氧化反应
D.正极上发生氧化反应
3.下列说法正确的是( )
A.原电池是把电能转变成化学能的装置
B.原电池中电子流出的一极是正极,发生氧化反应
C.原电池两极均发生氧化反应和还原反应
D.原电池内部的阳离子向正极移动
4.如图所示,两电极一极为碳棒,一极为铁片,若电流表的指针发生偏转,且a极上有大量气泡生成,则以下叙述正确的是( )
( http: / / www.21cnjy.com )
A.a为负极,是铁片,烧杯中的溶液为硫酸
B.b为负极,是铁片,烧杯中的溶液为硫酸铜溶液
C.a为正极,是碳棒,烧杯中的溶液为硫酸
D.b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液
5.某原电池的总反应的离子方程式是Zn+Cu2+===Zn2++Cu,则该反应的原电池组成正确的是( )
选项
A
B
C
D
正极
Zn
Cu
Ag
Cu
负极
Cu
Zn
Cu
Fe
电解质溶液
CuCl2
CuSO4
H2SO4
ZnCl2
6.化学反应A2+B2===2AB的能量变化如图所示,则下列说法正确的是( )
( http: / / www.21cnjy.com )
A.该反应是吸热反应
B.断裂1
mol
A—A键和1
mol
B—B键放出x
kJ能量
C.断裂2
mol
A—B键需要吸收y
kJ的能量
D.2
mol
AB的总能量高于1
mol
A2和1
mol
B2的总能量
7.已知2SO2+O22SO3为放热反应,对该反应的下列说法正确的是( )
A.O2的能量一定高于SO2的能量
B.2
mol
SO2和1
mol
O2的总能量一定高于2
mol
SO3的总能量
C.SO2的能量一定高于SO3的能量
D.因该反应为放热反应,故不必加热就可发生
8.下列变化中属于吸热反应的是( )
①液态水汽化 ②将胆矾加热变为白色粉末
( http: / / www.21cnjy.com )③苛性钠固体溶于水 ④氯酸钾分解制氧气 ⑤生石灰跟水反应生成熟石灰 ⑥干冰升华
A.①④
B.②④
C.③⑤
D.④⑥
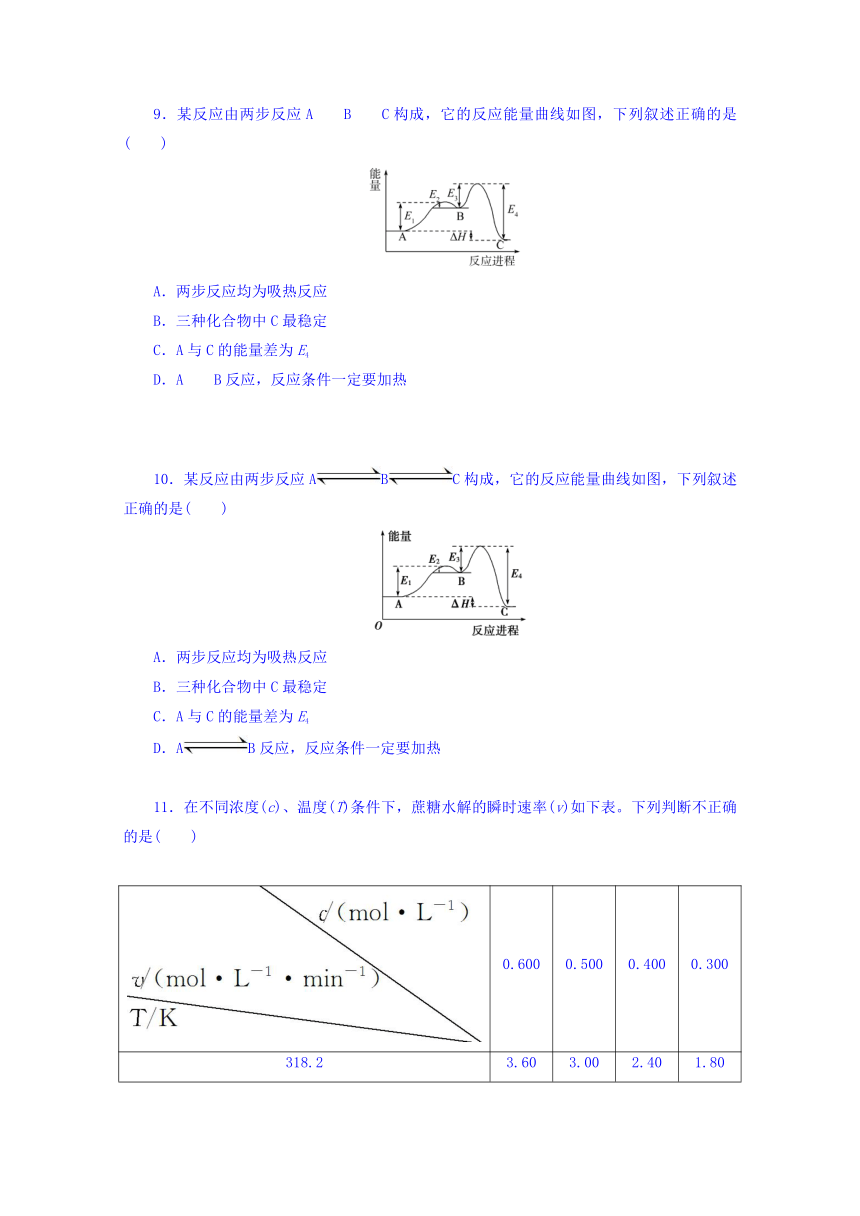
9.某反应由两步反应A??B??C构成,它的反应能量曲线如图,下列叙述正确的是( )
( http: / / www.21cnjy.com )
A.两步反应均为吸热反应
B.三种化合物中C最稳定
C.A与C的能量差为E4
D.A??B反应,反应条件一定要加热
10.某反应由两步反应ABC构成,它的反应能量曲线如图,下列叙述正确的是( )
( http: / / www.21cnjy.com )
A.两步反应均为吸热反应
B.三种化合物中C最稳定
C.A与C的能量差为E4
D.AB反应,反应条件一定要加热
11.在不同浓度(c)、温度(T)条件下,蔗糖水解的瞬时速率(v)如下表。下列判断不正确的是( )
( http: / / www.21cnjy.com )
0.600
0.500
0.400
0.300
318.2
3.60
3.00
2.40
1.80
328.2
9.00
7.50
a
4.50
b
2.16
1.80
1.44
1.08
A.a=6.00
B.同时改变反应温度和蔗糖的浓度,v可能不变
C.b<318.2
D.不同温度时,蔗糖浓度减少一半所需的时间相同
12.把下列4种X的溶液,分别加入盛有10
( http: / / www.21cnjy.com )
mL
2
mol/L的盐酸的烧杯中,并均加水稀释至50
mL,此时X和盐酸缓慢地进行反应,其中反应速率最大的是( )
A.20
mL,2
mol/L
B.20
mL,3
mol/L
C.10
mL,5
mol/L
D.10
mL,3
mol/L
13.向四个体积相同的密闭容器中分别充入一定量的SO2和O2,开始反应时,按反应速率由大到小的排列顺序正确的是( )
甲:500
℃,10
mol
SO2和5
mol
O2反应
乙:500
℃,V2O5作催化剂,10
mol
SO2和5
mol
O2反应
丙:450
℃,8
mol
SO2和5
mol
O2反应
丁:500
℃,8
mol
SO2和5
mol
O2反应
A.甲、乙、丙、丁
B.乙、甲、丙、丁
C.乙、甲、丁、丙
D.丁、丙、乙、甲
14.如图为氢氧燃料电池原理示意图,根据此图的提示,下列叙述不正确的是( )
( http: / / www.21cnjy.com )
A.a电极是负极
B.b电极的电极反应为4OH--4e-===2H2O+O2↑
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部贮存在电池内的新型发电装置
15.分子式为C4H10O并能与金属钠反应放出氢气的有机物有(不含立体异构)( )
A.3种
B.4种
C.5种
D.6种
16.结合乙烯和乙醇的结构与性质,推测丙烯醇
(CH2=CH-CH2OH)不能发生的化学反应有( )
A.加成反应
B.氧化反应
C.与Na反应
D.与Na2CO3溶液反应放出CO2
17.酒后驾车是引发交通事故的重要原因。交
( http: / / www.21cnjy.com )警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2O7酸性水溶液遇乙醇迅速生成蓝绿色Cr3+。下列对乙醇的描述与此测定原理有关的是( )
①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性 ④乙醇是烃的含氧衍生物
A.②④
B.②③
C.①③
D.①④
18.在常压和100
℃条
( http: / / www.21cnjy.com )件下,把乙醇汽化为蒸气,然后和乙烯以任意比例混合,混合气体的体积为V
L。将其完全燃烧,需消耗相同条件下的氧气的体积是( )
A.2V
L
B.2.5V
L
C.3V
L
D.无法计算
二、(46分)
19.(8分).燃料乙醇的生产过程可用下图表示:
( http: / / www.21cnjy.com )
(1)粉碎玉米的目的是______________________________________________。
(2)生产过程中为了检验淀粉水解是否完全,可使用的试剂是________________。
(3)步骤a的操作是________。
A.蒸发
B.萃取
C.蒸馏
D.分液
(4)发酵产生的CO2纯度可达到99%
( http: / / www.21cnjy.com ),能回收利用,请举出它的两项用途:______________、______________。
20.(8分)化学式为C2H6O的化合物A具有如下性质:
A+Na―→慢慢产生气泡
A+CH3COOH有香味的产物
(1)根据上述信息,对该化合物可作出的判断是________________。
A.一定含有—OH
B.一定含有—COOH
C.A为乙醇
D.A为乙醛
(2)含A的体积分数为75%的水溶液可以用作__________________________________。
(3)A与钠反应的化学方程式:_______________________________________
________________________________________________________________________。
(4)化合物A与CH3COOH反应生成的有香味的产物的结构简式为__________________。
21.(14分)有关催化剂的催化机
( http: / / www.21cnjy.com )理等问题可以从“乙醇催化氧化实验”中得到一些认识。某教师设计了如图所示装置(夹持装置等已省略),实验操作:先按图安装好实验装置,关闭活塞a、b、c,在铜丝的中间部分加热片刻,然后打开活塞a、b、c,通过控制活塞a和b,有节奏(间歇性)地通入气体,即可在M处观察到明显的实验现象。
( http: / / www.21cnjy.com )
试回答以下问题:
(1)A瓶中发生反应的化学方程式为_________________________
______________,B的作用是_____________________________
______________,C中热水的作用是______________________。
(2)M管中发生反应的化学方程式为______________________。
(3)从M管中可观察到的现象是__________________________
________________,从中可认识
( http: / / www.21cnjy.com )到该实验过程中催化剂________(填“参加”或“不参加”)化学反应,还可以认识到催化剂起催化作用需要一定的________。
(4)实验进行一段时间后,
( http: / / www.21cnjy.com )如果撤掉酒精灯,反应________(填“能”或“不能”)继续进行,其原因是____________________
_____________________________________________________。
22.(10分)某化学兴趣小组为了探究铝电极在电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
( http: / / www.21cnjy.com )
回答下列问题:
(1)实验1、2中Al所作的电极(指正极或负极)________(填“相同”或“不同”)。
(2)对实验3完成下列填空:
①铝为________极,电极反应式为___________________________。
②石墨为________极,电极反应式为__________________________。
③电池总反应式为________________________________。
(3)实验4中铝作________极(填“负”或“正”),理由是_______________。
此反应的离子方程式为_________________________。
(4)根据实验结果总结出影响铝在原电池
( http: / / www.21cnjy.com )中作正极或负极的因素为____________________________________________________________。
23.(6分)将V1
mL
1.0
m
( http: / / www.21cnjy.com )ol·L-1
HCl溶液和V2
mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50
mL)。请按要求填空:
( http: / / www.21cnjy.com )
(1)该实验表明此反应________(填“吸收”或“释放”)能量,即:________能可以转化为________能,通过图示分析可以得出:做该实验时,环境温度________(填“高于”、“低于”或“等于”)22
℃。
(2)根据图示计算该NaOH溶液的浓度约是________mol·L-1。
(3)如图所示,在锥形瓶放置有装有水的小
( http: / / www.21cnjy.com )试管,往小试管中分别加入下列物质时:①烧碱固体 ②浓硫酸 ③硝酸铵固体 ④NaCl固体,其中能使a端液面高于b端液面的是________(填序号)。
( http: / / www.21cnjy.com )
参考答案
1-5.CDDCB
6-10.CBBB
11-15.DBCBB
16-18
.DCC
19.答案 (1)增大反应物的接触面
( http: / / www.21cnjy.com )积或加快反应速率或使反应充分进行 (2)碘(I2)或碘酒或(答案合理即可) (3)C
(4)制饮料、制干冰、制纯碱、制碳酸钙(其他碳酸盐或碳酸氢盐)等中任选2个
20.答案 (1)AC
(2)医用消毒剂
(3)2Na+2CH3CH2OH―→2CH3CH2ONa+H2↑
(4)CH3COOCH2CH3
答案:(1)2H2O22H2O+O2
( http: / / www.21cnjy.com )↑ 干燥O2 使D中乙醇变为蒸气进入M管参加反应,并且用水浴加热能使乙醇气流更平稳 (2)2CH3CH2OH+O22CH3CHO+2H2O (3)受热部分的铜丝交替出现变黑、变红的现象 参加 温度 (4)能 该反应是放热反应,反应放出的热量能维持该反应的进行
22.【答案】 (1)不同
(2)①负 2Al-6e-===2Al3+ ②正 6H++6e-===3H2↑ ③2Al+6H+===2Al3++3H2↑
(3)负 铝与NaOH溶液可以发生自发的氧化还原反应 2Al+2OH-+2H2O===2AlO+3H2↑
(4)另一电极材料的活动性和电解质溶液的氧化性
【解析】 (1)当5
mL
H
( http: / / www.21cnjy.com )Cl和45
mL
NaOH反应时,此时最终溶液的温度为22
℃,所以做该实验时,环境温度应低于22
℃。(2)30
mL
HCl和20
mL
NaOH恰好完全反应,c(NaOH)==1.5
mol·L-1。(3)当a端高于b端时,则c处压强减小,温度降低,所以只有硝酸铵固体合适。
【答案】 (1)释放 化学 热 低于 (2)1.5 (3)③
高一化学试题
一、选择题(本题包括18个小题,每小题只有一个选项符合题意,每小题3分,共54分)
1.下列叙述不正确的是( )
A.根据一次能源和二次能源的划分,氢气为二次能源
B.电能是现代社会中应用最广泛、使用最方便、污染最小的一种二次能源
C.火力发电是将燃料中的化学能直接转变为电能的过程
D.在火力发电过程中,化学能转化为热能的过程实际上是氧化还原反应发生的过程,伴随着能量的变化
2.对于锌、铜和稀硫酸组成的原电池(如右图),下列有关说法不正确的是
( )
( http: / / www.21cnjy.com )
A.Zn是负极
B.Cu是正极
C.负极上发生氧化反应
D.正极上发生氧化反应
3.下列说法正确的是( )
A.原电池是把电能转变成化学能的装置
B.原电池中电子流出的一极是正极,发生氧化反应
C.原电池两极均发生氧化反应和还原反应
D.原电池内部的阳离子向正极移动
4.如图所示,两电极一极为碳棒,一极为铁片,若电流表的指针发生偏转,且a极上有大量气泡生成,则以下叙述正确的是( )
( http: / / www.21cnjy.com )
A.a为负极,是铁片,烧杯中的溶液为硫酸
B.b为负极,是铁片,烧杯中的溶液为硫酸铜溶液
C.a为正极,是碳棒,烧杯中的溶液为硫酸
D.b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液
5.某原电池的总反应的离子方程式是Zn+Cu2+===Zn2++Cu,则该反应的原电池组成正确的是( )
选项
A
B
C
D
正极
Zn
Cu
Ag
Cu
负极
Cu
Zn
Cu
Fe
电解质溶液
CuCl2
CuSO4
H2SO4
ZnCl2
6.化学反应A2+B2===2AB的能量变化如图所示,则下列说法正确的是( )
( http: / / www.21cnjy.com )
A.该反应是吸热反应
B.断裂1
mol
A—A键和1
mol
B—B键放出x
kJ能量
C.断裂2
mol
A—B键需要吸收y
kJ的能量
D.2
mol
AB的总能量高于1
mol
A2和1
mol
B2的总能量
7.已知2SO2+O22SO3为放热反应,对该反应的下列说法正确的是( )
A.O2的能量一定高于SO2的能量
B.2
mol
SO2和1
mol
O2的总能量一定高于2
mol
SO3的总能量
C.SO2的能量一定高于SO3的能量
D.因该反应为放热反应,故不必加热就可发生
8.下列变化中属于吸热反应的是( )
①液态水汽化 ②将胆矾加热变为白色粉末
( http: / / www.21cnjy.com )③苛性钠固体溶于水 ④氯酸钾分解制氧气 ⑤生石灰跟水反应生成熟石灰 ⑥干冰升华
A.①④
B.②④
C.③⑤
D.④⑥
9.某反应由两步反应A??B??C构成,它的反应能量曲线如图,下列叙述正确的是( )
( http: / / www.21cnjy.com )
A.两步反应均为吸热反应
B.三种化合物中C最稳定
C.A与C的能量差为E4
D.A??B反应,反应条件一定要加热
10.某反应由两步反应ABC构成,它的反应能量曲线如图,下列叙述正确的是( )
( http: / / www.21cnjy.com )
A.两步反应均为吸热反应
B.三种化合物中C最稳定
C.A与C的能量差为E4
D.AB反应,反应条件一定要加热
11.在不同浓度(c)、温度(T)条件下,蔗糖水解的瞬时速率(v)如下表。下列判断不正确的是( )
( http: / / www.21cnjy.com )
0.600
0.500
0.400
0.300
318.2
3.60
3.00
2.40
1.80
328.2
9.00
7.50
a
4.50
b
2.16
1.80
1.44
1.08
A.a=6.00
B.同时改变反应温度和蔗糖的浓度,v可能不变
C.b<318.2
D.不同温度时,蔗糖浓度减少一半所需的时间相同
12.把下列4种X的溶液,分别加入盛有10
( http: / / www.21cnjy.com )
mL
2
mol/L的盐酸的烧杯中,并均加水稀释至50
mL,此时X和盐酸缓慢地进行反应,其中反应速率最大的是( )
A.20
mL,2
mol/L
B.20
mL,3
mol/L
C.10
mL,5
mol/L
D.10
mL,3
mol/L
13.向四个体积相同的密闭容器中分别充入一定量的SO2和O2,开始反应时,按反应速率由大到小的排列顺序正确的是( )
甲:500
℃,10
mol
SO2和5
mol
O2反应
乙:500
℃,V2O5作催化剂,10
mol
SO2和5
mol
O2反应
丙:450
℃,8
mol
SO2和5
mol
O2反应
丁:500
℃,8
mol
SO2和5
mol
O2反应
A.甲、乙、丙、丁
B.乙、甲、丙、丁
C.乙、甲、丁、丙
D.丁、丙、乙、甲
14.如图为氢氧燃料电池原理示意图,根据此图的提示,下列叙述不正确的是( )
( http: / / www.21cnjy.com )
A.a电极是负极
B.b电极的电极反应为4OH--4e-===2H2O+O2↑
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部贮存在电池内的新型发电装置
15.分子式为C4H10O并能与金属钠反应放出氢气的有机物有(不含立体异构)( )
A.3种
B.4种
C.5种
D.6种
16.结合乙烯和乙醇的结构与性质,推测丙烯醇
(CH2=CH-CH2OH)不能发生的化学反应有( )
A.加成反应
B.氧化反应
C.与Na反应
D.与Na2CO3溶液反应放出CO2
17.酒后驾车是引发交通事故的重要原因。交
( http: / / www.21cnjy.com )警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2O7酸性水溶液遇乙醇迅速生成蓝绿色Cr3+。下列对乙醇的描述与此测定原理有关的是( )
①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性 ④乙醇是烃的含氧衍生物
A.②④
B.②③
C.①③
D.①④
18.在常压和100
℃条
( http: / / www.21cnjy.com )件下,把乙醇汽化为蒸气,然后和乙烯以任意比例混合,混合气体的体积为V
L。将其完全燃烧,需消耗相同条件下的氧气的体积是( )
A.2V
L
B.2.5V
L
C.3V
L
D.无法计算
二、(46分)
19.(8分).燃料乙醇的生产过程可用下图表示:
( http: / / www.21cnjy.com )
(1)粉碎玉米的目的是______________________________________________。
(2)生产过程中为了检验淀粉水解是否完全,可使用的试剂是________________。
(3)步骤a的操作是________。
A.蒸发
B.萃取
C.蒸馏
D.分液
(4)发酵产生的CO2纯度可达到99%
( http: / / www.21cnjy.com ),能回收利用,请举出它的两项用途:______________、______________。
20.(8分)化学式为C2H6O的化合物A具有如下性质:
A+Na―→慢慢产生气泡
A+CH3COOH有香味的产物
(1)根据上述信息,对该化合物可作出的判断是________________。
A.一定含有—OH
B.一定含有—COOH
C.A为乙醇
D.A为乙醛
(2)含A的体积分数为75%的水溶液可以用作__________________________________。
(3)A与钠反应的化学方程式:_______________________________________
________________________________________________________________________。
(4)化合物A与CH3COOH反应生成的有香味的产物的结构简式为__________________。
21.(14分)有关催化剂的催化机
( http: / / www.21cnjy.com )理等问题可以从“乙醇催化氧化实验”中得到一些认识。某教师设计了如图所示装置(夹持装置等已省略),实验操作:先按图安装好实验装置,关闭活塞a、b、c,在铜丝的中间部分加热片刻,然后打开活塞a、b、c,通过控制活塞a和b,有节奏(间歇性)地通入气体,即可在M处观察到明显的实验现象。
( http: / / www.21cnjy.com )
试回答以下问题:
(1)A瓶中发生反应的化学方程式为_________________________
______________,B的作用是_____________________________
______________,C中热水的作用是______________________。
(2)M管中发生反应的化学方程式为______________________。
(3)从M管中可观察到的现象是__________________________
________________,从中可认识
( http: / / www.21cnjy.com )到该实验过程中催化剂________(填“参加”或“不参加”)化学反应,还可以认识到催化剂起催化作用需要一定的________。
(4)实验进行一段时间后,
( http: / / www.21cnjy.com )如果撤掉酒精灯,反应________(填“能”或“不能”)继续进行,其原因是____________________
_____________________________________________________。
22.(10分)某化学兴趣小组为了探究铝电极在电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
( http: / / www.21cnjy.com )
回答下列问题:
(1)实验1、2中Al所作的电极(指正极或负极)________(填“相同”或“不同”)。
(2)对实验3完成下列填空:
①铝为________极,电极反应式为___________________________。
②石墨为________极,电极反应式为__________________________。
③电池总反应式为________________________________。
(3)实验4中铝作________极(填“负”或“正”),理由是_______________。
此反应的离子方程式为_________________________。
(4)根据实验结果总结出影响铝在原电池
( http: / / www.21cnjy.com )中作正极或负极的因素为____________________________________________________________。
23.(6分)将V1
mL
1.0
m
( http: / / www.21cnjy.com )ol·L-1
HCl溶液和V2
mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50
mL)。请按要求填空:
( http: / / www.21cnjy.com )
(1)该实验表明此反应________(填“吸收”或“释放”)能量,即:________能可以转化为________能,通过图示分析可以得出:做该实验时,环境温度________(填“高于”、“低于”或“等于”)22
℃。
(2)根据图示计算该NaOH溶液的浓度约是________mol·L-1。
(3)如图所示,在锥形瓶放置有装有水的小
( http: / / www.21cnjy.com )试管,往小试管中分别加入下列物质时:①烧碱固体 ②浓硫酸 ③硝酸铵固体 ④NaCl固体,其中能使a端液面高于b端液面的是________(填序号)。
( http: / / www.21cnjy.com )
参考答案
1-5.CDDCB
6-10.CBBB
11-15.DBCBB
16-18
.DCC
19.答案 (1)增大反应物的接触面
( http: / / www.21cnjy.com )积或加快反应速率或使反应充分进行 (2)碘(I2)或碘酒或(答案合理即可) (3)C
(4)制饮料、制干冰、制纯碱、制碳酸钙(其他碳酸盐或碳酸氢盐)等中任选2个
20.答案 (1)AC
(2)医用消毒剂
(3)2Na+2CH3CH2OH―→2CH3CH2ONa+H2↑
(4)CH3COOCH2CH3
答案:(1)2H2O22H2O+O2
( http: / / www.21cnjy.com )↑ 干燥O2 使D中乙醇变为蒸气进入M管参加反应,并且用水浴加热能使乙醇气流更平稳 (2)2CH3CH2OH+O22CH3CHO+2H2O (3)受热部分的铜丝交替出现变黑、变红的现象 参加 温度 (4)能 该反应是放热反应,反应放出的热量能维持该反应的进行
22.【答案】 (1)不同
(2)①负 2Al-6e-===2Al3+ ②正 6H++6e-===3H2↑ ③2Al+6H+===2Al3++3H2↑
(3)负 铝与NaOH溶液可以发生自发的氧化还原反应 2Al+2OH-+2H2O===2AlO+3H2↑
(4)另一电极材料的活动性和电解质溶液的氧化性
【解析】 (1)当5
mL
H
( http: / / www.21cnjy.com )Cl和45
mL
NaOH反应时,此时最终溶液的温度为22
℃,所以做该实验时,环境温度应低于22
℃。(2)30
mL
HCl和20
mL
NaOH恰好完全反应,c(NaOH)==1.5
mol·L-1。(3)当a端高于b端时,则c处压强减小,温度降低,所以只有硝酸铵固体合适。
【答案】 (1)释放 化学 热 低于 (2)1.5 (3)③
同课章节目录
