第3单元《物质构成的奥秘》精品复习课件(共85张PPT)
文档属性
| 名称 | 第3单元《物质构成的奥秘》精品复习课件(共85张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 971.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-06-03 00:00:00 | ||
图片预览










文档简介
课件85张PPT。
第三单元 物质构成的奥秘
课题1 分子和原子
学习目标
1.认识分子、原子等微观粒子,了解物质是由分子、原子等微观粒子构成的;
2.认识微观粒子的性质,并能够根据微观粒子的性质解释生活中的一些现象;
3.学习一些类比、模型等科学方法,从微观角度认识物质,培养抽象、想象思维能力。
核心考点:分子、原子的概念以及性质;认识物质的微粒性;能用微粒的观点来解释某些常见现象。
课前预习
1.物质是由_______、________等粒子构成的。
2.由分子构成的物质,分子是___________________的最小粒子;原子是_______________的最小粒子。
3.分子的性质有:分子的________________非常小;分子在_____________;分子间有_________;同种分子性质_______,不同分子性质________。
分子原子保持其化学性质化学变化中质量和体积不断运动着间隔相同不同课堂精讲
知识点1.物质由微观粒子构成(对应课本P48~P49)
科学的进步,证明了物质是由_原子_、_分子_等微观粒子构成的。通过先进的科学仪器我们不仅能够观察到一些分子和原子(如图3-1),还能移动原子(如图3-2)。
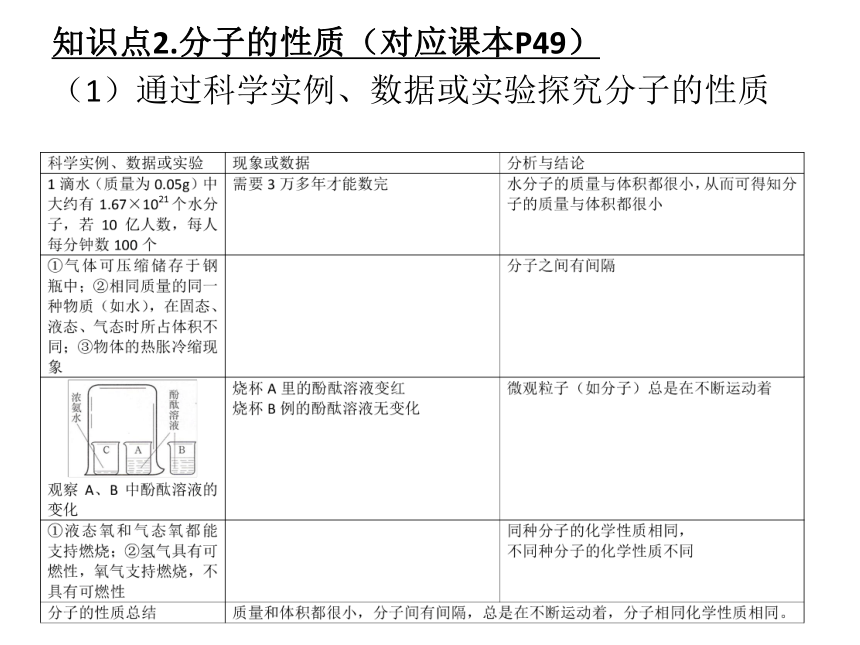
知识点2.分子的性质(对应课本P49)
(1)通过科学实例、数据或实验探究分子的性质
规律点拨:①温度越高,分子的运动速率越快,如品红在热水中的扩散速率比在冷水中的扩散速率快得多。
②通常情况下,温度越高,分子间的间隔越大;压强越大,分子间的间隔越小,如夏天充满气的自行车轮胎暴晒容易爆炸。
(2)直击广东中考
该知识点考查得较多的是“分子是在不停地运动”,运用分子的基本性质解释日常生活中的现象,是中考命题的热点,学生应该熟记分子的几个性质。
【例1】(2015?信阳校级模拟)对生活中下列现象的解释错误的是( )
变式拓展:
1.(2014?汕尾)吸烟有害健康,非吸烟者往往会因吸烟者吸烟而造成被动吸烟,这是因为( )
A.分子在不断运动 B.分子之间有间隔
C.分子的体积很小 D.分子的质量很小
2.(2014?杭州)液氧转化为氧气的过程中,发生的变化是( )
A.混合物变为纯净物 B.分子间的空隙增大
C.化学性质发生变化 D.分子总数增加
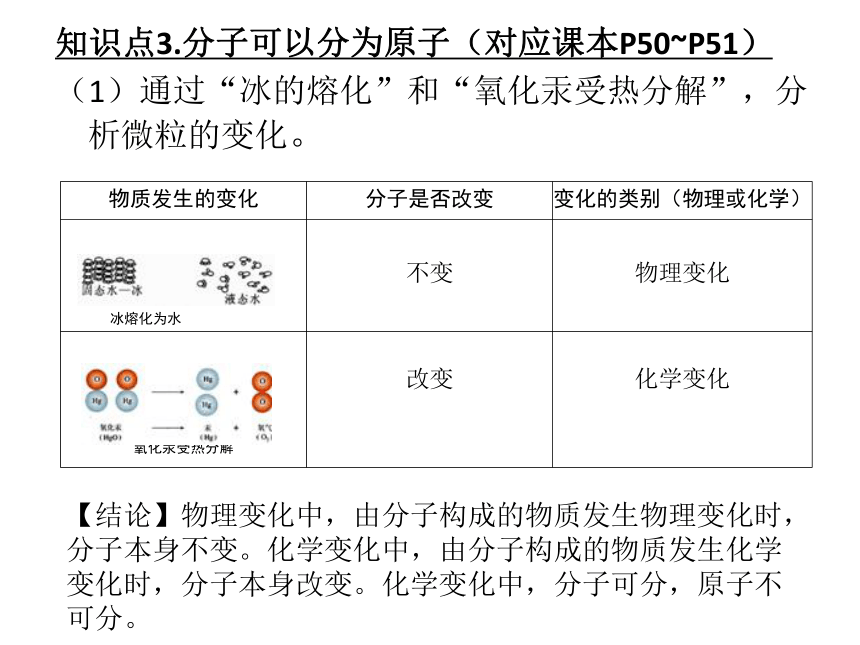
AB知识点3.分子可以分为原子(对应课本P50~P51)
(1)通过“冰的熔化”和“氧化汞受热分解”,分析微粒的变化。
【结论】物理变化中,由分子构成的物质发生物理变化时,分子本身不变。化学变化中,由分子构成的物质发生化学变化时,分子本身改变。化学变化中,分子可分,原子不可分。(2)分子的概念
由分子构成的物质在发生物理变化时,分子本身没有发生变化,它们的化学性质也各自保持不变。由分子构成的物质在发生化学变化时,一种物质的分子会变成其他物质的分子,原分子的化学性质不再保持。可见,由分子构成的物质,分子是保持其化学性质的最小粒子。
点拨:分子只能保持物质的化学性质,不能保持物质的物理性质。因为物质的物理性质(如状态、颜色)是由该物质的大量分子聚集后表现出来的性质,并不是单个分子能保持的。
(3)原子的概念
原子是化学变化中的最小粒子,在化学变化中,分子的种类可以发生变化,而原子的种类不会发生变化,只是重新结合生成了其他物质的分子。
点拨:原子也是构成物质的基本粒子之一,如金属、稀有气体是由原子直接构成的;由原子直接构成的物质,原子保持其化学性质。原子只是在化学变化中不能再分,即在化学变化中不能将原子分成更小的粒子,但脱离“化学反应”这一前提,原子可以分为更小的粒子。
(4)分子与原子的联系与区别
(5)直击广东中考
该知识点主要考查分子、原子的概念,学生最好从化学变化的微观本质角度去理解掌握,认识到化学变化的微观本质是分子分裂成原子,原子重新结合成新的分子。【例2】(2014?上海)关于原子、分子叙述错误的是( )
A.分子是由原子构成的
B.分子和原子都在不停运动
C.分子和原子在化学变化中都能够再分
D.分子和原子都是构成物质的微粒
【例3】如图3-3是表示气体分子的示意图,图中“●”“○”分别表示两种不同的原子,其中表示纯净物的是( )
图3-3
A. ①③ B. ②④ C. ③④ D. ②③
变式拓展:
3.(2015?本溪模拟)在学习分子和原子的知识后,四位同学对它们的区别作了如下发言,正确的是( )
A.小倩说“区别在于是否在不停地运动”
B.小丹说“区别在于化学反应中是否可分”
C.小鑫说“区别在于是否能够构成物质”
D.小娜说“区别在于分子和原子的大小和质量都不同”
4.(2014?始兴县校级一模)水是生命的源泉,是人类宝贵的资源。它有时能幻作朵朵白云,有时能化为绵绵细雨。下列过程中,你认为水分子发生了变化的是( )
A.水蒸气遇冷凝结成水 B.蔗糖和水混合后得到糖水
C.水通电变成氢气和氧气 D.蒸馏法淡化海水
CB随堂检测
1.(2015?枣庄模拟)图书馆常配备液态二氧化碳灭火器。使用时,打开阀门,液态二氧化碳便会迅速汽化喷出。下列对“汽化喷出”这一现象认识正确的是( )
A.分子种类发生了变化 B.分子间间隔发生了变化
C.分子大小发生了变化 D.分子的构成发生了变化
2.(2015?平凉一模)春天的柳湖公园,百花盛开,阵阵花香,沁人心脾。花香四溢的现象说明( )
A.分子是不断运动的 B.分子是由原子构成的
C.分子具有一定的质量 D.分子之间有一定的间隙
3.(2015?静安区一模)从化学的视角认识世界,下列对事实解释错误的是( )
A.食物腐败:分子发生了变化
B.热胀冷缩:分子大小随温度的变化而改变
C.花香四溢:分子不停地运动
D.氢气和氧气的性质不同:构成它们的分子不同
BBA4.(2014?祁阳县校级模拟)能保持氢气的化学性质的最小粒子是( )
A.氢原子 B.氢分子 C.两个氢原子 D.氢元素
5.(2014?衡阳模拟)能证明分子在化学反应中可以再分的变化是( )
A.碘受热变成碘蒸气
B.一定条件下用二氧化碳气体制干冰
C.块状硫研磨成硫粉
D.加热氧化汞产生氧气
6.(2014?闸北区一模)关于分子和原子的说法,正确的是( )
A.化学变化中分子种类不一定发生变化
B.不同种原子可以构成分子,同种原子不可以构成分子
C.原子也是构成物质的一种微粒
D.保持二氧化碳化学性质的最小微粒是碳原子和氧原子
BDC
课题2 原子的结构(一)
学习目标
1.了解原子的构成以及构成粒子之间的关系,了解原子结构示意图;
2.了解原子核外的电子排布,理解原子核外电子分层运动的想象。
核心考点:原子的构成;核电荷数、质子数、核外电子数之间的关系;核外电子的排布及分层运动。
课前预习
1.原子核是由______和_______两种粒子构成的。
2.原子不显电性,是因为质子数=_________=____________
3.在含有多个电子的原子中,核外电子具有不同的运动状态,离核近的电子能量较____,离核越远,电子的能力越_____。
质子中子核电荷数核外电子数低高课堂精讲
知识点1.原子的构成(对应课本P53)
(1)原子的构成
在化学变化中,原子是不可再分的最小粒子。而大量的科学实验证明,原子还是可以再分的。原子的构成如下:
质子(每个质子带1个单位正电荷)
(不带电)
核外电子 (每个电子带1个单位负电荷) 原子核 (居于原子中心)
原子 中子(2)核电荷数、质子数、核外电子数的关系
核电荷数是原子核所带的正电荷数。原子核是由质子和中子构成的,每个质子带1个单位的正电荷,中子不带电,因此原子核所带的正电荷数(核电荷数)就等于核内的质子数。原子核内质子所带的电荷与核外电子的电荷数量相等,且电性相反,每个质子带1个单位的正电荷,每个电子带1个单位的负电荷,所以质子数等于核外电子数,因此原子不显电性。
规律点拨:①在原子中:核电荷数=质子数=核外电子数;②并不是所有的原子核都是由质子和中子构成的,如氢原子核中只有质子,没有中子;③区分原子的种类的依据是原子的质子数(或核电荷数),不同种类的原子,核内的质子数(或核电荷数)不同。
(3)直击广东中考
本知识点是广东中考的高频考点,会结合后面学习的粒子结构示意图进行考察,学生在对该知识点的学习中应熟练掌握在原子结构中,质子数=核电荷数=核外电子数。
【例1】(2015?淮阳县校级一模)据中央电视台对云南抚仙湖底古城考古的现场报道,科学家曾经通过测定古生物遗骸中的碳-14来推断古城年代.碳-14原子的核电荷数为6,质子数和中子数之和为14,下列关于碳-14原子的说法中错误的是( )
A.质子数为6 B.中子数为6
C.电子数为6 D.电子数和中子数之和为14
【例2】1911年著名物理学家卢瑟福为探索原子的内部结构进行了实验。在用一束带正电的、质量比电子大得多的高速运动的α粒子轰击金箔时发现(如图3-5):
(1)大多数α粒子能穿透金箔而不改变原来的运动方向;
(2)一小部分α粒子改变了原来的运动方向;
(3)有极少部分α粒子被弹了回来。
下列对原子结构的认识错误的是( )
A.原子核体积很小
B.原子核带正电
C.原子内部有很大的空间
D.原子是实心的球体
变式拓展:
1.(2015?株洲模拟)构成原子核的粒子一定有( )
A.质子 B.中子 C.电子 D.质子和中子
2.(2015?静海县模拟)下列关于原子的叙述正确的是( )
①一切原子都是由质子、中子和电子构成的;
②原子在不停地运动;
③原子是化学变化中的最小拉子;
④原子由原子核和核外电子构成;
⑤原子中不存在电荷.因而原子不带电。
A.②③④ B.①②④
C.①③⑤ D.①②③④⑤
AA知识点2.原子核外电子的排布(对应课本P54)
(1)原子核外的电子层
在含有多个电子的原子中,核外电子具有不同的运动状态,离核近的电子能量较低,离核越远,电子的能量越高。为了方便研究,科学家形象地将这些区域称为电子层,原子核外的电子是分层排布的规律。迄今已知的原子核外电子最少的有一层,最多的有七层。
(2)核外电子的分层排布规律
核外电子的运动状态被科学家人为地分成了几个电子层,离核最近的称为第一层,离核最远的称为最外层。在每一层上的电子数是不同的:第一层最多容纳2个电子,第二层最多容纳8个电子,最外层电子数最多不超过8个(只有一层的,电子数不超过2个)。
(3)原子结构示意图
用原子结构示意图可以简明、方便地表示核外电子的分层排布,其各部分的意义如图3-6所示。
图3-6
(4)直击广东中考
该知识点为广东中考的高频考点,根据粒
子结构来推断粒子的种类,或确定质子数、核电
荷数、核外电子数等都是常考的题型,常与后面
学习的元素周期表结合考查,学生应掌握原子结
构示意图中各个部分所代表的意义。
原子核
质子数
第一电子层
第二电子层 第三电子层(最外电子层)【例3】(2014秋?滕州市校级月考)某粒子的结构示意图如图3-7所示,对该粒子的说法错误的是( )
A.核电荷数为12
B.核外有3个电子层
C.第3层上的电子携带的能量最高
D.圆圈代表电子
变式拓展:
3.下面是五种原子的结构示意图:
A. B. C.
(1)A原子中,质子数为______,电子层数为______,最外层电子数为______,电子总数为_______;
(2)B原子中,x=_______;C原子中,X=______
171737156随堂检测
1.原子是由( )
A.电子和质子构成的
B.质子和中子构成的
C.电子和中子构成的
D.原子核和电子构成的
2.一种硫原子中共有48个粒子,其中16个不带电,则它的电子数为( )
A.48 B.16 C.32 D.16
3.某原子的原子核内有1个质子和2个中子,则该原子的核电荷数为( )
A.1 B.3 C.2 D.无法判断
4.(2015?漳州模拟改编)下列关于原子的叙述中,不正确的是( )
A.原子可以构成分子
B.原子是化学反应中的最小微粒
C.原子是由原子核和核外电子构成的
D.原子不带电是因为原子中存在中子
DBAD5.某原子的结构示意图为 ,下列有关的叙述中,错误的是( )
A.质子数为12 B.核电荷数为11
B.电子层数为3 D.核外电子数为12
6.钠原子和氯原子的结构示意图如图3-8:
(1)钠原子原子核内有_______质子,
有_____电子层,第一层有________个电
子,最外层电子层上有_____个电子。
(2)氯原子的核电荷数是________
(3)钠原子与氯原子相同的是_______(填序号)
①质子数 ②电子数 ③电子层数 ④最外层电子数
B1132117 ③
课题2 原子的结构(二)
学习目标
1.了解原子的核外电子排布与性质之间的关系,了解典型元素(稀有气体、金属、非金属)原子核外电子的排布特点;
2.以氯化钠为例,了解离子形成;
3.了解相对原子质量的含义。
核心考点:原子核外电子排布与性质的关系;离子的形成;相对原子质量。
课前预习
1.原子的化学性质主要取决于原子的__________,最外层电子数为8个电子(第一层为最外层的是2个电子)的被认为是一种_________________。
2.离子的定义是:_______________________________。带正电的称为______,带负电的称为__________。
3. 以一种碳原子质量的1/12为标准,其他原子的质量与它相比较所得到的比,作为这种原子的________________,原子的质量主要集中在________上。
最外层电子数相对稳定的结构带电的原子叫做离子阳离子阴离子相对原子质量原子核课堂精讲
知识点1.原子结构与性质的关系
稀有气体原子的最外层电子数一般为8个(氦为2个);金属原子最外层电子数一般少于4个,在化学反应中易失电子;非金属原子的最外层电子数一般多于或等于4个,在化学反应中易得电子。
原子的化学性质主要取决于原子的最外层电子数。原子最外层电子数为8个电子(第一层为最外层的是2个电子)的被认为是一种相对稳定的结构。原子都趋于达到相对稳定的结构。
【例1】原子的化学性质主要取决于原子的最外层电子数。
(1)如图3-9所示,该原子的核电
荷数为______,名称是__________
,由它组成的物质被称为______气体,
化学性质_________
(2)下列原子结构属于稳定结构的是__________(填序号,下同);②粒子的化学性质与①、③、④、⑤粒子中 的化学性质相似,它们在化学反应中都容易 (填“得”或“失”)电子。
变式拓展:
1.(2014秋?酒泉校级期中)根据下列原子结构示意图判断,化学性质最相似的两种元素是( )
①和② B. ①和④
C. ②和③ D. ③和④
B知识点2.离子
(1)离子的定义:带电的原子(或原子团),如Na+、Cl-、NO3-。离子也是构成物质的粒子之一。
(2)离子的形成
①金属原子的最外层电子一般少于4个,在化学反应中易失电子,核电荷数大于核外电子数,带正电荷,为阳离子;
②非金属原子的最外层电子一般多于4个,在化学反应中易得电子,核电荷数少于核外电子数,带负电荷,为阴离子。
(3)离子化合物的形成过程
以氯化钠的形成过程为例,钠原子的最外层有1个电子,氯原子的最外层有7个电子,当钠与氯反应时,钠原子最外层的1个电子转移到氯原子的最外层上,二者在静电作用下相互结合,形成氯化钠。如图3-10所示。
图3-10
(4)离子的符号书写
在元素符号(或原子团)的右上角标明离子所带的电荷,数值在前,正、负号在后。当离子带1个单位的正电荷或1个单位负电荷时,“1”可以省略不写。例如,镁离子的数字“2”含义如下。
2Mg2+
【例2】根据下列微粒的结构示意图回答问题。
(1)属于稳定结构的是______(填序号,下同);
(2)D原子属于______(“金属”或“非金属”)原子,易______电子,形成_____离子。
(3)属于原子的是__________,属于阳离子的是_______,属于阴离子的是________
解析:原子最外层电子数为8个电子(第一层为最外层的是2个电子)的被认为是一种相对稳定的结构。金属原子的最外层电子一般少于4个,容易失去电子,形成阳离子。
【例3】下列符号能表示2个氧离子的是( )
A.2O2-
B.2O2
C.2O
D.O2
变式拓展:
2.(2014?巴中)下列对微粒的描述中,不正确的是( )
B.
易失电子 易形成阴离子
C. D.
阳离子 化学性质稳定
C知识点3.相对原子质量
(1)概念:以一种碳原子(原子核中含有6个质子和6个中子)质量的1/12为标准,其他原子的质量与它相比较所得到的比,作为这种原子的相对原子质量,符号为Ar。
(2)单位:相对原子质量是一个比值,单位为“1”,一般不读出也不写出。
(3)原子一般由质子、中子、电子构成,质子和中子的相对质量都约等于1,与质子和中子相比,电子的质量很小,可以忽略不计,因此原子的质量主要集中在原子核上,相对原子质量在数值上约等于质子数加上中子数。
规律点拨:相对原子质量不是一个原子的实际质量,它是一个比值,能够反映一个原子实际质量的相对大小。原子的质量越大,相对原子质量越大。
(4)直击广东中考
该知识点是广东中考的重点,常以选择题、填空题、以及与后面学习的知识结合,以简单计算题的形式出现,学生应熟悉掌握相对原子质量的含义。
【例4】(2014?郴州)原子的质量主要决定于原子的( )
A.质子数 B.中子数
C.中子数和核外电子数 D.质子数和中子数
变式拓展:
3.(2014秋?滕州市月考)一种原子的核内有6个中子和6个质子,另一种原子的核内有7个中子和6个质子,则它们不同的是( )
A.质子数 B.原子的相对原子质量
C.核电荷数 D.核外电子数
4.作为相对原子质量标准的碳12原子的实际质量为m Kg,则实际质量为2m Kg的一种原子的相对原子质量是( )
A.24 B.24g C.2 D.2g
BA随堂检测
1.(2014秋?天河区期末)下列关于原子的说法,正确的是( )
A. B.
C. D.
2.(2014秋?大庆校级期中)根据相对原子质量的定义进行判断,氧原子的相对原子质量是( )
A.16g B.2.657×10﹣26kg
C.16 D.1.66×10﹣27kg
CD3.(2015?潍坊校级一模改编)根据以下图3-11的粒子结构示意图,其中说法不正确的是( )
图3-11
A.它们核电荷数都相同
B.它们的核外电子数相同
C.它们都具有相对稳定的结构
D.它们依次表示原子、离子、离子
4.(2014?红桥区校级一模)下列关于Na、Na+两种粒子的判断中,正确的是( )
①核电荷数相同;②核外电子数相等;③电子层结构完全相同;④质量几乎相等;⑤质子数相等;⑥Na+比Na稳定。
A.①④⑤ B.①③⑤⑥ C.①④⑤⑥ D.②③④
AC5.(2014?达县校级模拟改编)下列说法中错误的是( )
A.离子是由原子得到电子或失去电子而形成的
B.元素的化学性质跟原子最外层电子数目关系密切
C.一种粒子最外层电子数目为8,此粒子一定是稀有气体元素的原子
D.当原子失去或得到电子后,其性质发生了改变
6.(2014?琼海校级三模改编)据最新报道元素钬可有效地治疗肝癌,已知其相对原子质量为166,核电荷数为67,则该原子核内中子数和核外电子数分别为( )
A.166和67 B.67和99
C.166和99 D.99和67
CD
课题3 元素(一)
学习目标
1.了解元素的含义以及一些常见元素的名称与符号;
2.了解分子、原子、离子、元素之间的关系,认识物质的多样性;
3.认识“化学变化过程中元素不变”观念。
核心考点:元素的概念;常见元素的名称与符号;分子、原子、离子、元素、物质之间的关系
课前预习
1. 元素是________相同的一类原子的总称,不同元素之间的本质区别是_________的不同。
2.地壳中含量最多的元素是_________,含量最多的金属元素是______,生物细胞中含量最多的元素是________。
3.书写元素符号,第一个字母要______,第二个字母要______。
质子数质子数氧氧铝大写小写课堂精讲
知识点1.元素(对应课本P59~P60)
(1)元素的含义
①概念:元素是质子数相同的一类原子的总称。
②决定元素种类的是原子核内的质子数(即核电荷数),不同元素之间的本质区别是质子数不同。
③物质发生化学变化时,原子的种类不变,元素也不会改变【例1】(2015?攸县校级模拟)一种元素与另一种元素的本质区别是( )
A.质子数不同 B.中子数不同
C.相对原子质量不同 D.电子数不同
(2)元素与原子的区别与联系
【例2】(2014?齐齐哈尔模拟)过氧化氢(H2O2)的水溶液俗称双氧水,关于过氧化氢的叙述正确的是( )
A.过氧化氢是由氢原子和氧原子组成的
B.过氧化氢是由一个氢分子和一个氧分子构成的
C.过氧化氢是由氢元素和氧元素组成的
D.过氧化氢是由两个氢原子和两个氧原子构成的
【例3】(2015?广东模拟)某药品说明书中标明:本品每克含碘150mg,镁65mg,铜2mg,锌1.5mg,锰1mg.这里所标的各成分是指( )
A.分子 B.原子 C.元素 D.离子
变式拓展:
1.(2015?思南县校级一模)下列说法正确的是( )
①一个二氧化碳分子由一个碳原子和两个氧原子构成;
②二氧化硫由一个硫原子和一个氧分子组成;
③二氧化硫由硫元素和氧元素组成;
④二氧化硫由一个硫元素和二个氧元素组成.
A.①③ B.③④ C.②③ D.①④
2.妈妈在厨房里使用了“加碘食盐”,这里的“碘”应该理解为( )
A.分子 B.单质 C.元素 D.原子AC(3)讨论下列化学变化中分子、原子、元素是否发生了变化
由上表讨论可知:在化学变化中,反应物和生成物相比较,分子_________,原子_________,元素___________改变不变不变(4)元素的存在
①物质是由元素组成的,目前发现的元素只有一百多种,但组成的物质的种类有几千万种。有的物质组成中只有一种元素,有的物质组成中有多种元素。
②地壳中各种元素的含量居于前四位的分别是:氧(48.60%)、硅(26.30%)、铝(7.73%)、铁(4.75%)
③生物细胞中元素含量居于前四的分别是:氧(65%)、碳(18%)、氢(10%)、氮(3%)
【例4】(2014?扬州)关于各元素相对含量说法正确的是( )
A.地壳中含量最高的元素是氧
B.海洋中含量最高的元素是氯
C.空气中含量最高的元素是碳
D.人体中含量最多的元素是氢
变式拓展:
3.(2014?内江模拟)人体是一座元素的“仓库”,地壳中天然存在的化学元素,大多数能在人体中找到,其中含量最高的元素是( )
A.氢 B.碳 C.氧 D.钙
C(5)元素的分类
元素分为三类:
①金属元素:汉字用“钅”字旁表示(汞和金除外),金属由原子直接构成;
②非金属元素:通常状况下,非金属元素有三种状态,一是有“气”字头的是气态非金属元素,二是有“氵”字旁的是液态非金属元素,三是有“石”字旁的是固态非金属元素。
③稀有气体元素:通常状况下,稀有气体为气体,该名称都用“气”字头,是由原子直接构成的。
【例5】组成物质的元素有一百多种.下列属于金属元素的是( )
磷 B.氯 C.镁 D.溴
变式拓展:
4.下列元素中,属于非金属元素的是( )
A.汞 B.钾 C.碘 D.铍
C(6)直击中考
该知识点是广东中考的高频考点,考查的重点是元素与微观粒子(分子、原子、离子)之间的区别,以及元素种类、元素之最等知识,学生应从微观和宏观的角度判别元素与微观粒子的区别,以及掌握元素的简单分类、元素之最等相关知识。
知识点2.元素符号
(1)元素符号的规定:国际上统一采用元素拉丁文名称的第一个字母(大写)来表示元素,若几种元素拉丁文名称的第一个字母相同,就附加一个小写字母来区别。
(2)元素符号的书写:第一个字母要大写,如H、K、C等;第二个字母要小写,如Na。
(3)元素符号的意义:表示一种元素(宏观),表示这种元素的一个原子(微观)
点拨:①元素符号前面加数字时,如“2O”,这时候只能表示两个氧原子,而不能表示氧元素;
②对于由原子直接构成的物质,如金属、稀有气体等,元素符号还能表示一种物质。
【例6】(2014?北海)镁元素的元素符号书写正确的是( )
A. mg B. Mg C.MG D. mG
变式拓展:
5.(2014?东莞市校级三模)元素符号“H”除表示氢元素外,还能表示( )
A.一个氢原子 B.一个氢离子
C.一个氢分子 D.氢气
A随堂检测
1.(2014?嘉兴)正在生产中的国产大型客机C919部分机身采用了
新型的铝锂合金,这种材料具有较高的强度和适宜的延展性.铝
锂合金中的铝(Al)元素和锂(Li)元素的本质区别是( )
A.元素符号不同 B.原子质量不同
C.原子的质子数不同 D.原子的电子数不同
2.(2014秋?咸阳期中)下列关于物质组成和结构的说法正确的是( )
A.水是由氢气和氧气组成的
B.氧气是由氧原子构成的 C.二氧化碳是由碳、氧两种元素组成的
D.过氧化氢中含有氢、氧两个元素
3.(2015?攸县校级模拟)地壳中含量最多的金属元素是( )
A.硅 B.氧 C.铁 D.铝
CCD4.(2014?玉林模拟)下列元素符号和名称,书写不完全正确的是( )
A. P 磷 B. mg 镁 C. Zn 锌 D. Cu 铜
5.(2014?祁阳县校级模拟)超市的商品中,标签上注明“高钙牛奶”、“加碘食盐”,这里的钙、碘等指的是( )
A.元素 B.原子 C.分子 D.单质
6.元素是具有相同的_________(即_________)同一类原子的总称。铁是由_______组成,氧化钙是由________和__________组成的。一个五氧化二磷分子(P205)是由2个______和5个_________构成的。地壳中含量最多的金属元素是__________
BA质子数核电荷数铁元素氧元素钙元素磷原子氧原子铝元素
课题3 元素(二)
学习目标
1.初步认识元素周期表,能够根据原子序数在元素周期表中找到指定的元素;
2.知道原子结构与周期表的关系,认识元素周期表的排列规律。
核心考点:根据元素周期表的排列规律,能够根据原子序数在元素周期表中找到指定元素;认识原子结构和周期表的关系。
课前预习
1.在元素周期中,每个横行叫做一个________,共有_____个周期;每一个纵行叫做一个_____,共有_____个族。
2.每一周期,从左到右原子序数依次增加,核电荷数(即质子数)依次______,最外层电子数依次______,原子序数
=___________=__________=__________,电子层数_________;每一周期开头的元素是_________(第一周期除外),靠近结尾的元素是___________,结尾的元素是_____________
3.每一族,从上到下电子层数依次______,最外层电子数_______(He除外)。
周期7族26增加增加核电荷数质子数核外电子数相同金属元素_稀有气体元素非金属元素增加相同课堂精讲
知识点1.元素周期表(对应课本P62~P63)
(1)根据元素的__结构__和__性质__,将已知的一百多种元素科学有序地排列起来所得到的表,叫做___元素周期表__;为了方便查找,元素周期表按元素__原子核电荷数___递增的顺序给元素编号,称为__原子序数__,在数值上与____原子核电荷数___相同。元素周期表上对金属元素、非金属元素(包括稀有气体元素)用不同的颜色做了分区。
(2)元素周期表的结构
①横行(周期):元素周期表共有_7_个横行,每一横行代表一个周期,有__7__个周期;
②纵行(族):元素周期表共有__18__个纵行,每一纵行叫做一个族,(8、9、10三个纵行共同组成一个族),所以总共有___16__个族。
③每一格:在元素周期表中,每一种元素均占据一格,每一格均包括元素的原子序数、元素符号、元素名称、相对原子质量等内容,如图3-15。
原子序数 元素符号
相对原子质量 元素名称(3)直击广东中考
该知识点是广东中考的高频考点,每年均会考查,考查的难度中等,主要考查根据元素周期表的信息进行分析解题的能力,通常会与原子结构示意图综合来考查,同学们在学习时应熟记有关元素周期表中各个数字所代表的含义,能根据元素周期表获得原子序数、相对原子质量、元素符号、元素种类等信息,并能根据图中的信息来进行解答。
【例1】(2014?天津)稀土元素是一类有重要用途的资源,铈(Ce)是一种常见的稀土元素,下列有关说法中错误的是( )
A.铈的原子序数为58
B.铈属于非金属元素
C.铈原子中的质子数为是58
D.铈的相对原子质量是140.1
变式拓展:
1.查阅课本附录元素周期表,回答下列问题。
(1)查找出原子序号为6、16的元素名称与符号①6:
_________、________
②16:_________、___________
(2)13号元素的相对原子质量为_______;相对原子质
量为22.99的元素的符号为______
2.(2014?广西)如图是元素周期表中某元素信息示意图,由图所获取的信息正确的是( )
A.该元素为金属元素
B.该元素的相对原子质量为35.453g
C.该元素位于元素周期表的第三周期
D.该元素在化学反应中容易失去电子
碳C硫S26.98NaB知识点2.元素周期表的规律(对应课本63及附录元素周期表)
(1)认真完成P63探究,寻找元素周期表中的规律。
①每一周期,从左到右原子序数依次增加,核电荷数(即质子数
)依次增加,最外层电子数依次增加,原子序数=核电荷数=质子数=核外电子数,电子层数相同;每一周期开头的元素是金属元素(第一周期除外),靠近结尾的元素是非金属元素,结尾的元素是稀有气体元素
②每一族,从上到下电子层数依次增加,最外层电子数相同(He除外)。
③元素所在的周期数由原子的电子层数决定,元素所在的族数由
原子的最外层电子数决定。
(2)直击中考
本考点为广东的高频考点,每年均会考查,主要考查根据
元素周期表的信息进行分析解题的能力,通常与原子结构示意图
结合来考查。要求同学们要熟记有关元素周期表的规律,能了解
每一格中各个数字所表示的意义,并且能根据图中的信息来进行
解答。
【例2】(2014?青岛改编)按元素周期表(局部)提供的信息,下列有关判断错误的是( )
A.铍(Be)和镁属于同一个族
B.第二、三周期元素的原子最外
层电子数从左到右依次增多
C.铝原子的核内中子数为13
D.钠原子在化学反应中容易失去电子变成阳离子
变式拓展:
3.(2014?松北区一模)下列结构示意图表示元素周期表中同一横行的原子的是( )
A.①②③ B.①⑤
C.②③④ D.②③⑤
B随堂检测
1.如图3-18是元素周期表中硫元素的信息示意图,对图中信息理解错误的是( )
A.原子序数 B.元素名称
C.元素符号 D.质子数
2.(2015?本溪模拟)如图3-19是元素周期表中的一格,从中获取的信息正确的是( )
A.该元素的元素符号为Ar
B.该元素属于金属元素
C.该元素的中子数是18
D.该元素一个原子的实际质量为39.95
DA3.(2014秋?沂水县校级月考)根据如图3-20提供的信息,下列判断正确的是( )
图3-20
A.元素所在的周期数等于其原子的最外层电子数
B.钠离子核外有三个电子层
C.第二、三周期元素的原子从左至右最外层电子数逐渐增多
D.在化学变化中镁元素容易失去最外层2个电子形成镁离子,其离子符号是Mg+
C4.(2010秋?祁阳县校级期末)元素周期表是化学学习和研究的重要工具.下图是元素周期表的一部分。
(1)从表中查出硫元素的相对原子质量为________
(2)6﹣11号元素中属于金属元素的有________(填元素符号)
(3)科学家宣布,现已人工合成了第120号元素,则此元素的核电荷数为________
(4)与磷元素化学性质相似的元素是___________(填元素名称)
32.06Na120氮
第三单元复习课
考点1.分子、原子、离子的性质及应用(高频考点)
1.(2014长沙)下列对原子、分子、离子的认识,错误的是( )
A.原子能构成分子,但不能直接构成物质
B.相同原子可以构成不同的分子
C.原子核里的质子数等于核外电子数
D.分子、原子、离子都是构成物质的粒子
2.(2014宜宾)以下事实对应的解释错误的是( )
AD考点2.粒子结构示意图(高频考点)
3.(2014通辽)如图是三种微粒的结构示意图,有关它们的说法正确的是( )
A.三种微粒的核外电子排布相同
B.三种微粒对应原子的最外层
电子数相同
C.三种微粒属于同种元素的微粒
D.三种微粒都是原子
4.(2014益阳)如图分别是某元素的原子结构示意图及该元素在元素周期表中的相关信息,下列说法正确的是( )
A.该元素原子的最外层电子数为7
B.该元素的原子序数为19
C.该元素是金属元素
D.在化学反应过程中该元素原子
容易失去电子形成阳离子
AA考点3.元素及元素符号(高频考点)
5.(2014柳州)我们在商场里常会看到标有“补钙”“补铁”“补锌”等字样的食品或保健品,这里所写的“钙”“铁”“锌”指的是( )
A.分子 B.原子 C.元素 D.单质
6.(2014滨州)下列各组元素中,元素符号的第一字母相同的一组是( )
A.氯、碳、钙、铜
B.氢、汞、铁、银
C.钠、镁、氧、氮
D.锰、硫、锌、钡
CA考点4.元素周期表(高频考点)
7.(2014江西)如图所示是元素周期表中某一周期元素的原子结构示意图:
(1)硼原子结构示意图中的X= 。
(2)镁原子的原子结构示意图为 ,图中与其化学性质相似的元素是 。
(3)图中元素从左至右排列所遵循的规律是(任写一条) 。
(4)根据图示信息,确定1个一氧化碳分子中所含电子总数为 。
5铍核电荷数依次增大排列14考点5.相对原子质量
8.已知某氧原子的相对原子质量为16,某硫原子的相对原子质量为32。如果该氧原子的质量为m,则该硫原子的质量为( )
A.32m
B.2m
C.m
D.不能确定
B
第三单元 物质构成的奥秘
课题1 分子和原子
学习目标
1.认识分子、原子等微观粒子,了解物质是由分子、原子等微观粒子构成的;
2.认识微观粒子的性质,并能够根据微观粒子的性质解释生活中的一些现象;
3.学习一些类比、模型等科学方法,从微观角度认识物质,培养抽象、想象思维能力。
核心考点:分子、原子的概念以及性质;认识物质的微粒性;能用微粒的观点来解释某些常见现象。
课前预习
1.物质是由_______、________等粒子构成的。
2.由分子构成的物质,分子是___________________的最小粒子;原子是_______________的最小粒子。
3.分子的性质有:分子的________________非常小;分子在_____________;分子间有_________;同种分子性质_______,不同分子性质________。
分子原子保持其化学性质化学变化中质量和体积不断运动着间隔相同不同课堂精讲
知识点1.物质由微观粒子构成(对应课本P48~P49)
科学的进步,证明了物质是由_原子_、_分子_等微观粒子构成的。通过先进的科学仪器我们不仅能够观察到一些分子和原子(如图3-1),还能移动原子(如图3-2)。
知识点2.分子的性质(对应课本P49)
(1)通过科学实例、数据或实验探究分子的性质
规律点拨:①温度越高,分子的运动速率越快,如品红在热水中的扩散速率比在冷水中的扩散速率快得多。
②通常情况下,温度越高,分子间的间隔越大;压强越大,分子间的间隔越小,如夏天充满气的自行车轮胎暴晒容易爆炸。
(2)直击广东中考
该知识点考查得较多的是“分子是在不停地运动”,运用分子的基本性质解释日常生活中的现象,是中考命题的热点,学生应该熟记分子的几个性质。
【例1】(2015?信阳校级模拟)对生活中下列现象的解释错误的是( )
变式拓展:
1.(2014?汕尾)吸烟有害健康,非吸烟者往往会因吸烟者吸烟而造成被动吸烟,这是因为( )
A.分子在不断运动 B.分子之间有间隔
C.分子的体积很小 D.分子的质量很小
2.(2014?杭州)液氧转化为氧气的过程中,发生的变化是( )
A.混合物变为纯净物 B.分子间的空隙增大
C.化学性质发生变化 D.分子总数增加
AB知识点3.分子可以分为原子(对应课本P50~P51)
(1)通过“冰的熔化”和“氧化汞受热分解”,分析微粒的变化。
【结论】物理变化中,由分子构成的物质发生物理变化时,分子本身不变。化学变化中,由分子构成的物质发生化学变化时,分子本身改变。化学变化中,分子可分,原子不可分。(2)分子的概念
由分子构成的物质在发生物理变化时,分子本身没有发生变化,它们的化学性质也各自保持不变。由分子构成的物质在发生化学变化时,一种物质的分子会变成其他物质的分子,原分子的化学性质不再保持。可见,由分子构成的物质,分子是保持其化学性质的最小粒子。
点拨:分子只能保持物质的化学性质,不能保持物质的物理性质。因为物质的物理性质(如状态、颜色)是由该物质的大量分子聚集后表现出来的性质,并不是单个分子能保持的。
(3)原子的概念
原子是化学变化中的最小粒子,在化学变化中,分子的种类可以发生变化,而原子的种类不会发生变化,只是重新结合生成了其他物质的分子。
点拨:原子也是构成物质的基本粒子之一,如金属、稀有气体是由原子直接构成的;由原子直接构成的物质,原子保持其化学性质。原子只是在化学变化中不能再分,即在化学变化中不能将原子分成更小的粒子,但脱离“化学反应”这一前提,原子可以分为更小的粒子。
(4)分子与原子的联系与区别
(5)直击广东中考
该知识点主要考查分子、原子的概念,学生最好从化学变化的微观本质角度去理解掌握,认识到化学变化的微观本质是分子分裂成原子,原子重新结合成新的分子。【例2】(2014?上海)关于原子、分子叙述错误的是( )
A.分子是由原子构成的
B.分子和原子都在不停运动
C.分子和原子在化学变化中都能够再分
D.分子和原子都是构成物质的微粒
【例3】如图3-3是表示气体分子的示意图,图中“●”“○”分别表示两种不同的原子,其中表示纯净物的是( )
图3-3
A. ①③ B. ②④ C. ③④ D. ②③
变式拓展:
3.(2015?本溪模拟)在学习分子和原子的知识后,四位同学对它们的区别作了如下发言,正确的是( )
A.小倩说“区别在于是否在不停地运动”
B.小丹说“区别在于化学反应中是否可分”
C.小鑫说“区别在于是否能够构成物质”
D.小娜说“区别在于分子和原子的大小和质量都不同”
4.(2014?始兴县校级一模)水是生命的源泉,是人类宝贵的资源。它有时能幻作朵朵白云,有时能化为绵绵细雨。下列过程中,你认为水分子发生了变化的是( )
A.水蒸气遇冷凝结成水 B.蔗糖和水混合后得到糖水
C.水通电变成氢气和氧气 D.蒸馏法淡化海水
CB随堂检测
1.(2015?枣庄模拟)图书馆常配备液态二氧化碳灭火器。使用时,打开阀门,液态二氧化碳便会迅速汽化喷出。下列对“汽化喷出”这一现象认识正确的是( )
A.分子种类发生了变化 B.分子间间隔发生了变化
C.分子大小发生了变化 D.分子的构成发生了变化
2.(2015?平凉一模)春天的柳湖公园,百花盛开,阵阵花香,沁人心脾。花香四溢的现象说明( )
A.分子是不断运动的 B.分子是由原子构成的
C.分子具有一定的质量 D.分子之间有一定的间隙
3.(2015?静安区一模)从化学的视角认识世界,下列对事实解释错误的是( )
A.食物腐败:分子发生了变化
B.热胀冷缩:分子大小随温度的变化而改变
C.花香四溢:分子不停地运动
D.氢气和氧气的性质不同:构成它们的分子不同
BBA4.(2014?祁阳县校级模拟)能保持氢气的化学性质的最小粒子是( )
A.氢原子 B.氢分子 C.两个氢原子 D.氢元素
5.(2014?衡阳模拟)能证明分子在化学反应中可以再分的变化是( )
A.碘受热变成碘蒸气
B.一定条件下用二氧化碳气体制干冰
C.块状硫研磨成硫粉
D.加热氧化汞产生氧气
6.(2014?闸北区一模)关于分子和原子的说法,正确的是( )
A.化学变化中分子种类不一定发生变化
B.不同种原子可以构成分子,同种原子不可以构成分子
C.原子也是构成物质的一种微粒
D.保持二氧化碳化学性质的最小微粒是碳原子和氧原子
BDC
课题2 原子的结构(一)
学习目标
1.了解原子的构成以及构成粒子之间的关系,了解原子结构示意图;
2.了解原子核外的电子排布,理解原子核外电子分层运动的想象。
核心考点:原子的构成;核电荷数、质子数、核外电子数之间的关系;核外电子的排布及分层运动。
课前预习
1.原子核是由______和_______两种粒子构成的。
2.原子不显电性,是因为质子数=_________=____________
3.在含有多个电子的原子中,核外电子具有不同的运动状态,离核近的电子能量较____,离核越远,电子的能力越_____。
质子中子核电荷数核外电子数低高课堂精讲
知识点1.原子的构成(对应课本P53)
(1)原子的构成
在化学变化中,原子是不可再分的最小粒子。而大量的科学实验证明,原子还是可以再分的。原子的构成如下:
质子(每个质子带1个单位正电荷)
(不带电)
核外电子 (每个电子带1个单位负电荷) 原子核 (居于原子中心)
原子 中子(2)核电荷数、质子数、核外电子数的关系
核电荷数是原子核所带的正电荷数。原子核是由质子和中子构成的,每个质子带1个单位的正电荷,中子不带电,因此原子核所带的正电荷数(核电荷数)就等于核内的质子数。原子核内质子所带的电荷与核外电子的电荷数量相等,且电性相反,每个质子带1个单位的正电荷,每个电子带1个单位的负电荷,所以质子数等于核外电子数,因此原子不显电性。
规律点拨:①在原子中:核电荷数=质子数=核外电子数;②并不是所有的原子核都是由质子和中子构成的,如氢原子核中只有质子,没有中子;③区分原子的种类的依据是原子的质子数(或核电荷数),不同种类的原子,核内的质子数(或核电荷数)不同。
(3)直击广东中考
本知识点是广东中考的高频考点,会结合后面学习的粒子结构示意图进行考察,学生在对该知识点的学习中应熟练掌握在原子结构中,质子数=核电荷数=核外电子数。
【例1】(2015?淮阳县校级一模)据中央电视台对云南抚仙湖底古城考古的现场报道,科学家曾经通过测定古生物遗骸中的碳-14来推断古城年代.碳-14原子的核电荷数为6,质子数和中子数之和为14,下列关于碳-14原子的说法中错误的是( )
A.质子数为6 B.中子数为6
C.电子数为6 D.电子数和中子数之和为14
【例2】1911年著名物理学家卢瑟福为探索原子的内部结构进行了实验。在用一束带正电的、质量比电子大得多的高速运动的α粒子轰击金箔时发现(如图3-5):
(1)大多数α粒子能穿透金箔而不改变原来的运动方向;
(2)一小部分α粒子改变了原来的运动方向;
(3)有极少部分α粒子被弹了回来。
下列对原子结构的认识错误的是( )
A.原子核体积很小
B.原子核带正电
C.原子内部有很大的空间
D.原子是实心的球体
变式拓展:
1.(2015?株洲模拟)构成原子核的粒子一定有( )
A.质子 B.中子 C.电子 D.质子和中子
2.(2015?静海县模拟)下列关于原子的叙述正确的是( )
①一切原子都是由质子、中子和电子构成的;
②原子在不停地运动;
③原子是化学变化中的最小拉子;
④原子由原子核和核外电子构成;
⑤原子中不存在电荷.因而原子不带电。
A.②③④ B.①②④
C.①③⑤ D.①②③④⑤
AA知识点2.原子核外电子的排布(对应课本P54)
(1)原子核外的电子层
在含有多个电子的原子中,核外电子具有不同的运动状态,离核近的电子能量较低,离核越远,电子的能量越高。为了方便研究,科学家形象地将这些区域称为电子层,原子核外的电子是分层排布的规律。迄今已知的原子核外电子最少的有一层,最多的有七层。
(2)核外电子的分层排布规律
核外电子的运动状态被科学家人为地分成了几个电子层,离核最近的称为第一层,离核最远的称为最外层。在每一层上的电子数是不同的:第一层最多容纳2个电子,第二层最多容纳8个电子,最外层电子数最多不超过8个(只有一层的,电子数不超过2个)。
(3)原子结构示意图
用原子结构示意图可以简明、方便地表示核外电子的分层排布,其各部分的意义如图3-6所示。
图3-6
(4)直击广东中考
该知识点为广东中考的高频考点,根据粒
子结构来推断粒子的种类,或确定质子数、核电
荷数、核外电子数等都是常考的题型,常与后面
学习的元素周期表结合考查,学生应掌握原子结
构示意图中各个部分所代表的意义。
原子核
质子数
第一电子层
第二电子层 第三电子层(最外电子层)【例3】(2014秋?滕州市校级月考)某粒子的结构示意图如图3-7所示,对该粒子的说法错误的是( )
A.核电荷数为12
B.核外有3个电子层
C.第3层上的电子携带的能量最高
D.圆圈代表电子
变式拓展:
3.下面是五种原子的结构示意图:
A. B. C.
(1)A原子中,质子数为______,电子层数为______,最外层电子数为______,电子总数为_______;
(2)B原子中,x=_______;C原子中,X=______
171737156随堂检测
1.原子是由( )
A.电子和质子构成的
B.质子和中子构成的
C.电子和中子构成的
D.原子核和电子构成的
2.一种硫原子中共有48个粒子,其中16个不带电,则它的电子数为( )
A.48 B.16 C.32 D.16
3.某原子的原子核内有1个质子和2个中子,则该原子的核电荷数为( )
A.1 B.3 C.2 D.无法判断
4.(2015?漳州模拟改编)下列关于原子的叙述中,不正确的是( )
A.原子可以构成分子
B.原子是化学反应中的最小微粒
C.原子是由原子核和核外电子构成的
D.原子不带电是因为原子中存在中子
DBAD5.某原子的结构示意图为 ,下列有关的叙述中,错误的是( )
A.质子数为12 B.核电荷数为11
B.电子层数为3 D.核外电子数为12
6.钠原子和氯原子的结构示意图如图3-8:
(1)钠原子原子核内有_______质子,
有_____电子层,第一层有________个电
子,最外层电子层上有_____个电子。
(2)氯原子的核电荷数是________
(3)钠原子与氯原子相同的是_______(填序号)
①质子数 ②电子数 ③电子层数 ④最外层电子数
B1132117 ③
课题2 原子的结构(二)
学习目标
1.了解原子的核外电子排布与性质之间的关系,了解典型元素(稀有气体、金属、非金属)原子核外电子的排布特点;
2.以氯化钠为例,了解离子形成;
3.了解相对原子质量的含义。
核心考点:原子核外电子排布与性质的关系;离子的形成;相对原子质量。
课前预习
1.原子的化学性质主要取决于原子的__________,最外层电子数为8个电子(第一层为最外层的是2个电子)的被认为是一种_________________。
2.离子的定义是:_______________________________。带正电的称为______,带负电的称为__________。
3. 以一种碳原子质量的1/12为标准,其他原子的质量与它相比较所得到的比,作为这种原子的________________,原子的质量主要集中在________上。
最外层电子数相对稳定的结构带电的原子叫做离子阳离子阴离子相对原子质量原子核课堂精讲
知识点1.原子结构与性质的关系
稀有气体原子的最外层电子数一般为8个(氦为2个);金属原子最外层电子数一般少于4个,在化学反应中易失电子;非金属原子的最外层电子数一般多于或等于4个,在化学反应中易得电子。
原子的化学性质主要取决于原子的最外层电子数。原子最外层电子数为8个电子(第一层为最外层的是2个电子)的被认为是一种相对稳定的结构。原子都趋于达到相对稳定的结构。
【例1】原子的化学性质主要取决于原子的最外层电子数。
(1)如图3-9所示,该原子的核电
荷数为______,名称是__________
,由它组成的物质被称为______气体,
化学性质_________
(2)下列原子结构属于稳定结构的是__________(填序号,下同);②粒子的化学性质与①、③、④、⑤粒子中 的化学性质相似,它们在化学反应中都容易 (填“得”或“失”)电子。
变式拓展:
1.(2014秋?酒泉校级期中)根据下列原子结构示意图判断,化学性质最相似的两种元素是( )
①和② B. ①和④
C. ②和③ D. ③和④
B知识点2.离子
(1)离子的定义:带电的原子(或原子团),如Na+、Cl-、NO3-。离子也是构成物质的粒子之一。
(2)离子的形成
①金属原子的最外层电子一般少于4个,在化学反应中易失电子,核电荷数大于核外电子数,带正电荷,为阳离子;
②非金属原子的最外层电子一般多于4个,在化学反应中易得电子,核电荷数少于核外电子数,带负电荷,为阴离子。
(3)离子化合物的形成过程
以氯化钠的形成过程为例,钠原子的最外层有1个电子,氯原子的最外层有7个电子,当钠与氯反应时,钠原子最外层的1个电子转移到氯原子的最外层上,二者在静电作用下相互结合,形成氯化钠。如图3-10所示。
图3-10
(4)离子的符号书写
在元素符号(或原子团)的右上角标明离子所带的电荷,数值在前,正、负号在后。当离子带1个单位的正电荷或1个单位负电荷时,“1”可以省略不写。例如,镁离子的数字“2”含义如下。
2Mg2+
【例2】根据下列微粒的结构示意图回答问题。
(1)属于稳定结构的是______(填序号,下同);
(2)D原子属于______(“金属”或“非金属”)原子,易______电子,形成_____离子。
(3)属于原子的是__________,属于阳离子的是_______,属于阴离子的是________
解析:原子最外层电子数为8个电子(第一层为最外层的是2个电子)的被认为是一种相对稳定的结构。金属原子的最外层电子一般少于4个,容易失去电子,形成阳离子。
【例3】下列符号能表示2个氧离子的是( )
A.2O2-
B.2O2
C.2O
D.O2
变式拓展:
2.(2014?巴中)下列对微粒的描述中,不正确的是( )
B.
易失电子 易形成阴离子
C. D.
阳离子 化学性质稳定
C知识点3.相对原子质量
(1)概念:以一种碳原子(原子核中含有6个质子和6个中子)质量的1/12为标准,其他原子的质量与它相比较所得到的比,作为这种原子的相对原子质量,符号为Ar。
(2)单位:相对原子质量是一个比值,单位为“1”,一般不读出也不写出。
(3)原子一般由质子、中子、电子构成,质子和中子的相对质量都约等于1,与质子和中子相比,电子的质量很小,可以忽略不计,因此原子的质量主要集中在原子核上,相对原子质量在数值上约等于质子数加上中子数。
规律点拨:相对原子质量不是一个原子的实际质量,它是一个比值,能够反映一个原子实际质量的相对大小。原子的质量越大,相对原子质量越大。
(4)直击广东中考
该知识点是广东中考的重点,常以选择题、填空题、以及与后面学习的知识结合,以简单计算题的形式出现,学生应熟悉掌握相对原子质量的含义。
【例4】(2014?郴州)原子的质量主要决定于原子的( )
A.质子数 B.中子数
C.中子数和核外电子数 D.质子数和中子数
变式拓展:
3.(2014秋?滕州市月考)一种原子的核内有6个中子和6个质子,另一种原子的核内有7个中子和6个质子,则它们不同的是( )
A.质子数 B.原子的相对原子质量
C.核电荷数 D.核外电子数
4.作为相对原子质量标准的碳12原子的实际质量为m Kg,则实际质量为2m Kg的一种原子的相对原子质量是( )
A.24 B.24g C.2 D.2g
BA随堂检测
1.(2014秋?天河区期末)下列关于原子的说法,正确的是( )
A. B.
C. D.
2.(2014秋?大庆校级期中)根据相对原子质量的定义进行判断,氧原子的相对原子质量是( )
A.16g B.2.657×10﹣26kg
C.16 D.1.66×10﹣27kg
CD3.(2015?潍坊校级一模改编)根据以下图3-11的粒子结构示意图,其中说法不正确的是( )
图3-11
A.它们核电荷数都相同
B.它们的核外电子数相同
C.它们都具有相对稳定的结构
D.它们依次表示原子、离子、离子
4.(2014?红桥区校级一模)下列关于Na、Na+两种粒子的判断中,正确的是( )
①核电荷数相同;②核外电子数相等;③电子层结构完全相同;④质量几乎相等;⑤质子数相等;⑥Na+比Na稳定。
A.①④⑤ B.①③⑤⑥ C.①④⑤⑥ D.②③④
AC5.(2014?达县校级模拟改编)下列说法中错误的是( )
A.离子是由原子得到电子或失去电子而形成的
B.元素的化学性质跟原子最外层电子数目关系密切
C.一种粒子最外层电子数目为8,此粒子一定是稀有气体元素的原子
D.当原子失去或得到电子后,其性质发生了改变
6.(2014?琼海校级三模改编)据最新报道元素钬可有效地治疗肝癌,已知其相对原子质量为166,核电荷数为67,则该原子核内中子数和核外电子数分别为( )
A.166和67 B.67和99
C.166和99 D.99和67
CD
课题3 元素(一)
学习目标
1.了解元素的含义以及一些常见元素的名称与符号;
2.了解分子、原子、离子、元素之间的关系,认识物质的多样性;
3.认识“化学变化过程中元素不变”观念。
核心考点:元素的概念;常见元素的名称与符号;分子、原子、离子、元素、物质之间的关系
课前预习
1. 元素是________相同的一类原子的总称,不同元素之间的本质区别是_________的不同。
2.地壳中含量最多的元素是_________,含量最多的金属元素是______,生物细胞中含量最多的元素是________。
3.书写元素符号,第一个字母要______,第二个字母要______。
质子数质子数氧氧铝大写小写课堂精讲
知识点1.元素(对应课本P59~P60)
(1)元素的含义
①概念:元素是质子数相同的一类原子的总称。
②决定元素种类的是原子核内的质子数(即核电荷数),不同元素之间的本质区别是质子数不同。
③物质发生化学变化时,原子的种类不变,元素也不会改变【例1】(2015?攸县校级模拟)一种元素与另一种元素的本质区别是( )
A.质子数不同 B.中子数不同
C.相对原子质量不同 D.电子数不同
(2)元素与原子的区别与联系
【例2】(2014?齐齐哈尔模拟)过氧化氢(H2O2)的水溶液俗称双氧水,关于过氧化氢的叙述正确的是( )
A.过氧化氢是由氢原子和氧原子组成的
B.过氧化氢是由一个氢分子和一个氧分子构成的
C.过氧化氢是由氢元素和氧元素组成的
D.过氧化氢是由两个氢原子和两个氧原子构成的
【例3】(2015?广东模拟)某药品说明书中标明:本品每克含碘150mg,镁65mg,铜2mg,锌1.5mg,锰1mg.这里所标的各成分是指( )
A.分子 B.原子 C.元素 D.离子
变式拓展:
1.(2015?思南县校级一模)下列说法正确的是( )
①一个二氧化碳分子由一个碳原子和两个氧原子构成;
②二氧化硫由一个硫原子和一个氧分子组成;
③二氧化硫由硫元素和氧元素组成;
④二氧化硫由一个硫元素和二个氧元素组成.
A.①③ B.③④ C.②③ D.①④
2.妈妈在厨房里使用了“加碘食盐”,这里的“碘”应该理解为( )
A.分子 B.单质 C.元素 D.原子AC(3)讨论下列化学变化中分子、原子、元素是否发生了变化
由上表讨论可知:在化学变化中,反应物和生成物相比较,分子_________,原子_________,元素___________改变不变不变(4)元素的存在
①物质是由元素组成的,目前发现的元素只有一百多种,但组成的物质的种类有几千万种。有的物质组成中只有一种元素,有的物质组成中有多种元素。
②地壳中各种元素的含量居于前四位的分别是:氧(48.60%)、硅(26.30%)、铝(7.73%)、铁(4.75%)
③生物细胞中元素含量居于前四的分别是:氧(65%)、碳(18%)、氢(10%)、氮(3%)
【例4】(2014?扬州)关于各元素相对含量说法正确的是( )
A.地壳中含量最高的元素是氧
B.海洋中含量最高的元素是氯
C.空气中含量最高的元素是碳
D.人体中含量最多的元素是氢
变式拓展:
3.(2014?内江模拟)人体是一座元素的“仓库”,地壳中天然存在的化学元素,大多数能在人体中找到,其中含量最高的元素是( )
A.氢 B.碳 C.氧 D.钙
C(5)元素的分类
元素分为三类:
①金属元素:汉字用“钅”字旁表示(汞和金除外),金属由原子直接构成;
②非金属元素:通常状况下,非金属元素有三种状态,一是有“气”字头的是气态非金属元素,二是有“氵”字旁的是液态非金属元素,三是有“石”字旁的是固态非金属元素。
③稀有气体元素:通常状况下,稀有气体为气体,该名称都用“气”字头,是由原子直接构成的。
【例5】组成物质的元素有一百多种.下列属于金属元素的是( )
磷 B.氯 C.镁 D.溴
变式拓展:
4.下列元素中,属于非金属元素的是( )
A.汞 B.钾 C.碘 D.铍
C(6)直击中考
该知识点是广东中考的高频考点,考查的重点是元素与微观粒子(分子、原子、离子)之间的区别,以及元素种类、元素之最等知识,学生应从微观和宏观的角度判别元素与微观粒子的区别,以及掌握元素的简单分类、元素之最等相关知识。
知识点2.元素符号
(1)元素符号的规定:国际上统一采用元素拉丁文名称的第一个字母(大写)来表示元素,若几种元素拉丁文名称的第一个字母相同,就附加一个小写字母来区别。
(2)元素符号的书写:第一个字母要大写,如H、K、C等;第二个字母要小写,如Na。
(3)元素符号的意义:表示一种元素(宏观),表示这种元素的一个原子(微观)
点拨:①元素符号前面加数字时,如“2O”,这时候只能表示两个氧原子,而不能表示氧元素;
②对于由原子直接构成的物质,如金属、稀有气体等,元素符号还能表示一种物质。
【例6】(2014?北海)镁元素的元素符号书写正确的是( )
A. mg B. Mg C.MG D. mG
变式拓展:
5.(2014?东莞市校级三模)元素符号“H”除表示氢元素外,还能表示( )
A.一个氢原子 B.一个氢离子
C.一个氢分子 D.氢气
A随堂检测
1.(2014?嘉兴)正在生产中的国产大型客机C919部分机身采用了
新型的铝锂合金,这种材料具有较高的强度和适宜的延展性.铝
锂合金中的铝(Al)元素和锂(Li)元素的本质区别是( )
A.元素符号不同 B.原子质量不同
C.原子的质子数不同 D.原子的电子数不同
2.(2014秋?咸阳期中)下列关于物质组成和结构的说法正确的是( )
A.水是由氢气和氧气组成的
B.氧气是由氧原子构成的 C.二氧化碳是由碳、氧两种元素组成的
D.过氧化氢中含有氢、氧两个元素
3.(2015?攸县校级模拟)地壳中含量最多的金属元素是( )
A.硅 B.氧 C.铁 D.铝
CCD4.(2014?玉林模拟)下列元素符号和名称,书写不完全正确的是( )
A. P 磷 B. mg 镁 C. Zn 锌 D. Cu 铜
5.(2014?祁阳县校级模拟)超市的商品中,标签上注明“高钙牛奶”、“加碘食盐”,这里的钙、碘等指的是( )
A.元素 B.原子 C.分子 D.单质
6.元素是具有相同的_________(即_________)同一类原子的总称。铁是由_______组成,氧化钙是由________和__________组成的。一个五氧化二磷分子(P205)是由2个______和5个_________构成的。地壳中含量最多的金属元素是__________
BA质子数核电荷数铁元素氧元素钙元素磷原子氧原子铝元素
课题3 元素(二)
学习目标
1.初步认识元素周期表,能够根据原子序数在元素周期表中找到指定的元素;
2.知道原子结构与周期表的关系,认识元素周期表的排列规律。
核心考点:根据元素周期表的排列规律,能够根据原子序数在元素周期表中找到指定元素;认识原子结构和周期表的关系。
课前预习
1.在元素周期中,每个横行叫做一个________,共有_____个周期;每一个纵行叫做一个_____,共有_____个族。
2.每一周期,从左到右原子序数依次增加,核电荷数(即质子数)依次______,最外层电子数依次______,原子序数
=___________=__________=__________,电子层数_________;每一周期开头的元素是_________(第一周期除外),靠近结尾的元素是___________,结尾的元素是_____________
3.每一族,从上到下电子层数依次______,最外层电子数_______(He除外)。
周期7族26增加增加核电荷数质子数核外电子数相同金属元素_稀有气体元素非金属元素增加相同课堂精讲
知识点1.元素周期表(对应课本P62~P63)
(1)根据元素的__结构__和__性质__,将已知的一百多种元素科学有序地排列起来所得到的表,叫做___元素周期表__;为了方便查找,元素周期表按元素__原子核电荷数___递增的顺序给元素编号,称为__原子序数__,在数值上与____原子核电荷数___相同。元素周期表上对金属元素、非金属元素(包括稀有气体元素)用不同的颜色做了分区。
(2)元素周期表的结构
①横行(周期):元素周期表共有_7_个横行,每一横行代表一个周期,有__7__个周期;
②纵行(族):元素周期表共有__18__个纵行,每一纵行叫做一个族,(8、9、10三个纵行共同组成一个族),所以总共有___16__个族。
③每一格:在元素周期表中,每一种元素均占据一格,每一格均包括元素的原子序数、元素符号、元素名称、相对原子质量等内容,如图3-15。
原子序数 元素符号
相对原子质量 元素名称(3)直击广东中考
该知识点是广东中考的高频考点,每年均会考查,考查的难度中等,主要考查根据元素周期表的信息进行分析解题的能力,通常会与原子结构示意图综合来考查,同学们在学习时应熟记有关元素周期表中各个数字所代表的含义,能根据元素周期表获得原子序数、相对原子质量、元素符号、元素种类等信息,并能根据图中的信息来进行解答。
【例1】(2014?天津)稀土元素是一类有重要用途的资源,铈(Ce)是一种常见的稀土元素,下列有关说法中错误的是( )
A.铈的原子序数为58
B.铈属于非金属元素
C.铈原子中的质子数为是58
D.铈的相对原子质量是140.1
变式拓展:
1.查阅课本附录元素周期表,回答下列问题。
(1)查找出原子序号为6、16的元素名称与符号①6:
_________、________
②16:_________、___________
(2)13号元素的相对原子质量为_______;相对原子质
量为22.99的元素的符号为______
2.(2014?广西)如图是元素周期表中某元素信息示意图,由图所获取的信息正确的是( )
A.该元素为金属元素
B.该元素的相对原子质量为35.453g
C.该元素位于元素周期表的第三周期
D.该元素在化学反应中容易失去电子
碳C硫S26.98NaB知识点2.元素周期表的规律(对应课本63及附录元素周期表)
(1)认真完成P63探究,寻找元素周期表中的规律。
①每一周期,从左到右原子序数依次增加,核电荷数(即质子数
)依次增加,最外层电子数依次增加,原子序数=核电荷数=质子数=核外电子数,电子层数相同;每一周期开头的元素是金属元素(第一周期除外),靠近结尾的元素是非金属元素,结尾的元素是稀有气体元素
②每一族,从上到下电子层数依次增加,最外层电子数相同(He除外)。
③元素所在的周期数由原子的电子层数决定,元素所在的族数由
原子的最外层电子数决定。
(2)直击中考
本考点为广东的高频考点,每年均会考查,主要考查根据
元素周期表的信息进行分析解题的能力,通常与原子结构示意图
结合来考查。要求同学们要熟记有关元素周期表的规律,能了解
每一格中各个数字所表示的意义,并且能根据图中的信息来进行
解答。
【例2】(2014?青岛改编)按元素周期表(局部)提供的信息,下列有关判断错误的是( )
A.铍(Be)和镁属于同一个族
B.第二、三周期元素的原子最外
层电子数从左到右依次增多
C.铝原子的核内中子数为13
D.钠原子在化学反应中容易失去电子变成阳离子
变式拓展:
3.(2014?松北区一模)下列结构示意图表示元素周期表中同一横行的原子的是( )
A.①②③ B.①⑤
C.②③④ D.②③⑤
B随堂检测
1.如图3-18是元素周期表中硫元素的信息示意图,对图中信息理解错误的是( )
A.原子序数 B.元素名称
C.元素符号 D.质子数
2.(2015?本溪模拟)如图3-19是元素周期表中的一格,从中获取的信息正确的是( )
A.该元素的元素符号为Ar
B.该元素属于金属元素
C.该元素的中子数是18
D.该元素一个原子的实际质量为39.95
DA3.(2014秋?沂水县校级月考)根据如图3-20提供的信息,下列判断正确的是( )
图3-20
A.元素所在的周期数等于其原子的最外层电子数
B.钠离子核外有三个电子层
C.第二、三周期元素的原子从左至右最外层电子数逐渐增多
D.在化学变化中镁元素容易失去最外层2个电子形成镁离子,其离子符号是Mg+
C4.(2010秋?祁阳县校级期末)元素周期表是化学学习和研究的重要工具.下图是元素周期表的一部分。
(1)从表中查出硫元素的相对原子质量为________
(2)6﹣11号元素中属于金属元素的有________(填元素符号)
(3)科学家宣布,现已人工合成了第120号元素,则此元素的核电荷数为________
(4)与磷元素化学性质相似的元素是___________(填元素名称)
32.06Na120氮
第三单元复习课
考点1.分子、原子、离子的性质及应用(高频考点)
1.(2014长沙)下列对原子、分子、离子的认识,错误的是( )
A.原子能构成分子,但不能直接构成物质
B.相同原子可以构成不同的分子
C.原子核里的质子数等于核外电子数
D.分子、原子、离子都是构成物质的粒子
2.(2014宜宾)以下事实对应的解释错误的是( )
AD考点2.粒子结构示意图(高频考点)
3.(2014通辽)如图是三种微粒的结构示意图,有关它们的说法正确的是( )
A.三种微粒的核外电子排布相同
B.三种微粒对应原子的最外层
电子数相同
C.三种微粒属于同种元素的微粒
D.三种微粒都是原子
4.(2014益阳)如图分别是某元素的原子结构示意图及该元素在元素周期表中的相关信息,下列说法正确的是( )
A.该元素原子的最外层电子数为7
B.该元素的原子序数为19
C.该元素是金属元素
D.在化学反应过程中该元素原子
容易失去电子形成阳离子
AA考点3.元素及元素符号(高频考点)
5.(2014柳州)我们在商场里常会看到标有“补钙”“补铁”“补锌”等字样的食品或保健品,这里所写的“钙”“铁”“锌”指的是( )
A.分子 B.原子 C.元素 D.单质
6.(2014滨州)下列各组元素中,元素符号的第一字母相同的一组是( )
A.氯、碳、钙、铜
B.氢、汞、铁、银
C.钠、镁、氧、氮
D.锰、硫、锌、钡
CA考点4.元素周期表(高频考点)
7.(2014江西)如图所示是元素周期表中某一周期元素的原子结构示意图:
(1)硼原子结构示意图中的X= 。
(2)镁原子的原子结构示意图为 ,图中与其化学性质相似的元素是 。
(3)图中元素从左至右排列所遵循的规律是(任写一条) 。
(4)根据图示信息,确定1个一氧化碳分子中所含电子总数为 。
5铍核电荷数依次增大排列14考点5.相对原子质量
8.已知某氧原子的相对原子质量为16,某硫原子的相对原子质量为32。如果该氧原子的质量为m,则该硫原子的质量为( )
A.32m
B.2m
C.m
D.不能确定
B
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
