6.3 二氧化碳和一氧化碳(38张PPT)
文档属性
| 名称 | 6.3 二氧化碳和一氧化碳(38张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-06-14 00:00:00 | ||
图片预览








文档简介
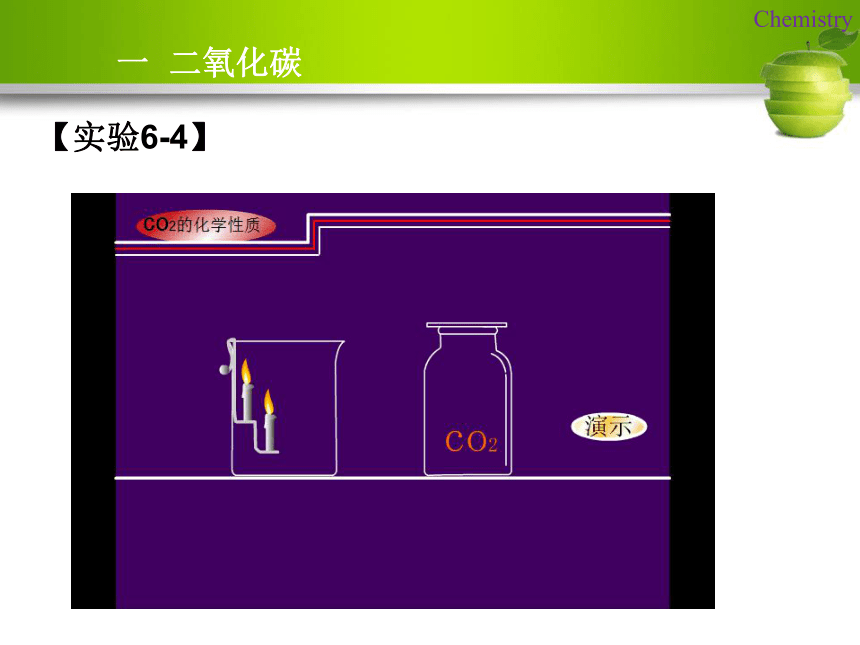
课件38张PPT。课题3 二氧化碳和一氧化碳By teacher zhou一 二氧化碳【实验6-4】阶梯下层的蜡烛先熄灭,上层蜡烛后熄灭。二氧化碳的密度比空气大
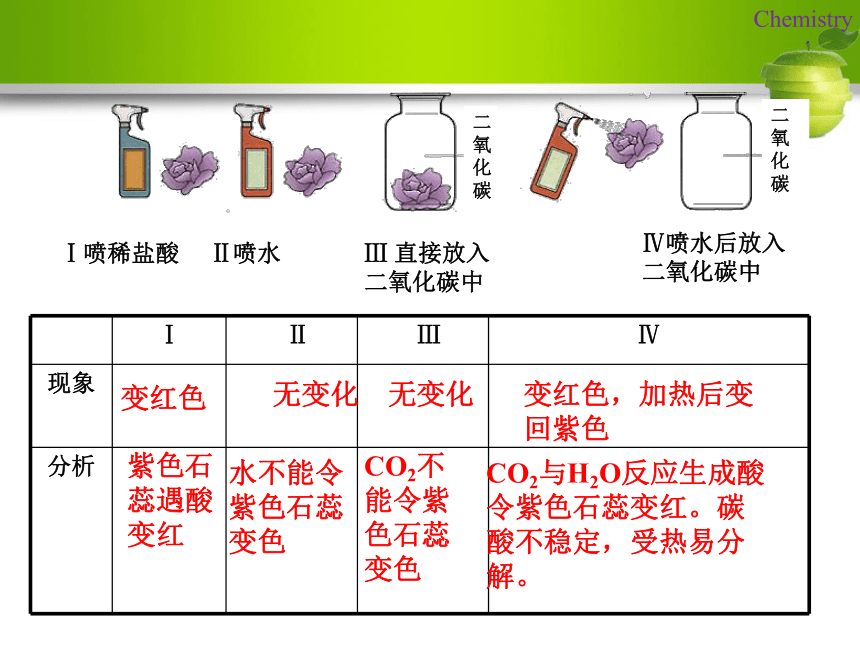
一般情况二氧化碳不能燃烧也不支持燃烧[实验6-5]如图所示,向一个收集满二氧化碳气体的质地较软的塑料瓶中加入约1/3的水,立即旋紧瓶盖,振荡。观察现象并分析。因为二氧化碳溶于水,使瓶内的气体减少,压强变小,外界大气压将瓶子压瘪。根据实验6-3、6-4完成下表(密度同空气比较)无色气体无味比空气的密度大能溶于水一般情况下,不支持燃烧想一想:我们平时打开碳酸饮料时,常有大量的气体产生,这是什么气体呢?这是利用哪一点性质?答:气体是二氧化碳,在通常状况下,1体积的水约能溶解1体积的二氧化碳,增大压强还会溶解得更多。生产汽水等碳酸型饮料就是利用了二氧化碳的这一性质。变红色无变化紫色石蕊遇酸变红水不能令紫色石蕊变色无变化CO2不能令紫色石蕊变色变红色,加热后变回紫色CO2与H2O反应生成酸令紫色石蕊变红。碳酸不稳定,受热易分解。Ⅰ喷稀盐酸 Ⅱ喷水Ⅳ喷水后放入二氧化碳中Ⅲ 直接放入二氧化碳中复习:如何检验一瓶无色无味的气体是CO2?步骤:注入少量澄清石灰水,振荡,现象:石灰水变白色浑浊。在一定条件下,二氧化碳气体会变成固体,固体二氧化碳叫“干冰”。干冰升华时,吸收大量的热,因此可作制冷剂。如人工降降雨等。 小 结 二 氧 化 碳 的 性 质1、二氧化碳的性质CO2的物理性质:1、无色、无味的气体
2、密度比空气大 ρ=1.977g/L
3、能溶于水
4、熔沸点较低,干冰—固态CO2CO2的化学性质:1、一般情况不能燃烧燃烧、也不支持燃烧;不能供给呼吸。
2、与水反应,生成碳酸。
CO2 + H2O == H2CO3 (碳酸使石蕊变红)
H2CO3 == H2O + CO2 ↑(碳酸不稳定)
3、CO2与石灰水的反应
CO2+Ca(OH)2=CaCO3 ↓+ H2O2、二氧化碳对生活和环境的影响二氧化碳的用途:(二氧化碳对人类有益的一面)① 植物光合作用② 温室中气体肥料③ 化工产品的原料④ 灭火贮存食品人造舞台云雾⑤干冰作制冷剂二氧化碳对人类及环境不利的一面(1)二氧化碳浓度过高会导致人和动物的死亡1%使人感到气闷、头昏、心悸4%~5%使人感到气喘、头痛、眩晕10 %使人神志不清、呼吸停止,以至死亡产生温室效应的气体二氧化碳、臭氧、甲烷、氟氯代烷二 一氧化碳物理性质:无色 无味的气体 密度 1.25 g/L(空气的密度1.29g/L)。难溶于水
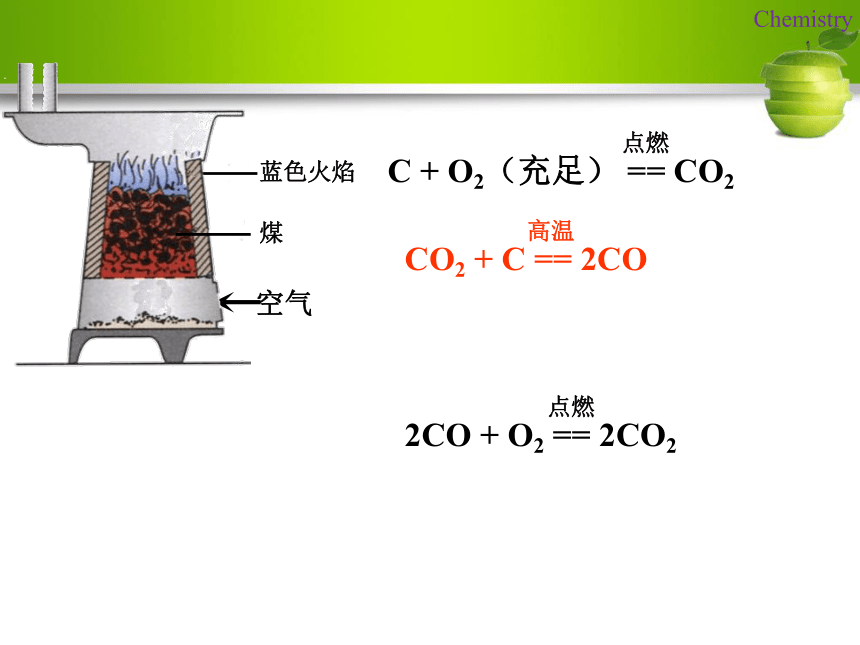
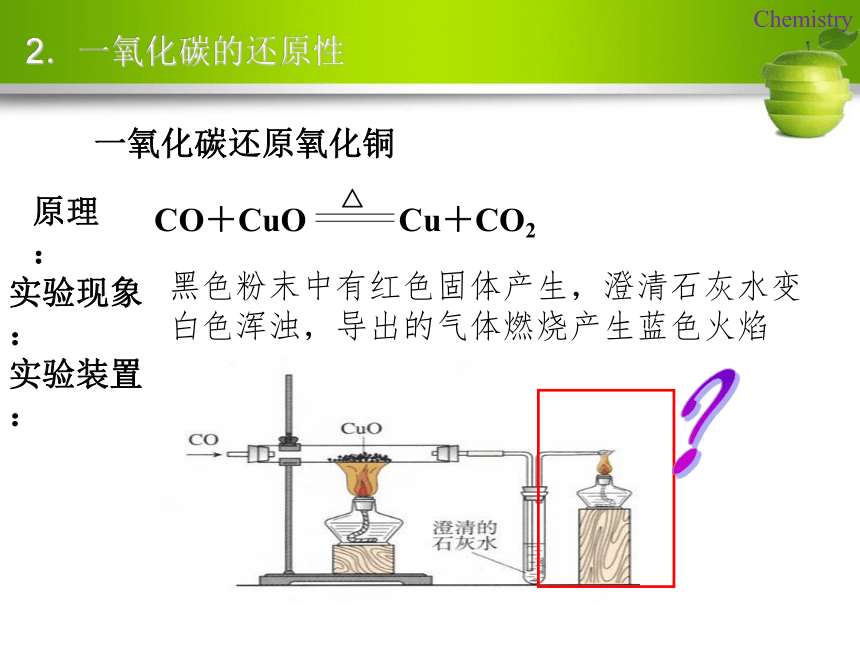
化学性质:现象:燃烧放出大量的热,火焰显蓝色 C + O2(充足) == CO2点燃CO2 + C == 2CO高温2CO + O2 == 2CO2点燃2.一氧化碳的还原性一氧化碳还原氧化铜原理:实验装置:实验现象:黑色粉末中有红色固体产生,澄清石灰水变白色浑浊,导出的气体燃烧产生蓝色火焰?实验步骤:
⑴先通入一氧化碳,在加热前必须先检验一氧化碳的纯度------排尽玻璃管中的空气,防止加热时引起空气和一氧化碳混合气体的爆炸⑵点燃酒精灯加热⑶实验完毕后先熄灭酒精灯,再通入一会儿一氧化碳直到试管冷却----防止生成的铜再被氧化成氧化铜尾气处理:(1)点燃法 (2)收集法3.一氧化碳的毒性 一氧化碳有剧毒。这是因为一氧化碳吸进肺里很容易跟血液里的血红蛋白结合,使血红蛋白不能很好地跟氧气结合,造成生物体缺氧。如果吸入较多的一氧化碳,会因缺少氧气而死亡。 预防煤气中毒,应该注意通风排气。 CO和CO2的比较点燃△高温点燃高温3.一氧化碳的毒性 一氧化碳有剧毒。这是因为一氧化碳吸进肺里很容易跟血液里的血红蛋白结合,使血红蛋白不能很好地跟氧气结合,造成生物体缺氧。如果吸入较多的一氧化碳,会因缺少氧气而死亡。 预防煤气中毒,应该注意通风排气。§6.3 二氧化碳和一氧化碳CO2CO第二课时 空气中的CO有一半来自于汽车排放的尾气。性 质气体色、态、味密 度溶 解 性COCO2无色无味的气体无色无味的气体比空气略小 比空气大难溶于水能溶于水比较 CO 和 CO2 的物理性质〈探讨〉CO和CO2 的物理性质不同的原因?相 同不相同不相同 虽然元素组成相同,但是分子构成不同,所以它们的物理性质有差异。⒈CO物理性质请选择收集CO的方法。CO的性质:⒈ CO难溶于水。⒉ CO密度比空气略小。⒊ CO具有毒性。收集CO的方法:收集 CO只能用排水法。 CO和CO2 的组成元素完全相同, 它们的化学性质是相似还是不同呢?⒈CO化学性质假设: CO和CO2性质相似或性质不同。
(以CO2的性质为基础提出性质的假设)1. 能否与水化合。2. 是否不可燃,也不支持燃烧。3. 能否与石灰水反应。4. 是否具有其它化学性质。⒉CO化学性质现象:结论:操作:将CO通入紫色的石蕊试液中。紫色石蕊没变色。CO不能与水反应生成碳酸。⒉CO化学性质现象:结论:操作:⑴点燃纯净的CO。⑴CO燃烧,产生蓝色火焰,放出热量。 ⑵在火焰上方罩一内壁涂有石灰水的烧杯。⑵澄清石灰水变浑浊。⑴CO具有燃性。⑵CO燃烧的产物是CO2。 在点燃CO之前是否也要通过验纯?为什么?你知道吗? 煤炉里的煤在燃烧过程中,发生了哪些化学反应? 液化气、天然气等含碳燃料在不充分燃烧时都会有CO生成。 CO是许多气体燃料如水煤气的主要成分。⒈CO化学性质现象:结论:操作: 将纯净的 CO 通过灼热的CuO,再将生成的气体通入澄清的石灰水中。并对尾气处理。⑴黑色的CuO粉逐渐变成红色。⑵产生的气体使澄清石灰水变浑浊。⑶此套装置中增添了尾气处理装置。 仔细观察CO和H2在还原CuO时,装置有何不同?为什么要这样设计装置? 对CO还原CuO实验中的尾气处理方法有哪几种?你认为哪种方法较好?请说明理由。对一氧化碳还原性的分析△CO CO2↑CuO Cu一氧化碳具有还原性,是还原剂;
在反应中被氧化,发生氧化反应。氧化铜具有氧化性,是氧化剂;
在反应中被还原,发生还原反应。⒉CO化学性质现象:结论:操作: 将CO通入澄清石灰水中观察现象。石灰水不变浑浊。 CO不与Ca(OH)2 反应。⒉CO化学性质现象:结论: 正常的血液呈深红色,当通入CO后,血液由深红色变成鲜红色。 CO有剧毒!人在CO达到总体积0.02%的空气中,持续2 h~3 h 即出现中毒症状。⒉CO化学性质动脉静脉CO与Hb的结合能力是O2与Hb结合能力的200~300倍⒉CO化学性质讨 论 题 ㈠ ⒈ 煤气厂为什么常在家用煤气(含有CO)中掺入微量具有难闻气味的气体? ⒉ 如发生煤气泄漏应当怎么办?注意哪些事项? 任何物质都必须合理运用。在应用中,物质的性质可能有利于人类,也可能不利于人类。请仿照示例填写下表:广泛用于支持燃烧;
供动植物呼吸可用于民用或工业燃料植物的光合作用;
灭火;人工降雨造成食物的腐烂;
钢铁的锈蚀使用不当容易引起中毒事故大气中含量过多会引起“温室效应” ⒈ 此实验装置还能做哪些改进?讨 论 题 ㈡ ⒉ 由此实验中的现象,可得出哪些物质的性质?你能写出哪些反应的化学方程式?⒊ 怎样实现下列变化?用化学方程式来表示。⑴⑵⑶⑷CaCO3⑸⑹总 结三、CO的性质。四、CO对生活和环境的影响。⒉CO的化学性质: 通常CO是无色无味的气体,难溶于水,密度比空气略小。⒈CO的物理性质:⑴CO具有可燃性。⑵CO具有还原性。⑶CO有剧毒。⑷CO既不与水反应,也不与石灰水反应。 使用清洁燃料和开放整洁的厨房,能最大限度地减少室内空气污染源,全面提高健康生活的质量。
一般情况二氧化碳不能燃烧也不支持燃烧[实验6-5]如图所示,向一个收集满二氧化碳气体的质地较软的塑料瓶中加入约1/3的水,立即旋紧瓶盖,振荡。观察现象并分析。因为二氧化碳溶于水,使瓶内的气体减少,压强变小,外界大气压将瓶子压瘪。根据实验6-3、6-4完成下表(密度同空气比较)无色气体无味比空气的密度大能溶于水一般情况下,不支持燃烧想一想:我们平时打开碳酸饮料时,常有大量的气体产生,这是什么气体呢?这是利用哪一点性质?答:气体是二氧化碳,在通常状况下,1体积的水约能溶解1体积的二氧化碳,增大压强还会溶解得更多。生产汽水等碳酸型饮料就是利用了二氧化碳的这一性质。变红色无变化紫色石蕊遇酸变红水不能令紫色石蕊变色无变化CO2不能令紫色石蕊变色变红色,加热后变回紫色CO2与H2O反应生成酸令紫色石蕊变红。碳酸不稳定,受热易分解。Ⅰ喷稀盐酸 Ⅱ喷水Ⅳ喷水后放入二氧化碳中Ⅲ 直接放入二氧化碳中复习:如何检验一瓶无色无味的气体是CO2?步骤:注入少量澄清石灰水,振荡,现象:石灰水变白色浑浊。在一定条件下,二氧化碳气体会变成固体,固体二氧化碳叫“干冰”。干冰升华时,吸收大量的热,因此可作制冷剂。如人工降降雨等。 小 结 二 氧 化 碳 的 性 质1、二氧化碳的性质CO2的物理性质:1、无色、无味的气体
2、密度比空气大 ρ=1.977g/L
3、能溶于水
4、熔沸点较低,干冰—固态CO2CO2的化学性质:1、一般情况不能燃烧燃烧、也不支持燃烧;不能供给呼吸。
2、与水反应,生成碳酸。
CO2 + H2O == H2CO3 (碳酸使石蕊变红)
H2CO3 == H2O + CO2 ↑(碳酸不稳定)
3、CO2与石灰水的反应
CO2+Ca(OH)2=CaCO3 ↓+ H2O2、二氧化碳对生活和环境的影响二氧化碳的用途:(二氧化碳对人类有益的一面)① 植物光合作用② 温室中气体肥料③ 化工产品的原料④ 灭火贮存食品人造舞台云雾⑤干冰作制冷剂二氧化碳对人类及环境不利的一面(1)二氧化碳浓度过高会导致人和动物的死亡1%使人感到气闷、头昏、心悸4%~5%使人感到气喘、头痛、眩晕10 %使人神志不清、呼吸停止,以至死亡产生温室效应的气体二氧化碳、臭氧、甲烷、氟氯代烷二 一氧化碳物理性质:无色 无味的气体 密度 1.25 g/L(空气的密度1.29g/L)。难溶于水
化学性质:现象:燃烧放出大量的热,火焰显蓝色 C + O2(充足) == CO2点燃CO2 + C == 2CO高温2CO + O2 == 2CO2点燃2.一氧化碳的还原性一氧化碳还原氧化铜原理:实验装置:实验现象:黑色粉末中有红色固体产生,澄清石灰水变白色浑浊,导出的气体燃烧产生蓝色火焰?实验步骤:
⑴先通入一氧化碳,在加热前必须先检验一氧化碳的纯度------排尽玻璃管中的空气,防止加热时引起空气和一氧化碳混合气体的爆炸⑵点燃酒精灯加热⑶实验完毕后先熄灭酒精灯,再通入一会儿一氧化碳直到试管冷却----防止生成的铜再被氧化成氧化铜尾气处理:(1)点燃法 (2)收集法3.一氧化碳的毒性 一氧化碳有剧毒。这是因为一氧化碳吸进肺里很容易跟血液里的血红蛋白结合,使血红蛋白不能很好地跟氧气结合,造成生物体缺氧。如果吸入较多的一氧化碳,会因缺少氧气而死亡。 预防煤气中毒,应该注意通风排气。 CO和CO2的比较点燃△高温点燃高温3.一氧化碳的毒性 一氧化碳有剧毒。这是因为一氧化碳吸进肺里很容易跟血液里的血红蛋白结合,使血红蛋白不能很好地跟氧气结合,造成生物体缺氧。如果吸入较多的一氧化碳,会因缺少氧气而死亡。 预防煤气中毒,应该注意通风排气。§6.3 二氧化碳和一氧化碳CO2CO第二课时 空气中的CO有一半来自于汽车排放的尾气。性 质气体色、态、味密 度溶 解 性COCO2无色无味的气体无色无味的气体比空气略小 比空气大难溶于水能溶于水比较 CO 和 CO2 的物理性质〈探讨〉CO和CO2 的物理性质不同的原因?相 同不相同不相同 虽然元素组成相同,但是分子构成不同,所以它们的物理性质有差异。⒈CO物理性质请选择收集CO的方法。CO的性质:⒈ CO难溶于水。⒉ CO密度比空气略小。⒊ CO具有毒性。收集CO的方法:收集 CO只能用排水法。 CO和CO2 的组成元素完全相同, 它们的化学性质是相似还是不同呢?⒈CO化学性质假设: CO和CO2性质相似或性质不同。
(以CO2的性质为基础提出性质的假设)1. 能否与水化合。2. 是否不可燃,也不支持燃烧。3. 能否与石灰水反应。4. 是否具有其它化学性质。⒉CO化学性质现象:结论:操作:将CO通入紫色的石蕊试液中。紫色石蕊没变色。CO不能与水反应生成碳酸。⒉CO化学性质现象:结论:操作:⑴点燃纯净的CO。⑴CO燃烧,产生蓝色火焰,放出热量。 ⑵在火焰上方罩一内壁涂有石灰水的烧杯。⑵澄清石灰水变浑浊。⑴CO具有燃性。⑵CO燃烧的产物是CO2。 在点燃CO之前是否也要通过验纯?为什么?你知道吗? 煤炉里的煤在燃烧过程中,发生了哪些化学反应? 液化气、天然气等含碳燃料在不充分燃烧时都会有CO生成。 CO是许多气体燃料如水煤气的主要成分。⒈CO化学性质现象:结论:操作: 将纯净的 CO 通过灼热的CuO,再将生成的气体通入澄清的石灰水中。并对尾气处理。⑴黑色的CuO粉逐渐变成红色。⑵产生的气体使澄清石灰水变浑浊。⑶此套装置中增添了尾气处理装置。 仔细观察CO和H2在还原CuO时,装置有何不同?为什么要这样设计装置? 对CO还原CuO实验中的尾气处理方法有哪几种?你认为哪种方法较好?请说明理由。对一氧化碳还原性的分析△CO CO2↑CuO Cu一氧化碳具有还原性,是还原剂;
在反应中被氧化,发生氧化反应。氧化铜具有氧化性,是氧化剂;
在反应中被还原,发生还原反应。⒉CO化学性质现象:结论:操作: 将CO通入澄清石灰水中观察现象。石灰水不变浑浊。 CO不与Ca(OH)2 反应。⒉CO化学性质现象:结论: 正常的血液呈深红色,当通入CO后,血液由深红色变成鲜红色。 CO有剧毒!人在CO达到总体积0.02%的空气中,持续2 h~3 h 即出现中毒症状。⒉CO化学性质动脉静脉CO与Hb的结合能力是O2与Hb结合能力的200~300倍⒉CO化学性质讨 论 题 ㈠ ⒈ 煤气厂为什么常在家用煤气(含有CO)中掺入微量具有难闻气味的气体? ⒉ 如发生煤气泄漏应当怎么办?注意哪些事项? 任何物质都必须合理运用。在应用中,物质的性质可能有利于人类,也可能不利于人类。请仿照示例填写下表:广泛用于支持燃烧;
供动植物呼吸可用于民用或工业燃料植物的光合作用;
灭火;人工降雨造成食物的腐烂;
钢铁的锈蚀使用不当容易引起中毒事故大气中含量过多会引起“温室效应” ⒈ 此实验装置还能做哪些改进?讨 论 题 ㈡ ⒉ 由此实验中的现象,可得出哪些物质的性质?你能写出哪些反应的化学方程式?⒊ 怎样实现下列变化?用化学方程式来表示。⑴⑵⑶⑷CaCO3⑸⑹总 结三、CO的性质。四、CO对生活和环境的影响。⒉CO的化学性质: 通常CO是无色无味的气体,难溶于水,密度比空气略小。⒈CO的物理性质:⑴CO具有可燃性。⑵CO具有还原性。⑶CO有剧毒。⑷CO既不与水反应,也不与石灰水反应。 使用清洁燃料和开放整洁的厨房,能最大限度地减少室内空气污染源,全面提高健康生活的质量。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
