[中学联盟]浙江省宁波诺丁汉大学附属中学2016-2017学年高二下学期期末考试化学试题(word版,含答案)
文档属性
| 名称 | [中学联盟]浙江省宁波诺丁汉大学附属中学2016-2017学年高二下学期期末考试化学试题(word版,含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 788.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-07-06 00:00:00 | ||
图片预览



文档简介
宁波诺丁汉大学附属中学
2016-2017学年度第二学期期末考试
高二年级化学试卷
答卷时间:90min
满分:100
命题人:张晓爽
可能用到的相对原子质量:
H—1
C—12
N—14
O—16
S—32
一、选择题(本题共25小题,每小题2分,共50分。每小题只有一个选项符合题意)
1.下列表示物质结构的化学用语或模型正确的是
A.醛基的电子式:
B.CH4
分子的球棍模型:
C.乙烯的最简式(实验式):CH2
D.苯乙醛结构简式:
2.下列各化合物的命名错误的是
A.
1,2
-
二甲苯
B.
CH2=CH—CH=CH2
1,3
-
二丁烯
C.
2
-
丁醇
D.
2
-
甲基丁烷
3.下列分子式只能表示一种物质的是
A.
C3H4Cl2
B.
C3H8
C.
C2H6O
D.
C2H4O2
4.有机物CH3CH=CHCl可能发生的反应有:
①取代反应;
②加成反应;
③消去反应;
④使溴水褪色;
⑤使酸性高锰酸钾溶液褪色;⑥与AgNO3溶液反应生成白色沉淀;
⑦聚合反应。
A.以上反应均可发生
B.只有⑦不能发生
C.只有⑥不可以发生
D.只有②不可以发生
5.通过核磁共振氢谱可以推知(CH3)2CHCH2CH2OH有多少种化学环境的氢原子
A.6
B.5
C.4
D.3
6.下列各组物质,互为同系物的是
A.
乙二醇与丙三醇
B.
乙烯与环丙烷
C.
乙酸与硬脂酸
D.
苯与苯乙烯
7.现有四氯化碳、苯、酒精、己烯四瓶无标签液体,要将它们鉴别开,下列试剂中可行的是
A.
水
B.
溴水
C.
浓硫酸
D.
石蕊试液
8.下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中产物中一定不存在同分异构体的是
A.邻羟基苯甲酸与NaHCO3溶液反应
B.
2-氯丁烷()与NaOH的乙醇溶液共热
C.
甲苯在一定条件下发生硝化生成一硝基甲苯的反应
D.
异戊二烯()与等物质的量的Br2发生加成反应
9.在核磁共振氢谱中出现两组峰,其氢原子数之比为3:2的化合物是
10.三聚氰胺是一种优良的化工原料,主要用来制涂料和黏合剂,它的相对分子质量介于100与200之间,碳的质量分数为28.57%,碳、氢的质量比为6∶1,其余为氮。则三聚氰胺的分子式为
A.(CH2N2)n
B.
C3H4ON5
C.
C3H6N6
D.
C4H4N5
11.下列说法正确的是
A.结构片段为的高聚物,其单体是甲醛和苯酚
B.
等质量的乙烯、乙醇、丙烯酸(CH2=CH-COOH)完全燃烧消耗氧气的量相等
C.
由甘氨酸、丙氨酸形成的二肽有三种
D.
石油的裂化、煤的气化与液化都属于化学变化,而石油的分馏与煤的干馏都属于物理变化
12.苯甲酸(C6H5COOH)和山梨酸(CH3—CH
=
CH—CH
=
CH—COOH)都是常用的食品防腐剂。下列物质中只能与其中一种酸发生反应的是
A.
金属钠
B.
氢氧化钠
C.
溴水
D.
乙醇
13.当一个碳原子连有4个不同的原子或原子团时,这种碳原子被称为“手性碳原子”,具有手性碳原子的化合物具有光学活性。例如右图所示物质,其中带
号的碳原子即是手性碳原子,现使该物质发生下列反应:
①与新制氢氧化铜反应,并酸化,得有机产物A
;
②与氢氧化钠水溶液共热得产物B和乙酸钠。
则对所得产物A、B的描述正确的是
A.A、B均具有光学活性
B.A具有光学活性,B不具有光学活性
C.A不具有光学活性,B具有光学活性
D.A、B均不具有光学活性
14.某物质可能含有甲酸、乙酸、甲醇和甲酸乙酯四种物质中的一种或几种,在鉴定时有下列现象:
①有银镜反应;
②加入新制Cu(OH)2悬浊液沉淀不溶解;
③与含酚酞的NaOH溶液共热,发现溶液中红色逐渐褪去以至无色。
下列叙述正确的是
A.
有甲酸乙酯和甲醇
B.
有甲酸乙酯和甲酸
C.
有甲酸乙酯,可能有甲醇
D.
几种物质都有
15.有机物甲的分子式为C9H18O2,在酸性条件下甲水解为乙和丙两种有机物,在相同的温度和压强下,同质量的乙和丙的蒸气所占体积相同,则甲的可能结构有
A.8种
B.
12种
C.
16种
D.
18种
16.某有机物甲经氧化后最终得到乙(分子式为C2H3O2Cl);而甲经水解可得丙,1
mol丙和2
mol乙反应得一种含氯的酯(C6H8O4Cl2);由此推断甲的结构简式为
A.ClCH2CH2OH
B.OHC-O-CH2Cl
C.ClCH2CHO
D.
HOCH2CH2O
17.某有机物结构为:,它可能具有的性质是
①能使KMnO4酸性溶液褪色;
②能与NaOH溶液反应;
③能发生聚合反应;
④能与[Ag(NH3)2]OH溶液发生银镜反应。
A.
只有①
②
B.
只有②
③
C.
只有①
②
③
D.
①
②
③
④
18.下列说法正确的是
A.试纸在检测溶液时不需要湿润,而检测气体时必须湿润
B.焰色反应使用的铂丝通常可用稀硫酸清洗
C.碘水中的碘可以用酒精萃取
D.在实验室遇酸灼伤,用水洗后再用稀NaOH溶液浸洗
19.
下列实验中,有关仪器的下端必须插入液面以下的是
①制备乙烯时用的温度计
②制备氯气装置中的分液漏斗
③制备氨水时将氨气溶于水的导管
④制备氢气的简易装置中加入稀硫酸用的长颈漏斗
⑤分馏石油时的温度计
⑥制备乙酸乙酯时,将乙酸乙酯蒸气通入饱和Na2CO3溶液的导管
A.①④
B.①②④⑤
C.①②③⑥
D.①③④
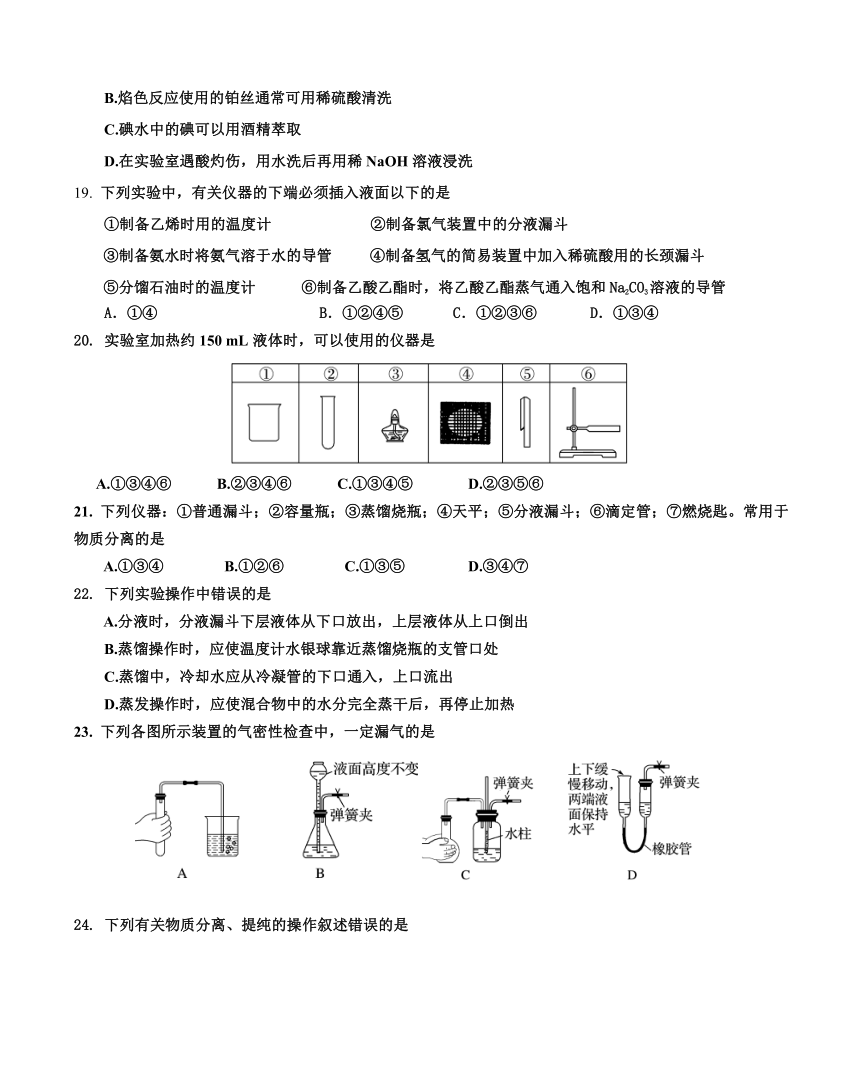
20.
实验室加热约150
mL液体时,可以使用的仪器是
INCLUDEPICTURE
"../../../"
\
MERGEFORMAT
A.①③④⑥
B.②③④⑥
C.①③④⑤
D.②③⑤⑥
21.
下列仪器:①普通漏斗;②容量瓶;③蒸馏烧瓶;④天平;⑤分液漏斗;⑥滴定管;⑦燃烧匙。常用于物质分离的是
A.①③④
B.①②⑥
C.①③⑤
D.③④⑦
22.
下列实验操作中错误的是
A.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.蒸馏中,冷却水应从冷凝管的下口通入,上口流出
D.蒸发操作时,应使混合物中的水分完全蒸干后,再停止加热
23.
下列各图所示装置的气密性检查中,一定漏气的是
INCLUDEPICTURE
"../../../"
\
MERGEFORMAT
INCLUDEPICTURE
"../../../"
\
MERGEFORMAT
24.
下列有关物质分离、提纯的操作叙述错误的是
A.
做蒸馏实验时,在蒸馏烧瓶中应加入沸石,以防暴沸。如果在沸腾前发现忘记加沸石,应立即停止加热,冷却后补加
B.
提纯混有少量硝酸钾的氯化钠,应采用在较高温度下制得浓溶液再冷却结晶、过滤、干燥的方法
C
.
1
己醇的沸点比己烷的沸点高,1 己醇和己烷可通过蒸馏初步分离
D.
提纯含有少量乙酸的乙酸乙酯:向含有少量乙酸的乙酸乙酯中加入适量饱和Na2CO3溶液,振荡后静置分液,并除去有机相的水
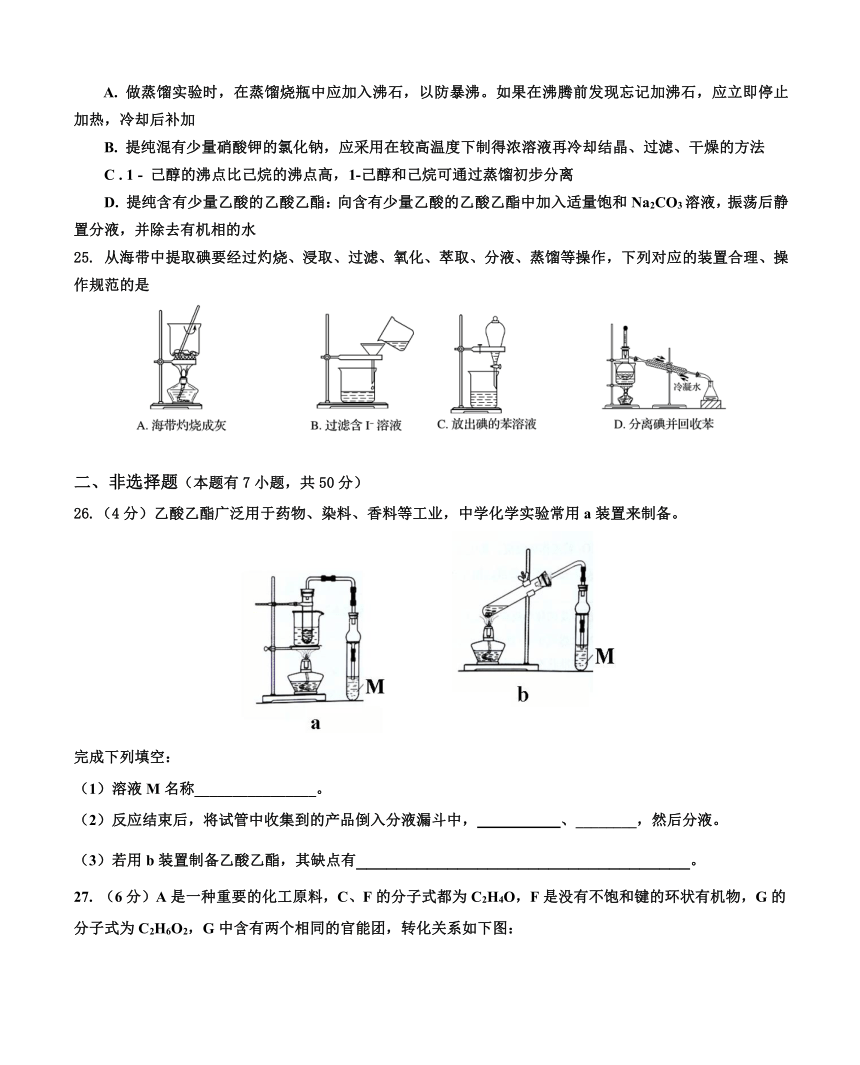
25.
从海带中提取碘要经过灼烧、浸取、过滤、氧化、萃取、分液、蒸馏等操作,下列对应的装置合理、操作规范的是
INCLUDEPICTURE
"../../../"
\
MERGEFORMAT
INCLUDEPICTURE
"../../../"
\
MERGEFORMAT
二、非选择题(本题有7小题,共50分)
26.(4分)乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用a装置来制备。
完成下列填空:
(1)溶液M名称________________。
(2)反应结束后,将试管中收集到的产品倒入分液漏斗中,
、________,然后分液。
(3)若用b装置制备乙酸乙酯,其缺点有_________________________________。
27.
(6分)A是一种重要的化工原料,C、F的分子式都为C2H4O,F是没有不饱和键的环状有机物,G的分子式为C2H6O2,G中含有两个相同的官能团,转化关系如下图:
己知:同一碳原子上连接2个或2个以上—OH是不稳定结构。
请回答:
(1)有机物C中含有的官能团名称是_________________。
(2)有机物E的结构简式______________。
(3)F→G的化学方程式是_______________。
(4)下列说法正确的是____________。
A.有机物D能使石蕊溶液变红
B.用新制碱性氢氧化铜悬浊液无法区分有机物B、C、D的水溶液
C.等物质的量的A和B分别完全燃烧消耗氧气的量相等
D.可用饱和碳酸钠溶液除去有机物E中混有的少量B、D
28.(每小题2分,共8分)甲、乙、丙、丁四种有机物的分子式均为C3H6O2,根据下列性质,写出符合条件的各有机物的结构简式或有关的化学方程式。
(1)甲能与NaHCO3反应放出CO2,该反应的离子方程式为:______________________。
(2)乙既能发生银镜反应又能发生水解反应,乙的结构简式为:_____________________。
(3)
丙只能发生水解反应,丙在碱性条件下发生水解反应的化学方程式为:___________。
(4)丁能使溴水褪色,也能发生加聚反应,丁的结构简式为:____________________。
29.(共6分)以淀粉和油脂为原料,制备生活中某些物质。
请回答下列问题:
(1)淀粉的分子式为
。
(2)F的化学式是______________________。
(3)E可能的结构简式为___________________________________。
30.(每小题2分,共8分)
查尔酮类化合物G是黄酮类药物的主要合成中间体,其中一种合成路线如下:
已知以下信息:
①芳香烃A的相对分子质量在100-110之间,1
mol
A充分燃烧可生成72
g水。
②C不能发生银镜反应。
③D能发生银镜反应、可溶于饱和Na2CO3溶液、核磁共振氢谱显示其有4种氢原子。
回答下列问题:
(1)A的化学名称为__________
。
(2)由B生成C的化学方程式为_____________________________________
。
(3)G的结构简式为____________________________
。
(4)F的同分异构体中,既能发生银镜反应,又能与FeCl3溶液发生显色反应的有很多种,其中核磁共振氢谱为5组峰,且峰面积比为2:2:2:1:1的为______________(写结构简式)。
31.(每空2分,共10分)实验室用加热l-丁醇、溴化钠和浓硫酸的混合物的方法来制备1-溴丁烷时,还会有烯、醚等副产物生成。反应结束后将反应混合物蒸馏,分离得到1—溴丁烷,已知相关有机物的性质如下:
物质
熔点/℃
沸点/℃
1-丁醇
-89.53
117.25
1-溴丁烷
-112.4
101.6
丁醚
-95.3
142.6
1-丁烯
-185.3
-6.5
(1)反应中由于发生副反应而生成醚的有机反应类型为
____。
(2)制备1-溴丁烷的装置应选用下图中的_____
__(填序号)。
反应加热时的温度不宜超过100℃,理由是_______________
____________。
A
B
C
D
(3)当给烧瓶中的混合物加热时,溶液会出现橘红色,其原因是___________________。
(4)反应结束后,将反应混合物中1-溴丁烷分离出来的操作方法名称为__
___。
32.
(8分)中华人民共和国国家标准(GB2760 2011)规定葡萄酒中SO2最大使用量为0.2500
g·L-1。某兴趣小组用图1装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定。
INCLUDEPICTURE
"../../../"
\
MERGEFORMAT
INCLUDEPICTURE
"../../../"
\
MERGEFORMAT
(1)
仪器A的名称是______________,水通入A的进口为________。
(2)
B中加入300.00
mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,其化学方程式为________________________________。
(3)
除去C中过量的H2O2,然后用0.090
00
mol·L-1NaOH标准溶液进行滴定,滴定前排气泡时,应选择图2中的________;
若滴定终点时溶液的pH=8.8,则选择的指示剂为____________;
若用50
mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积(填序号)________(①=10
mL,②=40
mL,③<10
mL,④>40
mL
)。
(4)
滴定至终点时,消耗NaOH溶液25.00
mL,该葡萄酒中SO2含量为___________g·L-1。
宁波诺丁汉大学附属中学2016-2017学年第二学期期末考试
姓名:
班级:
考场:
座号:
注意:1.考号及选择题必须用2B铅笔填涂,文字题用黑色水笔或签字笔在答题框内作答。2.请保持答卷平整,不要折叠。
考号(班号)填涂区
高二年级化学答题卷
一、选择题(共25个小题,每小题2分,共50分)
12345
678910
1112131415
1617181920
2122232425
二、非选择题(共7个小题,共50分)
2016-2017学年度第二学期期末考试
高二化学参考答案
一、选择题(本题共25小题,每小题2分,共50分)
题号
1
2
3
4
5
6
7
8
9
10
答案
C
B
B
C
B
C
B
A
D
C
题号
11
12
13
14
15
16
17
18
19
20
答案
A
C
B
C
C
A
C
A
A
A
题号
21
22
23
24
25
答案
C
D
D
B
D
二、非选择题(本题有7小题,共50分)
26.
(每空1分,共4分)
(1)饱和碳酸钠溶液
(2)振荡、静置
(3)原料损失较大、易发生副反应
27.
(6分)
(1)醛基(1分);
(2)CH3COOCH2CH3(1分);
(3)(2分);
(4)ACD(2分)。
28.(每空2分,共8分)
(1)
CH3CH2COOH
+
NaHCO3
→CH3CH2COONa
+
CO2
↑+H2O
(2)
HCOOCH2CH3
(3)
CH3COOCH3+
NaOH
—→CH3COONa
+
CH3OH
(4)
CH2
=
CH—O—CH2OH
29.(6分)
(1)(C6H10O5)n
(2)C17H35COONa
(3)
(各1分)
30.(每小题2分,共8分)
(1)苯乙烯
(2)
(3)
(4)
31.(每空2分,共10分)
(1)取代反应
(2)C
防止1-溴丁烷因气化而逸出,影响产率。
(3)-1价的溴被氧化生成溴单质,溶于反应液中。
(4)蒸馏。
32.
(8分)
(1)
冷凝管(或冷凝器)
b
(2)
SO2+H2O2===H2SO4
(3)
③
酚酞
④
(4)
0.2400
SO2 ~ H2SO4 ~ 2NaOH
64
g 2
mol
m(SO2)
0.090
00
mol·L-1×0.02500
L
解得:m(SO2)==0.07200
g,
故葡萄酒中SO2的含量为=0.2400
g·L-1。
H
26.
(4分)
(1)________________。
(2)__________,___________。
(3)_____________________________________________。
29.
(6分)
(1)________________。(2)____________________。
(3)_____________________________________________。
28.
(8分)
(1)___________________________________________________。
(2)_______________________。
(3)___________________________________________________。
(4)_______________________。
27.
(6分)
(1)__________。
(2)__________。
(3)_____________________________________________。
(4)__________。
30.
(8分)
(1)_______________________。
(2)___________________________________________________。
(3)_______________________。
(4)_______________________。
31.
(10分)
(1)________________。
(2)_________,________________________________________。
(3)___________________________________________________。
(4)_______________。
32.
(8分)
(1)_________,__________。
(2)__________________________________________。
(3)__________,
____________,
_____________。
(4)_____________。
Δ
2016-2017学年度第二学期期末考试
高二年级化学试卷
答卷时间:90min
满分:100
命题人:张晓爽
可能用到的相对原子质量:
H—1
C—12
N—14
O—16
S—32
一、选择题(本题共25小题,每小题2分,共50分。每小题只有一个选项符合题意)
1.下列表示物质结构的化学用语或模型正确的是
A.醛基的电子式:
B.CH4
分子的球棍模型:
C.乙烯的最简式(实验式):CH2
D.苯乙醛结构简式:
2.下列各化合物的命名错误的是
A.
1,2
-
二甲苯
B.
CH2=CH—CH=CH2
1,3
-
二丁烯
C.
2
-
丁醇
D.
2
-
甲基丁烷
3.下列分子式只能表示一种物质的是
A.
C3H4Cl2
B.
C3H8
C.
C2H6O
D.
C2H4O2
4.有机物CH3CH=CHCl可能发生的反应有:
①取代反应;
②加成反应;
③消去反应;
④使溴水褪色;
⑤使酸性高锰酸钾溶液褪色;⑥与AgNO3溶液反应生成白色沉淀;
⑦聚合反应。
A.以上反应均可发生
B.只有⑦不能发生
C.只有⑥不可以发生
D.只有②不可以发生
5.通过核磁共振氢谱可以推知(CH3)2CHCH2CH2OH有多少种化学环境的氢原子
A.6
B.5
C.4
D.3
6.下列各组物质,互为同系物的是
A.
乙二醇与丙三醇
B.
乙烯与环丙烷
C.
乙酸与硬脂酸
D.
苯与苯乙烯
7.现有四氯化碳、苯、酒精、己烯四瓶无标签液体,要将它们鉴别开,下列试剂中可行的是
A.
水
B.
溴水
C.
浓硫酸
D.
石蕊试液
8.下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中产物中一定不存在同分异构体的是
A.邻羟基苯甲酸与NaHCO3溶液反应
B.
2-氯丁烷()与NaOH的乙醇溶液共热
C.
甲苯在一定条件下发生硝化生成一硝基甲苯的反应
D.
异戊二烯()与等物质的量的Br2发生加成反应
9.在核磁共振氢谱中出现两组峰,其氢原子数之比为3:2的化合物是
10.三聚氰胺是一种优良的化工原料,主要用来制涂料和黏合剂,它的相对分子质量介于100与200之间,碳的质量分数为28.57%,碳、氢的质量比为6∶1,其余为氮。则三聚氰胺的分子式为
A.(CH2N2)n
B.
C3H4ON5
C.
C3H6N6
D.
C4H4N5
11.下列说法正确的是
A.结构片段为的高聚物,其单体是甲醛和苯酚
B.
等质量的乙烯、乙醇、丙烯酸(CH2=CH-COOH)完全燃烧消耗氧气的量相等
C.
由甘氨酸、丙氨酸形成的二肽有三种
D.
石油的裂化、煤的气化与液化都属于化学变化,而石油的分馏与煤的干馏都属于物理变化
12.苯甲酸(C6H5COOH)和山梨酸(CH3—CH
=
CH—CH
=
CH—COOH)都是常用的食品防腐剂。下列物质中只能与其中一种酸发生反应的是
A.
金属钠
B.
氢氧化钠
C.
溴水
D.
乙醇
13.当一个碳原子连有4个不同的原子或原子团时,这种碳原子被称为“手性碳原子”,具有手性碳原子的化合物具有光学活性。例如右图所示物质,其中带
号的碳原子即是手性碳原子,现使该物质发生下列反应:
①与新制氢氧化铜反应,并酸化,得有机产物A
;
②与氢氧化钠水溶液共热得产物B和乙酸钠。
则对所得产物A、B的描述正确的是
A.A、B均具有光学活性
B.A具有光学活性,B不具有光学活性
C.A不具有光学活性,B具有光学活性
D.A、B均不具有光学活性
14.某物质可能含有甲酸、乙酸、甲醇和甲酸乙酯四种物质中的一种或几种,在鉴定时有下列现象:
①有银镜反应;
②加入新制Cu(OH)2悬浊液沉淀不溶解;
③与含酚酞的NaOH溶液共热,发现溶液中红色逐渐褪去以至无色。
下列叙述正确的是
A.
有甲酸乙酯和甲醇
B.
有甲酸乙酯和甲酸
C.
有甲酸乙酯,可能有甲醇
D.
几种物质都有
15.有机物甲的分子式为C9H18O2,在酸性条件下甲水解为乙和丙两种有机物,在相同的温度和压强下,同质量的乙和丙的蒸气所占体积相同,则甲的可能结构有
A.8种
B.
12种
C.
16种
D.
18种
16.某有机物甲经氧化后最终得到乙(分子式为C2H3O2Cl);而甲经水解可得丙,1
mol丙和2
mol乙反应得一种含氯的酯(C6H8O4Cl2);由此推断甲的结构简式为
A.ClCH2CH2OH
B.OHC-O-CH2Cl
C.ClCH2CHO
D.
HOCH2CH2O
17.某有机物结构为:,它可能具有的性质是
①能使KMnO4酸性溶液褪色;
②能与NaOH溶液反应;
③能发生聚合反应;
④能与[Ag(NH3)2]OH溶液发生银镜反应。
A.
只有①
②
B.
只有②
③
C.
只有①
②
③
D.
①
②
③
④
18.下列说法正确的是
A.试纸在检测溶液时不需要湿润,而检测气体时必须湿润
B.焰色反应使用的铂丝通常可用稀硫酸清洗
C.碘水中的碘可以用酒精萃取
D.在实验室遇酸灼伤,用水洗后再用稀NaOH溶液浸洗
19.
下列实验中,有关仪器的下端必须插入液面以下的是
①制备乙烯时用的温度计
②制备氯气装置中的分液漏斗
③制备氨水时将氨气溶于水的导管
④制备氢气的简易装置中加入稀硫酸用的长颈漏斗
⑤分馏石油时的温度计
⑥制备乙酸乙酯时,将乙酸乙酯蒸气通入饱和Na2CO3溶液的导管
A.①④
B.①②④⑤
C.①②③⑥
D.①③④
20.
实验室加热约150
mL液体时,可以使用的仪器是
INCLUDEPICTURE
"../../../"
\
MERGEFORMAT
A.①③④⑥
B.②③④⑥
C.①③④⑤
D.②③⑤⑥
21.
下列仪器:①普通漏斗;②容量瓶;③蒸馏烧瓶;④天平;⑤分液漏斗;⑥滴定管;⑦燃烧匙。常用于物质分离的是
A.①③④
B.①②⑥
C.①③⑤
D.③④⑦
22.
下列实验操作中错误的是
A.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.蒸馏中,冷却水应从冷凝管的下口通入,上口流出
D.蒸发操作时,应使混合物中的水分完全蒸干后,再停止加热
23.
下列各图所示装置的气密性检查中,一定漏气的是
INCLUDEPICTURE
"../../../"
\
MERGEFORMAT
INCLUDEPICTURE
"../../../"
\
MERGEFORMAT
24.
下列有关物质分离、提纯的操作叙述错误的是
A.
做蒸馏实验时,在蒸馏烧瓶中应加入沸石,以防暴沸。如果在沸腾前发现忘记加沸石,应立即停止加热,冷却后补加
B.
提纯混有少量硝酸钾的氯化钠,应采用在较高温度下制得浓溶液再冷却结晶、过滤、干燥的方法
C
.
1
己醇的沸点比己烷的沸点高,1 己醇和己烷可通过蒸馏初步分离
D.
提纯含有少量乙酸的乙酸乙酯:向含有少量乙酸的乙酸乙酯中加入适量饱和Na2CO3溶液,振荡后静置分液,并除去有机相的水
25.
从海带中提取碘要经过灼烧、浸取、过滤、氧化、萃取、分液、蒸馏等操作,下列对应的装置合理、操作规范的是
INCLUDEPICTURE
"../../../"
\
MERGEFORMAT
INCLUDEPICTURE
"../../../"
\
MERGEFORMAT
二、非选择题(本题有7小题,共50分)
26.(4分)乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用a装置来制备。
完成下列填空:
(1)溶液M名称________________。
(2)反应结束后,将试管中收集到的产品倒入分液漏斗中,
、________,然后分液。
(3)若用b装置制备乙酸乙酯,其缺点有_________________________________。
27.
(6分)A是一种重要的化工原料,C、F的分子式都为C2H4O,F是没有不饱和键的环状有机物,G的分子式为C2H6O2,G中含有两个相同的官能团,转化关系如下图:
己知:同一碳原子上连接2个或2个以上—OH是不稳定结构。
请回答:
(1)有机物C中含有的官能团名称是_________________。
(2)有机物E的结构简式______________。
(3)F→G的化学方程式是_______________。
(4)下列说法正确的是____________。
A.有机物D能使石蕊溶液变红
B.用新制碱性氢氧化铜悬浊液无法区分有机物B、C、D的水溶液
C.等物质的量的A和B分别完全燃烧消耗氧气的量相等
D.可用饱和碳酸钠溶液除去有机物E中混有的少量B、D
28.(每小题2分,共8分)甲、乙、丙、丁四种有机物的分子式均为C3H6O2,根据下列性质,写出符合条件的各有机物的结构简式或有关的化学方程式。
(1)甲能与NaHCO3反应放出CO2,该反应的离子方程式为:______________________。
(2)乙既能发生银镜反应又能发生水解反应,乙的结构简式为:_____________________。
(3)
丙只能发生水解反应,丙在碱性条件下发生水解反应的化学方程式为:___________。
(4)丁能使溴水褪色,也能发生加聚反应,丁的结构简式为:____________________。
29.(共6分)以淀粉和油脂为原料,制备生活中某些物质。
请回答下列问题:
(1)淀粉的分子式为
。
(2)F的化学式是______________________。
(3)E可能的结构简式为___________________________________。
30.(每小题2分,共8分)
查尔酮类化合物G是黄酮类药物的主要合成中间体,其中一种合成路线如下:
已知以下信息:
①芳香烃A的相对分子质量在100-110之间,1
mol
A充分燃烧可生成72
g水。
②C不能发生银镜反应。
③D能发生银镜反应、可溶于饱和Na2CO3溶液、核磁共振氢谱显示其有4种氢原子。
回答下列问题:
(1)A的化学名称为__________
。
(2)由B生成C的化学方程式为_____________________________________
。
(3)G的结构简式为____________________________
。
(4)F的同分异构体中,既能发生银镜反应,又能与FeCl3溶液发生显色反应的有很多种,其中核磁共振氢谱为5组峰,且峰面积比为2:2:2:1:1的为______________(写结构简式)。
31.(每空2分,共10分)实验室用加热l-丁醇、溴化钠和浓硫酸的混合物的方法来制备1-溴丁烷时,还会有烯、醚等副产物生成。反应结束后将反应混合物蒸馏,分离得到1—溴丁烷,已知相关有机物的性质如下:
物质
熔点/℃
沸点/℃
1-丁醇
-89.53
117.25
1-溴丁烷
-112.4
101.6
丁醚
-95.3
142.6
1-丁烯
-185.3
-6.5
(1)反应中由于发生副反应而生成醚的有机反应类型为
____。
(2)制备1-溴丁烷的装置应选用下图中的_____
__(填序号)。
反应加热时的温度不宜超过100℃,理由是_______________
____________。
A
B
C
D
(3)当给烧瓶中的混合物加热时,溶液会出现橘红色,其原因是___________________。
(4)反应结束后,将反应混合物中1-溴丁烷分离出来的操作方法名称为__
___。
32.
(8分)中华人民共和国国家标准(GB2760 2011)规定葡萄酒中SO2最大使用量为0.2500
g·L-1。某兴趣小组用图1装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定。
INCLUDEPICTURE
"../../../"
\
MERGEFORMAT
INCLUDEPICTURE
"../../../"
\
MERGEFORMAT
(1)
仪器A的名称是______________,水通入A的进口为________。
(2)
B中加入300.00
mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,其化学方程式为________________________________。
(3)
除去C中过量的H2O2,然后用0.090
00
mol·L-1NaOH标准溶液进行滴定,滴定前排气泡时,应选择图2中的________;
若滴定终点时溶液的pH=8.8,则选择的指示剂为____________;
若用50
mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积(填序号)________(①=10
mL,②=40
mL,③<10
mL,④>40
mL
)。
(4)
滴定至终点时,消耗NaOH溶液25.00
mL,该葡萄酒中SO2含量为___________g·L-1。
宁波诺丁汉大学附属中学2016-2017学年第二学期期末考试
姓名:
班级:
考场:
座号:
注意:1.考号及选择题必须用2B铅笔填涂,文字题用黑色水笔或签字笔在答题框内作答。2.请保持答卷平整,不要折叠。
考号(班号)填涂区
高二年级化学答题卷
一、选择题(共25个小题,每小题2分,共50分)
12345
678910
1112131415
1617181920
2122232425
二、非选择题(共7个小题,共50分)
2016-2017学年度第二学期期末考试
高二化学参考答案
一、选择题(本题共25小题,每小题2分,共50分)
题号
1
2
3
4
5
6
7
8
9
10
答案
C
B
B
C
B
C
B
A
D
C
题号
11
12
13
14
15
16
17
18
19
20
答案
A
C
B
C
C
A
C
A
A
A
题号
21
22
23
24
25
答案
C
D
D
B
D
二、非选择题(本题有7小题,共50分)
26.
(每空1分,共4分)
(1)饱和碳酸钠溶液
(2)振荡、静置
(3)原料损失较大、易发生副反应
27.
(6分)
(1)醛基(1分);
(2)CH3COOCH2CH3(1分);
(3)(2分);
(4)ACD(2分)。
28.(每空2分,共8分)
(1)
CH3CH2COOH
+
NaHCO3
→CH3CH2COONa
+
CO2
↑+H2O
(2)
HCOOCH2CH3
(3)
CH3COOCH3+
NaOH
—→CH3COONa
+
CH3OH
(4)
CH2
=
CH—O—CH2OH
29.(6分)
(1)(C6H10O5)n
(2)C17H35COONa
(3)
(各1分)
30.(每小题2分,共8分)
(1)苯乙烯
(2)
(3)
(4)
31.(每空2分,共10分)
(1)取代反应
(2)C
防止1-溴丁烷因气化而逸出,影响产率。
(3)-1价的溴被氧化生成溴单质,溶于反应液中。
(4)蒸馏。
32.
(8分)
(1)
冷凝管(或冷凝器)
b
(2)
SO2+H2O2===H2SO4
(3)
③
酚酞
④
(4)
0.2400
SO2 ~ H2SO4 ~ 2NaOH
64
g 2
mol
m(SO2)
0.090
00
mol·L-1×0.02500
L
解得:m(SO2)==0.07200
g,
故葡萄酒中SO2的含量为=0.2400
g·L-1。
H
26.
(4分)
(1)________________。
(2)__________,___________。
(3)_____________________________________________。
29.
(6分)
(1)________________。(2)____________________。
(3)_____________________________________________。
28.
(8分)
(1)___________________________________________________。
(2)_______________________。
(3)___________________________________________________。
(4)_______________________。
27.
(6分)
(1)__________。
(2)__________。
(3)_____________________________________________。
(4)__________。
30.
(8分)
(1)_______________________。
(2)___________________________________________________。
(3)_______________________。
(4)_______________________。
31.
(10分)
(1)________________。
(2)_________,________________________________________。
(3)___________________________________________________。
(4)_______________。
32.
(8分)
(1)_________,__________。
(2)__________________________________________。
(3)__________,
____________,
_____________。
(4)_____________。
Δ
同课章节目录
