【备课推荐】2017年秋高二化学人教版选修四同步学案:第4章 第4节 金属的电化学腐蚀与防护
文档属性
| 名称 | 【备课推荐】2017年秋高二化学人教版选修四同步学案:第4章 第4节 金属的电化学腐蚀与防护 |

|
|
| 格式 | zip | ||
| 文件大小 | 335.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-09-07 00:00:00 | ||
图片预览



文档简介
第四节 金属的电化学腐蚀与防护
【学习目标】
1.认识金属腐蚀的危害,并能解释金属发生电化学腐蚀的原因,能正确书写析氢腐蚀和吸氧腐蚀的电极反应式和总反应式。
2.熟知金属腐蚀的防护方法。
一 金属的腐蚀
【新知导学】
1.回答下列问题:
(1)铁与氯气反应的化学方程式是__________________________________;纯锌片与盐酸反应的离子方程式是________________________________;上述两反应过程________(填“是”或“不是”)原电池反应。
(2)铁制品在潮湿的环境中比在干燥的环境中____生锈,其原因是______________________________________________________。
2.金属的腐蚀
(1)概念:金属与周围的________________________发生____________反应而引起损耗的现象。
(2)根据与金属接触的________________不同,金属腐蚀可分为两类:
①化学腐蚀:金属与接触到的________气体(如O2、Cl2、SO2等)或____________液体(如石油)等直接发生化学反应而引起的腐蚀。腐蚀的速率随温度升高而________。
②电化学腐蚀:________的金属跟________溶液接触时,会发生________反应,比较________的金属________电子而被氧化。
(3)用铝制饭盒盛放醋酸,一段时间后,饭盒被腐蚀,这种腐蚀属于____________,反应的化学方程式为______________________________________________________;若用铝制饭盒盛放食盐(含水时),一段时间后,饭盒被腐蚀,这种腐蚀属于________________,反应原理是(写电极反应式和总反应式):_____________________________________________。
3.钢铁的电化学腐蚀
根据钢铁表面水溶液薄膜的酸碱性不同,钢铁的电化学腐蚀分为析氢腐蚀和吸氧腐蚀,如下图所示:
(1)钢铁的析氢腐蚀:当钢铁表面的电解质溶液________较强时,腐蚀过程中有H2放出。Fe是负极,C是正极。发生的电极反应式及总反应式为
负极:________________________________________________________________________;
正极:________________________________________________________________________;
总反应:________________________________________________________________________。
(2)钢铁的吸氧腐蚀:当钢铁表面的电解质溶液呈______或呈________并溶有一定量的O2时,将会发生吸氧腐蚀。发生的电极反应式及总反应式为
负极:________________________________________________________________________;
正极:________________________________________________________________________;
总反应:________________________________________________________________________。
铁锈(Fe2O3·xH2O)的形成:________________________________________________
________________________________________________________________________。
【归纳总结】
1.金属腐蚀的本质
金属原子失去电子变为金属阳离子,金属发生氧化反应。
2.金属腐蚀的类型
(1)化学腐蚀与电化学腐蚀
类型
化学腐蚀
电化学腐蚀
条件
金属跟非金属单质或非电解质液体直接接触
不纯金属或合金跟电解质溶液接触
现象
无电流产生
有微弱电流产生
本质
金属被氧化
较活泼金属被氧化
两者往往同时发生,电化学腐蚀更普遍
(2)析氢腐蚀与吸氧腐蚀
类型
析氢腐蚀
吸氧腐蚀
条件
水膜酸性较强(pH≤4.3)
水膜酸性很弱或呈中性
电极反应
负极
Fe-2e-===Fe2+
正极
2H++2e-===H2↑
O2+2H2O+4e-===4OH-
总反应式
Fe+2H+===Fe2++H2↑
2Fe+O2+2H2O===2Fe(OH)2
吸氧腐蚀更普遍
提示 (1)金属活动顺序表中氢后的金属不能发生析氢腐蚀,只能发生吸氧腐蚀。
(2)金属活动顺序表中氢之前、镁之后金属的电化学腐蚀与钢铁的电化学腐蚀相似。
【活学活用】
1.下列关于金属腐蚀的说法正确的是( )
A.金属在潮湿空气中腐蚀的实质是M+nH2O===M(OH)n+H2↑
B.金属的化学腐蚀的实质是M-ne-===Mn+,电子直接转移给氧化剂
C.金属的化学腐蚀必须在酸性条件下进行
D.在潮湿的环境中,金属的电化学腐蚀一定是析氢腐蚀
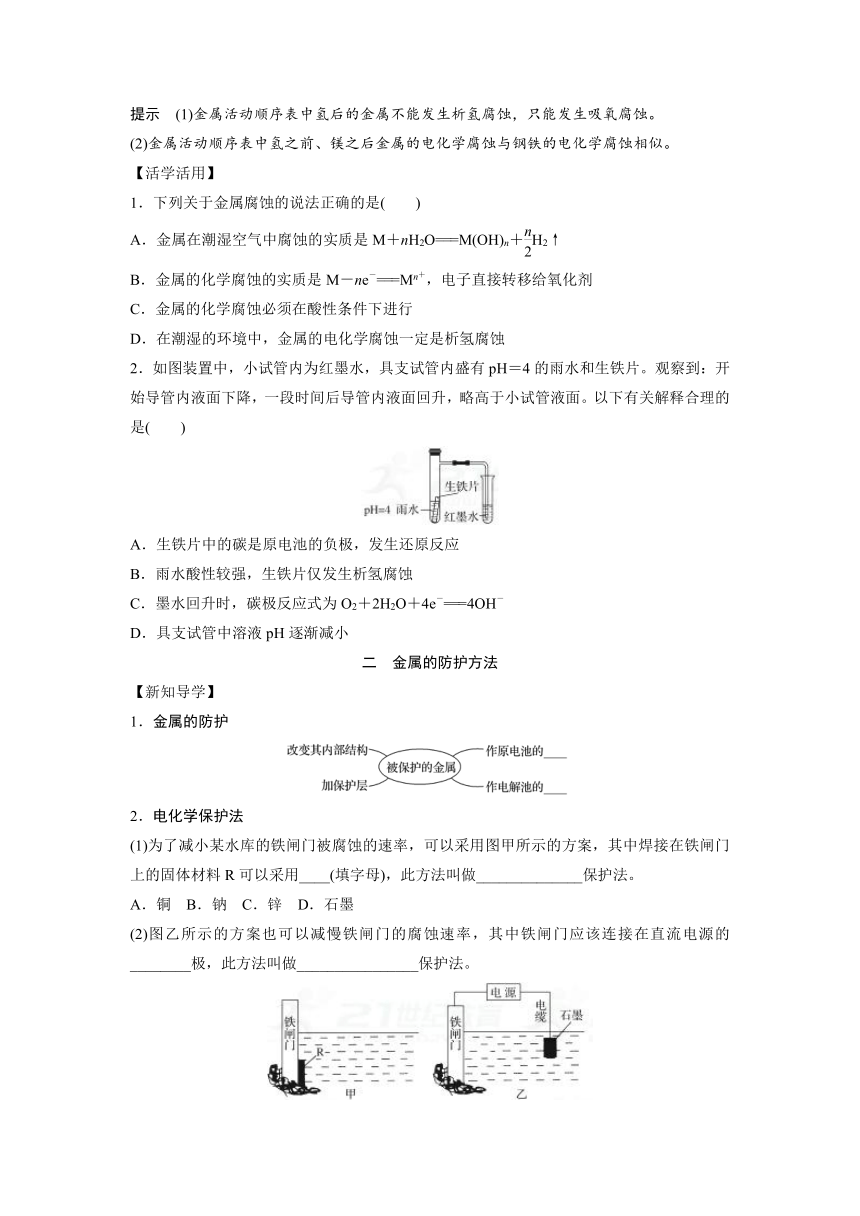
2.如图装置中,小试管内为红墨水,具支试管内盛有pH=4的雨水和生铁片。观察到:开始导管内液面下降,一段时间后导管内液面回升,略高于小试管液面。以下有关解释合理的是( )
A.生铁片中的碳是原电池的负极,发生还原反应
B.雨水酸性较强,生铁片仅发生析氢腐蚀
C.墨水回升时,碳极反应式为O2+2H2O+4e-===4OH-
D.具支试管中溶液pH逐渐减小
二 金属的防护方法
【新知导学】
1.金属的防护
2.电化学保护法
(1)为了减小某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R可以采用____(填字母),此方法叫做______________保护法。
A.铜
B.钠
C.锌
D.石墨
(2)图乙所示的方案也可以减慢铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的________极,此方法叫做________________保护法。
【归纳总结】
1.金属的电化学防护方法
类型
方法
原理
实例
牺牲阳极的阴极保护法
在被保护的设备上装上比它________的金属
被保护的金属作原电池的________
船舶的外壳上装锌块
外加电流的阴极保护法
将被保护的设备与惰性电极置于电解质溶液里,接上____________
被保护的金属作电解池的________
保护海水中的钢闸门
2.判断金属腐蚀快慢的方法
(1)同一金属在相同电解质溶液中,金属腐蚀的快慢是电解池的阳极>原电池的负极>化学腐蚀>原电池的正极>电解池的阴极。
(2)同一金属在相同电解质溶液中,电解质浓度越大,腐蚀越快。
(3)同一金属在不同电解质溶液中,金属腐蚀的快慢是强电解质溶液>弱电解质溶液>非电解质溶液。
【活学活用】
3.为了防止钢铁锈蚀,下列防护方法中正确的是( )
A.在精密机床的铁床上安装铜螺钉
B.在排放海水的钢铁闸门上用导线连接一块石墨,一同浸入海水中
C.在海轮舷上用铁丝系住锌板浸在海水里
D.在地下输油的铸铁管上接直流电源的正极
4.下列关于如图所示的实验装置的判断中错误的是( )
A.若X为碳棒,开关K置于A处可减缓铁的腐蚀
B.若X为锌棒,开关K置于A或B处均可减缓铁的腐蚀
C.若X为锌棒,开关K置于B处时,为牺牲阳极的阴极保护法
D.若X为碳棒,开关K置于B处时,铁电极上发生的反应为2H++2e-===H2↑
【学习小结】
【达标检测】
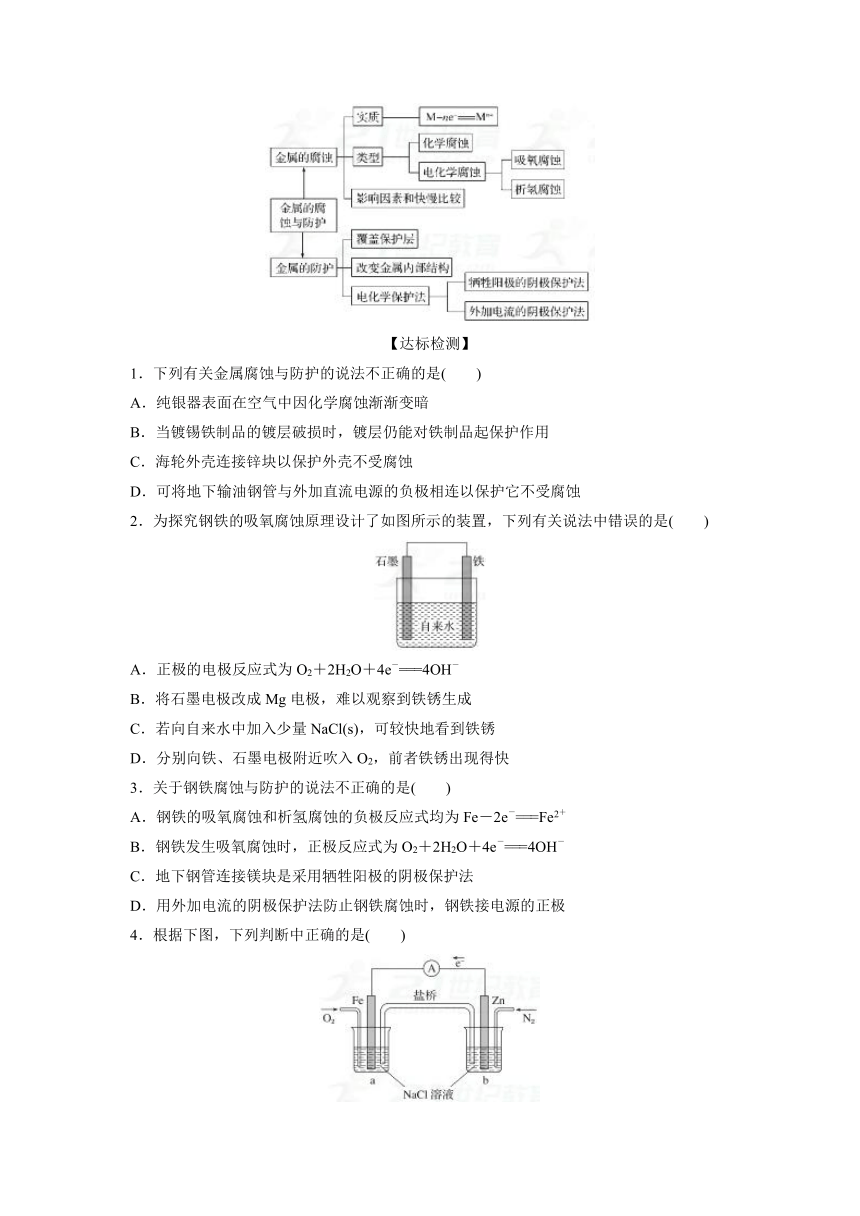
1.下列有关金属腐蚀与防护的说法不正确的是( )
A.纯银器表面在空气中因化学腐蚀渐渐变暗
B.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
C.海轮外壳连接锌块以保护外壳不受腐蚀
D.可将地下输油钢管与外加直流电源的负极相连以保护它不受腐蚀
2.为探究钢铁的吸氧腐蚀原理设计了如图所示的装置,下列有关说法中错误的是( )
A.正极的电极反应式为O2+2H2O+4e-===4OH-
B.将石墨电极改成Mg电极,难以观察到铁锈生成
C.若向自来水中加入少量NaCl(s),可较快地看到铁锈
D.分别向铁、石墨电极附近吹入O2,前者铁锈出现得快
3.关于钢铁腐蚀与防护的说法不正确的是( )
A.钢铁的吸氧腐蚀和析氢腐蚀的负极反应式均为Fe-2e-===Fe2+
B.钢铁发生吸氧腐蚀时,正极反应式为O2+2H2O+4e-===4OH-
C.地下钢管连接镁块是采用牺牲阳极的阴极保护法
D.用外加电流的阴极保护法防止钢铁腐蚀时,钢铁接电源的正极
4.根据下图,下列判断中正确的是( )
A.烧杯a中的溶液pH降低
B.烧杯b中发生氧化反应
C.烧杯a中发生的反应为2H++2e-===H2↑
D.烧杯b中发生的反应为2Cl--2e-===Cl2↑
5.回答下列问题:
(1)如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。
①该电化腐蚀称为______________。
②图中A、B、C、D四个区域,生成铁锈最多的是________(填字母)。
③以锌为负极,采用牺牲阳极的阴极保护法防止铁闸的腐蚀,图中锌块的固定位置最好应在________处(填字母)。
(2)石墨可用于自然水体中铜件的电化学防腐,完成如图防腐示意图,并作相应标注:
(3)下图所示的各容器中均盛有海水,铁在其中被腐蚀时由快到慢的顺序是__________________。
(4)如图,将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中,下列分析正确的是________(填字母)。
A.K1闭合,铁棒上发生的反应为2H++2e-===H2↑
B.K1闭合,石墨棒周围溶液pH逐渐升高
C.K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法
D.K2闭合,电路中通过0.002NA个电子时,两极共产生0.001
mol气体
答案精析
一
新知导学
1.(1)2Fe+3Cl22FeCl3 Zn+2H+===Zn2++H2↑ 不是 (2)易 铁制品中含有杂质碳,在潮湿环境下的电解质溶液中构成原电池,加快了铁被氧化的反应速率
2.(1)气体或液体物质 氧化还原 (2)气体或液体物质 ①干燥 非电解质 加快 ②不纯 电解质 原电池 活泼 失去 (3)化学腐蚀 2Al+6CH3COOH===2(CH3COO)3Al+3H2↑ 电化学腐蚀 负极:Al-3e-===Al3+,正极:O2+2H2O+4e-===4OH-,总反应:4Al+3O2+6H2O===4Al(OH)3
3.(1)酸性 Fe-2e-===Fe2+ 2H++2e-===H2↑ Fe+2H+===Fe2++H2↑ (2)中性 弱酸性 2Fe-4e-===2Fe2+ 2H2O+O2+4e-===4OH- 2Fe+2H2O+O2===2Fe(OH)2 2Fe(OH)3===Fe2O3·xH2O+(3-x)H2O
活学活用
1.B [金属腐蚀的实质是金属失去电子,在酸性较强的电解质溶液中发生析氢腐蚀放出H2,而在中性或酸性较弱的电解质溶液中发生吸氧腐蚀,析氢腐蚀和吸氧腐蚀均属于电化学腐蚀。]
2.C [生铁片中的碳是原电池的正极,A错误;雨水酸性较强,开始时铁片发生析氢腐蚀,产生氢气,导管内液面下降,一段时间后铁片发生吸氧腐蚀,吸收氧气,导管内液面回升,B错误;墨水回升时,铁片发生吸氧腐蚀,碳极为正极,电极反应式为O2+2H2O+4e-===4OH-,C正确;铁片无论是发生析氢腐蚀还是吸氧腐蚀,具支试管中溶液pH均增大,D错误。]
二
新知导学
1.正极 阴极
2.(1)C 牺牲阳极的阴极 (2)负 外加电流的阴极
归纳总结
1.(从左到右,从上到下)更活泼 正极 外加直流电源 阴极
活学活用
3.C [A、B中形成的原电池都是铁作负极,加速钢铁腐蚀;D中铸铁管作阳极,加速腐蚀;C中锌比铁活泼,铁作正极。]
4.D [若X为碳棒,开关K置于A处,Fe作电解池的阴极,属外加电流的阴极保护法,A项正确;若X为碳棒,开关K置于B处,Fe作原电池的负极,电极反应为Fe-2e-===Fe2+,D项不正确;若X为锌棒,K置于A处,Fe作电解池的阴极,属外加电流的阴极保护法,K置于B处时,Fe作原电池的正极,属牺牲阳极的阴极保护法,B项和C项均正确。]
达标检测 提升技能
1.B [银器在空气中久置会被氧化变黑,为化学腐蚀,A正确;当镀层破损时,Sn、Fe可形成原电池,Fe为负极,不再起到保护作用,B错;Fe与Zn块形成原电池,Zn作负极,从而保护Fe(正极),C正确;外加电流的阴极保护法应使被保护对象与直流电源的负极相连,故D正确。]
2.D [铁是负极,失电子被氧化成Fe2+,在正极氧气得电子发生还原反应生成OH-,反应式为O2+2H2O+4e-===4OH-,A项正确;将氧气吹向石墨电极的腐蚀速率比吹向铁电极快,D项错误;向自来水中加入NaCl(s),可使电解质溶液的导电能力增强,加快腐蚀速率,C项正确;但若将石墨电极换成Mg电极,则负极为Mg,Fe被保护,难以看到铁生锈,B项正确。]
3.D [钢铁的吸氧腐蚀和析氢腐蚀都是铁失去电子作负极,电极反应式为Fe-2e-===Fe2+,钢铁发生吸氧腐蚀时O2+2H2O+4e-===4OH-,A、B正确;地下钢管连接镁块,镁比铁活泼,作负极,铁作正极得到保护,C正确;用外加电流的阴极保护法防止钢铁腐蚀时,钢铁连接电源的负极,D错误。]
4.B
5.(1)①吸氧腐蚀 ②B ③C
(2) (3)④>②>①>③ (4)B
解析 (1)①金属在中性或较弱的酸性条件下发生的是吸氧腐蚀。②发生吸氧腐蚀,越靠近液面接触到的O2越多,腐蚀得越严重。③锌块应固定在腐蚀最严重的C处形成原电池,锌作负极,铁闸作正极,得到保护。(2)要用石墨通过电化学腐蚀保护铜,只能用电解池原理,碳接电源正极,铜接电源负极。(3)当电解质溶液相同时,同一金属腐蚀的快慢是电解池的阳极>原电池的负极>化学腐蚀>原电池的正极>电解池的阴极。故本题中,铁腐蚀由快到慢的顺序为④>②>①>③。(4)A项,K1闭合时,该装置构成了Fe-C-NaCl溶液原电池,铁作负极,发生氧化反应,电极反应式是Fe-2e-===Fe2+;B项,石墨棒作正极,发生的电极反应式是2H2O+O2+4e-===4OH-,故石墨棒周围溶液pH逐渐升高;C项,K2闭合时,该装置构成了Fe-C-外加电源的电解池,石墨棒作阳极,Fe作阴极而不被腐蚀,该方法称为外加电流的阴极保护法;D项,K2闭合时,阳极的电极反应式是2Cl--2e-===Cl2↑,阴极的电极反应式是2H++2e-===H2↑,所以当电路中通过0.002NA个即0.002
mol电子时,生成H2和Cl2的物质的量均为0.001
mol,则两极共产生0.002
mol气体。
【学习目标】
1.认识金属腐蚀的危害,并能解释金属发生电化学腐蚀的原因,能正确书写析氢腐蚀和吸氧腐蚀的电极反应式和总反应式。
2.熟知金属腐蚀的防护方法。
一 金属的腐蚀
【新知导学】
1.回答下列问题:
(1)铁与氯气反应的化学方程式是__________________________________;纯锌片与盐酸反应的离子方程式是________________________________;上述两反应过程________(填“是”或“不是”)原电池反应。
(2)铁制品在潮湿的环境中比在干燥的环境中____生锈,其原因是______________________________________________________。
2.金属的腐蚀
(1)概念:金属与周围的________________________发生____________反应而引起损耗的现象。
(2)根据与金属接触的________________不同,金属腐蚀可分为两类:
①化学腐蚀:金属与接触到的________气体(如O2、Cl2、SO2等)或____________液体(如石油)等直接发生化学反应而引起的腐蚀。腐蚀的速率随温度升高而________。
②电化学腐蚀:________的金属跟________溶液接触时,会发生________反应,比较________的金属________电子而被氧化。
(3)用铝制饭盒盛放醋酸,一段时间后,饭盒被腐蚀,这种腐蚀属于____________,反应的化学方程式为______________________________________________________;若用铝制饭盒盛放食盐(含水时),一段时间后,饭盒被腐蚀,这种腐蚀属于________________,反应原理是(写电极反应式和总反应式):_____________________________________________。
3.钢铁的电化学腐蚀
根据钢铁表面水溶液薄膜的酸碱性不同,钢铁的电化学腐蚀分为析氢腐蚀和吸氧腐蚀,如下图所示:
(1)钢铁的析氢腐蚀:当钢铁表面的电解质溶液________较强时,腐蚀过程中有H2放出。Fe是负极,C是正极。发生的电极反应式及总反应式为
负极:________________________________________________________________________;
正极:________________________________________________________________________;
总反应:________________________________________________________________________。
(2)钢铁的吸氧腐蚀:当钢铁表面的电解质溶液呈______或呈________并溶有一定量的O2时,将会发生吸氧腐蚀。发生的电极反应式及总反应式为
负极:________________________________________________________________________;
正极:________________________________________________________________________;
总反应:________________________________________________________________________。
铁锈(Fe2O3·xH2O)的形成:________________________________________________
________________________________________________________________________。
【归纳总结】
1.金属腐蚀的本质
金属原子失去电子变为金属阳离子,金属发生氧化反应。
2.金属腐蚀的类型
(1)化学腐蚀与电化学腐蚀
类型
化学腐蚀
电化学腐蚀
条件
金属跟非金属单质或非电解质液体直接接触
不纯金属或合金跟电解质溶液接触
现象
无电流产生
有微弱电流产生
本质
金属被氧化
较活泼金属被氧化
两者往往同时发生,电化学腐蚀更普遍
(2)析氢腐蚀与吸氧腐蚀
类型
析氢腐蚀
吸氧腐蚀
条件
水膜酸性较强(pH≤4.3)
水膜酸性很弱或呈中性
电极反应
负极
Fe-2e-===Fe2+
正极
2H++2e-===H2↑
O2+2H2O+4e-===4OH-
总反应式
Fe+2H+===Fe2++H2↑
2Fe+O2+2H2O===2Fe(OH)2
吸氧腐蚀更普遍
提示 (1)金属活动顺序表中氢后的金属不能发生析氢腐蚀,只能发生吸氧腐蚀。
(2)金属活动顺序表中氢之前、镁之后金属的电化学腐蚀与钢铁的电化学腐蚀相似。
【活学活用】
1.下列关于金属腐蚀的说法正确的是( )
A.金属在潮湿空气中腐蚀的实质是M+nH2O===M(OH)n+H2↑
B.金属的化学腐蚀的实质是M-ne-===Mn+,电子直接转移给氧化剂
C.金属的化学腐蚀必须在酸性条件下进行
D.在潮湿的环境中,金属的电化学腐蚀一定是析氢腐蚀
2.如图装置中,小试管内为红墨水,具支试管内盛有pH=4的雨水和生铁片。观察到:开始导管内液面下降,一段时间后导管内液面回升,略高于小试管液面。以下有关解释合理的是( )
A.生铁片中的碳是原电池的负极,发生还原反应
B.雨水酸性较强,生铁片仅发生析氢腐蚀
C.墨水回升时,碳极反应式为O2+2H2O+4e-===4OH-
D.具支试管中溶液pH逐渐减小
二 金属的防护方法
【新知导学】
1.金属的防护
2.电化学保护法
(1)为了减小某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R可以采用____(填字母),此方法叫做______________保护法。
A.铜
B.钠
C.锌
D.石墨
(2)图乙所示的方案也可以减慢铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的________极,此方法叫做________________保护法。
【归纳总结】
1.金属的电化学防护方法
类型
方法
原理
实例
牺牲阳极的阴极保护法
在被保护的设备上装上比它________的金属
被保护的金属作原电池的________
船舶的外壳上装锌块
外加电流的阴极保护法
将被保护的设备与惰性电极置于电解质溶液里,接上____________
被保护的金属作电解池的________
保护海水中的钢闸门
2.判断金属腐蚀快慢的方法
(1)同一金属在相同电解质溶液中,金属腐蚀的快慢是电解池的阳极>原电池的负极>化学腐蚀>原电池的正极>电解池的阴极。
(2)同一金属在相同电解质溶液中,电解质浓度越大,腐蚀越快。
(3)同一金属在不同电解质溶液中,金属腐蚀的快慢是强电解质溶液>弱电解质溶液>非电解质溶液。
【活学活用】
3.为了防止钢铁锈蚀,下列防护方法中正确的是( )
A.在精密机床的铁床上安装铜螺钉
B.在排放海水的钢铁闸门上用导线连接一块石墨,一同浸入海水中
C.在海轮舷上用铁丝系住锌板浸在海水里
D.在地下输油的铸铁管上接直流电源的正极
4.下列关于如图所示的实验装置的判断中错误的是( )
A.若X为碳棒,开关K置于A处可减缓铁的腐蚀
B.若X为锌棒,开关K置于A或B处均可减缓铁的腐蚀
C.若X为锌棒,开关K置于B处时,为牺牲阳极的阴极保护法
D.若X为碳棒,开关K置于B处时,铁电极上发生的反应为2H++2e-===H2↑
【学习小结】
【达标检测】
1.下列有关金属腐蚀与防护的说法不正确的是( )
A.纯银器表面在空气中因化学腐蚀渐渐变暗
B.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
C.海轮外壳连接锌块以保护外壳不受腐蚀
D.可将地下输油钢管与外加直流电源的负极相连以保护它不受腐蚀
2.为探究钢铁的吸氧腐蚀原理设计了如图所示的装置,下列有关说法中错误的是( )
A.正极的电极反应式为O2+2H2O+4e-===4OH-
B.将石墨电极改成Mg电极,难以观察到铁锈生成
C.若向自来水中加入少量NaCl(s),可较快地看到铁锈
D.分别向铁、石墨电极附近吹入O2,前者铁锈出现得快
3.关于钢铁腐蚀与防护的说法不正确的是( )
A.钢铁的吸氧腐蚀和析氢腐蚀的负极反应式均为Fe-2e-===Fe2+
B.钢铁发生吸氧腐蚀时,正极反应式为O2+2H2O+4e-===4OH-
C.地下钢管连接镁块是采用牺牲阳极的阴极保护法
D.用外加电流的阴极保护法防止钢铁腐蚀时,钢铁接电源的正极
4.根据下图,下列判断中正确的是( )
A.烧杯a中的溶液pH降低
B.烧杯b中发生氧化反应
C.烧杯a中发生的反应为2H++2e-===H2↑
D.烧杯b中发生的反应为2Cl--2e-===Cl2↑
5.回答下列问题:
(1)如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。
①该电化腐蚀称为______________。
②图中A、B、C、D四个区域,生成铁锈最多的是________(填字母)。
③以锌为负极,采用牺牲阳极的阴极保护法防止铁闸的腐蚀,图中锌块的固定位置最好应在________处(填字母)。
(2)石墨可用于自然水体中铜件的电化学防腐,完成如图防腐示意图,并作相应标注:
(3)下图所示的各容器中均盛有海水,铁在其中被腐蚀时由快到慢的顺序是__________________。
(4)如图,将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中,下列分析正确的是________(填字母)。
A.K1闭合,铁棒上发生的反应为2H++2e-===H2↑
B.K1闭合,石墨棒周围溶液pH逐渐升高
C.K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法
D.K2闭合,电路中通过0.002NA个电子时,两极共产生0.001
mol气体
答案精析
一
新知导学
1.(1)2Fe+3Cl22FeCl3 Zn+2H+===Zn2++H2↑ 不是 (2)易 铁制品中含有杂质碳,在潮湿环境下的电解质溶液中构成原电池,加快了铁被氧化的反应速率
2.(1)气体或液体物质 氧化还原 (2)气体或液体物质 ①干燥 非电解质 加快 ②不纯 电解质 原电池 活泼 失去 (3)化学腐蚀 2Al+6CH3COOH===2(CH3COO)3Al+3H2↑ 电化学腐蚀 负极:Al-3e-===Al3+,正极:O2+2H2O+4e-===4OH-,总反应:4Al+3O2+6H2O===4Al(OH)3
3.(1)酸性 Fe-2e-===Fe2+ 2H++2e-===H2↑ Fe+2H+===Fe2++H2↑ (2)中性 弱酸性 2Fe-4e-===2Fe2+ 2H2O+O2+4e-===4OH- 2Fe+2H2O+O2===2Fe(OH)2 2Fe(OH)3===Fe2O3·xH2O+(3-x)H2O
活学活用
1.B [金属腐蚀的实质是金属失去电子,在酸性较强的电解质溶液中发生析氢腐蚀放出H2,而在中性或酸性较弱的电解质溶液中发生吸氧腐蚀,析氢腐蚀和吸氧腐蚀均属于电化学腐蚀。]
2.C [生铁片中的碳是原电池的正极,A错误;雨水酸性较强,开始时铁片发生析氢腐蚀,产生氢气,导管内液面下降,一段时间后铁片发生吸氧腐蚀,吸收氧气,导管内液面回升,B错误;墨水回升时,铁片发生吸氧腐蚀,碳极为正极,电极反应式为O2+2H2O+4e-===4OH-,C正确;铁片无论是发生析氢腐蚀还是吸氧腐蚀,具支试管中溶液pH均增大,D错误。]
二
新知导学
1.正极 阴极
2.(1)C 牺牲阳极的阴极 (2)负 外加电流的阴极
归纳总结
1.(从左到右,从上到下)更活泼 正极 外加直流电源 阴极
活学活用
3.C [A、B中形成的原电池都是铁作负极,加速钢铁腐蚀;D中铸铁管作阳极,加速腐蚀;C中锌比铁活泼,铁作正极。]
4.D [若X为碳棒,开关K置于A处,Fe作电解池的阴极,属外加电流的阴极保护法,A项正确;若X为碳棒,开关K置于B处,Fe作原电池的负极,电极反应为Fe-2e-===Fe2+,D项不正确;若X为锌棒,K置于A处,Fe作电解池的阴极,属外加电流的阴极保护法,K置于B处时,Fe作原电池的正极,属牺牲阳极的阴极保护法,B项和C项均正确。]
达标检测 提升技能
1.B [银器在空气中久置会被氧化变黑,为化学腐蚀,A正确;当镀层破损时,Sn、Fe可形成原电池,Fe为负极,不再起到保护作用,B错;Fe与Zn块形成原电池,Zn作负极,从而保护Fe(正极),C正确;外加电流的阴极保护法应使被保护对象与直流电源的负极相连,故D正确。]
2.D [铁是负极,失电子被氧化成Fe2+,在正极氧气得电子发生还原反应生成OH-,反应式为O2+2H2O+4e-===4OH-,A项正确;将氧气吹向石墨电极的腐蚀速率比吹向铁电极快,D项错误;向自来水中加入NaCl(s),可使电解质溶液的导电能力增强,加快腐蚀速率,C项正确;但若将石墨电极换成Mg电极,则负极为Mg,Fe被保护,难以看到铁生锈,B项正确。]
3.D [钢铁的吸氧腐蚀和析氢腐蚀都是铁失去电子作负极,电极反应式为Fe-2e-===Fe2+,钢铁发生吸氧腐蚀时O2+2H2O+4e-===4OH-,A、B正确;地下钢管连接镁块,镁比铁活泼,作负极,铁作正极得到保护,C正确;用外加电流的阴极保护法防止钢铁腐蚀时,钢铁连接电源的负极,D错误。]
4.B
5.(1)①吸氧腐蚀 ②B ③C
(2) (3)④>②>①>③ (4)B
解析 (1)①金属在中性或较弱的酸性条件下发生的是吸氧腐蚀。②发生吸氧腐蚀,越靠近液面接触到的O2越多,腐蚀得越严重。③锌块应固定在腐蚀最严重的C处形成原电池,锌作负极,铁闸作正极,得到保护。(2)要用石墨通过电化学腐蚀保护铜,只能用电解池原理,碳接电源正极,铜接电源负极。(3)当电解质溶液相同时,同一金属腐蚀的快慢是电解池的阳极>原电池的负极>化学腐蚀>原电池的正极>电解池的阴极。故本题中,铁腐蚀由快到慢的顺序为④>②>①>③。(4)A项,K1闭合时,该装置构成了Fe-C-NaCl溶液原电池,铁作负极,发生氧化反应,电极反应式是Fe-2e-===Fe2+;B项,石墨棒作正极,发生的电极反应式是2H2O+O2+4e-===4OH-,故石墨棒周围溶液pH逐渐升高;C项,K2闭合时,该装置构成了Fe-C-外加电源的电解池,石墨棒作阳极,Fe作阴极而不被腐蚀,该方法称为外加电流的阴极保护法;D项,K2闭合时,阳极的电极反应式是2Cl--2e-===Cl2↑,阴极的电极反应式是2H++2e-===H2↑,所以当电路中通过0.002NA个即0.002
mol电子时,生成H2和Cl2的物质的量均为0.001
mol,则两极共产生0.002
mol气体。
