湖南省长沙市湘府中学人教版高中化学必修二_1.3.1化学键 课件
文档属性
| 名称 | 湖南省长沙市湘府中学人教版高中化学必修二_1.3.1化学键 课件 |

|
|
| 格式 | zip | ||
| 文件大小 | 504.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-09-24 00:00:00 | ||
图片预览




文档简介
课件15张PPT。§1.3 化学键
(第1课时)
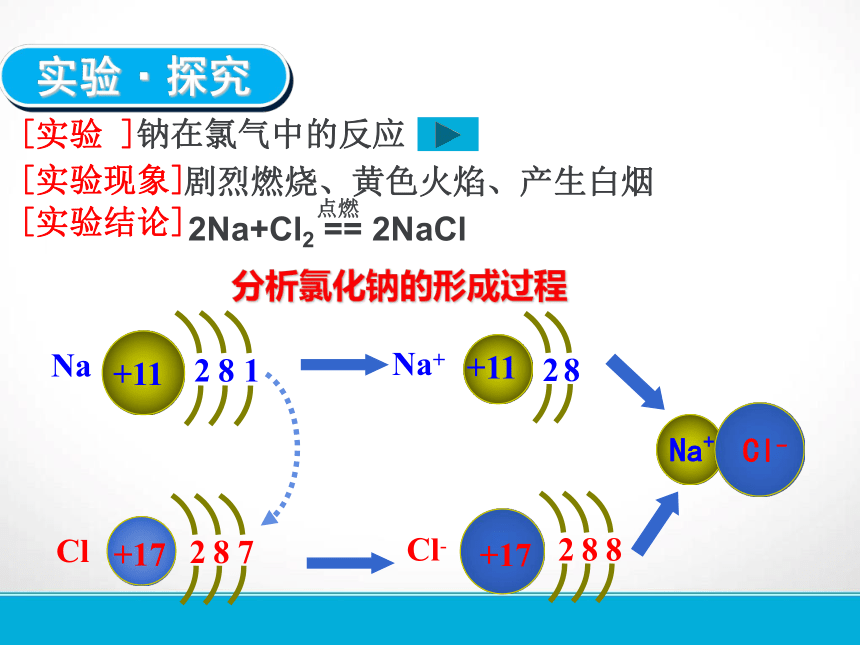
[实验 ]钠在氯气中的反应[实验现象]剧烈燃烧、黄色火焰、产生白烟[实验结论]分析氯化钠的形成过程实验·探究思考·交流在氯化钠中Na+和Cl- 间存在哪些作用力?Na+和Cl-间的静电吸引作用;阴、阳离子的电子间、原子核间的静电排斥作用。一、离子键1、定义:带相反电荷离子之间的相互作用 (或使阴、阳离子结合成化合物的静电作用)。(一)离子键(1)成键微粒:(2)相互作用:静电作用(静电引力和斥力)。阴、阳离子。(3)成键过程:阴、阳离子接近到某一距离,吸引与排斥达到平衡就形成离子键。2、形成条件:(1)二元素化合物:活泼的金属元素(第ⅠA、ⅡA族)和活泼的非金属元素(第ⅥA、ⅦA族)之间形成的化合物。(2)多元素化合物:①强碱:NaOH、KOH②含氧酸盐:Na2SO4、KNO3③氨盐:NH4Cl、NH4NO3(二)离子化合物1、定义:由离子键构成的化合物2、存在:金属氧化物,活泼金属氢化物,强碱和绝大部分的盐。练习:写出下列离子的电子式:K+、O2-、N3-3、离子化合物的电子式: a、由阴、阳离子的电子式组合而成. b、相同离子不能合并 c、尽可能对称AB型AB2型A2B型练习:写出MgO、K2S、CaF2的电子式4、用电子式表示离子化合物的形成过程例:练习:写出K2S、MgBr2的形成过程1.左边的原子用电子式表示,而不用分子式或分子的电子式表示;
2.阴离子要用方括号括起来并且标明电荷数;
3.左边相同的原子可以合并写,右边相同的离子要单个写;
4.不能把“→”写成“==”;
5.用箭头标明电子转移方向,也可不标。书写要点:小 结离子键概念形成条件(静电作用)离子化合物电子式书写含离子键种类当堂检测1、下列说法正确的是( )
A.含有金属元素的化合物一定是离子化合物
B.第IA族和第VIIA族原子化合时,一定生成离子键
C.由非金属元素形成的化合物一定不是离子化合物
D.活泼金属与非金属化合时,能形成离子键2、与Ne的核外电子排布相同的离子跟与Ar的核外电子排布相同的离子所形成的化合物是( )
A. Na2S B. CCl4 C. KCl D. NaFDA4、下列各数值表示有关元素的原子序数,能形成AB2型
离子化合物的是( )
A.6与8 B.11与13 C. 11与16 D.12与173.下列说法正确是(?????)
A.离子键就是阴阳离子间的静电引力
B.所有金属元素与所有非金属元素间都能形成离子键
C.钠原子与氯原子结合成氯化钠后体系能量降低
D.在离子化合物CaCl2中,两个氯离子间也存在离子键当堂检测CD5.下列电子式是否正确:O: [:Na:]+ [:S:]-2:.::Ca2+[:Cl:]2- Na2+[:O:]2-:::::×××××当堂检测6.用电子式表示氧化钠的形成过程
(第1课时)
[实验 ]钠在氯气中的反应[实验现象]剧烈燃烧、黄色火焰、产生白烟[实验结论]分析氯化钠的形成过程实验·探究思考·交流在氯化钠中Na+和Cl- 间存在哪些作用力?Na+和Cl-间的静电吸引作用;阴、阳离子的电子间、原子核间的静电排斥作用。一、离子键1、定义:带相反电荷离子之间的相互作用 (或使阴、阳离子结合成化合物的静电作用)。(一)离子键(1)成键微粒:(2)相互作用:静电作用(静电引力和斥力)。阴、阳离子。(3)成键过程:阴、阳离子接近到某一距离,吸引与排斥达到平衡就形成离子键。2、形成条件:(1)二元素化合物:活泼的金属元素(第ⅠA、ⅡA族)和活泼的非金属元素(第ⅥA、ⅦA族)之间形成的化合物。(2)多元素化合物:①强碱:NaOH、KOH②含氧酸盐:Na2SO4、KNO3③氨盐:NH4Cl、NH4NO3(二)离子化合物1、定义:由离子键构成的化合物2、存在:金属氧化物,活泼金属氢化物,强碱和绝大部分的盐。练习:写出下列离子的电子式:K+、O2-、N3-3、离子化合物的电子式: a、由阴、阳离子的电子式组合而成. b、相同离子不能合并 c、尽可能对称AB型AB2型A2B型练习:写出MgO、K2S、CaF2的电子式4、用电子式表示离子化合物的形成过程例:练习:写出K2S、MgBr2的形成过程1.左边的原子用电子式表示,而不用分子式或分子的电子式表示;
2.阴离子要用方括号括起来并且标明电荷数;
3.左边相同的原子可以合并写,右边相同的离子要单个写;
4.不能把“→”写成“==”;
5.用箭头标明电子转移方向,也可不标。书写要点:小 结离子键概念形成条件(静电作用)离子化合物电子式书写含离子键种类当堂检测1、下列说法正确的是( )
A.含有金属元素的化合物一定是离子化合物
B.第IA族和第VIIA族原子化合时,一定生成离子键
C.由非金属元素形成的化合物一定不是离子化合物
D.活泼金属与非金属化合时,能形成离子键2、与Ne的核外电子排布相同的离子跟与Ar的核外电子排布相同的离子所形成的化合物是( )
A. Na2S B. CCl4 C. KCl D. NaFDA4、下列各数值表示有关元素的原子序数,能形成AB2型
离子化合物的是( )
A.6与8 B.11与13 C. 11与16 D.12与173.下列说法正确是(?????)
A.离子键就是阴阳离子间的静电引力
B.所有金属元素与所有非金属元素间都能形成离子键
C.钠原子与氯原子结合成氯化钠后体系能量降低
D.在离子化合物CaCl2中,两个氯离子间也存在离子键当堂检测CD5.下列电子式是否正确:O: [:Na:]+ [:S:]-2:.::Ca2+[:Cl:]2- Na2+[:O:]2-:::::×××××当堂检测6.用电子式表示氧化钠的形成过程
