九年级科学国庆八天练 - 3硫酸
图片预览

文档简介
21世纪教育网 –中小学教育资源及组卷应用平台
九年级科学国庆八天练之硫酸
1﹒下列关于H2SO4性质描述中,不属于酸的通性的是( )
A.使紫色石蕊溶液变红
B.与NaOH发生中和反应
C.浓硫酸滴到白纸上使纸变黑
D.与Mg反应放出氢气
2﹒下列有关硫酸的说法,正确的是( )
A.打开盛有浓硫酸的试剂瓶塞,瓶口出现白雾
B.浓硫酸不慎沾到皮肤上,立即用大量的水冲洗,然后再涂上3%-5%的氢氧化钠溶液
C.实验室用稀硫酸和块状石灰石制取二氧化碳
D.硫酸可用于生产化肥、农药、染料以及冶炼金属等
3﹒如图表示化学反应中溶液的颜色变化.下列叙述错误的是( )
A.若X是稀硫酸,a可能是紫色石蕊试液
B.若X是稀硫酸,b可能是氧化物
C.若X是稀盐酸,c不可能是单质
D.若X是稀盐酸,d不可能是单质
4﹒某课外兴趣小组的同学,通过实验测定浓 ( http: / / www.21cnjy.com )硫酸吸水性的有关数据,绘制成如图的函数图象,其中横坐标表示时间,纵坐标可以表示:①溶质的质量分数;②溶液的质量;③溶液的体积;④溶液中所含水的质量。其中正确的是( )21世纪教育网版权所有
A.①② B.②③ C.②③④ D.①②③④
5﹒将过量的稀硫酸加入到有生锈铁钉的试管中,不能观察到的现象是( )
A.铁钉表面的锈迹消失,逐渐变得光亮
B.溶液由无色变为黄色,又由黄色变为浅绿色
C.一段时间后,铁钉表面有气泡生成
D.试管底部有红褐色沉淀生成
6﹒将Cu2O和Cu的固体混合物5.2g放 ( http: / / www.21cnjy.com )入烧杯中,加入过量的20%的稀硫酸,充分反应后,过滤、洗涤、干燥,得到3.2g固体.下列说法错误的是(已知:Cu不与稀硫酸反应,Cu2O+H2SO4═CuSO4+Cu+H2O)( )21教育网
A.剩余固体为纯净物
B.反应过程中,溶液逐渐变蓝
C.原固体混合物中Cu的质量大于Cu2O
D.在最后一次洗涤后的滤液中滴加BaCl2溶液,检验固体是否洗涤干净
7﹒将14.6g表面氧化的锌片,加入到100g19.6%的稀硫酸中,充分反应后,得到114.4g溶液,则下列说法正确的是( )21cnjy.com
A.稀硫酸一加入立即有气泡产生
B.所得溶液中的溶质为H2SO4和ZnSO4
C.反应后生成ZnSO432.2g
D.14.6g表面氧化的锌片中含锌元素质量为6.5g
8﹒化学是研究物质的组成、结构、性质、用途及其变化规律的基础自然科学,请回答下列问题:
(1)从微粒角度看:硫酸是由 H+
(填离子符号)和SO42-构成的;
(2)从性质角度看:稀硫酸溶液可使石蕊试液 ( http: / / www.21cnjy.com )显红色,说明其具有 酸
性,请写出其与氢氧化钠反应的化学方程式 。
9﹒在盛有稀硫酸的烧杯中 ( http: / / www.21cnjy.com ),漂浮着一木块,如图所示。如果往烧杯中中入少量某种固体物质后,木块浸没在水中的体积变大,加入固体物质可能是 Ba(OH)2
(写化学式),理由是 稀硫酸和氢氧化钡反应生成硫酸钡沉淀和水,反应后,溶液的密度变小,而木块所受的浮力不变,由F=ρgV排知,木块排开水的体积将变大
。
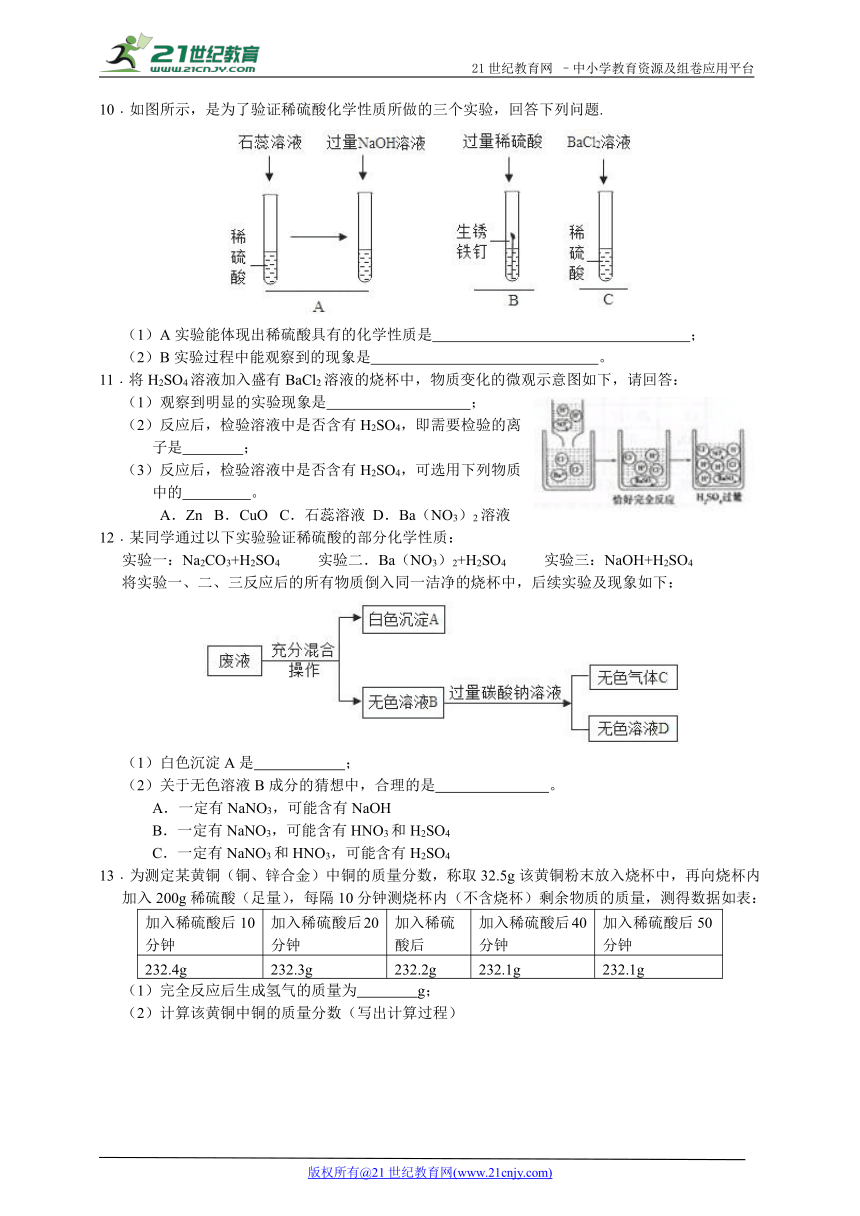
10﹒如图所示,是为了验证稀硫酸化学性质所做的三个实验,回答下列问题.
( http: / / www.21cnjy.com / )
(1)A实验能体现出稀硫酸具有的化学性质是 酸能与碱反应
;
(2)B实验过程中能观察到的现象是 铁锈消失,溶液变红;过一会儿有气体放出
。
11﹒将H2SO4溶液加入盛有BaCl2溶液的烧杯中,物质变化的微观示意图如下,请回答:
(1)观察到明显的实验现象是 有白色沉淀生成
;
(2)反应后,检验溶液中是否含有H2SO4,即需要检验的离子是 硫酸根离子
;
(3)反应后,检验溶液中是否含有H2SO4,可选用下列物质中的 D
。
A.Zn B.CuO C.石蕊溶液 D.Ba(NO3)2溶液
12﹒某同学通过以下实验验证稀硫酸的部分化学性质:
实验一:Na2CO3+H2SO4 实验二.Ba(NO3)2+H2SO4 实验三:NaOH+H2SO4
将实验一、二、三反应后的所有物质倒入同一洁净的烧杯中,后续实验及现象如下:
( http: / / www.21cnjy.com / )
(1)白色沉淀A是 BaSO4
;
(2)关于无色溶液B成分的猜想中,合理的是 C
。
A.一定有NaNO3,可能含有NaOH
B.一定有NaNO3,可能含有HNO3和H2SO4
C.一定有NaNO3和HNO3,可能含有H2SO4
13﹒为测定某黄铜(铜、锌合金)中铜的 ( http: / / www.21cnjy.com )质量分数,称取32.5g该黄铜粉末放入烧杯中,再向烧杯内加入200g稀硫酸(足量),每隔10分钟测烧杯内(不含烧杯)剩余物质的质量,测得数据如表:
加入稀硫酸后10分钟 加入稀硫酸后20分钟 加入稀硫酸后 加入稀硫酸后40分钟 加入稀硫酸后50分钟
232.4g 232.3g 232.2g 232.1g 232.1g
(1)完全反应后生成氢气的质量为 0.4
g;
(2)计算该黄铜中铜的质量分数(写出计算过程)
参考答案
说明:选择题7*3+填空题12*2+解答题5=50分
题号 1 2 3 4 5 6 7
答案 C D C C D C C
8﹒(1)H+
(2)酸 H2SO4+2NaOH=Na2SO4+2H2O
9﹒Ba(OH)2 稀硫酸 ( http: / / www.21cnjy.com )和氢氧化钡反应生成硫酸钡沉淀和水,反应后,溶液的密度变小,而木块所受的浮力不变,由F=ρgV排知,木块排开水的体积将变大21·cn·jy·com
10﹒(1)酸能与碱反应
(2)铁锈消失,溶液变红,过一会儿有气体放出
11﹒(1)有白色沉淀生成
(2)硫酸根离子;
(3)D
12﹒(1)BaSO4 (2)C
13﹒解:根据质量守恒定律可得,生成的氢气的质量为32.5g+200g-232.1g=0.4g
设参加反应的锌的质量为x
Zn+H2SO4=ZnSO4+H2↑
65 2
x 0.4g
x=13g
该黄铜中铜的质量分数为×100%=60%
答:该黄铜中铜的质量分数为60%
( http: / / www.21cnjy.com / )
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://www.21cnjy.com/" 版权所有@21世纪教育网(www.21cnjy.com)
九年级科学国庆八天练之硫酸
1﹒下列关于H2SO4性质描述中,不属于酸的通性的是( )
A.使紫色石蕊溶液变红
B.与NaOH发生中和反应
C.浓硫酸滴到白纸上使纸变黑
D.与Mg反应放出氢气
2﹒下列有关硫酸的说法,正确的是( )
A.打开盛有浓硫酸的试剂瓶塞,瓶口出现白雾
B.浓硫酸不慎沾到皮肤上,立即用大量的水冲洗,然后再涂上3%-5%的氢氧化钠溶液
C.实验室用稀硫酸和块状石灰石制取二氧化碳
D.硫酸可用于生产化肥、农药、染料以及冶炼金属等
3﹒如图表示化学反应中溶液的颜色变化.下列叙述错误的是( )
A.若X是稀硫酸,a可能是紫色石蕊试液
B.若X是稀硫酸,b可能是氧化物
C.若X是稀盐酸,c不可能是单质
D.若X是稀盐酸,d不可能是单质
4﹒某课外兴趣小组的同学,通过实验测定浓 ( http: / / www.21cnjy.com )硫酸吸水性的有关数据,绘制成如图的函数图象,其中横坐标表示时间,纵坐标可以表示:①溶质的质量分数;②溶液的质量;③溶液的体积;④溶液中所含水的质量。其中正确的是( )21世纪教育网版权所有
A.①② B.②③ C.②③④ D.①②③④
5﹒将过量的稀硫酸加入到有生锈铁钉的试管中,不能观察到的现象是( )
A.铁钉表面的锈迹消失,逐渐变得光亮
B.溶液由无色变为黄色,又由黄色变为浅绿色
C.一段时间后,铁钉表面有气泡生成
D.试管底部有红褐色沉淀生成
6﹒将Cu2O和Cu的固体混合物5.2g放 ( http: / / www.21cnjy.com )入烧杯中,加入过量的20%的稀硫酸,充分反应后,过滤、洗涤、干燥,得到3.2g固体.下列说法错误的是(已知:Cu不与稀硫酸反应,Cu2O+H2SO4═CuSO4+Cu+H2O)( )21教育网
A.剩余固体为纯净物
B.反应过程中,溶液逐渐变蓝
C.原固体混合物中Cu的质量大于Cu2O
D.在最后一次洗涤后的滤液中滴加BaCl2溶液,检验固体是否洗涤干净
7﹒将14.6g表面氧化的锌片,加入到100g19.6%的稀硫酸中,充分反应后,得到114.4g溶液,则下列说法正确的是( )21cnjy.com
A.稀硫酸一加入立即有气泡产生
B.所得溶液中的溶质为H2SO4和ZnSO4
C.反应后生成ZnSO432.2g
D.14.6g表面氧化的锌片中含锌元素质量为6.5g
8﹒化学是研究物质的组成、结构、性质、用途及其变化规律的基础自然科学,请回答下列问题:
(1)从微粒角度看:硫酸是由 H+
(填离子符号)和SO42-构成的;
(2)从性质角度看:稀硫酸溶液可使石蕊试液 ( http: / / www.21cnjy.com )显红色,说明其具有 酸
性,请写出其与氢氧化钠反应的化学方程式 。
9﹒在盛有稀硫酸的烧杯中 ( http: / / www.21cnjy.com ),漂浮着一木块,如图所示。如果往烧杯中中入少量某种固体物质后,木块浸没在水中的体积变大,加入固体物质可能是 Ba(OH)2
(写化学式),理由是 稀硫酸和氢氧化钡反应生成硫酸钡沉淀和水,反应后,溶液的密度变小,而木块所受的浮力不变,由F=ρgV排知,木块排开水的体积将变大
。
10﹒如图所示,是为了验证稀硫酸化学性质所做的三个实验,回答下列问题.
( http: / / www.21cnjy.com / )
(1)A实验能体现出稀硫酸具有的化学性质是 酸能与碱反应
;
(2)B实验过程中能观察到的现象是 铁锈消失,溶液变红;过一会儿有气体放出
。
11﹒将H2SO4溶液加入盛有BaCl2溶液的烧杯中,物质变化的微观示意图如下,请回答:
(1)观察到明显的实验现象是 有白色沉淀生成
;
(2)反应后,检验溶液中是否含有H2SO4,即需要检验的离子是 硫酸根离子
;
(3)反应后,检验溶液中是否含有H2SO4,可选用下列物质中的 D
。
A.Zn B.CuO C.石蕊溶液 D.Ba(NO3)2溶液
12﹒某同学通过以下实验验证稀硫酸的部分化学性质:
实验一:Na2CO3+H2SO4 实验二.Ba(NO3)2+H2SO4 实验三:NaOH+H2SO4
将实验一、二、三反应后的所有物质倒入同一洁净的烧杯中,后续实验及现象如下:
( http: / / www.21cnjy.com / )
(1)白色沉淀A是 BaSO4
;
(2)关于无色溶液B成分的猜想中,合理的是 C
。
A.一定有NaNO3,可能含有NaOH
B.一定有NaNO3,可能含有HNO3和H2SO4
C.一定有NaNO3和HNO3,可能含有H2SO4
13﹒为测定某黄铜(铜、锌合金)中铜的 ( http: / / www.21cnjy.com )质量分数,称取32.5g该黄铜粉末放入烧杯中,再向烧杯内加入200g稀硫酸(足量),每隔10分钟测烧杯内(不含烧杯)剩余物质的质量,测得数据如表:
加入稀硫酸后10分钟 加入稀硫酸后20分钟 加入稀硫酸后 加入稀硫酸后40分钟 加入稀硫酸后50分钟
232.4g 232.3g 232.2g 232.1g 232.1g
(1)完全反应后生成氢气的质量为 0.4
g;
(2)计算该黄铜中铜的质量分数(写出计算过程)
参考答案
说明:选择题7*3+填空题12*2+解答题5=50分
题号 1 2 3 4 5 6 7
答案 C D C C D C C
8﹒(1)H+
(2)酸 H2SO4+2NaOH=Na2SO4+2H2O
9﹒Ba(OH)2 稀硫酸 ( http: / / www.21cnjy.com )和氢氧化钡反应生成硫酸钡沉淀和水,反应后,溶液的密度变小,而木块所受的浮力不变,由F=ρgV排知,木块排开水的体积将变大21·cn·jy·com
10﹒(1)酸能与碱反应
(2)铁锈消失,溶液变红,过一会儿有气体放出
11﹒(1)有白色沉淀生成
(2)硫酸根离子;
(3)D
12﹒(1)BaSO4 (2)C
13﹒解:根据质量守恒定律可得,生成的氢气的质量为32.5g+200g-232.1g=0.4g
设参加反应的锌的质量为x
Zn+H2SO4=ZnSO4+H2↑
65 2
x 0.4g
x=13g
该黄铜中铜的质量分数为×100%=60%
答:该黄铜中铜的质量分数为60%
( http: / / www.21cnjy.com / )
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://www.21cnjy.com/" 版权所有@21世纪教育网(www.21cnjy.com)
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
