第1章 物质及其变化——酸碱盐专题复习
文档属性
| 名称 | 第1章 物质及其变化——酸碱盐专题复习 |  | |
| 格式 | zip | ||
| 文件大小 | 639.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2017-10-05 20:47:32 | ||
图片预览


文档简介
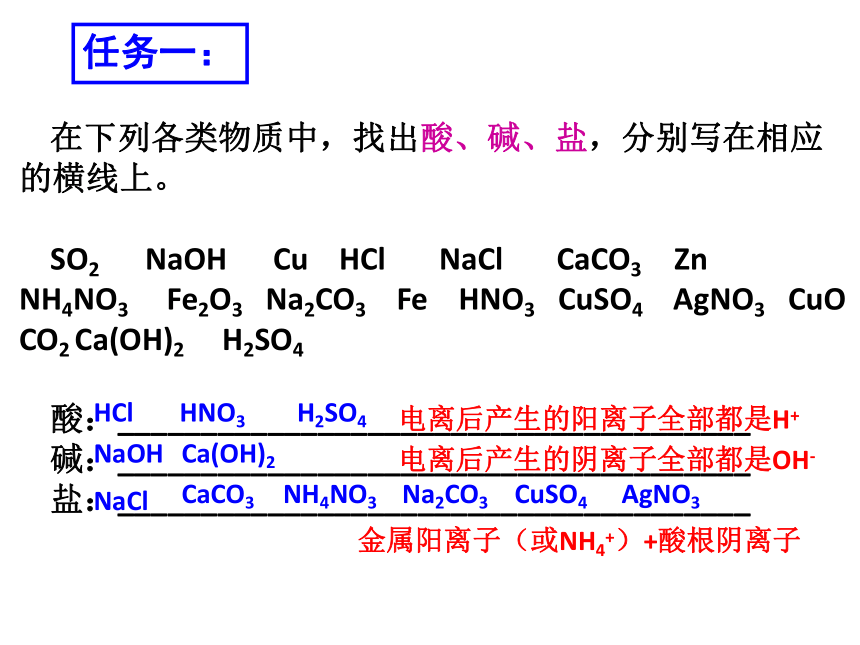
课件25张PPT。在下列各类物质中,找出酸、碱、盐,分别写在相应的横线上。
SO2 NaOH Cu HCl NaCl CaCO3 Zn NH4NO3 Fe2O3 Na2CO3 Fe HNO3 CuSO4 AgNO3 CuO CO2 Ca(OH)2 H2SO4
酸:______________________________________
碱:______________________________________
盐:______________________________________任务一:HCl HNO3 H2SO4NaOHCa(OH)2NaClCaCO3NH4NO3Na2CO3CuSO4AgNO3电离后产生的阳离子全部都是H+电离后产生的阴离子全部都是OH-金属阳离子(或NH4+)+酸根阴离子例1、[2014·嘉兴]人们对事物的认识常需经历一个不断修正和完善的过程,如对酸的认识就是如此。下列各项是不同时期对酸的认识,其中与我们现在所学酸的定义最相近的是 ( )
A.有酸味的物质
B.只有氢才是酸不可缺少的元素
C.一切酸中都含有氧
D.与碱作用时失去原有性质的物质B溶液酸碱
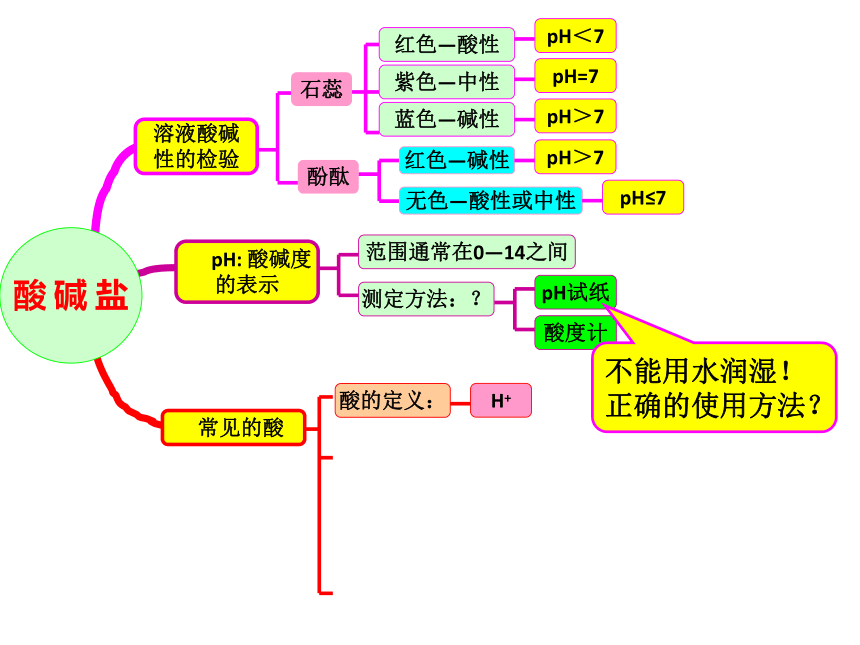
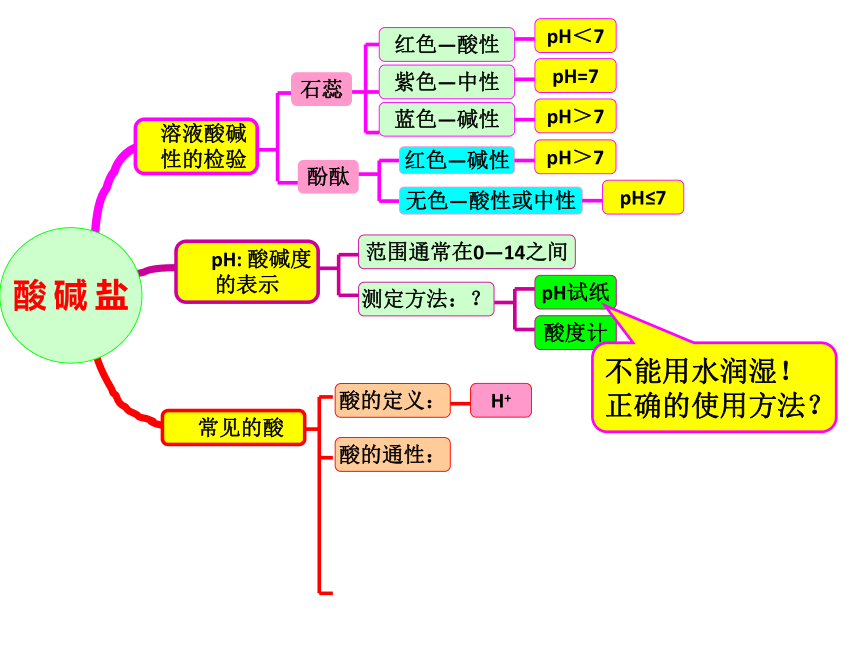
性的检验 酚酞 石蕊 红色—酸性 紫色—中性 蓝色—碱性 pH<7 pH=7pH>7 红色—碱性 无色—酸性或中性 pH>7 pH≤7 pH: 酸碱度
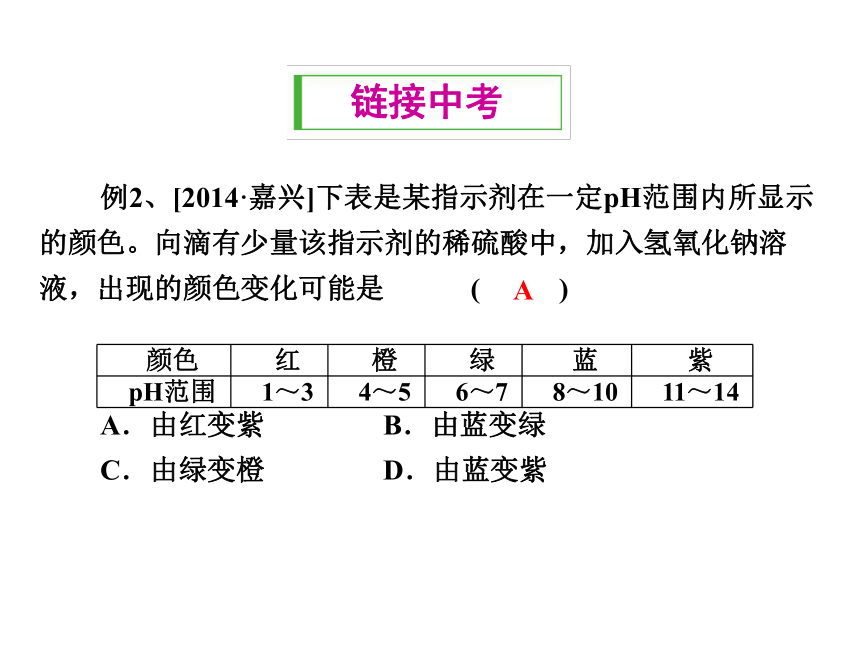
的表示 范围通常在0—14之间 测定方法:? pH试纸 酸度计 常见的酸 酸的定义:H+酸 碱 盐例2、[2014·嘉兴]下表是某指示剂在一定pH范围内所显示的颜色。向滴有少量该指示剂的稀硫酸中,加入氢氧化钠溶液,出现的颜色变化可能是 ( )
A.由红变紫 B.由蓝变绿
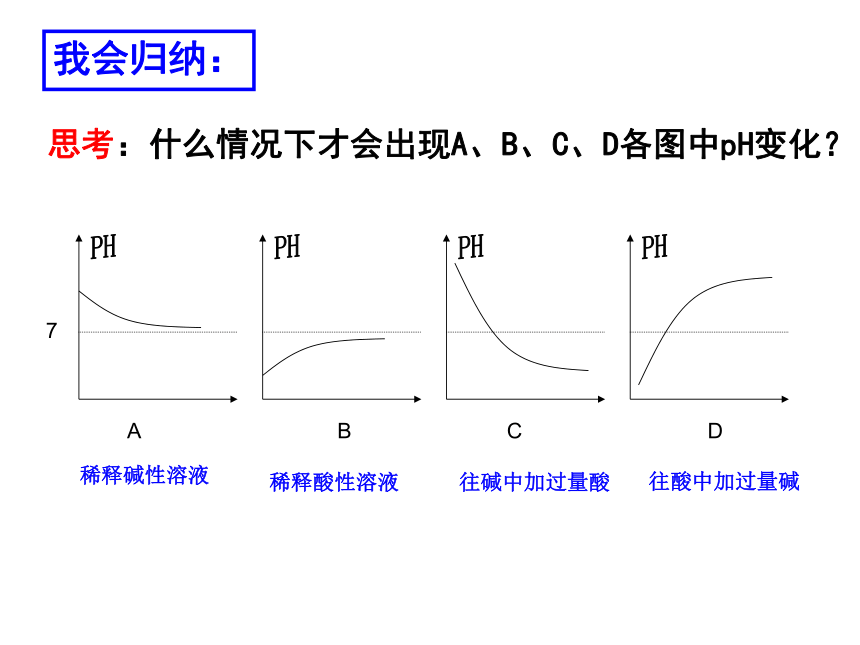
C.由绿变橙 D.由蓝变紫A思考:什么情况下才会出现A、B、C、D各图中pH变化?我会归纳:稀释碱性溶液稀释酸性溶液往碱中加过量酸往酸中加过量碱 溶液酸碱
性的检验 酚酞 石蕊 红色—酸性 紫色—中性 蓝色—碱性 pH<7 pH=7pH>7 红色—碱性 无色—酸性或中性 pH>7 pH≤7 pH: 酸碱度
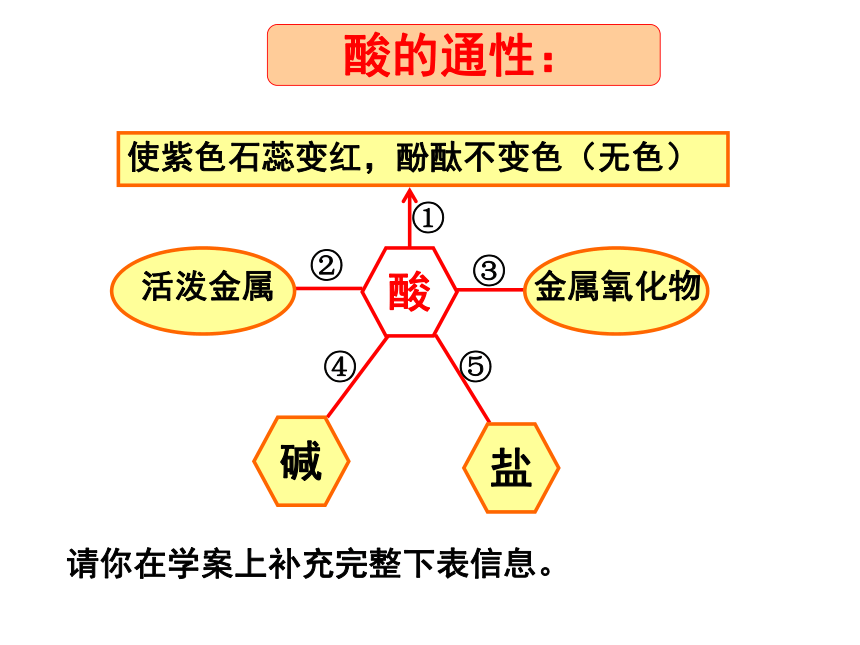
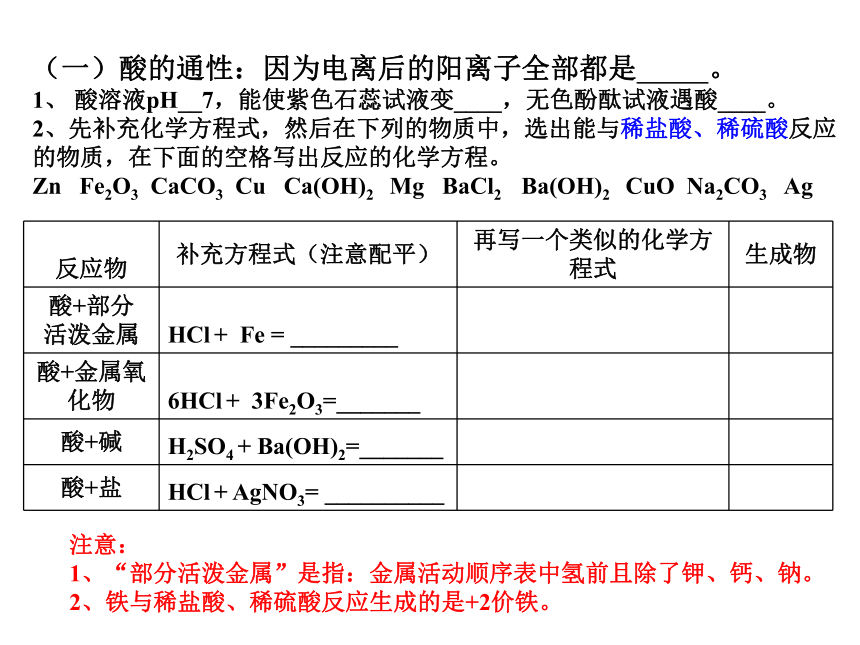
的表示 范围通常在0—14之间 测定方法:? pH试纸 酸度计 常见的酸 酸的定义:H+酸 碱 盐酸的通性:酸使紫色石蕊变红,酚酞不变色(无色)活泼金属金属氧化物碱盐酸的通性:①②④⑤③请你在学案上补充完整下表信息。(一)酸的通性:因为电离后的阳离子全部都是 。
1、 酸溶液pH__7,能使紫色石蕊试液变____,无色酚酞试液遇酸____。
2、先补充化学方程式,然后在下列的物质中,选出能与稀盐酸、稀硫酸反应的物质,在下面的空格写出反应的化学方程。
Zn Fe2O3 CaCO3 Cu Ca(OH)2 Mg BaCl2 Ba(OH)2 CuO Na2CO3 Ag 注意:
1、“部分活泼金属”是指:金属活动顺序表中氢前且除了钾、钙、钠。
2、铁与稀盐酸、稀硫酸反应生成的是+2价铁。2、试管内壁附着的下列物质中,不能用稀盐酸浸泡而除去的是( )
A.氯化铁溶液与氢氧化钠溶液反应后留下的红褐色固体
B.碱式碳酸铜受热分解后的黑色固体
C.用足量氢气还原氧化铜后留下的红色固体
D.盛放石灰水后留下的白色固体对应练习:C1、由于人的胃里有_________,因此胃液分泌过多会引起胃病,服用含有氢氧化铝的药物可缓解病痛。其治疗的化学原理为(用化学方程式表示)__________。盐酸3HCl+Al(OH)3=AlCl3+3H2O酸碱盐溶液酸碱
性的检验酚酞石蕊红色—酸性紫色—中性蓝色—碱性pH<7pH=7pH>7红色—碱性无色—酸性或中性pH>7pH≤7pH: 酸碱度
的表示范围通常在0—14之间测定方法:?pH试纸酸度计常见的酸酸的定义:酸的个性:H+浓盐酸有挥发性
腐蚀性打开瓶塞瓶口有白雾能否用它制取CO2 ?浓硫酸有吸水性有脱水性有强氧化性有腐蚀性溶解放热作干燥剂化学性质不能用来制取H2沾到皮肤如何处理?如何稀释?浓硝酸碳酸醋酸酸的通性:例3、[2013·福州]配制稀硫酸的部分操作过程如图所示,其中错误的是( )
C 溶液酸碱
性的检验 酚酞 石蕊 红色—酸性 紫色—中性 蓝色—碱性 pH<7 pH=7pH>7 红色—碱性 无色—酸性或中性 pH>7 pH≤7 pH: 酸碱度
的表示 范围通常在0—14之间 测定方法:? pH试纸 酸度计 常见的酸 酸的定义:H+酸 碱 盐酸的通性:酸的个性:浓盐酸有挥发性
腐蚀性打开瓶塞瓶口有白雾能否用它制取CO2 ?浓硫酸有吸水性有脱水性有强氧化性有腐蚀性溶解放热作干燥剂化学性质不能用来制取H2沾到皮肤如何处理?如何稀释?浓硝酸有挥发性、腐蚀性、见光易分解碳酸醋酸易分解例4、[2013·金华]为区别稀盐酸和稀硫酸,小强同学设计如图所示的实验方案:在每组的两支试管中分别盛放稀盐酸和稀硫酸;向同组的两支试管各滴加同种试剂。其中能达到实验目的的是 ( )
D酸碱盐 溶液酸碱
性的检验酚酞石蕊红色—酸性紫色—中性蓝色—碱性pH<7pH=7pH>7红色—碱性无色—酸性或中性pH>7pH≤7 pH: 酸碱度
的表示范围通常在0—14之间测定方法:?pH试纸酸度计 常见的酸酸的定义:酸的个性:酸的通性:H+浓盐酸有挥发性
腐蚀性打开瓶塞瓶口有白雾能否用它制取CO2 ?浓硫酸有吸水性有脱水性有强氧化性有腐蚀性溶解放热作干燥剂化学性质不能用来制取H2沾到皮肤如何处理?如何稀释?浓硝酸有挥发性、腐蚀性、见光易分解碳酸醋酸易分解常见的碱碱的定义:OH—碱的通性:酸使紫色石蕊变红,酚酞不变色(无色)活泼金属金属氧化物碱盐①②③④碱的通性:使紫色石蕊变蓝,使酚酞变红非金属氧化物酸盐碱请你在学案上补充完整下表信息。(二)碱的通性:因为电离后的阴离子全部都是 。
1、碱溶液PH__7,使紫色石蕊试液变_______,无色酚酞试液遇到碱____。
2、先补充化学方程式,然后在下列的物质中,选出能与碱反应的物质,在下面的空格写出反应的化学方程。
SO2 AgCl CaCO3 CO2 NH4Cl CuCl2 Na2CO3 HCl BaCl2 CuSO4 H2SO4 注意:
1、碱与盐反应时,反应物必须均可溶,且还要符合复分解反应发生的条件(↑↓H2O)。
2、难溶碱:Mg(OH)2和Al(OH)3 (白色)、 Fe(OH)3 (红褐色)、Cu(OH)2(蓝色)。
酸碱盐 溶液酸碱
性的检验酚酞石蕊红色—酸性紫色—中性蓝色—碱性pH<7pH=7pH>7红色—碱性无色—酸性或中性pH>7pH≤7 pH: 酸碱度
的表示范围通常在0—14之间测定方法:?pH试纸酸度计 常见的酸酸的定义:酸的个性:酸的通性:H+浓盐酸有挥发性
腐蚀性打开瓶塞瓶口有白雾能否用它制取CO2 ?浓硫酸有吸水性有脱水性有强氧化性有腐蚀性溶解放热作干燥剂化学性质不能用来制取H2沾到皮肤如何处理?如何稀释?浓硝酸有挥发性、腐蚀性、见光易分解碳酸醋酸易分解常见的碱碱的定义:OH—碱的个性:NaOH俗名物理性质易潮解强腐蚀性极易溶于水(放热)Ca(OH)2俗名物理性质白色固体微溶于水溶解度随温度升高而减小NH4OH有氨臭味
易挥发制氮肥碱的通性: 例5、[2014·金华]研究氢氧化钠性质实验中的部分实验及现象记录如下,其中现象不合理的是 ( )C[变式训练]敞口放置的氢氧化钠溶液易吸收空气中的二氧化碳而变质,请写出此过程的化学方程式:________________。现向一定质量且部分变质的氢氧化钠溶液中逐滴加入稀盐酸,并振荡。如图25-9表示反应过程中溶液质量随加入盐酸质量的变化而变化的情况。那么,图像BC段对应的实验现象是______________,在C点时溶液中的溶质是__________________。图25-92NaOH+CO2 ===Na2CO3+H2O有气泡产生NaCl(或氯化钠)酸使紫色石蕊变红,酚酞不变色(无色)活泼金属金属氧化物碱盐①②③④使紫色石蕊变蓝,使酚酞变红非金属氧化物酸盐碱观察酸的通性和碱的通性,你是否找到了它们的共同性质?③酸碱反应:(1)含义:由酸和碱作用生成盐和水的复分解反应。(3)应用:中和反应在工农业、生活、实验研究中应用广泛。如:用__________中和酸性土壤,用胃舒平(主要成分氢氧化铝)中和胃酸过多等。(2)本质:酸碱反应的实质是H+和OH-结合生成水。酸碱反应是放热反应。熟石灰将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示:(1)由图知,稀盐酸与氢氧化钠溶液发生的反应是______ (填“放热”或“吸热”)反应。
(2)从A到B过程中,烧杯中溶液的pH逐渐___________。
B点表示的含义是______________________________。放热变小/减小酸碱恰好完全中和或酸碱恰好完全反应对应练习:课堂小结:
SO2 NaOH Cu HCl NaCl CaCO3 Zn NH4NO3 Fe2O3 Na2CO3 Fe HNO3 CuSO4 AgNO3 CuO CO2 Ca(OH)2 H2SO4
酸:______________________________________
碱:______________________________________
盐:______________________________________任务一:HCl HNO3 H2SO4NaOHCa(OH)2NaClCaCO3NH4NO3Na2CO3CuSO4AgNO3电离后产生的阳离子全部都是H+电离后产生的阴离子全部都是OH-金属阳离子(或NH4+)+酸根阴离子例1、[2014·嘉兴]人们对事物的认识常需经历一个不断修正和完善的过程,如对酸的认识就是如此。下列各项是不同时期对酸的认识,其中与我们现在所学酸的定义最相近的是 ( )
A.有酸味的物质
B.只有氢才是酸不可缺少的元素
C.一切酸中都含有氧
D.与碱作用时失去原有性质的物质B溶液酸碱
性的检验 酚酞 石蕊 红色—酸性 紫色—中性 蓝色—碱性 pH<7 pH=7pH>7 红色—碱性 无色—酸性或中性 pH>7 pH≤7 pH: 酸碱度
的表示 范围通常在0—14之间 测定方法:? pH试纸 酸度计 常见的酸 酸的定义:H+酸 碱 盐例2、[2014·嘉兴]下表是某指示剂在一定pH范围内所显示的颜色。向滴有少量该指示剂的稀硫酸中,加入氢氧化钠溶液,出现的颜色变化可能是 ( )
A.由红变紫 B.由蓝变绿
C.由绿变橙 D.由蓝变紫A思考:什么情况下才会出现A、B、C、D各图中pH变化?我会归纳:稀释碱性溶液稀释酸性溶液往碱中加过量酸往酸中加过量碱 溶液酸碱
性的检验 酚酞 石蕊 红色—酸性 紫色—中性 蓝色—碱性 pH<7 pH=7pH>7 红色—碱性 无色—酸性或中性 pH>7 pH≤7 pH: 酸碱度
的表示 范围通常在0—14之间 测定方法:? pH试纸 酸度计 常见的酸 酸的定义:H+酸 碱 盐酸的通性:酸使紫色石蕊变红,酚酞不变色(无色)活泼金属金属氧化物碱盐酸的通性:①②④⑤③请你在学案上补充完整下表信息。(一)酸的通性:因为电离后的阳离子全部都是 。
1、 酸溶液pH__7,能使紫色石蕊试液变____,无色酚酞试液遇酸____。
2、先补充化学方程式,然后在下列的物质中,选出能与稀盐酸、稀硫酸反应的物质,在下面的空格写出反应的化学方程。
Zn Fe2O3 CaCO3 Cu Ca(OH)2 Mg BaCl2 Ba(OH)2 CuO Na2CO3 Ag 注意:
1、“部分活泼金属”是指:金属活动顺序表中氢前且除了钾、钙、钠。
2、铁与稀盐酸、稀硫酸反应生成的是+2价铁。2、试管内壁附着的下列物质中,不能用稀盐酸浸泡而除去的是( )
A.氯化铁溶液与氢氧化钠溶液反应后留下的红褐色固体
B.碱式碳酸铜受热分解后的黑色固体
C.用足量氢气还原氧化铜后留下的红色固体
D.盛放石灰水后留下的白色固体对应练习:C1、由于人的胃里有_________,因此胃液分泌过多会引起胃病,服用含有氢氧化铝的药物可缓解病痛。其治疗的化学原理为(用化学方程式表示)__________。盐酸3HCl+Al(OH)3=AlCl3+3H2O酸碱盐溶液酸碱
性的检验酚酞石蕊红色—酸性紫色—中性蓝色—碱性pH<7pH=7pH>7红色—碱性无色—酸性或中性pH>7pH≤7pH: 酸碱度
的表示范围通常在0—14之间测定方法:?pH试纸酸度计常见的酸酸的定义:酸的个性:H+浓盐酸有挥发性
腐蚀性打开瓶塞瓶口有白雾能否用它制取CO2 ?浓硫酸有吸水性有脱水性有强氧化性有腐蚀性溶解放热作干燥剂化学性质不能用来制取H2沾到皮肤如何处理?如何稀释?浓硝酸碳酸醋酸酸的通性:例3、[2013·福州]配制稀硫酸的部分操作过程如图所示,其中错误的是( )
C 溶液酸碱
性的检验 酚酞 石蕊 红色—酸性 紫色—中性 蓝色—碱性 pH<7 pH=7pH>7 红色—碱性 无色—酸性或中性 pH>7 pH≤7 pH: 酸碱度
的表示 范围通常在0—14之间 测定方法:? pH试纸 酸度计 常见的酸 酸的定义:H+酸 碱 盐酸的通性:酸的个性:浓盐酸有挥发性
腐蚀性打开瓶塞瓶口有白雾能否用它制取CO2 ?浓硫酸有吸水性有脱水性有强氧化性有腐蚀性溶解放热作干燥剂化学性质不能用来制取H2沾到皮肤如何处理?如何稀释?浓硝酸有挥发性、腐蚀性、见光易分解碳酸醋酸易分解例4、[2013·金华]为区别稀盐酸和稀硫酸,小强同学设计如图所示的实验方案:在每组的两支试管中分别盛放稀盐酸和稀硫酸;向同组的两支试管各滴加同种试剂。其中能达到实验目的的是 ( )
D酸碱盐 溶液酸碱
性的检验酚酞石蕊红色—酸性紫色—中性蓝色—碱性pH<7pH=7pH>7红色—碱性无色—酸性或中性pH>7pH≤7 pH: 酸碱度
的表示范围通常在0—14之间测定方法:?pH试纸酸度计 常见的酸酸的定义:酸的个性:酸的通性:H+浓盐酸有挥发性
腐蚀性打开瓶塞瓶口有白雾能否用它制取CO2 ?浓硫酸有吸水性有脱水性有强氧化性有腐蚀性溶解放热作干燥剂化学性质不能用来制取H2沾到皮肤如何处理?如何稀释?浓硝酸有挥发性、腐蚀性、见光易分解碳酸醋酸易分解常见的碱碱的定义:OH—碱的通性:酸使紫色石蕊变红,酚酞不变色(无色)活泼金属金属氧化物碱盐①②③④碱的通性:使紫色石蕊变蓝,使酚酞变红非金属氧化物酸盐碱请你在学案上补充完整下表信息。(二)碱的通性:因为电离后的阴离子全部都是 。
1、碱溶液PH__7,使紫色石蕊试液变_______,无色酚酞试液遇到碱____。
2、先补充化学方程式,然后在下列的物质中,选出能与碱反应的物质,在下面的空格写出反应的化学方程。
SO2 AgCl CaCO3 CO2 NH4Cl CuCl2 Na2CO3 HCl BaCl2 CuSO4 H2SO4 注意:
1、碱与盐反应时,反应物必须均可溶,且还要符合复分解反应发生的条件(↑↓H2O)。
2、难溶碱:Mg(OH)2和Al(OH)3 (白色)、 Fe(OH)3 (红褐色)、Cu(OH)2(蓝色)。
酸碱盐 溶液酸碱
性的检验酚酞石蕊红色—酸性紫色—中性蓝色—碱性pH<7pH=7pH>7红色—碱性无色—酸性或中性pH>7pH≤7 pH: 酸碱度
的表示范围通常在0—14之间测定方法:?pH试纸酸度计 常见的酸酸的定义:酸的个性:酸的通性:H+浓盐酸有挥发性
腐蚀性打开瓶塞瓶口有白雾能否用它制取CO2 ?浓硫酸有吸水性有脱水性有强氧化性有腐蚀性溶解放热作干燥剂化学性质不能用来制取H2沾到皮肤如何处理?如何稀释?浓硝酸有挥发性、腐蚀性、见光易分解碳酸醋酸易分解常见的碱碱的定义:OH—碱的个性:NaOH俗名物理性质易潮解强腐蚀性极易溶于水(放热)Ca(OH)2俗名物理性质白色固体微溶于水溶解度随温度升高而减小NH4OH有氨臭味
易挥发制氮肥碱的通性: 例5、[2014·金华]研究氢氧化钠性质实验中的部分实验及现象记录如下,其中现象不合理的是 ( )C[变式训练]敞口放置的氢氧化钠溶液易吸收空气中的二氧化碳而变质,请写出此过程的化学方程式:________________。现向一定质量且部分变质的氢氧化钠溶液中逐滴加入稀盐酸,并振荡。如图25-9表示反应过程中溶液质量随加入盐酸质量的变化而变化的情况。那么,图像BC段对应的实验现象是______________,在C点时溶液中的溶质是__________________。图25-92NaOH+CO2 ===Na2CO3+H2O有气泡产生NaCl(或氯化钠)酸使紫色石蕊变红,酚酞不变色(无色)活泼金属金属氧化物碱盐①②③④使紫色石蕊变蓝,使酚酞变红非金属氧化物酸盐碱观察酸的通性和碱的通性,你是否找到了它们的共同性质?③酸碱反应:(1)含义:由酸和碱作用生成盐和水的复分解反应。(3)应用:中和反应在工农业、生活、实验研究中应用广泛。如:用__________中和酸性土壤,用胃舒平(主要成分氢氧化铝)中和胃酸过多等。(2)本质:酸碱反应的实质是H+和OH-结合生成水。酸碱反应是放热反应。熟石灰将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示:(1)由图知,稀盐酸与氢氧化钠溶液发生的反应是______ (填“放热”或“吸热”)反应。
(2)从A到B过程中,烧杯中溶液的pH逐渐___________。
B点表示的含义是______________________________。放热变小/减小酸碱恰好完全中和或酸碱恰好完全反应对应练习:课堂小结:
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
