2017-2018年高中化学必修二:3.3生活中两种常见的有机物 课件 (共59张PPT)
文档属性
| 名称 | 2017-2018年高中化学必修二:3.3生活中两种常见的有机物 课件 (共59张PPT) |  | |
| 格式 | zip | ||
| 文件大小 | 3.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-03-18 16:13:38 | ||
图片预览








文档简介
课件59张PPT。第三章 有机化合物第三节 生活中两种常见的有机物新课标人教版高中化学课件系列化学 必修2工业酒精 约含乙醇96%以上(质量分数)无水酒精 99.5%以上(质量分数) 医用酒精 75%(体积分数)饮用酒 视度数而定体积分数。
啤酒的度数指麦芽含量⑵ 如何检验酒精是否含水? 用工业酒精与新制生石灰混合蒸馏,可得无水酒精。用无水硫酸铜检验 ⑴ 如何由工业酒精制取无水酒精? 【问题】小常识一、乙醇(一)、物理性质颜 色:
气 味:
状 态:
挥发性:
熔沸点:
密 度:
溶解性:无色透明特殊香味液 体小(密度:0.789g /㎝3)
易挥发低(沸点:78.5℃熔点:-117.3℃)能与水以任意比互溶,能溶解多种
有机物和无机物 Br2、I2等
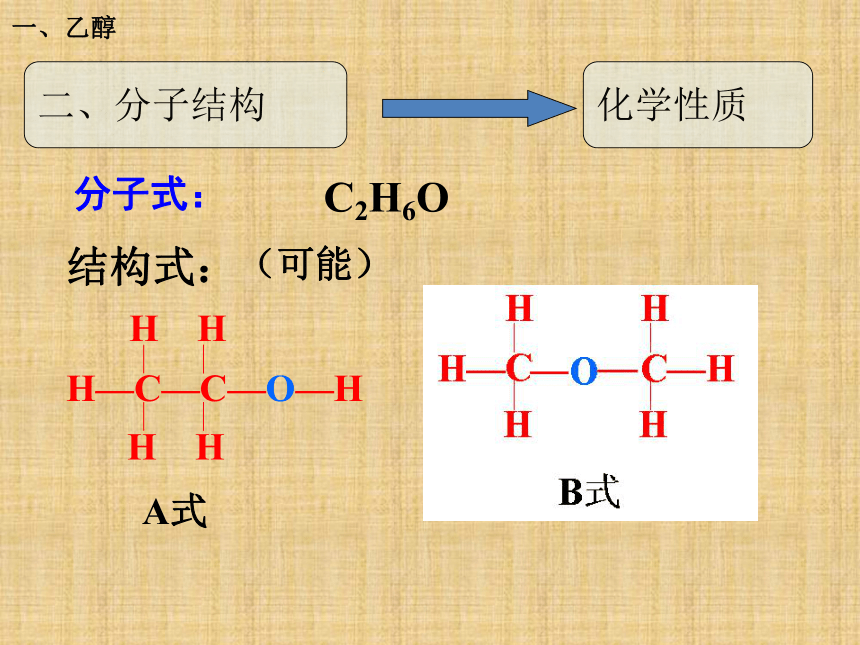
一、乙醇分子式:结构式:
C2H6O二、分子结构化学性质(可能)一、乙醇实验3-2 乙醇与金属钠的反应现象:钠沉在乙醇底部,表面有无色气泡产生,没有
迅速熔成小球。倒置小烧杯内表面有水珠生成,澄清
石灰水倒入烧杯内,未见浑浊。探究:乙醇的分子结构观察与思考:
1.金属钠的变化?
2.气体燃烧的现象?
3.气体产物是什么?一、乙醇
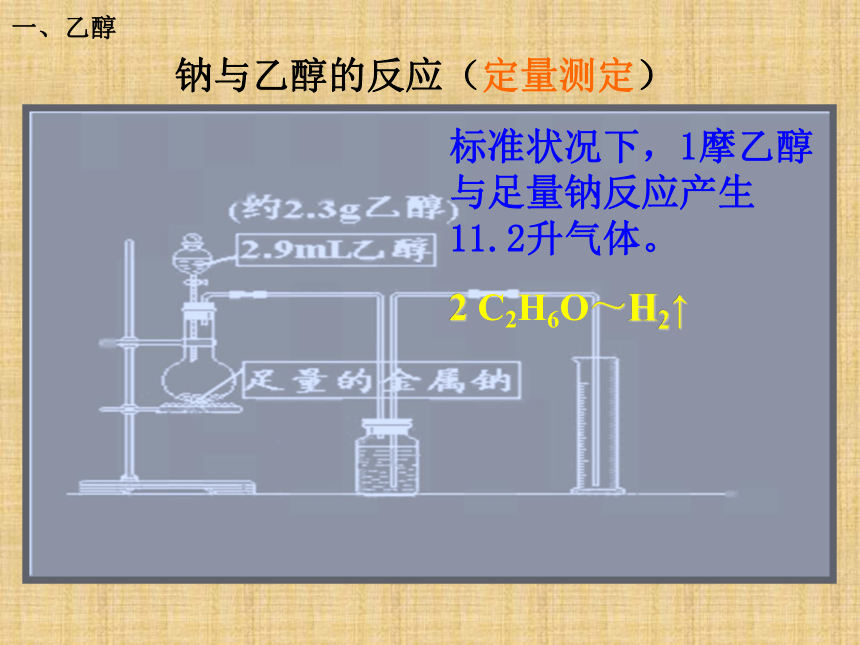
钠与乙醇的反应(定量测定)标准状况下,1摩乙醇与足量钠反应产生11.2升气体。
2 C2H6O~H2↑一、乙醇分子式:结构式:
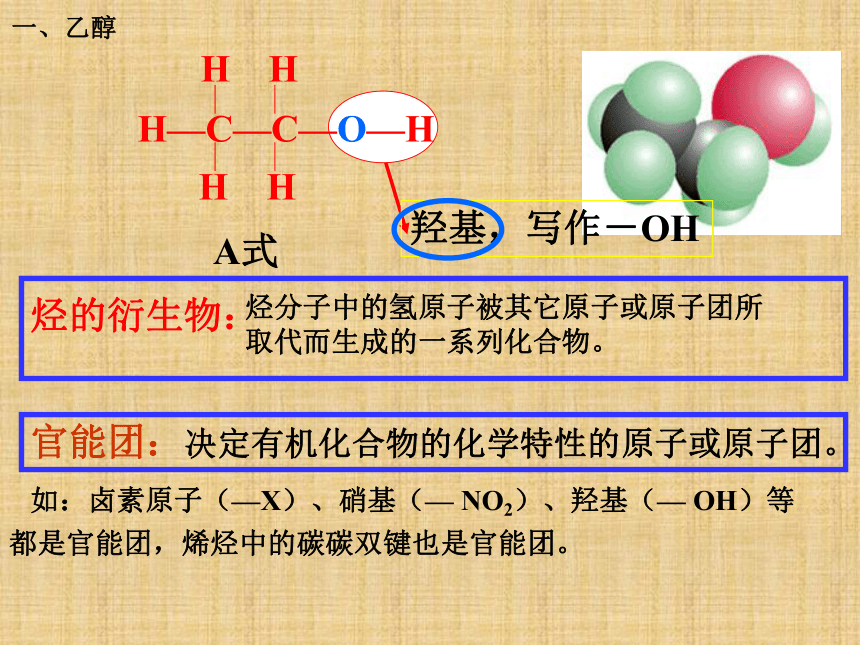
C2H6O(二)分子结构化学性质(可能)结构简式:CH3CH2OH或C2H5OH一、乙醇烃的衍生物:
官能团:决定有机化合物的化学特性的原子或原子团。 羟基,写作-OH 如:卤素原子(—X)、硝基(— NO2)、羟基(— OH)等都是官能团,烯烃中的碳碳双键也是官能团。烃分子中的氢原子被其它原子或原子团所取代而生成的一系列化合物。一、乙醇“浮、熔、
游、响” 钠块沉于乙醇底部、不熔成小球、也不发出响声 发出淡蓝
色火焰。 安静燃烧,发出
淡蓝色火焰,
烧杯内壁有水珠加酚酞后溶液变红,
说明有碱性物质
(NaOH)生成。 加酚酞后溶液变红,
说明有碱性物质生成;
烧杯中石灰水无明显现
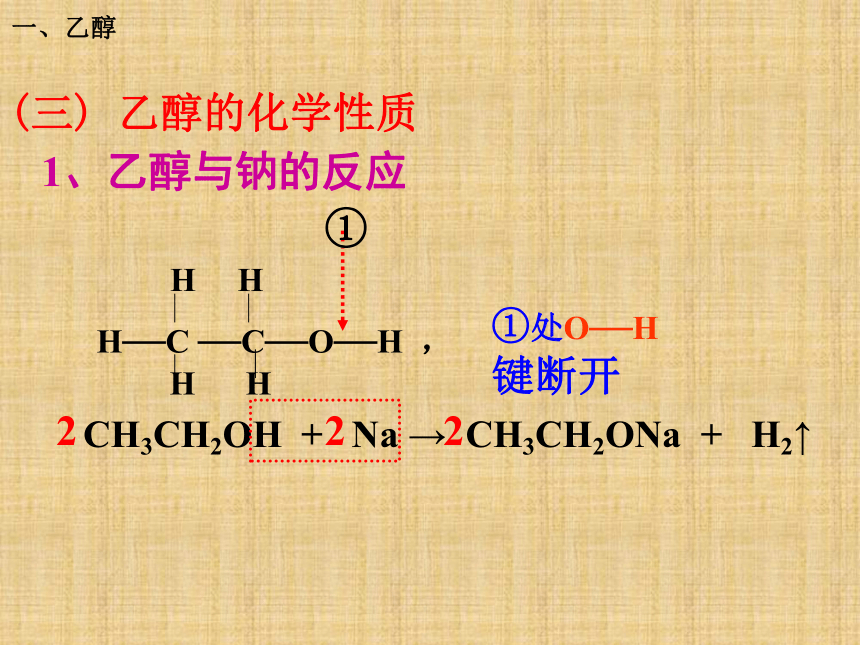
象,说明无CO2生成。 比较水、乙醇与钠反应 一、乙醇 1、钠浮在水面上,而沉在乙醇中水的密度>钠的密度>乙醇的密度2、钠与乙醇的反应速率比钠与水的反应速率慢, 说明羟基中的H原子的活泼性:乙醇<水对比实验现象说明了什么问题?请你讨论一、乙醇(三) 乙醇的化学性质 1、乙醇与钠的反应CH3CH2OH + Na → CH3CH2ONa + H2↑2 2 2一、乙醇[练习]其它活泼金属如钾、镁和铝等也可与乙醇反应,均可产生H2,请写出镁与乙醇反应的化学方程式。一、乙醇2.氧化反应 (1)燃烧(彻底氧化)一、乙醇1焊接银器、铜器时,表面会生成发黑的氧化膜,工匠说,可以先把铜、银在火上烧热,马上蘸一下酒精,铜银会光亮如初!你知道么?一、乙醇 实验3-3把灼热的铜丝插入乙醇中,观察铜丝颜色变化,并小心闻试管中液体产生的气味。铜丝有刺激性气味(2)乙醇的催化氧化 (工业制乙醛) 一、乙醇实验现象:红热的铜丝,移离火焰变黑,迅速伸入乙醇中,铜丝由黑变红,同时产生刺激性气味。铜丝变黑又变红产生刺激性气味CH3CHO 乙醛+H2O 总反应方程式:(2)乙醇的催化氧化 (工业制乙醛) 一、乙醇乙醇催氧化过程一、乙醇乙醇的催化氧化键的断裂一、乙醇焊接银器、铜器时,表面会生成发黑的氧化膜,工匠说,可以先把铜、银在火上烧热,马上蘸一下酒精,铜银会光亮如初!原来如此!一、乙醇 试判断下列醇能否发生催化氧化的反应:CH3CH2CH2OH CH3CH(OH)CH3
(CH3)3CCH2OH结论:与-OH的碳原子上连接必须有H, 才发生催化氧化请你帮帮我一、乙醇交警判断驾驶员是否酒后驾车的方法 ?一、乙醇酸性高锰
酸钾溶液乙 醇酸性重铬
酸钾溶液乙 醇身边的化学 ——酒后驾车的检查原理??一、乙醇(3)被酸性KMnO4 、K2Cr2O7 溶液氧化为乙酸一、乙醇取代催化氧化结构决定性质让我们来总结一下一、乙醇乙醇乙醛乙酸CO2+H2O +热量CH3CHO知识拓展:一、乙醇切莫贪杯一、乙醇(四)、乙醇的用途乙 醇饮 料化工原料溶 剂医 药燃料一、乙醇作燃料 —— 飞机、汽车、火锅、酒精灯等作消毒剂 —— 医用酒精等一、乙醇制酒精型饮料 —— 啤酒、红酒等工业制取乙酸一、乙醇 (一)、乙醇的物理性质:
(二)、乙醇的结构:
(三)、乙醇的化学性质:
1、乙醇与活泼金属反应
2C2H5OH+2Na→2C2H5ONa+H2↑
2、乙醇的氧化反应
①燃 烧:
②催化氧化:
(四)、乙醇的用途:小结Cu一、乙醇课堂练习1、如右图所示:简述乙醇发生各种反应是键的断裂情况2、将等量的铜片在酒精灯上加热后,分别插入下列溶液中,放置片刻后铜片质量与加热前相同的是( )
A.硝酸 B. 无水乙醇 C. 石灰水 D. 盐酸B一、乙醇拓展练习2、A、B、C三种醇同足量的金属钠完全反应,在相同条件下产生相同体积的氢气,消耗这三种醇的物质的量之比为3∶6∶2,则A、B、C三种醇分子中羟基数之比是( ) A. 3∶2∶1 B. 2∶6∶3
C. 3∶1∶2 D. 2∶1∶3一、乙醇拓展练习一、乙醇二、乙酸 传说古代山西省有个酿酒高手叫杜康。他儿子黑塔跟父亲也学会了酿酒技术。后来,从山西迁到镇江。黑塔觉得酿酒后把酒糟扔掉可惜,把酒糟浸泡在水缸里。到了第二十一日的酉时,一开缸,一股浓郁的香气扑鼻而来。黑塔忍不住尝了一口,酸酸的,味道很美。烧菜时放了一些,味道特别鲜美,便贮藏着作为“调味酱”。这“调味酱”就是今天的醋。醋的来历?二、乙酸酉廿一日二、乙酸乙酸的物理性质 通过观察乙酸,阅读课本总结乙酸的物理性质(颜色、状态、气味、溶解性、熔沸点等角度分析).二、乙酸乙酸分子的结构甲基羧基—官能团分子式:结构式结构简式或C2H4O2 CH3COOH二、乙酸水垢主要成份:
Mg(OH)2和CaCO3 通过这个生活常识你能得到什么启示?二、乙酸科学探究1:根据下列提供的药品,设计 实验证明乙酸的酸性药品: 镁带、NaOH溶液 、 Na2CO3粉末、
乙酸溶液、酚酞、石蕊。二、乙酸证明乙酸的酸性的可行方案: 二、乙酸如何设计实验比较酸性强弱:CH3COOH、H2CO3酸性:CH3COOH>H2CO3[科学探究2]实验方案:
1、向一试管中加入碳酸钠粉末。
2、向试管中加入醋酸,观察现象。 二、乙酸“酒是陈的香”为什么呢?二、乙酸 厨师烧鱼时常加醋并加点酒,这样鱼的味道就变得无腥、香醇,特别鲜美。为什么呢?二、乙酸实验 3-4二、乙酸实验现象:
1、饱和Na2CO3溶液上层有透明的不
溶于水的油状液体产生。
2、闻到香味-------乙酸乙酯
二、乙酸①图中发生装置有何特点?为什么使用长导
管?导管口为什么要在溶液的液面上方?②药品的添加顺序如何?③浓硫酸的作用是什么?导管的作用:导气、冷疑不能伸到液面下(防倒吸)注意:先加乙醇再加浓H2SO4最后加乙酸催化剂、吸水剂观察与讨论二、乙酸④得到的产物是否纯净?
主要杂质有哪些?⑤为什么要用饱和的碳酸
钠溶液来吸收产品?含有乙醇、乙酸几种物质的物理性质中和乙酸、溶解乙醇,
降低乙酸乙酯在水中的溶解度观察与讨论二、乙酸酯化反应乙酸 乙醇 乙酸乙酯酯化反应的概念: 酸和醇反应生成酯和水的反应可逆反应二、乙酸可能一可能二同位素示踪法:酯化反应断键的方式:酸脱羟基、醇脱氢。 二、乙酸酯化反应的实质:酸脱羟基、醇脱氢。 乙酸甲酯二、乙酸酸性酯化结构决定性质本节课的重点:二、乙酸黄豆泡醋可以降血压 生活小帮手无“醋” 不在二、乙酸乙酸可以生产农药乙酸是重要的化工原料二、乙酸乙酸可以生产涂料乙酸是重要的化工原料二、乙酸乙酸的用途乙酸二、乙酸小 结一.乙酸的物理性质
二.乙酸的分子结构
结构简式: 特征基团:
三.乙酸的化学性质
1.乙酸的酸性:乙酸是一种一元弱酸,其酸性大于碳酸
2.乙酸的酯化反应(取代) CH3COOH—COOH(羧基)四.乙酸的用途二、乙酸1、关于乙酸的下列说法中不正确的是 ( )
A.乙酸易溶于水和乙醇
B.无水乙酸又称冰醋酸,它是纯净物
C.乙酸是一种重要的有机酸,是有刺激性气味的液体
D.乙酸分子里有四个氢原子,所以不是一元酸D请你来练练二、乙酸2、酯化反应属于( )
A.中和反应 B.不可逆反应
C.离子反应 D.取代反应D3、确定乙酸是弱酸的依据是( )
A. 乙酸可以和乙醇发生酯化反应
B. 乙酸钠的水溶液显碱性
C. 乙酸能使石蕊试液变红
D. Na2CO3中加入乙酸产生CO2B二、乙酸
啤酒的度数指麦芽含量⑵ 如何检验酒精是否含水? 用工业酒精与新制生石灰混合蒸馏,可得无水酒精。用无水硫酸铜检验 ⑴ 如何由工业酒精制取无水酒精? 【问题】小常识一、乙醇(一)、物理性质颜 色:
气 味:
状 态:
挥发性:
熔沸点:
密 度:
溶解性:无色透明特殊香味液 体小(密度:0.789g /㎝3)
易挥发低(沸点:78.5℃熔点:-117.3℃)能与水以任意比互溶,能溶解多种
有机物和无机物 Br2、I2等
一、乙醇分子式:结构式:
C2H6O二、分子结构化学性质(可能)一、乙醇实验3-2 乙醇与金属钠的反应现象:钠沉在乙醇底部,表面有无色气泡产生,没有
迅速熔成小球。倒置小烧杯内表面有水珠生成,澄清
石灰水倒入烧杯内,未见浑浊。探究:乙醇的分子结构观察与思考:
1.金属钠的变化?
2.气体燃烧的现象?
3.气体产物是什么?一、乙醇
钠与乙醇的反应(定量测定)标准状况下,1摩乙醇与足量钠反应产生11.2升气体。
2 C2H6O~H2↑一、乙醇分子式:结构式:
C2H6O(二)分子结构化学性质(可能)结构简式:CH3CH2OH或C2H5OH一、乙醇烃的衍生物:
官能团:决定有机化合物的化学特性的原子或原子团。 羟基,写作-OH 如:卤素原子(—X)、硝基(— NO2)、羟基(— OH)等都是官能团,烯烃中的碳碳双键也是官能团。烃分子中的氢原子被其它原子或原子团所取代而生成的一系列化合物。一、乙醇“浮、熔、
游、响” 钠块沉于乙醇底部、不熔成小球、也不发出响声 发出淡蓝
色火焰。 安静燃烧,发出
淡蓝色火焰,
烧杯内壁有水珠加酚酞后溶液变红,
说明有碱性物质
(NaOH)生成。 加酚酞后溶液变红,
说明有碱性物质生成;
烧杯中石灰水无明显现
象,说明无CO2生成。 比较水、乙醇与钠反应 一、乙醇 1、钠浮在水面上,而沉在乙醇中水的密度>钠的密度>乙醇的密度2、钠与乙醇的反应速率比钠与水的反应速率慢, 说明羟基中的H原子的活泼性:乙醇<水对比实验现象说明了什么问题?请你讨论一、乙醇(三) 乙醇的化学性质 1、乙醇与钠的反应CH3CH2OH + Na → CH3CH2ONa + H2↑2 2 2一、乙醇[练习]其它活泼金属如钾、镁和铝等也可与乙醇反应,均可产生H2,请写出镁与乙醇反应的化学方程式。一、乙醇2.氧化反应 (1)燃烧(彻底氧化)一、乙醇1焊接银器、铜器时,表面会生成发黑的氧化膜,工匠说,可以先把铜、银在火上烧热,马上蘸一下酒精,铜银会光亮如初!你知道么?一、乙醇 实验3-3把灼热的铜丝插入乙醇中,观察铜丝颜色变化,并小心闻试管中液体产生的气味。铜丝有刺激性气味(2)乙醇的催化氧化 (工业制乙醛) 一、乙醇实验现象:红热的铜丝,移离火焰变黑,迅速伸入乙醇中,铜丝由黑变红,同时产生刺激性气味。铜丝变黑又变红产生刺激性气味CH3CHO 乙醛+H2O 总反应方程式:(2)乙醇的催化氧化 (工业制乙醛) 一、乙醇乙醇催氧化过程一、乙醇乙醇的催化氧化键的断裂一、乙醇焊接银器、铜器时,表面会生成发黑的氧化膜,工匠说,可以先把铜、银在火上烧热,马上蘸一下酒精,铜银会光亮如初!原来如此!一、乙醇 试判断下列醇能否发生催化氧化的反应:CH3CH2CH2OH CH3CH(OH)CH3
(CH3)3CCH2OH结论:与-OH的碳原子上连接必须有H, 才发生催化氧化请你帮帮我一、乙醇交警判断驾驶员是否酒后驾车的方法 ?一、乙醇酸性高锰
酸钾溶液乙 醇酸性重铬
酸钾溶液乙 醇身边的化学 ——酒后驾车的检查原理??一、乙醇(3)被酸性KMnO4 、K2Cr2O7 溶液氧化为乙酸一、乙醇取代催化氧化结构决定性质让我们来总结一下一、乙醇乙醇乙醛乙酸CO2+H2O +热量CH3CHO知识拓展:一、乙醇切莫贪杯一、乙醇(四)、乙醇的用途乙 醇饮 料化工原料溶 剂医 药燃料一、乙醇作燃料 —— 飞机、汽车、火锅、酒精灯等作消毒剂 —— 医用酒精等一、乙醇制酒精型饮料 —— 啤酒、红酒等工业制取乙酸一、乙醇 (一)、乙醇的物理性质:
(二)、乙醇的结构:
(三)、乙醇的化学性质:
1、乙醇与活泼金属反应
2C2H5OH+2Na→2C2H5ONa+H2↑
2、乙醇的氧化反应
①燃 烧:
②催化氧化:
(四)、乙醇的用途:小结Cu一、乙醇课堂练习1、如右图所示:简述乙醇发生各种反应是键的断裂情况2、将等量的铜片在酒精灯上加热后,分别插入下列溶液中,放置片刻后铜片质量与加热前相同的是( )
A.硝酸 B. 无水乙醇 C. 石灰水 D. 盐酸B一、乙醇拓展练习2、A、B、C三种醇同足量的金属钠完全反应,在相同条件下产生相同体积的氢气,消耗这三种醇的物质的量之比为3∶6∶2,则A、B、C三种醇分子中羟基数之比是( ) A. 3∶2∶1 B. 2∶6∶3
C. 3∶1∶2 D. 2∶1∶3一、乙醇拓展练习一、乙醇二、乙酸 传说古代山西省有个酿酒高手叫杜康。他儿子黑塔跟父亲也学会了酿酒技术。后来,从山西迁到镇江。黑塔觉得酿酒后把酒糟扔掉可惜,把酒糟浸泡在水缸里。到了第二十一日的酉时,一开缸,一股浓郁的香气扑鼻而来。黑塔忍不住尝了一口,酸酸的,味道很美。烧菜时放了一些,味道特别鲜美,便贮藏着作为“调味酱”。这“调味酱”就是今天的醋。醋的来历?二、乙酸酉廿一日二、乙酸乙酸的物理性质 通过观察乙酸,阅读课本总结乙酸的物理性质(颜色、状态、气味、溶解性、熔沸点等角度分析).二、乙酸乙酸分子的结构甲基羧基—官能团分子式:结构式结构简式或C2H4O2 CH3COOH二、乙酸水垢主要成份:
Mg(OH)2和CaCO3 通过这个生活常识你能得到什么启示?二、乙酸科学探究1:根据下列提供的药品,设计 实验证明乙酸的酸性药品: 镁带、NaOH溶液 、 Na2CO3粉末、
乙酸溶液、酚酞、石蕊。二、乙酸证明乙酸的酸性的可行方案: 二、乙酸如何设计实验比较酸性强弱:CH3COOH、H2CO3酸性:CH3COOH>H2CO3[科学探究2]实验方案:
1、向一试管中加入碳酸钠粉末。
2、向试管中加入醋酸,观察现象。 二、乙酸“酒是陈的香”为什么呢?二、乙酸 厨师烧鱼时常加醋并加点酒,这样鱼的味道就变得无腥、香醇,特别鲜美。为什么呢?二、乙酸实验 3-4二、乙酸实验现象:
1、饱和Na2CO3溶液上层有透明的不
溶于水的油状液体产生。
2、闻到香味-------乙酸乙酯
二、乙酸①图中发生装置有何特点?为什么使用长导
管?导管口为什么要在溶液的液面上方?②药品的添加顺序如何?③浓硫酸的作用是什么?导管的作用:导气、冷疑不能伸到液面下(防倒吸)注意:先加乙醇再加浓H2SO4最后加乙酸催化剂、吸水剂观察与讨论二、乙酸④得到的产物是否纯净?
主要杂质有哪些?⑤为什么要用饱和的碳酸
钠溶液来吸收产品?含有乙醇、乙酸几种物质的物理性质中和乙酸、溶解乙醇,
降低乙酸乙酯在水中的溶解度观察与讨论二、乙酸酯化反应乙酸 乙醇 乙酸乙酯酯化反应的概念: 酸和醇反应生成酯和水的反应可逆反应二、乙酸可能一可能二同位素示踪法:酯化反应断键的方式:酸脱羟基、醇脱氢。 二、乙酸酯化反应的实质:酸脱羟基、醇脱氢。 乙酸甲酯二、乙酸酸性酯化结构决定性质本节课的重点:二、乙酸黄豆泡醋可以降血压 生活小帮手无“醋” 不在二、乙酸乙酸可以生产农药乙酸是重要的化工原料二、乙酸乙酸可以生产涂料乙酸是重要的化工原料二、乙酸乙酸的用途乙酸二、乙酸小 结一.乙酸的物理性质
二.乙酸的分子结构
结构简式: 特征基团:
三.乙酸的化学性质
1.乙酸的酸性:乙酸是一种一元弱酸,其酸性大于碳酸
2.乙酸的酯化反应(取代) CH3COOH—COOH(羧基)四.乙酸的用途二、乙酸1、关于乙酸的下列说法中不正确的是 ( )
A.乙酸易溶于水和乙醇
B.无水乙酸又称冰醋酸,它是纯净物
C.乙酸是一种重要的有机酸,是有刺激性气味的液体
D.乙酸分子里有四个氢原子,所以不是一元酸D请你来练练二、乙酸2、酯化反应属于( )
A.中和反应 B.不可逆反应
C.离子反应 D.取代反应D3、确定乙酸是弱酸的依据是( )
A. 乙酸可以和乙醇发生酯化反应
B. 乙酸钠的水溶液显碱性
C. 乙酸能使石蕊试液变红
D. Na2CO3中加入乙酸产生CO2B二、乙酸
