2017-2018年高中化学必修二课件元素周期律
文档属性
| 名称 | 2017-2018年高中化学必修二课件元素周期律 |

|
|
| 格式 | zip | ||
| 文件大小 | 147.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-11-20 00:00:00 | ||
图片预览







文档简介
课件65张PPT。第一章 物质结构 元素周期律
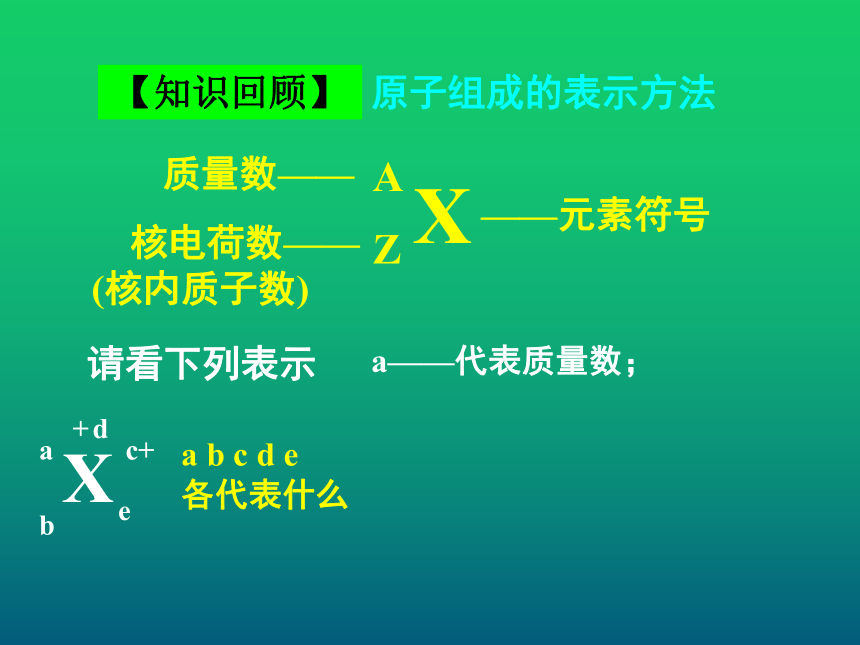
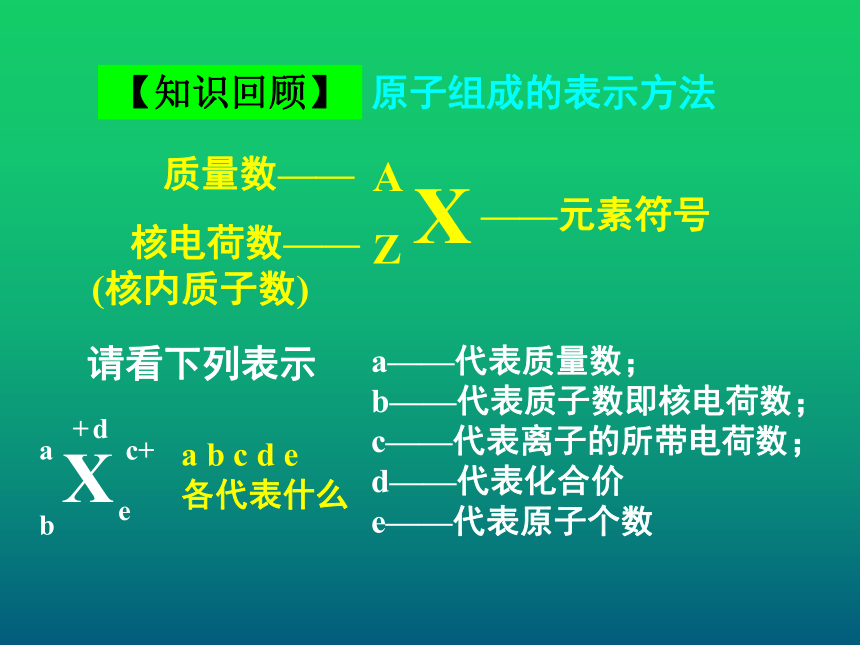
第一节 元素周期表XAZ——元素符号质量数—— 核电荷数——
(核内质子数)【知识回顾】原子组成的表示方法XAZ——元素符号质量数—— 核电荷数——
(核内质子数)请看下列表示【知识回顾】原子组成的表示方法XAZ——元素符号质量数—— 核电荷数——
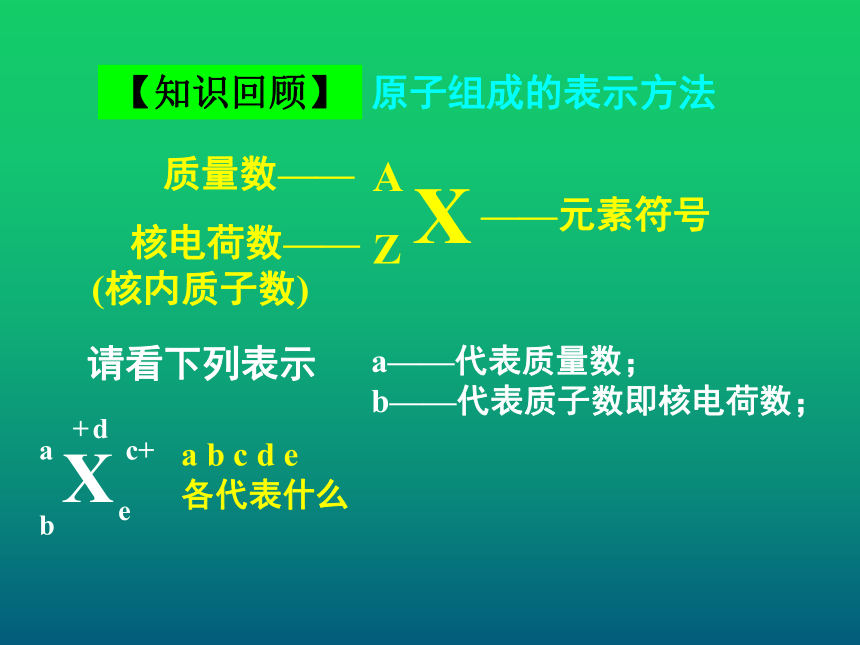
(核内质子数)a b c d e
各代表什么请看下列表示【知识回顾】原子组成的表示方法XAZ——元素符号质量数—— 核电荷数——
(核内质子数)a——代表质量数;a b c d e
各代表什么请看下列表示【知识回顾】原子组成的表示方法XAZ——元素符号质量数—— 核电荷数——
(核内质子数)a——代表质量数;
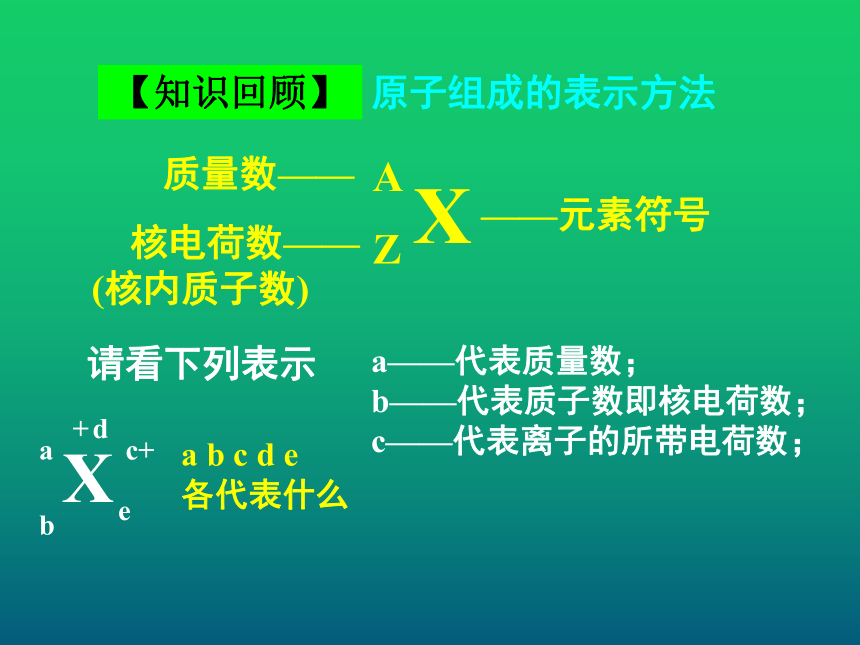
b——代表质子数即核电荷数;a b c d e 各代表什么请看下列表示【知识回顾】原子组成的表示方法XAZ——元素符号质量数—— 核电荷数—— (核内质子数)a——代表质量数;
b——代表质子数即核电荷数;
c——代表离子的所带电荷数;a b c d e 各代表什么请看下列表示【知识回顾】原子组成的表示方法XAZ——元素符号质量数—— 核电荷数—— (核内质子数)a——代表质量数;
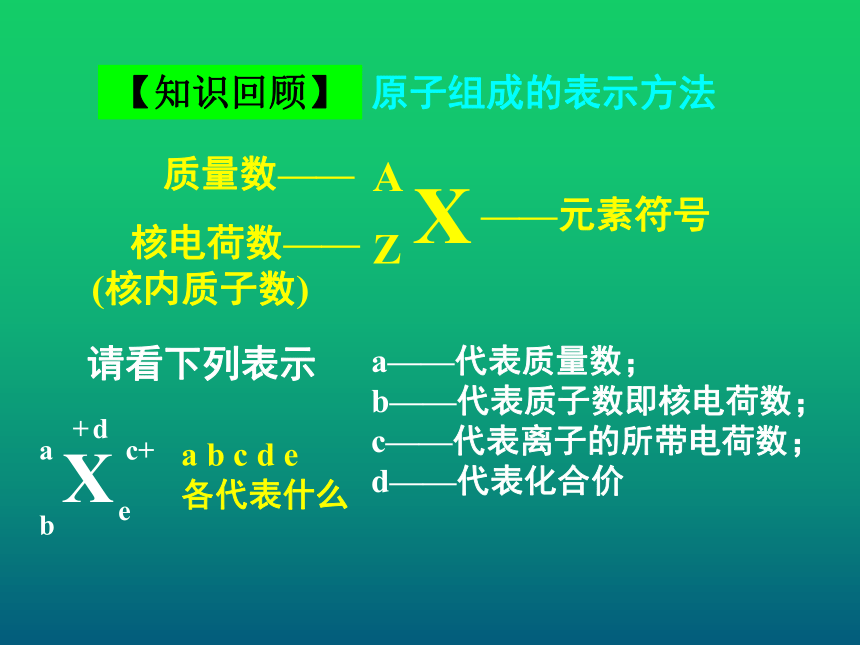
b——代表质子数即核电荷数;
c——代表离子的所带电荷数;
d——代表化合价a b c d e 各代表什么请看下列表示【知识回顾】原子组成的表示方法XAZ——元素符号质量数—— 核电荷数—— (核内质子数)a——代表质量数;
b——代表质子数即核电荷数;
c——代表离子的所带电荷数;
d——代表化合价
e——代表原子个数a b c d e 各代表什么请看下列表示【知识回顾】原子组成的表示方法(1)元素:具有相同__________的_____原子 的总称。
(2)核素:具有一定数目的_____和一定数目 的_____的_____原子。
(3)同位素:_______相同而_______不同的 同一元素的_____原子,互称同位素。元素、核素、同位素概念辨析(1)元素:具有相同__________的_____原子 的总称。
(2)核素:具有一定数目的_____和一定数目 的_____的_____原子。
(3)同位素:_______相同而_______不同的 同一元素的_____原子,互称同位素。核电荷数一类元素、核素、同位素概念辨析(1)元素:具有相同__________的_____原子 的总称。
(2)核素:具有一定数目的_____和一定数目 的_____的_____原子。
(3)同位素:_______相同而_______不同的 同一元素的_____原子,互称同位素。核电荷数一类质子中子一种元素、核素、同位素概念辨析(1)元素:具有相同__________的_____原子 的总称。
(2)核素:具有一定数目的_____和一定数目 的_____的_____原子。
(3)同位素:_______相同而_______不同的 同一元素的_____原子,互称同位素。核电荷数一类质子中子一种质子数中子数不同元素、核素、同位素概念辨析1.下列互为同位素的是( )
A.H2 D2 B.14N 14C
C.16O 17O D.金刚石 石墨【巩固练习】1.下列互为同位素的是( )
A.H2 D2 B.14N 14C
C.16O 17O D.金刚石 石墨C【巩固练习】(3)同位素的应用
(a)考古利用14C测定一些文物的年代;
(b)2H、3H用于氢弹;
(c)利用一些放射性同位素释放的射线育种 和治疗肿瘤
……3.相对原子质量1.核素的相对原子质量3.相对原子质量1.核素的相对原子质量2.元素的相对原子质量3.相对原子质量1.核素的相对原子质量核素相对原子质量:M = 某核素的实际质量 1/12×12C原子的质量2.元素的相对原子质量3.相对原子质量1.核素的相对原子质量核素相对原子质量:M = 某核素的实际质量 1/12×12C原子的质量2.元素的相对原子质量3.相对原子质量质量数等于核素的相对原子质量的近似值(取整数)1.核素的相对原子质量核素相对原子质量:M = 某核素的实际质量 1/12×12C原子的质量2.元素的相对原子质量元素的相对原子质量=核素1的相对原子质量×其原 子数目百分比+核素2的相对原子质量×其原子数目 百分比+…… 3.相对原子质量质量数等于核素的相对原子质量的近似值(取整数)1.核素的相对原子质量核素相对原子质量:M = 某核素的实际质量 1/12×12C原子的质量2.元素的相对原子质量元素的相对原子质量=核素1的相对原子质量×其原 子数目百分比+核素2的相对原子质量×其原子数目 百分比+……
M = M1(或A1)×n1%+ M2(或A2)×n2%+……3.相对原子质量质量数等于核素的相对原子质量的近似值(取整数) 例: 17Cl的相对原子质量为34.969,原子 数目百分数为75.77%,17Cl的相对原子质量为 36.966,原子数目百分数为24.23%,则氯元素 的相对原子质量是多少? 3537 例: 17Cl的相对原子质量为34.969,原子 数目百分数为75.77%,17Cl的相对原子质量为 36.966,原子数目百分数为24.23%,则氯元素 的相对原子质量是多少? 3537解:氯元素的相对原子质量 例: 17Cl的相对原子质量为34.969,原子 数目百分数为75.77%,17Cl的相对原子质量为 36.966,原子数目百分数为24.23%,则氯元素 的相对原子质量是多少? 3537解:氯元素的相对原子质量 =34.969 × 75.77% + 36.966 × 24.23% 例: 17Cl的相对原子质量为34.969,原子 数目百分数为75.77%,17Cl的相对原子质量为 36.966,原子数目百分数为24.23%,则氯元素 的相对原子质量是多少? 3537解:氯元素的相对原子质量 =34.969 × 75.77% + 36.966 × 24.23% =35.453化学 (必修②) 第一章第 1 节元素周期律—— 核素—— 原子核外电子的排布化学必修2 第一章第2节一、原子核外电子的排布 一、原子核外电子的排布 1.电子层的划分 一、原子核外电子的排布 1.电子层的划分 电子层(用n表示) 1、2、3、4…… 一、原子核外电子的排布 1.电子层的划分 电子层(用n表示) 1、2、3、4…… 电子层符号 K、L、M、N…… 一、原子核外电子的排布 1.电子层的划分 电子层(用n表示) 1、2、3、4…… 离核距离 ? 近 远电子层符号 K、L、M、N…… 一、原子核外电子的排布 1.电子层的划分 电子层(用n表示) 1、2、3、4…… 电子层符号 K、L、M、N…… 离核距离 ? 近 远能量高低? 低 高2.核外电子的排布规律 2.核外电子的排布规律 (1)各电子层最多容纳的电子数是2n2(n表 示电子层) 2.核外电子的排布规律 (1)各电子层最多容纳的电子数是2n2(n表 示电子层)
(2)最外层电子数不超过8个(K层是最外层 时,最多不超过2个);次外层电子数目不超过 18个,倒数第三层不超过32个。2.核外电子的排布规律 (1)各电子层最多容纳的电子数是2n2(n表 示电子层)
(2)最外层电子数不超过8个(K层是最外层 时,最多不超过2个);次外层电子数目不超过 18个,倒数第三层不超过32个。
(3)核外电子总是尽先排布在能量最低的电 子层,然后由里向外从能量低的电子层逐步向 能量高的电子层排布(即排满K层再排L 层,排 满L层才排M层)。 在多电子原子中,同一能层的电子,能量可以 不同,还可以把它们分成能级。能级:问题探究 根据已有知识,试写出K原子的可能电子 排布式与原子结构示意图?问题探究 根据已有知识,试写出K原子的可能电子 排布式与原子结构示意图?猜想一: 1s22s22p63s23p63d1 问题探究 根据已有知识,试写出K原子的可能电子 排布式与原子结构示意图?猜想一: 1s22s22p63s23p63d1 +192 8 9问题探究 根据已有知识,试写出K原子的可能电子 排布式与原子结构示意图?猜想一: 1s22s22p63s23p63d1 +192 8 9×问题探究 根据已有知识,试写出K原子的可能电子 排布式与原子结构示意图?猜想一: 1s22s22p63s23p63d1 +192 8 9+192 8 8 1×问题探究 根据已有知识,试写出K原子的可能电子 排布式与原子结构示意图?猜想一: 1s22s22p63s23p63d1 +192 8 9+192 8 8 1猜想二: 1s22s22p63s23p64s1 ×问题探究 根据已有知识,试写出K原子的可能电子 排布式与原子结构示意图?猜想一: 1s22s22p63s23p63d1 +192 8 9+192 8 8 1猜想二: 1s22s22p63s23p64s1 √× 构造原理与电子排布式 构造原理: 随原子核电荷数 递增,绝大多数 原子核外电子的 排布遵循如右图 的排布顺序,这 个排布顺序被称 为构造原理。 构造原理与电子排布式 构造原理: 随原子核电荷数 递增,绝大多数 原子核外电子的 排布遵循如右图 的排布顺序,这 个排布顺序被称 为构造原理。构造原理: 1s;2s 2p;3s 3p;4s 3d 4p;
规律 5s 4d 5p; 6s 4f 5d 6p;7s 5f 6d原子的简化电子排布:原子实Na的简化电子排布:原子的简化电子排布:原子实[Ne]3s1Na的简化电子排布:原子的简化电子排布:原子实[Ne]3s1上式方括号里的符号的意义是:Na的简化电子排布:原子的简化电子排布:原子实[Ne]3s1上式方括号里的符号的意义是:该元素前一个周期的惰性气体电子排布结构Na的简化电子排布:原子的简化电子排布:原子实[Ne]3s1 练习:写出第8号元素氧、第14号元素 硅和第26号元素铁的简化电子排布式吗?上式方括号里的符号的意义是:该元素前一个周期的惰性气体电子排布结构Na的简化电子排布:原子的简化电子排布:原子实[Ne]3s1 练习:写出第8号元素氧、第14号元素 硅和第26号元素铁的简化电子排布式吗?上式方括号里的符号的意义是:该元素前一个周期的惰性气体电子排布结构Na的简化电子排布:O:
Si:
Fe:原子的简化电子排布:原子实[Ne]3s1 练习:写出第8号元素氧、第14号元素 硅和第26号元素铁的简化电子排布式吗?上式方括号里的符号的意义是:该元素前一个周期的惰性气体电子排布结构Na的简化电子排布:[He]2s22p4O:
Si:
Fe:原子的简化电子排布:原子实[Ne]3s1 练习:写出第8号元素氧、第14号元素 硅和第26号元素铁的简化电子排布式吗?上式方括号里的符号的意义是:该元素前一个周期的惰性气体电子排布结构Na的简化电子排布:[He]2s22p4[Ne]3s23p2O:
Si:
Fe:原子的简化电子排布:原子实[Ne]3s1 练习:写出第8号元素氧、第14号元素 硅和第26号元素铁的简化电子排布式吗?上式方括号里的符号的意义是:该元素前一个周期的惰性气体电子排布结构Na的简化电子排布:[He]2s22p4[Ne]3s23p2[Ar]3d64s2O:
Si:
Fe:例1.用1-18号元素的原子符号回答下列问题:
(1)最外层有2个电子的是( ) (2)最外层电子数等于次外层电子数的有( )
(3)最外层电子数是次外层电子数2倍的是( )
(4)最外层电子数是最内层电子数一半的是( )
(5)电子层数与最外层电子数相等的是( )例1.用1-18号元素的原子符号回答下列问题:
(1)最外层有2个电子的是( ) (2)最外层电子数等于次外层电子数的有( )
(3)最外层电子数是次外层电子数2倍的是( )
(4)最外层电子数是最内层电子数一半的是( )
(5)电子层数与最外层电子数相等的是( )He、Be、Mg例1.用1-18号元素的原子符号回答下列问题:
(1)最外层有2个电子的是( ) (2)最外层电子数等于次外层电子数的有( )
(3)最外层电子数是次外层电子数2倍的是( )
(4)最外层电子数是最内层电子数一半的是( )
(5)电子层数与最外层电子数相等的是( )Be、ArHe、Be、Mg例1.用1-18号元素的原子符号回答下列问题:
(1)最外层有2个电子的是( ) (2)最外层电子数等于次外层电子数的有( )
(3)最外层电子数是次外层电子数2倍的是( )
(4)最外层电子数是最内层电子数一半的是( )
(5)电子层数与最外层电子数相等的是( )CBe、ArHe、Be、Mg例1.用1-18号元素的原子符号回答下列问题:
(1)最外层有2个电子的是( ) (2)最外层电子数等于次外层电子数的有( )
(3)最外层电子数是次外层电子数2倍的是( )
(4)最外层电子数是最内层电子数一半的是( )
(5)电子层数与最外层电子数相等的是( )Li、NaCBe、ArHe、Be、Mg例1.用1-18号元素的原子符号回答下列问题:
(1)最外层有2个电子的是( ) (2)最外层电子数等于次外层电子数的有( )
(3)最外层电子数是次外层电子数2倍的是( )
(4)最外层电子数是最内层电子数一半的是( )
(5)电子层数与最外层电子数相等的是( )H、Be、AlLi、NaCBe、ArHe、Be、Mg1.通常情况下,微粒A和B为分子,C和E为阳 离子,D为阴离子,它们都含有10个电子;B溶于 A后所得的物质可电离出C和D;A、B、E三种微 粒反应后可得C和一种白色沉淀。请回答:
(1)用化学符号表示下列4种微粒:
A:________;B:________;
C:________;D:________。
(2)写出A、B、E三种微粒反应的离子方程式: ___________________________________。 2.用A+、B-、C2-、D、E、F、G和H分别表 示含有18个电子八种微粒(离子或分子)。请回答:
(1)A元素是???①??、B元素是????②??????、C元素是 ????③??????(用元素符号表示)
(2)D是由两种元素组成的双原子分子,其分子 式是????④????
(3)E是所有含18个电子的微粒中氧化能力最强 的分子,其分子式是????⑤????
(4)F是由两种元素组成的三原子分子,其分子 式是????⑥????,电子式是????⑦??
(5)G分子中含有4个原子,其分子式是????⑧????
(6)H分子中含有8个原子,其分子式是????⑨????
b——代表质子数即核电荷数;a b c d e 各代表什么请看下列表示【知识回顾】原子组成的表示方法XAZ——元素符号质量数—— 核电荷数—— (核内质子数)a——代表质量数;
b——代表质子数即核电荷数;
c——代表离子的所带电荷数;a b c d e 各代表什么请看下列表示【知识回顾】原子组成的表示方法XAZ——元素符号质量数—— 核电荷数—— (核内质子数)a——代表质量数;
b——代表质子数即核电荷数;
c——代表离子的所带电荷数;
d——代表化合价a b c d e 各代表什么请看下列表示【知识回顾】原子组成的表示方法XAZ——元素符号质量数—— 核电荷数—— (核内质子数)a——代表质量数;
b——代表质子数即核电荷数;
c——代表离子的所带电荷数;
d——代表化合价
e——代表原子个数a b c d e 各代表什么请看下列表示【知识回顾】原子组成的表示方法(1)元素:具有相同__________的_____原子 的总称。
(2)核素:具有一定数目的_____和一定数目 的_____的_____原子。
(3)同位素:_______相同而_______不同的 同一元素的_____原子,互称同位素。元素、核素、同位素概念辨析(1)元素:具有相同__________的_____原子 的总称。
(2)核素:具有一定数目的_____和一定数目 的_____的_____原子。
(3)同位素:_______相同而_______不同的 同一元素的_____原子,互称同位素。核电荷数一类元素、核素、同位素概念辨析(1)元素:具有相同__________的_____原子 的总称。
(2)核素:具有一定数目的_____和一定数目 的_____的_____原子。
(3)同位素:_______相同而_______不同的 同一元素的_____原子,互称同位素。核电荷数一类质子中子一种元素、核素、同位素概念辨析(1)元素:具有相同__________的_____原子 的总称。
(2)核素:具有一定数目的_____和一定数目 的_____的_____原子。
(3)同位素:_______相同而_______不同的 同一元素的_____原子,互称同位素。核电荷数一类质子中子一种质子数中子数不同元素、核素、同位素概念辨析1.下列互为同位素的是( )
A.H2 D2 B.14N 14C
C.16O 17O D.金刚石 石墨【巩固练习】1.下列互为同位素的是( )
A.H2 D2 B.14N 14C
C.16O 17O D.金刚石 石墨C【巩固练习】(3)同位素的应用
(a)考古利用14C测定一些文物的年代;
(b)2H、3H用于氢弹;
(c)利用一些放射性同位素释放的射线育种 和治疗肿瘤
……3.相对原子质量1.核素的相对原子质量3.相对原子质量1.核素的相对原子质量2.元素的相对原子质量3.相对原子质量1.核素的相对原子质量核素相对原子质量:M = 某核素的实际质量 1/12×12C原子的质量2.元素的相对原子质量3.相对原子质量1.核素的相对原子质量核素相对原子质量:M = 某核素的实际质量 1/12×12C原子的质量2.元素的相对原子质量3.相对原子质量质量数等于核素的相对原子质量的近似值(取整数)1.核素的相对原子质量核素相对原子质量:M = 某核素的实际质量 1/12×12C原子的质量2.元素的相对原子质量元素的相对原子质量=核素1的相对原子质量×其原 子数目百分比+核素2的相对原子质量×其原子数目 百分比+…… 3.相对原子质量质量数等于核素的相对原子质量的近似值(取整数)1.核素的相对原子质量核素相对原子质量:M = 某核素的实际质量 1/12×12C原子的质量2.元素的相对原子质量元素的相对原子质量=核素1的相对原子质量×其原 子数目百分比+核素2的相对原子质量×其原子数目 百分比+……
M = M1(或A1)×n1%+ M2(或A2)×n2%+……3.相对原子质量质量数等于核素的相对原子质量的近似值(取整数) 例: 17Cl的相对原子质量为34.969,原子 数目百分数为75.77%,17Cl的相对原子质量为 36.966,原子数目百分数为24.23%,则氯元素 的相对原子质量是多少? 3537 例: 17Cl的相对原子质量为34.969,原子 数目百分数为75.77%,17Cl的相对原子质量为 36.966,原子数目百分数为24.23%,则氯元素 的相对原子质量是多少? 3537解:氯元素的相对原子质量 例: 17Cl的相对原子质量为34.969,原子 数目百分数为75.77%,17Cl的相对原子质量为 36.966,原子数目百分数为24.23%,则氯元素 的相对原子质量是多少? 3537解:氯元素的相对原子质量 =34.969 × 75.77% + 36.966 × 24.23% 例: 17Cl的相对原子质量为34.969,原子 数目百分数为75.77%,17Cl的相对原子质量为 36.966,原子数目百分数为24.23%,则氯元素 的相对原子质量是多少? 3537解:氯元素的相对原子质量 =34.969 × 75.77% + 36.966 × 24.23% =35.453化学 (必修②) 第一章第 1 节元素周期律—— 核素—— 原子核外电子的排布化学必修2 第一章第2节一、原子核外电子的排布 一、原子核外电子的排布 1.电子层的划分 一、原子核外电子的排布 1.电子层的划分 电子层(用n表示) 1、2、3、4…… 一、原子核外电子的排布 1.电子层的划分 电子层(用n表示) 1、2、3、4…… 电子层符号 K、L、M、N…… 一、原子核外电子的排布 1.电子层的划分 电子层(用n表示) 1、2、3、4…… 离核距离 ? 近 远电子层符号 K、L、M、N…… 一、原子核外电子的排布 1.电子层的划分 电子层(用n表示) 1、2、3、4…… 电子层符号 K、L、M、N…… 离核距离 ? 近 远能量高低? 低 高2.核外电子的排布规律 2.核外电子的排布规律 (1)各电子层最多容纳的电子数是2n2(n表 示电子层) 2.核外电子的排布规律 (1)各电子层最多容纳的电子数是2n2(n表 示电子层)
(2)最外层电子数不超过8个(K层是最外层 时,最多不超过2个);次外层电子数目不超过 18个,倒数第三层不超过32个。2.核外电子的排布规律 (1)各电子层最多容纳的电子数是2n2(n表 示电子层)
(2)最外层电子数不超过8个(K层是最外层 时,最多不超过2个);次外层电子数目不超过 18个,倒数第三层不超过32个。
(3)核外电子总是尽先排布在能量最低的电 子层,然后由里向外从能量低的电子层逐步向 能量高的电子层排布(即排满K层再排L 层,排 满L层才排M层)。 在多电子原子中,同一能层的电子,能量可以 不同,还可以把它们分成能级。能级:问题探究 根据已有知识,试写出K原子的可能电子 排布式与原子结构示意图?问题探究 根据已有知识,试写出K原子的可能电子 排布式与原子结构示意图?猜想一: 1s22s22p63s23p63d1 问题探究 根据已有知识,试写出K原子的可能电子 排布式与原子结构示意图?猜想一: 1s22s22p63s23p63d1 +192 8 9问题探究 根据已有知识,试写出K原子的可能电子 排布式与原子结构示意图?猜想一: 1s22s22p63s23p63d1 +192 8 9×问题探究 根据已有知识,试写出K原子的可能电子 排布式与原子结构示意图?猜想一: 1s22s22p63s23p63d1 +192 8 9+192 8 8 1×问题探究 根据已有知识,试写出K原子的可能电子 排布式与原子结构示意图?猜想一: 1s22s22p63s23p63d1 +192 8 9+192 8 8 1猜想二: 1s22s22p63s23p64s1 ×问题探究 根据已有知识,试写出K原子的可能电子 排布式与原子结构示意图?猜想一: 1s22s22p63s23p63d1 +192 8 9+192 8 8 1猜想二: 1s22s22p63s23p64s1 √× 构造原理与电子排布式 构造原理: 随原子核电荷数 递增,绝大多数 原子核外电子的 排布遵循如右图 的排布顺序,这 个排布顺序被称 为构造原理。 构造原理与电子排布式 构造原理: 随原子核电荷数 递增,绝大多数 原子核外电子的 排布遵循如右图 的排布顺序,这 个排布顺序被称 为构造原理。构造原理: 1s;2s 2p;3s 3p;4s 3d 4p;
规律 5s 4d 5p; 6s 4f 5d 6p;7s 5f 6d原子的简化电子排布:原子实Na的简化电子排布:原子的简化电子排布:原子实[Ne]3s1Na的简化电子排布:原子的简化电子排布:原子实[Ne]3s1上式方括号里的符号的意义是:Na的简化电子排布:原子的简化电子排布:原子实[Ne]3s1上式方括号里的符号的意义是:该元素前一个周期的惰性气体电子排布结构Na的简化电子排布:原子的简化电子排布:原子实[Ne]3s1 练习:写出第8号元素氧、第14号元素 硅和第26号元素铁的简化电子排布式吗?上式方括号里的符号的意义是:该元素前一个周期的惰性气体电子排布结构Na的简化电子排布:原子的简化电子排布:原子实[Ne]3s1 练习:写出第8号元素氧、第14号元素 硅和第26号元素铁的简化电子排布式吗?上式方括号里的符号的意义是:该元素前一个周期的惰性气体电子排布结构Na的简化电子排布:O:
Si:
Fe:原子的简化电子排布:原子实[Ne]3s1 练习:写出第8号元素氧、第14号元素 硅和第26号元素铁的简化电子排布式吗?上式方括号里的符号的意义是:该元素前一个周期的惰性气体电子排布结构Na的简化电子排布:[He]2s22p4O:
Si:
Fe:原子的简化电子排布:原子实[Ne]3s1 练习:写出第8号元素氧、第14号元素 硅和第26号元素铁的简化电子排布式吗?上式方括号里的符号的意义是:该元素前一个周期的惰性气体电子排布结构Na的简化电子排布:[He]2s22p4[Ne]3s23p2O:
Si:
Fe:原子的简化电子排布:原子实[Ne]3s1 练习:写出第8号元素氧、第14号元素 硅和第26号元素铁的简化电子排布式吗?上式方括号里的符号的意义是:该元素前一个周期的惰性气体电子排布结构Na的简化电子排布:[He]2s22p4[Ne]3s23p2[Ar]3d64s2O:
Si:
Fe:例1.用1-18号元素的原子符号回答下列问题:
(1)最外层有2个电子的是( ) (2)最外层电子数等于次外层电子数的有( )
(3)最外层电子数是次外层电子数2倍的是( )
(4)最外层电子数是最内层电子数一半的是( )
(5)电子层数与最外层电子数相等的是( )例1.用1-18号元素的原子符号回答下列问题:
(1)最外层有2个电子的是( ) (2)最外层电子数等于次外层电子数的有( )
(3)最外层电子数是次外层电子数2倍的是( )
(4)最外层电子数是最内层电子数一半的是( )
(5)电子层数与最外层电子数相等的是( )He、Be、Mg例1.用1-18号元素的原子符号回答下列问题:
(1)最外层有2个电子的是( ) (2)最外层电子数等于次外层电子数的有( )
(3)最外层电子数是次外层电子数2倍的是( )
(4)最外层电子数是最内层电子数一半的是( )
(5)电子层数与最外层电子数相等的是( )Be、ArHe、Be、Mg例1.用1-18号元素的原子符号回答下列问题:
(1)最外层有2个电子的是( ) (2)最外层电子数等于次外层电子数的有( )
(3)最外层电子数是次外层电子数2倍的是( )
(4)最外层电子数是最内层电子数一半的是( )
(5)电子层数与最外层电子数相等的是( )CBe、ArHe、Be、Mg例1.用1-18号元素的原子符号回答下列问题:
(1)最外层有2个电子的是( ) (2)最外层电子数等于次外层电子数的有( )
(3)最外层电子数是次外层电子数2倍的是( )
(4)最外层电子数是最内层电子数一半的是( )
(5)电子层数与最外层电子数相等的是( )Li、NaCBe、ArHe、Be、Mg例1.用1-18号元素的原子符号回答下列问题:
(1)最外层有2个电子的是( ) (2)最外层电子数等于次外层电子数的有( )
(3)最外层电子数是次外层电子数2倍的是( )
(4)最外层电子数是最内层电子数一半的是( )
(5)电子层数与最外层电子数相等的是( )H、Be、AlLi、NaCBe、ArHe、Be、Mg1.通常情况下,微粒A和B为分子,C和E为阳 离子,D为阴离子,它们都含有10个电子;B溶于 A后所得的物质可电离出C和D;A、B、E三种微 粒反应后可得C和一种白色沉淀。请回答:
(1)用化学符号表示下列4种微粒:
A:________;B:________;
C:________;D:________。
(2)写出A、B、E三种微粒反应的离子方程式: ___________________________________。 2.用A+、B-、C2-、D、E、F、G和H分别表 示含有18个电子八种微粒(离子或分子)。请回答:
(1)A元素是???①??、B元素是????②??????、C元素是 ????③??????(用元素符号表示)
(2)D是由两种元素组成的双原子分子,其分子 式是????④????
(3)E是所有含18个电子的微粒中氧化能力最强 的分子,其分子式是????⑤????
(4)F是由两种元素组成的三原子分子,其分子 式是????⑥????,电子式是????⑦??
(5)G分子中含有4个原子,其分子式是????⑧????
(6)H分子中含有8个原子,其分子式是????⑨????
