2.2《重要的酸》练习(课时3)
图片预览




文档简介
21世纪教育网 –中小学教育资源及组卷应用平台
《重要的酸》练习
1、 选择题
1、下列方案不可行的是( )
A、用氢氧化钠干燥二氧化碳气体 B、用稀硫酸除去炭粉中的氧化铜
C、用硝酸钡溶液区别硫酸和盐酸 D、用稀盐酸和大理石制取二氧化碳
2、下列各组离子反应可用H++OH-=H2O表示的是( )
A、氢氧化钡和硫酸
B、氢氧化铜和盐酸
C、盐酸和氢氧化钠
D、硫酸和氢氧化镁
3、下列各组物质,相互不能发生反应的是( )
A、氢氧化钠溶液和硫酸
B、氧化铜和盐酸
C、二氧化碳和氢氧化钠溶液
D、硫酸和二氧化碳
4、在A+B→盐+水的反应中,A、B分別是( )
A、纯碱和熟石灰
B、小苏打和盐酸
C、硫酸和熟石灰
D、熟石灰和氯化铵
5、下列各组溶液,相互能发生反应的是( )
①碳酸钠和氯化钙 ②氢氧化 ( http: / / www.21cnjy.com )钾和盐酸 ③硫酸和氯化钠 ⑤碳酸钾和硝酸 ⑤硫酸铜和氯化铵www.21-cn-jy.com
A、①②④
B、②④⑤
C、③④⑤
D、①②③
6、下列各组物质中,能相互反应且反应前后溶液总质量随时间变化符合如图所示的是( )
( http: / / www.21cnjy.com / )
A、铁和硝酸银溶液
B、硫酸和烧碱溶液
C、氧化铜和盐酸
D、硝酸钾溶液和稀硫酸
7、关于硫酸和盐酸,下列说法不正确的是( )
A、其浓溶液露置在空气中一段时间,质量分数都会减小
B、其稀溶液都能使紫色石蕊试液变红色
C、其稀溶液都可用于除去钢铁制品表面的铁锈
D、都能与Ba(NO3)2溶液反应生成白色沉淀
序号 甲 乙
① 铜、锌的混合物 稀
② 生锈的铁钉 稀
③ 稀的混合溶液 氯化钡溶液
④ 硫酸和硫酸铜的混合溶液 氢氧化钠溶液
8、向表中的甲物质中逐滴加入相应的乙溶液至过量,反应过程中生成的气体或沉淀的质量与加入乙的质量关系用如图所示曲线表示的是()21教育网
( http: / / www.21cnjy.com / )
A、①③
B、①④
C、②③
D、②④
二、非选择题
9、硫酸和盐酸既是实验室常用的试剂,也是重要的化工原料.它们既有相似之处,又有不同之处
(1)它们的水溶液的pH都 7 (填“大于”、“小于”、“等于”).
(2)它们都能除去铁锈,写出盐酸与铁锈主要成分反应的化学方程式:
(3)打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶敞口放置,瓶口出现白雾的是
(4)请写出把硫酸转变为盐酸的化学方程式
10、硫酸和盐酸既是实验室常用的试剂,也是重要的化工原料.
(1)从组成上看,两者的不同点是
(2)打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶,瓶口出现白雾的是
(3)只用一种试剂,鉴别两瓶失去标签的稀盐酸和稀硫酸溶液,你选用的试剂是
(4)用熟石灰中和一定量的稀盐酸时,溶液的 ( http: / / www.21cnjy.com )pH与加入的熟石灰质量的关系如图所示,若改用n克熟石灰去中和相同质量和质量分数的稀硫酸,所得溶液的pH 7(选填“>”、“<”或“=”). 21世纪教育网版权所有
11、 在一次学生分组实验之后,小红同学利 ( http: / / www.21cnjy.com )用课外活动时间来到实验室帮助老师整理实验药品.在一个实验台前,小红发现实验台上散乱地摆放着下列药品2·1·c·n·j·y
( http: / / www.21cnjy.com / )
(1)小红发现有两瓶盛有无 ( http: / / www.21cnjy.com )色溶液的试剂瓶④⑦,标签已经脱落,分别是硫酸和盐酸.请你帮助他设计一个小实验来鉴别两瓶试剂.(写出实验方法和判断依据)
(2)小红将脱落的标签贴上后,他按氧化物、酸、碱、盐的顺序将七种药品分类摆放,请根据他的分类的情况用序号填空:氧化物 .
(3)小红从上面七种药品选择两种,他准备做一个中和反应的实验.他在做中和反应实验时为了便于观察反应是否发生,他在所取的少量溶液中加入几滴酚酞试液,试液变红,当他向所取的溶液中再滴加酸时,观察到红色变成无色.根据实验现象写出一个中和反应的化学方程式.
(4)小红还发现试剂瓶①没有盖上瓶塞,一直敞口放置着.他猜想可能有一部分生石灰已变质生成了碳酸钙.为确认这一猜想,小红称取了10g样品(假设样品中只含有生石灰和碳酸钙,且混合均匀),加入过量稀盐酸60g,至样品不再有气体放出为止,称量反应残余物质质量为69.56g.他根据有关的数据确认了生石灰发生了变质及变质的程度,请你计算此瓶生石灰的纯度.【来源:21·世纪·教育·网】
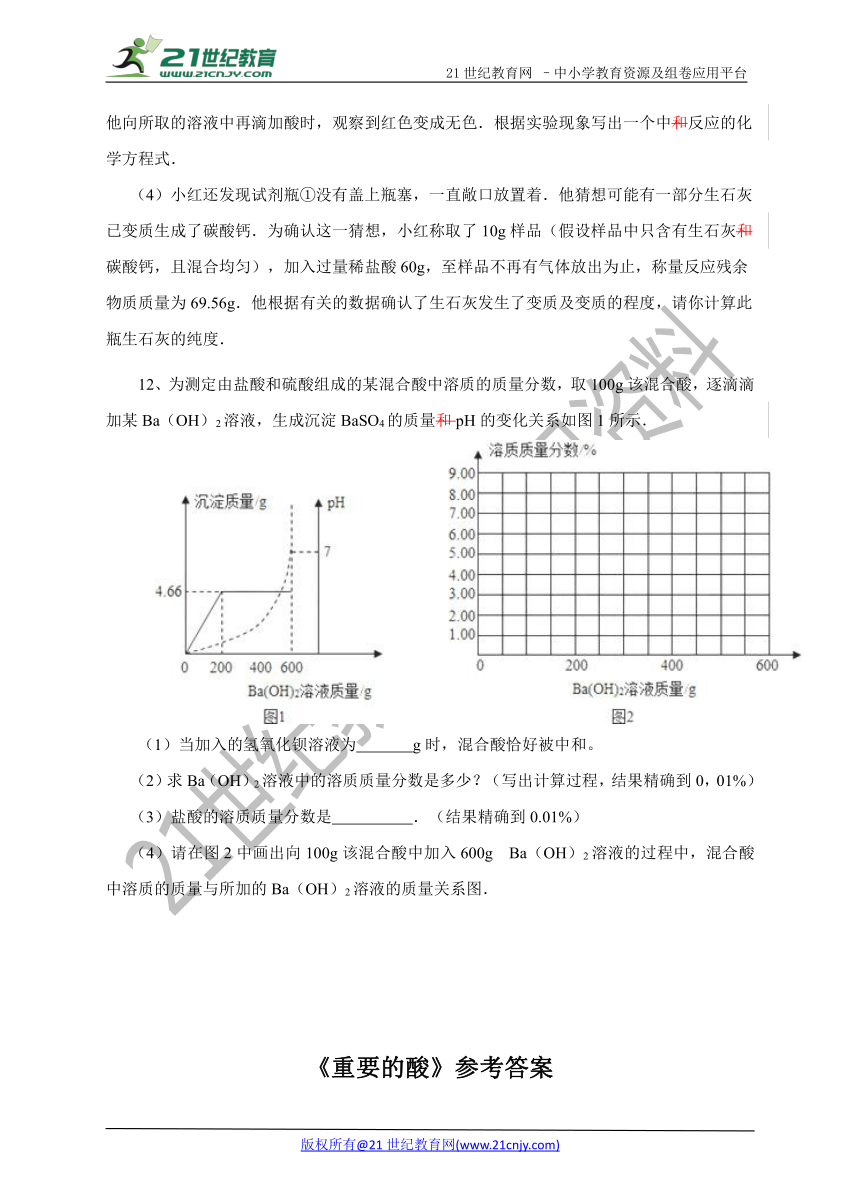
12、为测定由盐酸和硫酸组成的某混合酸 ( http: / / www.21cnjy.com )中溶质的质量分数,取100g该混合酸,逐滴滴加某Ba(OH)2溶液,生成沉淀BaSO4的质量和pH的变化关系如图1所示.
( http: / / www.21cnjy.com / )(1)当加入的氢氧化钡溶液为 g时,混合酸恰好被中和。
(2)求Ba(OH)2溶液中的溶质质量分数是多少?(写出计算过程,结果精确到0,01%)
(3)盐酸的溶质质量分数是 .(结果精确到0.01%)
(4)请在图2中画出向100g该混 ( http: / / www.21cnjy.com )合酸中加入600g Ba(OH)2溶液的过程中,混合酸中溶质的质量与所加的Ba(OH)2溶液的质量关系图.21·世纪*教育网
《重要的酸》参考答案
1、【答案】A
【解析】解:A、二氧化碳能和氢氧化 ( http: / / www.21cnjy.com )钠反应生成碳酸钠和水,所以不能用氢氧化钠干燥二氧化碳气体,故A错误;B、硫酸和氧化铜反应生成可溶性的硫酸铜和水,而硫酸和炭粉不反应,所以可用稀硫酸除去炭粉中的氧化铜,故B正确;C、硝酸钡溶液能和硫酸反应生成硫酸钡沉淀和硝酸,而硝酸钡溶液不和盐酸反应,所以可用硝酸钡溶液区别硫酸和盐酸,故C正确;D、稀盐酸和大理石反应生成氯化钙、水和二氧化碳,所以可用稀盐酸和大理石制取二氧化碳,故D正确.
故选:A.www-2-1-cnjy-com
2、【答案】D
【解析】A.氨水为弱碱,一水合氨按不能拆开, ( http: / / www.21cnjy.com )该反应的离子方程式为:H++NH3 H2O=NH4++H2O,不能用离子方程式 H++OH-=H2O 表示,故A错误;B.醋酸为弱酸,离子方程式中不能拆开,该反应的离子方程式为:CH3COOH+OH-=CH3COO-+H2O,不能用离子方程式 H++OH-=H2O 表示,故B错误;C.硫酸和氢氧化钡溶液反应生成硫酸钡沉淀和水,该反应的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,不能用离子方程式 H++OH-=H2O 表示,故C错误;D.石灰水中的氢氧化钙在离子方程式中需要拆开,该反应可以用离子方程式 H++OH-=H2O表示,故D正确;
故选D2-1-c-n-j-y
3、【答案】D
【解析】A、氢氧化钠溶液和 ( http: / / www.21cnjy.com )硫酸反应后有水生成,故能反应,故此选项错误.B、碱性氧化物能与酸反应,氧化铜是碱性氧化物,故此选项错误.C、酸性氧化物能与碱反应,二氧化碳是酸性氧化物,故此选项错误.D、酸性氧化物不能与酸反应,二氧化碳是酸性氧化物,故此选项正确.
故选D21*cnjy*com
4、【答案】C
【解析】A、纯碱和熟石灰 ( http: / / www.21cnjy.com )反应生成碳酸钙沉淀和氢氧化钠,生成物是盐和碱,故选项错误.B、小苏打和盐酸反应生成氯化钠、水和二氧化碳,生成物是盐、水和二氧化碳,故选项错误.C、硫酸和熟石灰发生中和反应生成硫酸钙和水,生成物是盐和水,故选项正确.D、熟石灰和氯化铵反应生成氯化钙、氨气和水,生成物是盐、水和氨气,故选项错误.
故选:C.
5、【答案】A
【解析】①碳酸钠和氯化钙反应生成碳酸钙 ( http: / / www.21cnjy.com )沉淀和氯化钠,有沉淀生成;②氢氧化钾和盐酸生成水和氯化钾,有水生成;④碳酸钾和硝酸反应生成二氧化碳气体和硝酸钾和水,有气体和水生成,所以①②④能发生反应.而③硫酸和氯化钠、⑤硫酸铜和氯化铵交换成分后没有水、气体、沉淀生成,故不能反应.【来源:21cnj*y.co*m】
故选:A.
6、【答案】A
【解析】A、铁和硝酸银溶液反应生成物是 ( http: / / www.21cnjy.com )银和硝酸亚铁,进入溶液中的是铁相对原子质量为56,置换出来的是银的相对原子质量为108,则进入的少,出来得多,所以溶液质量减少了,故正确;B、硫酸和烧碱溶液生产硫酸钠和水,溶液质量不变,故错误;C、氧化铜固体和盐酸反应生成氯化铁和水,溶液质量增加,故错误;D、硝酸钾溶液和稀硫酸不反应,溶液质量不变,故错误;【版权所有:21教育】
故选:A.
7、【答案】D
【解析】解:A、浓盐酸易挥发,其浓 ( http: / / www.21cnjy.com )溶液露置在空气中一段时间,质量分数减小;浓硫酸能够吸收空气中的水,其浓溶液露置在空气中一段时间,质量分数减小.正确.B、稀盐酸、稀硫酸显酸性,都能够使紫色石蕊试液变红色.正确.C、稀盐酸能和铁锈中的氧化铁反应生成氯化铁和水,稀硫酸能和铁锈中的氧化铁反应生成硫酸铁和水,所以其稀溶液都可用于除去钢铁制品表面的铁锈.正确.D、硝酸钡能和稀硫酸反应生成硫酸钡沉淀和硝酸,而稀盐酸不能和硝酸钡反应.不正确.21教育名师原创作品
故选:D.
8、【答案】D
【解析】:①铜锌合金和稀硫酸混合时,根据 ( http: / / www.21cnjy.com )金属的活动性规律,其中锌和稀硫酸反应,生成物中一开始一定就有氢气生成,与第二个图中给予的气体,加入一定量的稀盐酸后有气体产生不符;②生铁的铁钉,与稀盐酸混合时,首先稀盐酸和铁锈反应,过一会多余的稀盐酸才和铁反应生成氢气,所以符合图示的信息;③盐酸和稀硫酸混合物,与氯化钡溶液混合时,一开始就有硫酸钡沉淀生成,同样与第二个图中的信息加一会氯化钡溶液才生成不符;④氢氧化钠和硫酸铜反应产生的氢氧化铜沉淀,能和硫酸反应生成硫酸铜和水,所以开始没有沉淀出现,当硫酸消耗完后才出现沉淀,符合图中信息,所以只有②④符合图中给予的信息.21cnjy.com
故选:D.
9、
( http: / / www.21cnjy.com / )
【解析】(1)酸的水溶液显酸性,pH ( http: / / www.21cnjy.com )值小于7;
(2)盐酸、硫酸都可与氧化铁反应,分别生成氯化铁和硫酸铁溶液,所以会观察到铁锈逐渐消失,溶液显黄色,盐酸与铁锈反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O;(3)浓盐酸易挥发出氯化氢气体,氯化氢气体极易溶于水,会与空气中的水蒸气结合形成盐酸小液滴,故打开瓶塞会看到有白雾产生,而浓硫酸没有挥发性,没有白雾生成;
(4)依据复分解反应的发生条件可知硫酸转变为盐酸可以是硫酸与氯化钡的反应,其化学方程式为:BaCl2+H2SO4═BaSO4↓+2HCl;21*cnjy*com
10、
( http: / / www.21cnjy.com / )【解析】(1)硫酸和盐酸都属于酸,两者的不同主要是酸根的不同;(2)由于浓盐酸具有强烈的挥发性而浓硫酸没有,所以打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶,瓶口出现白雾的是浓盐酸;(3)硫酸溶液能与硝酸钡等含有钡离子的溶液反应生成硫酸钡白色沉淀,而盐酸不能,因此可以选择硝酸钡(或氯化钡或氢氧化钡)鉴别;(4)Ca(OH)2+2HCl=CaCl2+2H20; Ca(OH)2+H2SO4=CaSO4 +2H2O可知,氢氧化钙和盐酸反应的质量比是74:73.,而和硫酸反应的质量比为74:98,等质量的氢氧化钙需用的硫酸多,因此硫酸不够把氢氧化钙反应完,剩氢氧化钙,溶液显碱性,pH大于7.
11、【答案】(1)分别向④⑦两种溶液分别加硝酸钡溶液[或BaCl2溶液],有沉淀生成的为稀硫酸,无沉淀生成的为稀盐酸;
(2)①③
(3)HCl+NaOH=NaCl+H2O(或H2SO4+2NaOH=Na2SO4+2H2O);
(4)90%
【解析】(1)鉴别盐酸和硫酸可采取滴加 ( http: / / www.21cnjy.com )硝酸钡或氯化钡溶液观察是否产生沉淀的方法,生成白色沉淀的为硫酸,盐酸与硝酸钡或氯化钡溶液不发生反应,因而无明显现象;(2)由两种元素组成且含氧元素的物质为氧化物,生石灰为氧化钙的俗称,由钙、氧两种元素组成,CuO为铜和氧元素组成,所以生石灰和CuO都属于氧化物;(3)酸与碱生成盐和水的反应称为中和反应,烧碱为氢氧化钠的俗称属于碱,硫酸、盐酸都属于酸,所以,可选择氢氧化钠与硫酸或盐酸反应,与硫酸反应生成硫酸钠和水,与盐酸反应生成氯化钠和水;(4)反应放出二氧化碳气体质量=10g+60g-69.56g=0.44g
设放出0.44gCO2时参加反应的碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 41
X 0.44
( http: / / www.21cnjy.com / )
x=1g
则此瓶生石灰的纯度=×100%=90%
12、【答案】(1)600g
(2)1.71%
(3)2.92%
(4)
( http: / / www.21cnjy.com / )
【解析】:
( http: / / www.21cnjy.com / );
(2)由图示可知,生成沉淀的最 ( http: / / www.21cnjy.com )大量为4.66g,
设恰好完全反应时,消耗Ba(OH)2的质量为x,
Ba(OH)2+H2SO4=BaSO4↓+2H2O【出处:21教育名师】
171 233
x 4.66
=
x=3.42g
Ba(OH)2溶液的溶质质量分数是:×100%=1.71%;
(3)设盐酸的溶质质量分数是y,生成氯化钡质量为z
Ba(OH)2+2HCl=BaCl2+2H2O21·cn·jy·com
171 73 208
400g×1.71% y×100g z
( http: / / www.21cnjy.com / )
y=2.92%; z=8.32g
(4)通过上面的反应原理可知氢氧化钡和硫酸 ( http: / / www.21cnjy.com )反应生成硫酸钡沉淀和水,开始不会生成溶质,盐酸和氢氧化钡反应生成氯化钡和水,溶质质量不断增加,然后不变,所以
( http: / / www.21cnjy.com / )
( http: / / www.21cnjy.com / )
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://www.21cnjy.com/" 版权所有@21世纪教育网(www.21cnjy.com)
《重要的酸》练习
1、 选择题
1、下列方案不可行的是( )
A、用氢氧化钠干燥二氧化碳气体 B、用稀硫酸除去炭粉中的氧化铜
C、用硝酸钡溶液区别硫酸和盐酸 D、用稀盐酸和大理石制取二氧化碳
2、下列各组离子反应可用H++OH-=H2O表示的是( )
A、氢氧化钡和硫酸
B、氢氧化铜和盐酸
C、盐酸和氢氧化钠
D、硫酸和氢氧化镁
3、下列各组物质,相互不能发生反应的是( )
A、氢氧化钠溶液和硫酸
B、氧化铜和盐酸
C、二氧化碳和氢氧化钠溶液
D、硫酸和二氧化碳
4、在A+B→盐+水的反应中,A、B分別是( )
A、纯碱和熟石灰
B、小苏打和盐酸
C、硫酸和熟石灰
D、熟石灰和氯化铵
5、下列各组溶液,相互能发生反应的是( )
①碳酸钠和氯化钙 ②氢氧化 ( http: / / www.21cnjy.com )钾和盐酸 ③硫酸和氯化钠 ⑤碳酸钾和硝酸 ⑤硫酸铜和氯化铵www.21-cn-jy.com
A、①②④
B、②④⑤
C、③④⑤
D、①②③
6、下列各组物质中,能相互反应且反应前后溶液总质量随时间变化符合如图所示的是( )
( http: / / www.21cnjy.com / )
A、铁和硝酸银溶液
B、硫酸和烧碱溶液
C、氧化铜和盐酸
D、硝酸钾溶液和稀硫酸
7、关于硫酸和盐酸,下列说法不正确的是( )
A、其浓溶液露置在空气中一段时间,质量分数都会减小
B、其稀溶液都能使紫色石蕊试液变红色
C、其稀溶液都可用于除去钢铁制品表面的铁锈
D、都能与Ba(NO3)2溶液反应生成白色沉淀
序号 甲 乙
① 铜、锌的混合物 稀
② 生锈的铁钉 稀
③ 稀的混合溶液 氯化钡溶液
④ 硫酸和硫酸铜的混合溶液 氢氧化钠溶液
8、向表中的甲物质中逐滴加入相应的乙溶液至过量,反应过程中生成的气体或沉淀的质量与加入乙的质量关系用如图所示曲线表示的是()21教育网
( http: / / www.21cnjy.com / )
A、①③
B、①④
C、②③
D、②④
二、非选择题
9、硫酸和盐酸既是实验室常用的试剂,也是重要的化工原料.它们既有相似之处,又有不同之处
(1)它们的水溶液的pH都 7 (填“大于”、“小于”、“等于”).
(2)它们都能除去铁锈,写出盐酸与铁锈主要成分反应的化学方程式:
(3)打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶敞口放置,瓶口出现白雾的是
(4)请写出把硫酸转变为盐酸的化学方程式
10、硫酸和盐酸既是实验室常用的试剂,也是重要的化工原料.
(1)从组成上看,两者的不同点是
(2)打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶,瓶口出现白雾的是
(3)只用一种试剂,鉴别两瓶失去标签的稀盐酸和稀硫酸溶液,你选用的试剂是
(4)用熟石灰中和一定量的稀盐酸时,溶液的 ( http: / / www.21cnjy.com )pH与加入的熟石灰质量的关系如图所示,若改用n克熟石灰去中和相同质量和质量分数的稀硫酸,所得溶液的pH 7(选填“>”、“<”或“=”). 21世纪教育网版权所有
11、 在一次学生分组实验之后,小红同学利 ( http: / / www.21cnjy.com )用课外活动时间来到实验室帮助老师整理实验药品.在一个实验台前,小红发现实验台上散乱地摆放着下列药品2·1·c·n·j·y
( http: / / www.21cnjy.com / )
(1)小红发现有两瓶盛有无 ( http: / / www.21cnjy.com )色溶液的试剂瓶④⑦,标签已经脱落,分别是硫酸和盐酸.请你帮助他设计一个小实验来鉴别两瓶试剂.(写出实验方法和判断依据)
(2)小红将脱落的标签贴上后,他按氧化物、酸、碱、盐的顺序将七种药品分类摆放,请根据他的分类的情况用序号填空:氧化物 .
(3)小红从上面七种药品选择两种,他准备做一个中和反应的实验.他在做中和反应实验时为了便于观察反应是否发生,他在所取的少量溶液中加入几滴酚酞试液,试液变红,当他向所取的溶液中再滴加酸时,观察到红色变成无色.根据实验现象写出一个中和反应的化学方程式.
(4)小红还发现试剂瓶①没有盖上瓶塞,一直敞口放置着.他猜想可能有一部分生石灰已变质生成了碳酸钙.为确认这一猜想,小红称取了10g样品(假设样品中只含有生石灰和碳酸钙,且混合均匀),加入过量稀盐酸60g,至样品不再有气体放出为止,称量反应残余物质质量为69.56g.他根据有关的数据确认了生石灰发生了变质及变质的程度,请你计算此瓶生石灰的纯度.【来源:21·世纪·教育·网】
12、为测定由盐酸和硫酸组成的某混合酸 ( http: / / www.21cnjy.com )中溶质的质量分数,取100g该混合酸,逐滴滴加某Ba(OH)2溶液,生成沉淀BaSO4的质量和pH的变化关系如图1所示.
( http: / / www.21cnjy.com / )(1)当加入的氢氧化钡溶液为 g时,混合酸恰好被中和。
(2)求Ba(OH)2溶液中的溶质质量分数是多少?(写出计算过程,结果精确到0,01%)
(3)盐酸的溶质质量分数是 .(结果精确到0.01%)
(4)请在图2中画出向100g该混 ( http: / / www.21cnjy.com )合酸中加入600g Ba(OH)2溶液的过程中,混合酸中溶质的质量与所加的Ba(OH)2溶液的质量关系图.21·世纪*教育网
《重要的酸》参考答案
1、【答案】A
【解析】解:A、二氧化碳能和氢氧化 ( http: / / www.21cnjy.com )钠反应生成碳酸钠和水,所以不能用氢氧化钠干燥二氧化碳气体,故A错误;B、硫酸和氧化铜反应生成可溶性的硫酸铜和水,而硫酸和炭粉不反应,所以可用稀硫酸除去炭粉中的氧化铜,故B正确;C、硝酸钡溶液能和硫酸反应生成硫酸钡沉淀和硝酸,而硝酸钡溶液不和盐酸反应,所以可用硝酸钡溶液区别硫酸和盐酸,故C正确;D、稀盐酸和大理石反应生成氯化钙、水和二氧化碳,所以可用稀盐酸和大理石制取二氧化碳,故D正确.
故选:A.www-2-1-cnjy-com
2、【答案】D
【解析】A.氨水为弱碱,一水合氨按不能拆开, ( http: / / www.21cnjy.com )该反应的离子方程式为:H++NH3 H2O=NH4++H2O,不能用离子方程式 H++OH-=H2O 表示,故A错误;B.醋酸为弱酸,离子方程式中不能拆开,该反应的离子方程式为:CH3COOH+OH-=CH3COO-+H2O,不能用离子方程式 H++OH-=H2O 表示,故B错误;C.硫酸和氢氧化钡溶液反应生成硫酸钡沉淀和水,该反应的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,不能用离子方程式 H++OH-=H2O 表示,故C错误;D.石灰水中的氢氧化钙在离子方程式中需要拆开,该反应可以用离子方程式 H++OH-=H2O表示,故D正确;
故选D2-1-c-n-j-y
3、【答案】D
【解析】A、氢氧化钠溶液和 ( http: / / www.21cnjy.com )硫酸反应后有水生成,故能反应,故此选项错误.B、碱性氧化物能与酸反应,氧化铜是碱性氧化物,故此选项错误.C、酸性氧化物能与碱反应,二氧化碳是酸性氧化物,故此选项错误.D、酸性氧化物不能与酸反应,二氧化碳是酸性氧化物,故此选项正确.
故选D21*cnjy*com
4、【答案】C
【解析】A、纯碱和熟石灰 ( http: / / www.21cnjy.com )反应生成碳酸钙沉淀和氢氧化钠,生成物是盐和碱,故选项错误.B、小苏打和盐酸反应生成氯化钠、水和二氧化碳,生成物是盐、水和二氧化碳,故选项错误.C、硫酸和熟石灰发生中和反应生成硫酸钙和水,生成物是盐和水,故选项正确.D、熟石灰和氯化铵反应生成氯化钙、氨气和水,生成物是盐、水和氨气,故选项错误.
故选:C.
5、【答案】A
【解析】①碳酸钠和氯化钙反应生成碳酸钙 ( http: / / www.21cnjy.com )沉淀和氯化钠,有沉淀生成;②氢氧化钾和盐酸生成水和氯化钾,有水生成;④碳酸钾和硝酸反应生成二氧化碳气体和硝酸钾和水,有气体和水生成,所以①②④能发生反应.而③硫酸和氯化钠、⑤硫酸铜和氯化铵交换成分后没有水、气体、沉淀生成,故不能反应.【来源:21cnj*y.co*m】
故选:A.
6、【答案】A
【解析】A、铁和硝酸银溶液反应生成物是 ( http: / / www.21cnjy.com )银和硝酸亚铁,进入溶液中的是铁相对原子质量为56,置换出来的是银的相对原子质量为108,则进入的少,出来得多,所以溶液质量减少了,故正确;B、硫酸和烧碱溶液生产硫酸钠和水,溶液质量不变,故错误;C、氧化铜固体和盐酸反应生成氯化铁和水,溶液质量增加,故错误;D、硝酸钾溶液和稀硫酸不反应,溶液质量不变,故错误;【版权所有:21教育】
故选:A.
7、【答案】D
【解析】解:A、浓盐酸易挥发,其浓 ( http: / / www.21cnjy.com )溶液露置在空气中一段时间,质量分数减小;浓硫酸能够吸收空气中的水,其浓溶液露置在空气中一段时间,质量分数减小.正确.B、稀盐酸、稀硫酸显酸性,都能够使紫色石蕊试液变红色.正确.C、稀盐酸能和铁锈中的氧化铁反应生成氯化铁和水,稀硫酸能和铁锈中的氧化铁反应生成硫酸铁和水,所以其稀溶液都可用于除去钢铁制品表面的铁锈.正确.D、硝酸钡能和稀硫酸反应生成硫酸钡沉淀和硝酸,而稀盐酸不能和硝酸钡反应.不正确.21教育名师原创作品
故选:D.
8、【答案】D
【解析】:①铜锌合金和稀硫酸混合时,根据 ( http: / / www.21cnjy.com )金属的活动性规律,其中锌和稀硫酸反应,生成物中一开始一定就有氢气生成,与第二个图中给予的气体,加入一定量的稀盐酸后有气体产生不符;②生铁的铁钉,与稀盐酸混合时,首先稀盐酸和铁锈反应,过一会多余的稀盐酸才和铁反应生成氢气,所以符合图示的信息;③盐酸和稀硫酸混合物,与氯化钡溶液混合时,一开始就有硫酸钡沉淀生成,同样与第二个图中的信息加一会氯化钡溶液才生成不符;④氢氧化钠和硫酸铜反应产生的氢氧化铜沉淀,能和硫酸反应生成硫酸铜和水,所以开始没有沉淀出现,当硫酸消耗完后才出现沉淀,符合图中信息,所以只有②④符合图中给予的信息.21cnjy.com
故选:D.
9、
( http: / / www.21cnjy.com / )
【解析】(1)酸的水溶液显酸性,pH ( http: / / www.21cnjy.com )值小于7;
(2)盐酸、硫酸都可与氧化铁反应,分别生成氯化铁和硫酸铁溶液,所以会观察到铁锈逐渐消失,溶液显黄色,盐酸与铁锈反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O;(3)浓盐酸易挥发出氯化氢气体,氯化氢气体极易溶于水,会与空气中的水蒸气结合形成盐酸小液滴,故打开瓶塞会看到有白雾产生,而浓硫酸没有挥发性,没有白雾生成;
(4)依据复分解反应的发生条件可知硫酸转变为盐酸可以是硫酸与氯化钡的反应,其化学方程式为:BaCl2+H2SO4═BaSO4↓+2HCl;21*cnjy*com
10、
( http: / / www.21cnjy.com / )【解析】(1)硫酸和盐酸都属于酸,两者的不同主要是酸根的不同;(2)由于浓盐酸具有强烈的挥发性而浓硫酸没有,所以打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶,瓶口出现白雾的是浓盐酸;(3)硫酸溶液能与硝酸钡等含有钡离子的溶液反应生成硫酸钡白色沉淀,而盐酸不能,因此可以选择硝酸钡(或氯化钡或氢氧化钡)鉴别;(4)Ca(OH)2+2HCl=CaCl2+2H20; Ca(OH)2+H2SO4=CaSO4 +2H2O可知,氢氧化钙和盐酸反应的质量比是74:73.,而和硫酸反应的质量比为74:98,等质量的氢氧化钙需用的硫酸多,因此硫酸不够把氢氧化钙反应完,剩氢氧化钙,溶液显碱性,pH大于7.
11、【答案】(1)分别向④⑦两种溶液分别加硝酸钡溶液[或BaCl2溶液],有沉淀生成的为稀硫酸,无沉淀生成的为稀盐酸;
(2)①③
(3)HCl+NaOH=NaCl+H2O(或H2SO4+2NaOH=Na2SO4+2H2O);
(4)90%
【解析】(1)鉴别盐酸和硫酸可采取滴加 ( http: / / www.21cnjy.com )硝酸钡或氯化钡溶液观察是否产生沉淀的方法,生成白色沉淀的为硫酸,盐酸与硝酸钡或氯化钡溶液不发生反应,因而无明显现象;(2)由两种元素组成且含氧元素的物质为氧化物,生石灰为氧化钙的俗称,由钙、氧两种元素组成,CuO为铜和氧元素组成,所以生石灰和CuO都属于氧化物;(3)酸与碱生成盐和水的反应称为中和反应,烧碱为氢氧化钠的俗称属于碱,硫酸、盐酸都属于酸,所以,可选择氢氧化钠与硫酸或盐酸反应,与硫酸反应生成硫酸钠和水,与盐酸反应生成氯化钠和水;(4)反应放出二氧化碳气体质量=10g+60g-69.56g=0.44g
设放出0.44gCO2时参加反应的碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 41
X 0.44
( http: / / www.21cnjy.com / )
x=1g
则此瓶生石灰的纯度=×100%=90%
12、【答案】(1)600g
(2)1.71%
(3)2.92%
(4)
( http: / / www.21cnjy.com / )
【解析】:
( http: / / www.21cnjy.com / );
(2)由图示可知,生成沉淀的最 ( http: / / www.21cnjy.com )大量为4.66g,
设恰好完全反应时,消耗Ba(OH)2的质量为x,
Ba(OH)2+H2SO4=BaSO4↓+2H2O【出处:21教育名师】
171 233
x 4.66
=
x=3.42g
Ba(OH)2溶液的溶质质量分数是:×100%=1.71%;
(3)设盐酸的溶质质量分数是y,生成氯化钡质量为z
Ba(OH)2+2HCl=BaCl2+2H2O21·cn·jy·com
171 73 208
400g×1.71% y×100g z
( http: / / www.21cnjy.com / )
y=2.92%; z=8.32g
(4)通过上面的反应原理可知氢氧化钡和硫酸 ( http: / / www.21cnjy.com )反应生成硫酸钡沉淀和水,开始不会生成溶质,盐酸和氢氧化钡反应生成氯化钡和水,溶质质量不断增加,然后不变,所以
( http: / / www.21cnjy.com / )
( http: / / www.21cnjy.com / )
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://www.21cnjy.com/" 版权所有@21世纪教育网(www.21cnjy.com)
