2017-2018年苏教版高中化学选修三:4.2.3《配合物的形成和应用》——配合物的应用 课件 (共13张PPT)
文档属性
| 名称 | 2017-2018年苏教版高中化学选修三:4.2.3《配合物的形成和应用》——配合物的应用 课件 (共13张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 909.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-11-24 00:00:00 | ||
图片预览




文档简介
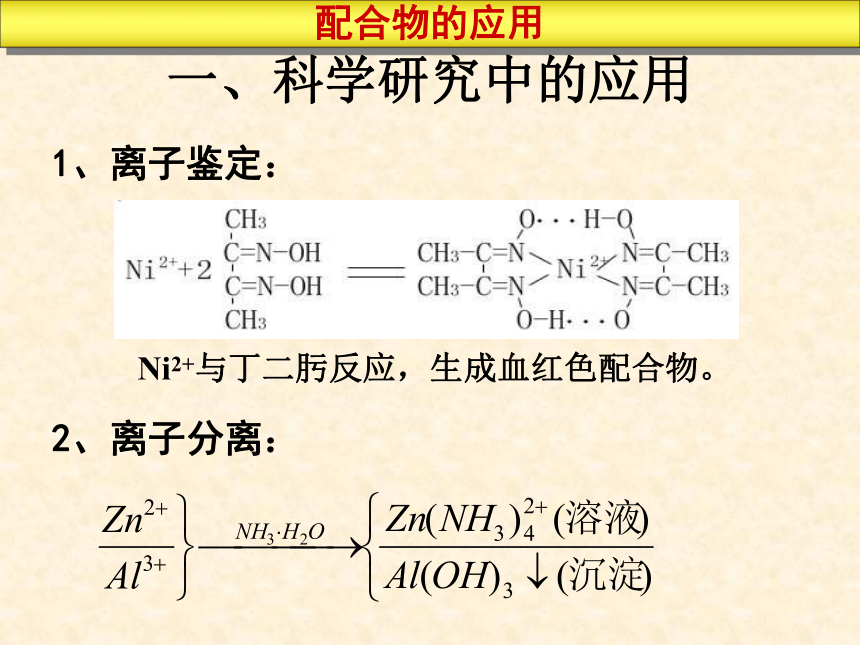
课件13张PPT。第二单元 配合物的形成和应用 配合物的应用专题4 分子空间结构与物质性质配合物在许多方面有广泛的应用 在实验研究中,常用形成配合物的方法来检验金属离子、分离物质、定量测定物质的组成。 在生产中,配合物被广泛应用于染色、电镀、硬水软化、金属冶炼领域。 在许多尖端领域如激光材料、超导材料、抗癌药物的研究、催化剂的研制等方面,配合物发挥着越来越大的作用。 一、科学研究中的应用1、离子鉴定:Ni2+与丁二肟反应,生成血红色配合物。2、离子分离:配合物的应用乙烯催化氧化制乙醛催化机理配合物的应用二、工业催化中的应用三、冶金电镀中的应用高纯度金属制备(Fe,Ni,Co)贵金属的提取配合物的应用四、生物医药中的应用医药行业
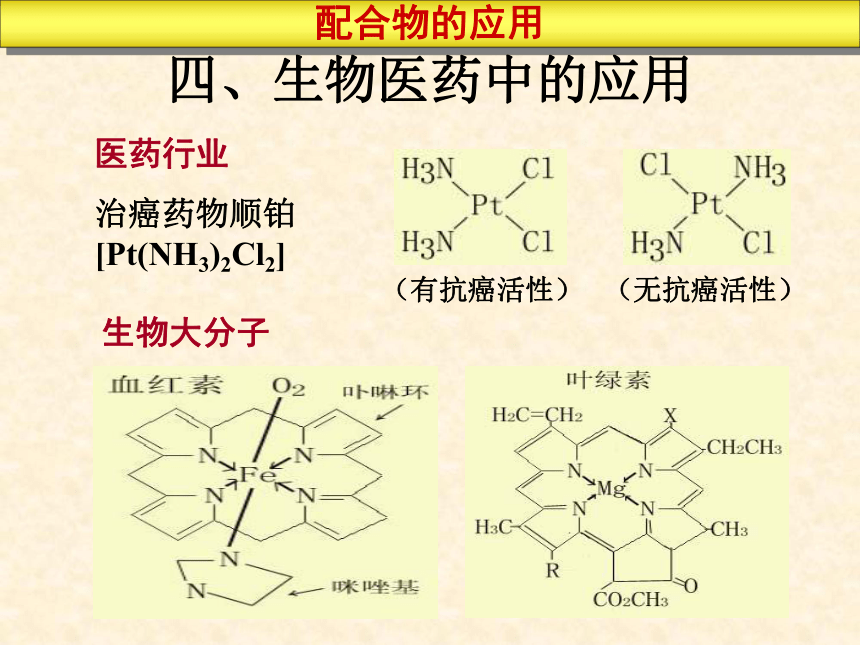
治癌药物顺铂[Pt(NH3)2Cl2]生物大分子(有抗癌活性) (无抗癌活性)配合物的应用五、配合物与生物固氮合氮酶中Fe-Mo中心结构示意图配合物的应用 将大气中游离态氮转化为化合态氮的过程叫氮的固定起固定氮作用的化学反应是
A、氮气与氢气在一定条件下反应生成氨气
B、一氧化氮与氧气反应生成二氧化氮
C、氨气经催化氧化生成一氧化氮 D、由氨气制碳酸氢铵和硫酸铵答案:A思考题: 要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时,最佳顺序为
①加入足量氯水 ②加入足量酸性高锰酸钾溶液 ③加入少量NH4SCN溶液
A.①③ B.③②
C.③① D.①②③ 答案:C思考题: 在做银镜反应实验时,需要配制银氨溶液。请回答:银氨溶液的配制过程,实验现象,写出相应的化学方程式。配制过程:在5%的硝酸银溶液中逐滴加入2mol/L的氨水,直至生成的沉淀恰好完全溶解。思考题:实验现象:先出现沉淀,继续滴加氨水后沉淀溶解生成无色澄清溶液。AgNO3+NH3·H2O==AgOH↓+NH4NO3 AgOH+2NH3·H2O==[Ag(NH3)2]OH +2H2O 某白色固体可能由①NH4Cl ②AlCl3 ③NaCl ④AgNO3 ⑤KOH中的一种或几种组成,此固体投入水中得澄清溶液,该溶液可使酚酞呈红色,若向溶液中加稀硝酸到过量,有白色沉淀生成。对原固体的判断不正确的是
A.肯定存在①
B.至少存在②和⑤
C.无法确定是否有③
D.至少存在①、④、⑤答案:B思考题: 从金矿中提取金,传统的方法是用氰化提金法。氰化提金法的原理是:用稀的氰化钠溶液处理粉碎了的金矿石,通入空气,使金矿中的金粒溶解,生成能溶于水的物质Na[Au(CN)2]。试写出并配平金粒溶解的化学方程式 。然后再用锌从溶液中把金置换出来,试写出并配平该化学方程式 。 4Au + 8NaCN + O2 + 2H2O = 4 Na[Au(CN)2] + 4NaOH+1Zn + 2Na[Au(CN)2] = 2Au + Na2[Zn(CN)4] 思考题:Au + NaCN + O2 + H2O → Na[Au(CN)2] + NaOH
治癌药物顺铂[Pt(NH3)2Cl2]生物大分子(有抗癌活性) (无抗癌活性)配合物的应用五、配合物与生物固氮合氮酶中Fe-Mo中心结构示意图配合物的应用 将大气中游离态氮转化为化合态氮的过程叫氮的固定起固定氮作用的化学反应是
A、氮气与氢气在一定条件下反应生成氨气
B、一氧化氮与氧气反应生成二氧化氮
C、氨气经催化氧化生成一氧化氮 D、由氨气制碳酸氢铵和硫酸铵答案:A思考题: 要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时,最佳顺序为
①加入足量氯水 ②加入足量酸性高锰酸钾溶液 ③加入少量NH4SCN溶液
A.①③ B.③②
C.③① D.①②③ 答案:C思考题: 在做银镜反应实验时,需要配制银氨溶液。请回答:银氨溶液的配制过程,实验现象,写出相应的化学方程式。配制过程:在5%的硝酸银溶液中逐滴加入2mol/L的氨水,直至生成的沉淀恰好完全溶解。思考题:实验现象:先出现沉淀,继续滴加氨水后沉淀溶解生成无色澄清溶液。AgNO3+NH3·H2O==AgOH↓+NH4NO3 AgOH+2NH3·H2O==[Ag(NH3)2]OH +2H2O 某白色固体可能由①NH4Cl ②AlCl3 ③NaCl ④AgNO3 ⑤KOH中的一种或几种组成,此固体投入水中得澄清溶液,该溶液可使酚酞呈红色,若向溶液中加稀硝酸到过量,有白色沉淀生成。对原固体的判断不正确的是
A.肯定存在①
B.至少存在②和⑤
C.无法确定是否有③
D.至少存在①、④、⑤答案:B思考题: 从金矿中提取金,传统的方法是用氰化提金法。氰化提金法的原理是:用稀的氰化钠溶液处理粉碎了的金矿石,通入空气,使金矿中的金粒溶解,生成能溶于水的物质Na[Au(CN)2]。试写出并配平金粒溶解的化学方程式 。然后再用锌从溶液中把金置换出来,试写出并配平该化学方程式 。 4Au + 8NaCN + O2 + 2H2O = 4 Na[Au(CN)2] + 4NaOH+1Zn + 2Na[Au(CN)2] = 2Au + Na2[Zn(CN)4] 思考题:Au + NaCN + O2 + H2O → Na[Au(CN)2] + NaOH
