人教版高中化学选修四3-4-2沉淀溶解平衡(课件)(共36张PPT)
文档属性
| 名称 | 人教版高中化学选修四3-4-2沉淀溶解平衡(课件)(共36张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 735.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-11-29 00:00:00 | ||
图片预览








文档简介
课件36张PPT。第4节 难溶电解质的溶解平衡
第2课时 沉淀溶解平衡第三章 水溶液中的离子平衡石灰石岩层在经历了数万年的岁月侵蚀之后,会形成
各种奇形异状的溶洞。你知道它们是如何形成的吗?学习目标1.能用平衡移动原理分析理解沉淀的溶解与生成、沉淀转化的实质。
2.学会用沉淀溶解平衡的移动解决生产、生活中的实际问题。学习重点沉淀的溶解与生成、沉淀转化的实质学习难点沉淀的溶解与生成、沉淀转化的实质溶液过饱和,有沉淀析出溶液饱和,沉淀与溶解处于平衡状态溶液未饱和,可继续溶解该难溶电解质溶度积(Ksp)与 离子积( QC )温故知新1、沉淀的生成(1)应用:生成难溶电解质的沉淀,是工业生产、环保工程和科学研究中除杂或提纯物质的重要方法之一。(2)沉淀的方法① 调pH值如:工业原料氯化铵中混有氯化铁,使其溶解于水,再加氨水调 pH值至7~8,可使Fe3+转变为Fe(OH)3沉淀而除去。Fe3+ + 3NH3?H2O=Fe(OH)3↓+3NH4+ ② 加沉淀剂
如:沉淀Cu2+、Hg2+等,以Na2S、H2S做沉淀剂Cu2++S2-= CuS↓
Hg2++S2-= HgS↓1、除去NaCl溶液中的SO42-,选择加 入CaCl2还是BaCl2做沉淀剂?为什么?加入钡盐,因为BaSO4比CaSO4更难溶,使用钡盐可使SO42-沉淀更完全 沉淀离子浓度小于10-5mol/L交流研讨
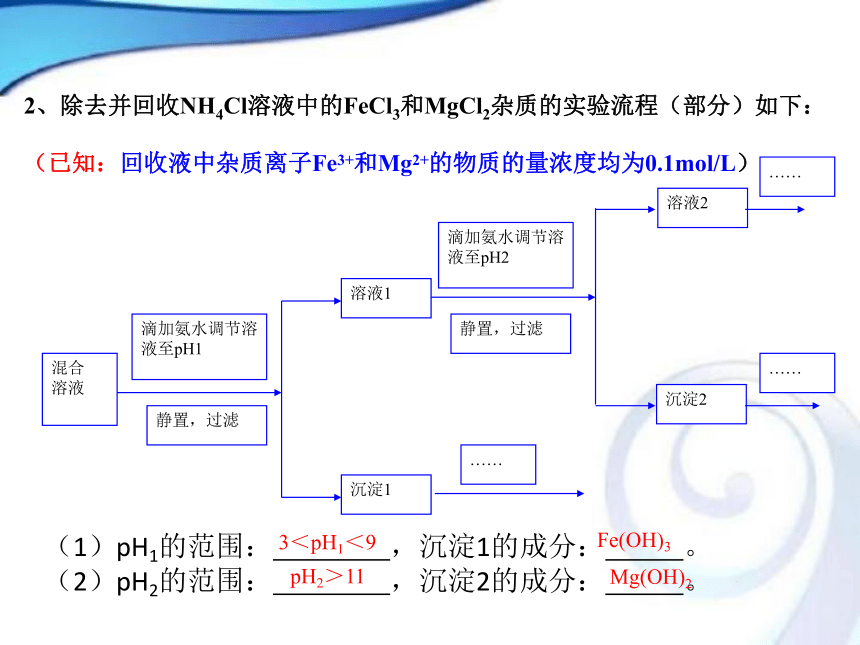
2、除去并回收NH4Cl溶液中的FeCl3和MgCl2杂质的实验流程(部分)如下:
(已知:回收液中杂质离子Fe3+和Mg2+的物质的量浓度均为0.1mol/L)(1)pH1的范围: ,沉淀1的成分: 。
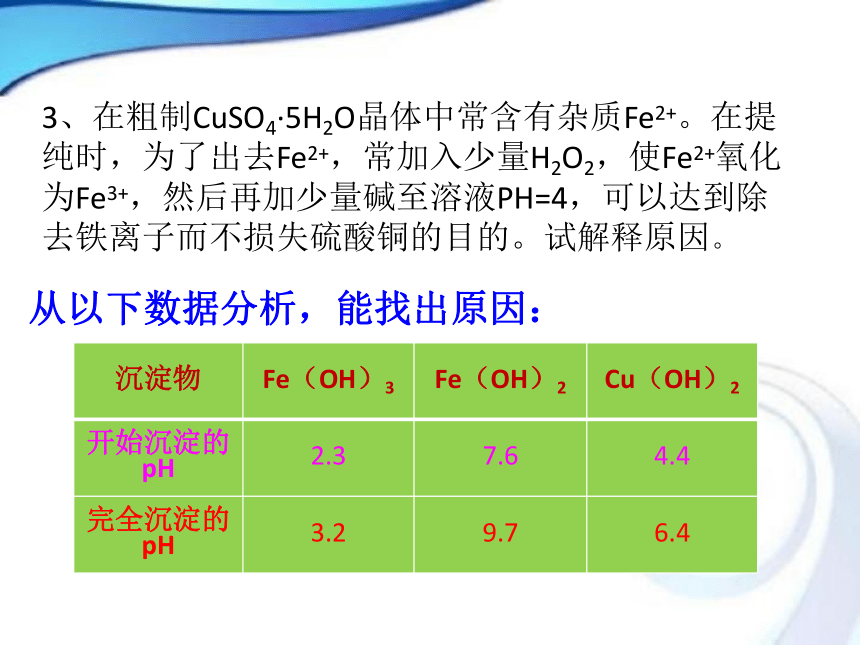
(2)pH2的范围: ,沉淀2的成分: 。 3<pH1<9Fe(OH)3pH2>11Mg(OH)23、在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。在提纯时,为了出去Fe2+,常加入少量H2O2,使Fe2+氧化为Fe3+,然后再加少量碱至溶液PH=4,可以达到除去铁离子而不损失硫酸铜的目的。试解释原因。从以下数据分析,能找出原因:2. 沉淀的溶解
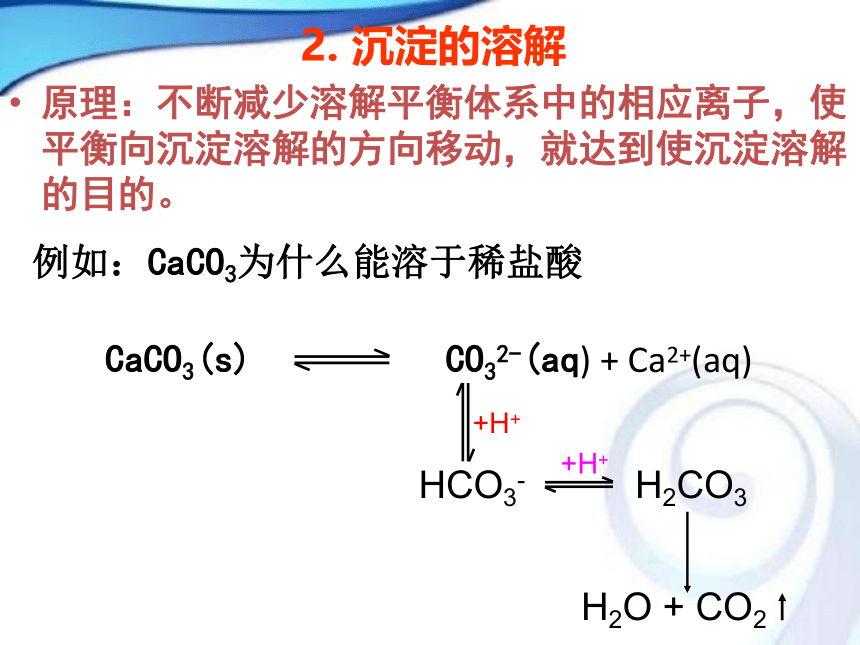
原理:不断减少溶解平衡体系中的相应离子,使平衡向沉淀溶解的方向移动,就达到使沉淀溶解的目的。
CaCO3(s) CO32-(aq) + Ca2+(aq)
HCO3-+H++H+H2CO3H2O + CO2例如:CaCO3为什么能溶于稀盐酸[思考]:写出氢氧化镁沉淀溶解平衡的表达式. 若使氢氧化镁沉淀溶解,可以采取什么方法?所依据的原理是什么?
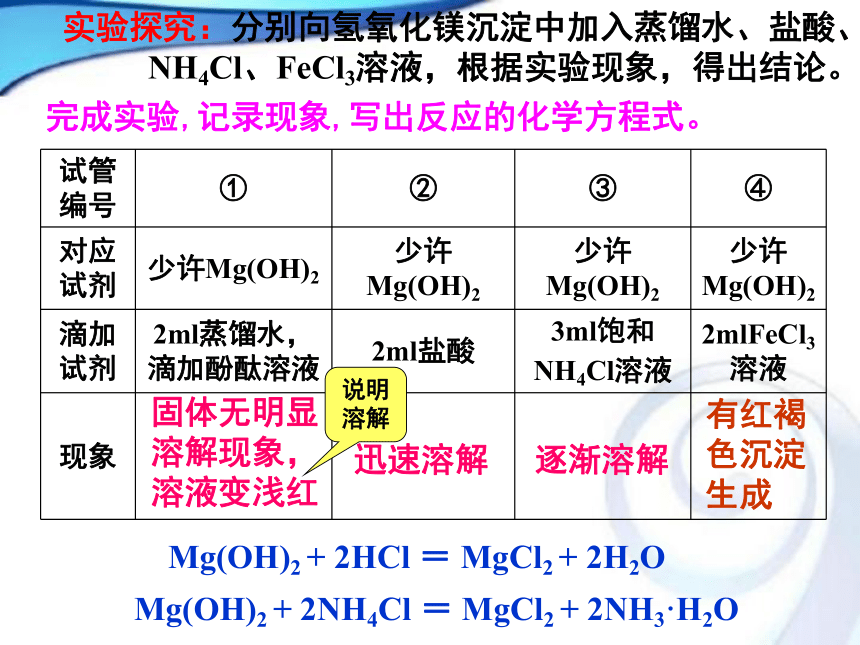
Mg(OH)2(s) Mg2+(aq)+2OH-(aq)溶解沉淀 根据勒夏特列原理,使沉淀溶解平衡向溶解方向移动可采取的方法有:升温、加水、加盐酸…..还可以加什么物质呢?交流研讨固体无明显溶解现象,溶液变浅红迅速溶解逐渐溶解Mg(OH)2 + 2HCl = MgCl2 + 2H2OMg(OH)2 + 2NH4Cl = MgCl2 + 2NH3·H2O完成实验,记录现象,写出反应的化学方程式。有红褐色沉淀生成说明溶解实验探究:分别向氢氧化镁沉淀中加入蒸馏水、盐酸、
NH4Cl、FeCl3溶液,根据实验现象,得出结论。在溶液中存在Mg(OH)2的溶解平衡:
Mg(OH)2(s) ?Mg2+(aq)+2OH-(aq) 加入盐酸时,H+中和OH-,使c(OH-)减小,平衡右移,从而使Mg(OH)2溶解。 加入NH4Cl时,NH4+与OH-结合,生成弱电解质NH3·H2O(它在水中比Mg(OH)2更难电离出OH-),使c(OH-)减小,平衡右移,从而使Mg(OH)2的沉淀溶解平衡向溶解方向移动。【思考与交流】: 应用平衡移动原理分析、解释实验中 发生的反应,并试从中找出使沉淀溶解的规律。【解释】[思考]:白色的氢氧化镁沉淀加入氯化铁溶液后,
为什么会有红褐色沉淀生成?
Mg(OH)2(s) ?Mg2+(aq)+2OH-(aq),Fe(OH)3↓这就是----沉淀的转化FeCl3 = 3Cl - + Fe3++Fe(OH)3的Ksp远小于Mg(OH)2的Ksp,说明Fe(OH)3比Mg(OH)2更难溶。参见P65页表3-5【实验3-4】有白色沉淀析出白色沉淀转化为黄色黄色沉淀转化为黑色AgClAgIAg2S向MgCl2溶液中滴加NaOH溶液生成白色沉淀向有白色沉淀的溶液中滴加FeCl3溶液白色沉淀转变为红褐色静置红褐色沉淀析出,溶液变无色【实验3-5】(实验3-4、3-5 沉淀转化)AgClAgIAg2SMg(OH)2Fe(OH)3[讨论]:从实验中可以得到什么结论?实验说明:沉淀可以从溶解度小的向溶解度更小的方向转化,两者差别越大,转化越容易。
沉淀一般从溶解度小的向溶解度更小的方向转化。沉淀的转化示意图KI = I- + K++AgI(s)s(AgCl)=1.5×10-4gs(AgI)=3.7×10-7gs(Ag2S)=1.3×10-16g沉淀从溶解度小的向溶解度更小的方向转化。1.根据你所观察到的现象,写出所发生的反应。
2.如果将上述两个实验中的沉淀生成和转化的步骤颠倒顺序,会产生什么结果?试用平衡移动原理和两种沉淀溶解度上的差别加以解释,找出这类反应发生的特点。溶解度小的沉淀转化为溶解度更小的沉淀。两者差别越大,转化越容易。AgCl+I-=AgI+Cl-2AgI+S2-=Ag2S+2I-3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+转化不会发生交流研讨沉淀转化的实质
沉淀转化的实质是沉淀溶解平衡移动。一般溶解度小的沉淀转化成溶解度更小的沉淀容易实现。
沉淀转化的应用
沉淀的转化在科研和生产中具有重要的应用价值。1.向盛有0.1mol/LAgNO3溶液的试管中滴加0.1mol/LNaCl溶液,至不再有白色沉淀生成为止。取其中澄清溶液,逐滴加入饱和Na2S溶液,有无沉淀生成?
如果先向AgNO3溶液中加Na2S溶液至沉淀完全,再向上层清液中滴加NaCl,情况又如何?试解释原因。
没有沉淀生成。Ag2S饱和溶液中Ag+太少,不能生成AgCl沉淀。有黑色沉淀生成。学以致用+
CO32-CaCO3 应用1:锅炉除水垢:P—64
锅炉的水垢中含有CaSO4 ,可先用Na2CO3溶液处理,使 之转化为疏松、易溶于酸的CaCO3。化学法除锅炉水垢的流程图水垢成分CaCO3
Mg(OH)2 CaSO4 用饱和Na2CO3
溶液浸泡数天疏松的水垢CaCO3
Mg(OH)2
写出除去水垢过程中发生的所有离子方程式用盐酸或
饱氯化铵液除去水垢应用2:一些自然现象的解释2HCO3-各种原生铜的硫化物经氧化、淋滤作用
后可变成CuSO4溶液,并向深部渗透,
遇到深层的闪锌矿(ZnS)和方铅矿(PbS),
便慢慢地使之转变为铜蓝(CuS)。 应用3:为什么医学上常用BaSO4作为内服造影剂“钡餐”, 而不用BaCO3作为内服造影剂“钡餐”? 由于人体内胃酸的酸性较强(pH=0.9~1.5),如果服下BaCO3,胃酸会与CO32-反应生成CO2和水,使CO32-浓度降低,使BaCO3的沉淀溶解平衡向右移动,使体内的Ba2+浓度增大而引起人体中毒。所以,不能用BaCO3作为内服造影剂“钡餐”。而SO42-不与H+结合生成硫酸,胃酸中的H+对BaSO4的溶解平衡没有影响,Ba2+浓度保持在安全浓度标准下,所以用BaSO4 作“钡餐”。
沉淀的生成、溶解、转化实质上都是沉淀溶解平衡的移动的过程,其基本依据主要有:
①浓度:加水,平衡向溶解方向移动。
②温度:升温,多数平衡向溶解方向移动。
③加入相同离子,平衡向沉淀方向移动。
④加入可与体系中某些离子反应生成更难溶或更难电离或气体的离子,使平衡向溶解的方向移动。归纳总结牙齿表面由一层硬的、组成为Ca5(PO4)3OH的物质保护着,它在唾液中存在下列平衡:
Ca5(PO4)3OH(s) 5 Ca2+ +3PO43-+OH- 进食后,细菌和酶作用于食物,产生有机酸,这时牙齿就会受到腐蚀,其原因是
。
已知Ca5(PO4)3F(s)的溶解度比上面的矿化产物更小、质地更坚固。用离子方程表示当牙膏中配有氟化物添加剂后能防止龋齿的原因:
因 。 生成的有机酸能中和OH-,使平衡向脱矿方向移动,加速
腐蚀牙齿 5Ca2++3PO43-+F-=Ca5(PO4)3F↓ 学以致用归纳总结A 当堂检测2.某温度时,BaSO4在水中的
沉淀溶解平衡曲线如图所示。
下列说法正确的是( )
A.加入Na2SO4可以使溶液由a点变
到b点
B.通过蒸发可以使溶液由d点变到c点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的KspC2×10-34×10-3c(SO42-)/(mol·L-1)2×10-34×10-3c(Ba2+)/(mol·L-1)abcd3.下列情况下,有无CaCO3沉淀生成?[Ksp(CaCO3)=2.8×
10-9 mol2·L-2]
(1)往1.0 L纯水中加入0.1 mL浓度为0.01 mol·L-1的
CaCl2溶液和Na2CO3溶液;【提示】c(Ca2+)=c(CO )=0.1?10-3? 0.01/1.0=
10-6 mol·L-1
Q=c(Ca2+)×c(CO )=10-12 mol2·L-2 < Ksp(CaCO3)=
2.8?10-9 mol2·L-2
因此无CaCO3沉淀生成。(2)改变CaCl2和Na2CO3的浓度为1.0 mol·L-1呢?【提示】 c(Ca2+)=c(CO ) = 10-4 mol·L-1
Q=c(Ca2+)×c(CO )=10-8 mol2·L-2 >Ksp(CaCO3)。故有
CaCO3沉淀生成。要铭记在心:每天都是一生中最美好的日子。
各种奇形异状的溶洞。你知道它们是如何形成的吗?学习目标1.能用平衡移动原理分析理解沉淀的溶解与生成、沉淀转化的实质。
2.学会用沉淀溶解平衡的移动解决生产、生活中的实际问题。学习重点沉淀的溶解与生成、沉淀转化的实质学习难点沉淀的溶解与生成、沉淀转化的实质溶液过饱和,有沉淀析出溶液饱和,沉淀与溶解处于平衡状态溶液未饱和,可继续溶解该难溶电解质溶度积(Ksp)与 离子积( QC )温故知新1、沉淀的生成(1)应用:生成难溶电解质的沉淀,是工业生产、环保工程和科学研究中除杂或提纯物质的重要方法之一。(2)沉淀的方法① 调pH值如:工业原料氯化铵中混有氯化铁,使其溶解于水,再加氨水调 pH值至7~8,可使Fe3+转变为Fe(OH)3沉淀而除去。Fe3+ + 3NH3?H2O=Fe(OH)3↓+3NH4+ ② 加沉淀剂
如:沉淀Cu2+、Hg2+等,以Na2S、H2S做沉淀剂Cu2++S2-= CuS↓
Hg2++S2-= HgS↓1、除去NaCl溶液中的SO42-,选择加 入CaCl2还是BaCl2做沉淀剂?为什么?加入钡盐,因为BaSO4比CaSO4更难溶,使用钡盐可使SO42-沉淀更完全 沉淀离子浓度小于10-5mol/L交流研讨
2、除去并回收NH4Cl溶液中的FeCl3和MgCl2杂质的实验流程(部分)如下:
(已知:回收液中杂质离子Fe3+和Mg2+的物质的量浓度均为0.1mol/L)(1)pH1的范围: ,沉淀1的成分: 。
(2)pH2的范围: ,沉淀2的成分: 。 3<pH1<9Fe(OH)3pH2>11Mg(OH)23、在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。在提纯时,为了出去Fe2+,常加入少量H2O2,使Fe2+氧化为Fe3+,然后再加少量碱至溶液PH=4,可以达到除去铁离子而不损失硫酸铜的目的。试解释原因。从以下数据分析,能找出原因:2. 沉淀的溶解
原理:不断减少溶解平衡体系中的相应离子,使平衡向沉淀溶解的方向移动,就达到使沉淀溶解的目的。
CaCO3(s) CO32-(aq) + Ca2+(aq)
HCO3-+H++H+H2CO3H2O + CO2例如:CaCO3为什么能溶于稀盐酸[思考]:写出氢氧化镁沉淀溶解平衡的表达式. 若使氢氧化镁沉淀溶解,可以采取什么方法?所依据的原理是什么?
Mg(OH)2(s) Mg2+(aq)+2OH-(aq)溶解沉淀 根据勒夏特列原理,使沉淀溶解平衡向溶解方向移动可采取的方法有:升温、加水、加盐酸…..还可以加什么物质呢?交流研讨固体无明显溶解现象,溶液变浅红迅速溶解逐渐溶解Mg(OH)2 + 2HCl = MgCl2 + 2H2OMg(OH)2 + 2NH4Cl = MgCl2 + 2NH3·H2O完成实验,记录现象,写出反应的化学方程式。有红褐色沉淀生成说明溶解实验探究:分别向氢氧化镁沉淀中加入蒸馏水、盐酸、
NH4Cl、FeCl3溶液,根据实验现象,得出结论。在溶液中存在Mg(OH)2的溶解平衡:
Mg(OH)2(s) ?Mg2+(aq)+2OH-(aq) 加入盐酸时,H+中和OH-,使c(OH-)减小,平衡右移,从而使Mg(OH)2溶解。 加入NH4Cl时,NH4+与OH-结合,生成弱电解质NH3·H2O(它在水中比Mg(OH)2更难电离出OH-),使c(OH-)减小,平衡右移,从而使Mg(OH)2的沉淀溶解平衡向溶解方向移动。【思考与交流】: 应用平衡移动原理分析、解释实验中 发生的反应,并试从中找出使沉淀溶解的规律。【解释】[思考]:白色的氢氧化镁沉淀加入氯化铁溶液后,
为什么会有红褐色沉淀生成?
Mg(OH)2(s) ?Mg2+(aq)+2OH-(aq),Fe(OH)3↓这就是----沉淀的转化FeCl3 = 3Cl - + Fe3++Fe(OH)3的Ksp远小于Mg(OH)2的Ksp,说明Fe(OH)3比Mg(OH)2更难溶。参见P65页表3-5【实验3-4】有白色沉淀析出白色沉淀转化为黄色黄色沉淀转化为黑色AgClAgIAg2S向MgCl2溶液中滴加NaOH溶液生成白色沉淀向有白色沉淀的溶液中滴加FeCl3溶液白色沉淀转变为红褐色静置红褐色沉淀析出,溶液变无色【实验3-5】(实验3-4、3-5 沉淀转化)AgClAgIAg2SMg(OH)2Fe(OH)3[讨论]:从实验中可以得到什么结论?实验说明:沉淀可以从溶解度小的向溶解度更小的方向转化,两者差别越大,转化越容易。
沉淀一般从溶解度小的向溶解度更小的方向转化。沉淀的转化示意图KI = I- + K++AgI(s)s(AgCl)=1.5×10-4gs(AgI)=3.7×10-7gs(Ag2S)=1.3×10-16g沉淀从溶解度小的向溶解度更小的方向转化。1.根据你所观察到的现象,写出所发生的反应。
2.如果将上述两个实验中的沉淀生成和转化的步骤颠倒顺序,会产生什么结果?试用平衡移动原理和两种沉淀溶解度上的差别加以解释,找出这类反应发生的特点。溶解度小的沉淀转化为溶解度更小的沉淀。两者差别越大,转化越容易。AgCl+I-=AgI+Cl-2AgI+S2-=Ag2S+2I-3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+转化不会发生交流研讨沉淀转化的实质
沉淀转化的实质是沉淀溶解平衡移动。一般溶解度小的沉淀转化成溶解度更小的沉淀容易实现。
沉淀转化的应用
沉淀的转化在科研和生产中具有重要的应用价值。1.向盛有0.1mol/LAgNO3溶液的试管中滴加0.1mol/LNaCl溶液,至不再有白色沉淀生成为止。取其中澄清溶液,逐滴加入饱和Na2S溶液,有无沉淀生成?
如果先向AgNO3溶液中加Na2S溶液至沉淀完全,再向上层清液中滴加NaCl,情况又如何?试解释原因。
没有沉淀生成。Ag2S饱和溶液中Ag+太少,不能生成AgCl沉淀。有黑色沉淀生成。学以致用+
CO32-CaCO3 应用1:锅炉除水垢:P—64
锅炉的水垢中含有CaSO4 ,可先用Na2CO3溶液处理,使 之转化为疏松、易溶于酸的CaCO3。化学法除锅炉水垢的流程图水垢成分CaCO3
Mg(OH)2 CaSO4 用饱和Na2CO3
溶液浸泡数天疏松的水垢CaCO3
Mg(OH)2
写出除去水垢过程中发生的所有离子方程式用盐酸或
饱氯化铵液除去水垢应用2:一些自然现象的解释2HCO3-各种原生铜的硫化物经氧化、淋滤作用
后可变成CuSO4溶液,并向深部渗透,
遇到深层的闪锌矿(ZnS)和方铅矿(PbS),
便慢慢地使之转变为铜蓝(CuS)。 应用3:为什么医学上常用BaSO4作为内服造影剂“钡餐”, 而不用BaCO3作为内服造影剂“钡餐”? 由于人体内胃酸的酸性较强(pH=0.9~1.5),如果服下BaCO3,胃酸会与CO32-反应生成CO2和水,使CO32-浓度降低,使BaCO3的沉淀溶解平衡向右移动,使体内的Ba2+浓度增大而引起人体中毒。所以,不能用BaCO3作为内服造影剂“钡餐”。而SO42-不与H+结合生成硫酸,胃酸中的H+对BaSO4的溶解平衡没有影响,Ba2+浓度保持在安全浓度标准下,所以用BaSO4 作“钡餐”。
沉淀的生成、溶解、转化实质上都是沉淀溶解平衡的移动的过程,其基本依据主要有:
①浓度:加水,平衡向溶解方向移动。
②温度:升温,多数平衡向溶解方向移动。
③加入相同离子,平衡向沉淀方向移动。
④加入可与体系中某些离子反应生成更难溶或更难电离或气体的离子,使平衡向溶解的方向移动。归纳总结牙齿表面由一层硬的、组成为Ca5(PO4)3OH的物质保护着,它在唾液中存在下列平衡:
Ca5(PO4)3OH(s) 5 Ca2+ +3PO43-+OH- 进食后,细菌和酶作用于食物,产生有机酸,这时牙齿就会受到腐蚀,其原因是
。
已知Ca5(PO4)3F(s)的溶解度比上面的矿化产物更小、质地更坚固。用离子方程表示当牙膏中配有氟化物添加剂后能防止龋齿的原因:
因 。 生成的有机酸能中和OH-,使平衡向脱矿方向移动,加速
腐蚀牙齿 5Ca2++3PO43-+F-=Ca5(PO4)3F↓ 学以致用归纳总结A 当堂检测2.某温度时,BaSO4在水中的
沉淀溶解平衡曲线如图所示。
下列说法正确的是( )
A.加入Na2SO4可以使溶液由a点变
到b点
B.通过蒸发可以使溶液由d点变到c点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的KspC2×10-34×10-3c(SO42-)/(mol·L-1)2×10-34×10-3c(Ba2+)/(mol·L-1)abcd3.下列情况下,有无CaCO3沉淀生成?[Ksp(CaCO3)=2.8×
10-9 mol2·L-2]
(1)往1.0 L纯水中加入0.1 mL浓度为0.01 mol·L-1的
CaCl2溶液和Na2CO3溶液;【提示】c(Ca2+)=c(CO )=0.1?10-3? 0.01/1.0=
10-6 mol·L-1
Q=c(Ca2+)×c(CO )=10-12 mol2·L-2 < Ksp(CaCO3)=
2.8?10-9 mol2·L-2
因此无CaCO3沉淀生成。(2)改变CaCl2和Na2CO3的浓度为1.0 mol·L-1呢?【提示】 c(Ca2+)=c(CO ) = 10-4 mol·L-1
Q=c(Ca2+)×c(CO )=10-8 mol2·L-2 >Ksp(CaCO3)。故有
CaCO3沉淀生成。要铭记在心:每天都是一生中最美好的日子。
