浙教版九年级上第1章第二节探索酸的性质(第一课时)[上学期]
文档属性
| 名称 | 浙教版九年级上第1章第二节探索酸的性质(第一课时)[上学期] |

|
|
| 格式 | rar | ||
| 文件大小 | 4.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2008-12-23 00:00:00 | ||
图片预览










文档简介
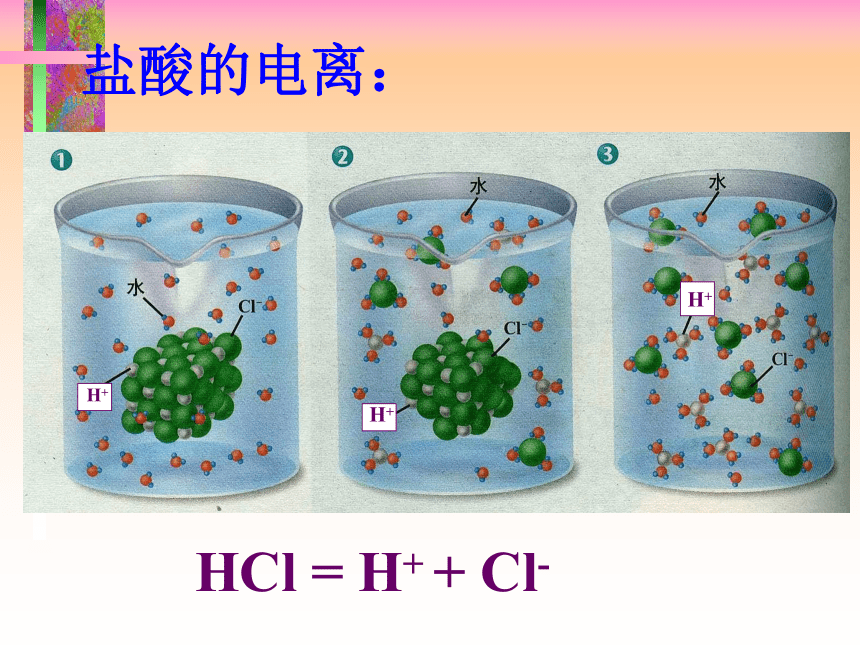
课件30张PPT。第二节 探索酸的性质第一课时酸。一、什么是酸 你若有呕吐的经历,你会感受到胃液是酸的。在日常生活中,有酸味的物质还有醋、放置时间过长的面包、杏、苹果、橘子等。我们知道:食醋——醋酸,胃液——盐酸,柠檬、柑橘等水果中含有柠檬酸。 这些物质在水中电离时,生成的阳离子全部都是氢离子(H+)。那么,为什么说这些物质都是酸呢?盐酸的电离:HCl = H+ + Cl-H+H+H+一些物质的电离2、电离:带电的原子或原子集团。1、离子:一些物质溶解于水或受热熔化时,产生自由移动的离子的过程,叫做电离。带正电荷的叫阳离子。带负电荷的叫阴离子。电解质是指在水溶液中或熔融状态下能够导电的化合物,例如酸、碱和盐等。
凡在上述情况下不能导电的化合物叫非电解质,例如蔗糖、酒精等。电解质和非电解质判断某化合物是否是电解质,不能只凭它在水溶液中导电与否,还需要进一步考察其晶体结构因素。
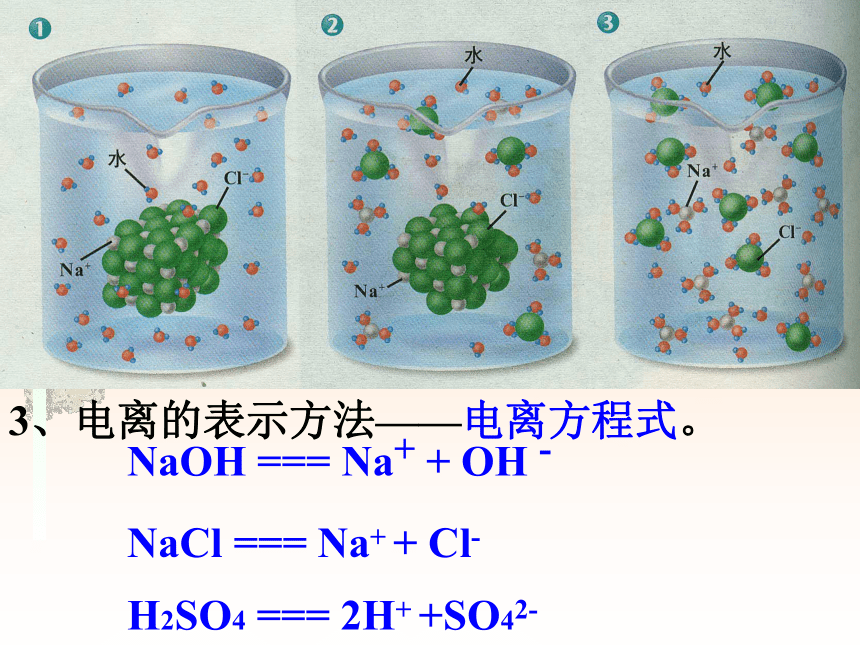
例如,硫酸钡、碳酸钙不溶于水,但受热熔化时能导电是电解质。 如SO2本身不能电离,而它和水反应,生成亚硫酸能导电,亚硫酸为电解质 , SO2不是电解质有些能导电的物质,如铜、铝等不是电解质。因它们不是化合物,而是单质,不符合电解质的定义。一些物质的电离2、电离:带电的原子或原子集团。1、离子:一些物质溶解于水或受热熔化时,产生自由移动的离子的过程,叫做电离。带正电荷的叫阳离子。带负电荷的叫阴离子。3、电离的表示方法——电离方程式。NaOH === Na+ + OH -NaCl === Na+ + Cl-H2SO4 === 2H+ +SO42-4、一些物质电离时产生的阴阳离子所带电荷的总数一定相等。所以,这些物质的溶液不显电性。5、电离方程式书写时,不必写条件,但要配平,使正负电荷总数相等,而原子团不能拆开。练习:
1、下列电离方程式正确的是( )
A、H2SO4 =H+ + SO42-
B、 Al2(SO4)3 = 2Al3++ 3SO4 2 -
C、 Ba(OH)2= Ba 2+ + (OH)-
D、NaCl=Na1+ +Cl1-
2、写出下列物质的电离方程式:
H2CO3 =
Ca(OH)2 =
Na2CO3 = CuSO4 =
BaCl2 = NaHSO4 =B3、判断下列电离方程式是否正确,若不正确,请改正:
1、KOH = K++OH-1
2、Ba(OH)2 = Ba2++2(OH)-
3、KNO3 = K++N++O32-
4、H2SO4 = H2++SO42-
5、AlCl3 = Al3++Cl-1.溶液中有N个K+,则SO42-应为 个2.溶液中有A个Mg2+和B个Na+,则NO3-应为 个。N/22A+B主板书盐酸:
硝酸:
硫酸:HCI === H + + CI-电离方程式:H NO3 === H + + NO3-H2SO4 == 2H + + SO 42-
电离通式:酸= H+ + 酸根阴离子什么是酸?酸的涵义:电离时产生的阳离子
只有氢离子的化合物 强酸:盐酸(HCl)、硫酸(H2SO4)、
硝酸(HNO3)
弱酸:醋酸(CH3COOH)讨论1:NaHSO4=Na++H++SO42-
NaHSO4是不是一种酸? 讨论2:下列物质里含有什么酸?
食醋里含有--------
人的胃液里含有-------
柠檬、柑橘等水果中含有------
实验室常见的酸有---------醋酸-盐酸-柠檬酸盐酸、硫酸、硝酸pH>7,碱性; pH =7,中性;pH<7,酸性。那么,你知道还有什么方法可以测定物质的酸碱性?酸碱指示剂二、酸碱指示剂1、定义:在酸或碱溶液里能显示出不同颜色的物质。2、常见的酸碱指示剂有:紫色石蕊试液无色酚酞试液3、酸碱指示剂可以定性地测定溶液的
酸碱性。4、常见指示剂在酸、碱性溶液中的颜色红色红色红色无色蓝色蓝色不变色不变色石蕊遇酸变红,遇碱变蓝;
酚酞遇酸不变色,遇碱变红。结论:1、用玻璃棒分别蘸取少许水、酸果汁、白醋、盐酸,点在pH试纸中部,观察试纸的颜色变化。
2、在白色点滴板的空穴(或小试管)里分别滴入几滴上述样品,再滴加2—3滴紫色石蕊试液,观察其颜色的变化,并将结果填入表中。实验结论:物 质 的 颜 色 变 化红或蓝红红红紫色红红红结论:pH试纸能显示酸性的强弱,而指示剂则只能指示溶液是否显酸性。三、自制酸碱指示剂1、取一些月季花、菊花、丝瓜花、一串红等植物的花、果、枝叶切碎、捣烂,用酒精浸制,所得的浸出液可以作为酸碱指示剂。P82、取食盐水、白醋、石灰水加以试验。并纪录变色情况。那么你会自制酸碱指示剂吗?
许多植物的花果茎叶中都含有某些显色的物质,它们在酸性溶液或碱性溶液里会显示不同的颜色.方法是取这些植物的花果枝叶切碎捣烂,用酒精浸制,所得的浸出液可以作为酸碱指示剂. 红某些花浸出液的变色情况练习:
1、某无色溶液PH=2,该溶液呈 性,它能使紫色石蕊试液变 ,无色酚酞试液 ,使蓝色石蕊试纸变 。酸红色不变色红色2、测得某溶液中仅含Cu2+、K+、Cl-、SO42-四种离子,且阳离子的数量比为Cu2+:K+:Cl-= 3:4:6,则SO42-:Cl- 的比值是………( )
A、3:2 B、1:3
C、1:8 D、2:5 B3、下列物质中存在着能自由移动的氯离子的是---------( )
A、液态氯化氢; B、KCl晶体;
C、KClO3溶液; D、熔化的MgCl2
4、下列各组离子属于酸的电离的是…( )
A、H+、SO42-、Na+ B、OH-、Ba2+
C、H+、NO3- D、Na+、HCO3-DC1、下列物质不属于酸的是 ( )
A、HNO3 B、NaHCO3
C、H3PO4 D、HI
?
2、用简单的方法区别水和硫酸,并写出实验步骤
3、思考:一位科学家在做研究时不小心将盐酸滴到了紫花上,紫花逐渐变红色。看到这么个现象,许多问题在他的脑子里涌现出来,如果你是那个科学家,你会有什么问题,你会有什么想法?
B
凡在上述情况下不能导电的化合物叫非电解质,例如蔗糖、酒精等。电解质和非电解质判断某化合物是否是电解质,不能只凭它在水溶液中导电与否,还需要进一步考察其晶体结构因素。
例如,硫酸钡、碳酸钙不溶于水,但受热熔化时能导电是电解质。 如SO2本身不能电离,而它和水反应,生成亚硫酸能导电,亚硫酸为电解质 , SO2不是电解质有些能导电的物质,如铜、铝等不是电解质。因它们不是化合物,而是单质,不符合电解质的定义。一些物质的电离2、电离:带电的原子或原子集团。1、离子:一些物质溶解于水或受热熔化时,产生自由移动的离子的过程,叫做电离。带正电荷的叫阳离子。带负电荷的叫阴离子。3、电离的表示方法——电离方程式。NaOH === Na+ + OH -NaCl === Na+ + Cl-H2SO4 === 2H+ +SO42-4、一些物质电离时产生的阴阳离子所带电荷的总数一定相等。所以,这些物质的溶液不显电性。5、电离方程式书写时,不必写条件,但要配平,使正负电荷总数相等,而原子团不能拆开。练习:
1、下列电离方程式正确的是( )
A、H2SO4 =H+ + SO42-
B、 Al2(SO4)3 = 2Al3++ 3SO4 2 -
C、 Ba(OH)2= Ba 2+ + (OH)-
D、NaCl=Na1+ +Cl1-
2、写出下列物质的电离方程式:
H2CO3 =
Ca(OH)2 =
Na2CO3 = CuSO4 =
BaCl2 = NaHSO4 =B3、判断下列电离方程式是否正确,若不正确,请改正:
1、KOH = K++OH-1
2、Ba(OH)2 = Ba2++2(OH)-
3、KNO3 = K++N++O32-
4、H2SO4 = H2++SO42-
5、AlCl3 = Al3++Cl-1.溶液中有N个K+,则SO42-应为 个2.溶液中有A个Mg2+和B个Na+,则NO3-应为 个。N/22A+B主板书盐酸:
硝酸:
硫酸:HCI === H + + CI-电离方程式:H NO3 === H + + NO3-H2SO4 == 2H + + SO 42-
电离通式:酸= H+ + 酸根阴离子什么是酸?酸的涵义:电离时产生的阳离子
只有氢离子的化合物 强酸:盐酸(HCl)、硫酸(H2SO4)、
硝酸(HNO3)
弱酸:醋酸(CH3COOH)讨论1:NaHSO4=Na++H++SO42-
NaHSO4是不是一种酸? 讨论2:下列物质里含有什么酸?
食醋里含有--------
人的胃液里含有-------
柠檬、柑橘等水果中含有------
实验室常见的酸有---------醋酸-盐酸-柠檬酸盐酸、硫酸、硝酸pH>7,碱性; pH =7,中性;pH<7,酸性。那么,你知道还有什么方法可以测定物质的酸碱性?酸碱指示剂二、酸碱指示剂1、定义:在酸或碱溶液里能显示出不同颜色的物质。2、常见的酸碱指示剂有:紫色石蕊试液无色酚酞试液3、酸碱指示剂可以定性地测定溶液的
酸碱性。4、常见指示剂在酸、碱性溶液中的颜色红色红色红色无色蓝色蓝色不变色不变色石蕊遇酸变红,遇碱变蓝;
酚酞遇酸不变色,遇碱变红。结论:1、用玻璃棒分别蘸取少许水、酸果汁、白醋、盐酸,点在pH试纸中部,观察试纸的颜色变化。
2、在白色点滴板的空穴(或小试管)里分别滴入几滴上述样品,再滴加2—3滴紫色石蕊试液,观察其颜色的变化,并将结果填入表中。实验结论:物 质 的 颜 色 变 化红或蓝红红红紫色红红红结论:pH试纸能显示酸性的强弱,而指示剂则只能指示溶液是否显酸性。三、自制酸碱指示剂1、取一些月季花、菊花、丝瓜花、一串红等植物的花、果、枝叶切碎、捣烂,用酒精浸制,所得的浸出液可以作为酸碱指示剂。P82、取食盐水、白醋、石灰水加以试验。并纪录变色情况。那么你会自制酸碱指示剂吗?
许多植物的花果茎叶中都含有某些显色的物质,它们在酸性溶液或碱性溶液里会显示不同的颜色.方法是取这些植物的花果枝叶切碎捣烂,用酒精浸制,所得的浸出液可以作为酸碱指示剂. 红某些花浸出液的变色情况练习:
1、某无色溶液PH=2,该溶液呈 性,它能使紫色石蕊试液变 ,无色酚酞试液 ,使蓝色石蕊试纸变 。酸红色不变色红色2、测得某溶液中仅含Cu2+、K+、Cl-、SO42-四种离子,且阳离子的数量比为Cu2+:K+:Cl-= 3:4:6,则SO42-:Cl- 的比值是………( )
A、3:2 B、1:3
C、1:8 D、2:5 B3、下列物质中存在着能自由移动的氯离子的是---------( )
A、液态氯化氢; B、KCl晶体;
C、KClO3溶液; D、熔化的MgCl2
4、下列各组离子属于酸的电离的是…( )
A、H+、SO42-、Na+ B、OH-、Ba2+
C、H+、NO3- D、Na+、HCO3-DC1、下列物质不属于酸的是 ( )
A、HNO3 B、NaHCO3
C、H3PO4 D、HI
?
2、用简单的方法区别水和硫酸,并写出实验步骤
3、思考:一位科学家在做研究时不小心将盐酸滴到了紫花上,紫花逐渐变红色。看到这么个现象,许多问题在他的脑子里涌现出来,如果你是那个科学家,你会有什么问题,你会有什么想法?
B
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
