3.1 构成物质的基本微粒 (共63张PPT)
文档属性
| 名称 | 3.1 构成物质的基本微粒 (共63张PPT) |
|
|
| 格式 | zip | ||
| 文件大小 | 7.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-12-17 00:00:00 | ||
图片预览







文档简介
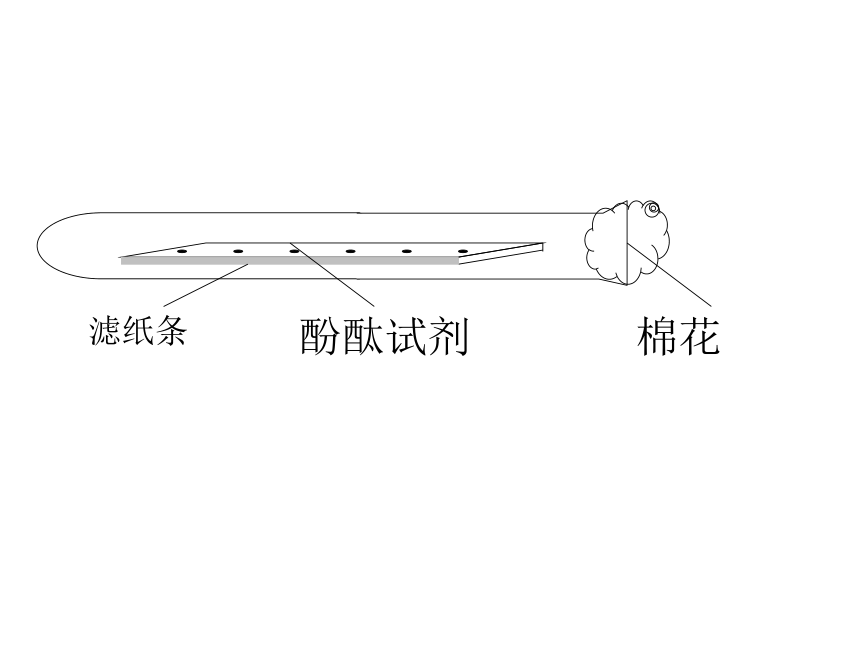
课件63张PPT。 第1节 构成物质的基本微粒 一、微粒的性质湿衣服凉干;
远处闻到花香;
物质的挥发、溶解;
“酒好不怕巷子深”。
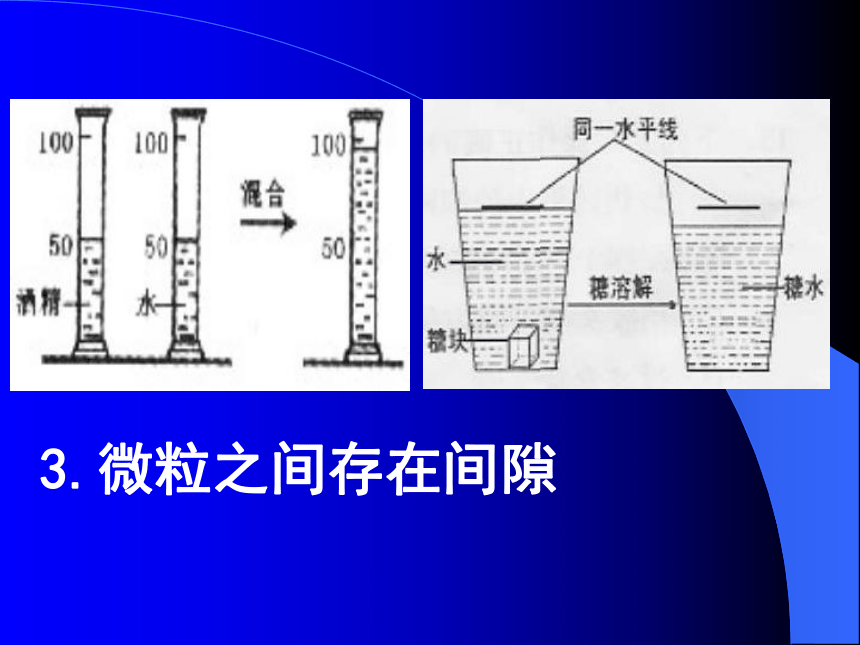
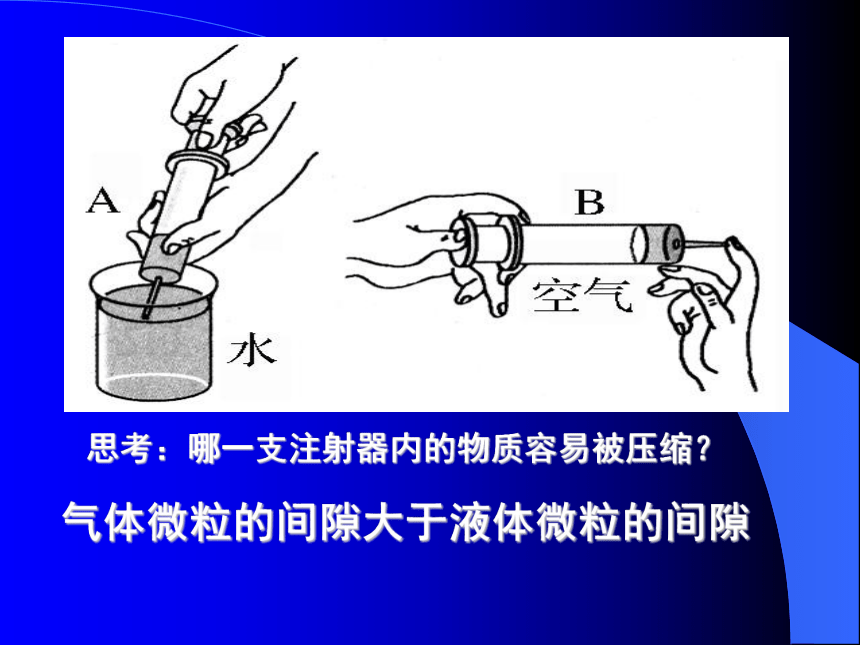
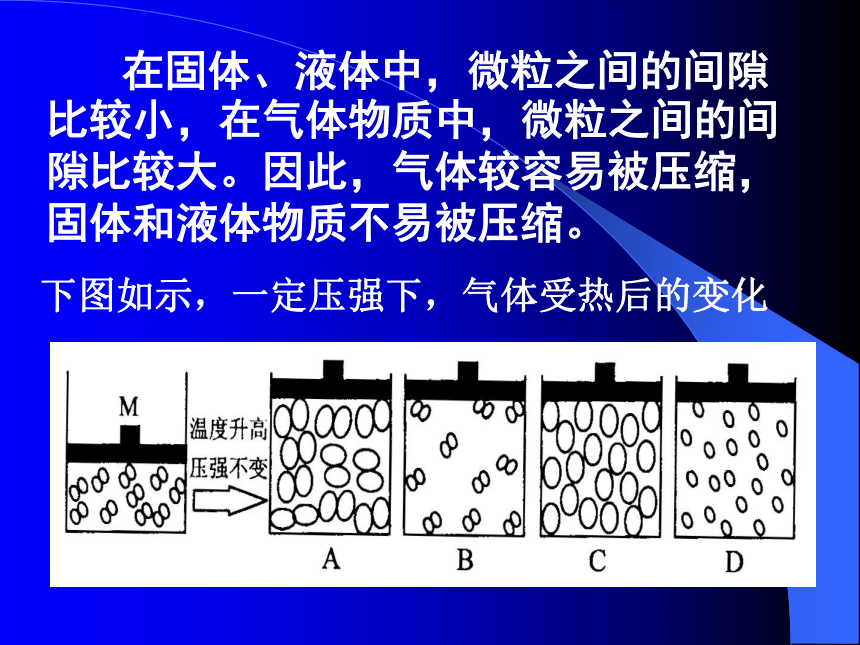
......1.氨水能使无色酚酞变红结论1(氨水中的微粒从一只烧杯跑进另一烧杯中,发生化学变化,使无色酚酞变红)2.微粒总在不停地做无规则运动3.微粒之间存在间隙固态固态 液态液态 气态物质状态的变化微观三维模拟动画思考:哪一支注射器内的物质容易被压缩?气体微粒的间隙大于液体微粒的间隙 在固体、液体中,微粒之间的间隙比较小,在气体物质中,微粒之间的间隙比较大。因此,气体较容易被压缩,固体和液体物质不易被压缩。下图如示,一定压强下,气体受热后的变化( 微粒本身没有变化 )物质的“固态、液态、气态的三态”变化实际上就是微粒之间的间隙发生改变的过程。1.物质都是由极其细小的、肉眼看不见的微粒构成的。
2.微粒总在不停地做无规则的运动;温度越高运动速度越快。
3.构成物质的微粒间存在一定的间隙;固体、液体微粒间间隙小,气体微粒间间隙大。知识梳理构成物质的基本粒子有分子、原子和离子二、分子阿佛加德罗(意大利)
提出了分子学说。分子是构成物质的一种微粒。氧气、水等大多数物质是由分子构成,而且它们的分子不同,导致性质不同。(一)定义分子是保持物质化学性质的最小微粒每个水分子约为3×10-26kg,计算一下一滴水(1/20g)中含有水分子的个数为 多少?
答案:1.7×1021 个 分子有一定的质量和体积,但分子很小,
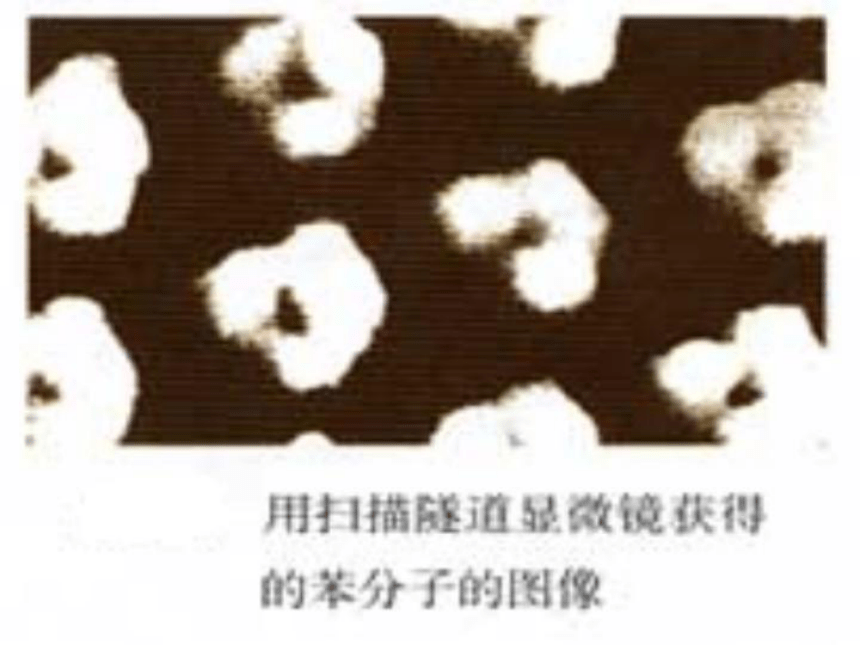
肉眼看不见,不能用天平来称量。分子总在不断运动,分子间有一定间隔。同种分子性质相同,不同种分子性质不同。(二)分子的性质1.分子很小(小)
2.分子不停地运动(动)
3.分子间有空隙(隙)“小东西”三、原子(一)定义:原子是化学变化中的最小微粒原子学说创始人-道尔顿通过移动硅原子构成的文字原子操纵技术(二)性质1. 原子很小
2. 原子不断地运动
3. 原子间有间隙分子与原子的比较在化学变化中,分子可以 再分,而原子不可以再分。原子→分子→物质分子与原子的本质区别:①金属(铜、铁等)
②稀有气体(氦气、氩气等)③部分固态非金属由原子直接构成的物质(金刚石、石墨、磷等 )(三)原子的构成( 汤姆生发现电子 )质子中子电子原子核核外电子原子质子中子一个质子带1个单位正电荷
中子不带电
一个电子带1个单位负电荷1. 几种原子的构成2.核电荷数=质子数=电子数
所以整个原子呈电中性3.原子核在原子中所占的体积很小。电子在核外作高速运动。4. 氢原子: 1个质子、
没有中子、 1个电子。 想一想:1.原子是由哪些粒子构成的?2.原子显电性吗?为什么?例1.原子是( )
不可分割的实心球体
可以构成分子, 也可以直接构成物质
是构成物质的最小微粒
是电中性的微粒,其中组成的各部分
均不显电性B例2.卢瑟福在测定原子构成时做了如下实验:取一极薄的金箔,用一高速运动的a粒子射击,结果发现大多数a粒子通过了金箔,极少数a粒子发生偏转或被弹回。根据上述现象得出的以下结论中,正确的是( )
金原子是实心球体,紧密结合排列
金原子核带正电荷
相对于金原子而言,金原子核体积小,质量大
金原子质量与a粒子质量相当B C (四)原子的质量1. 原子有一定的质量,主要集中在原子核相对原子质量=1个原子质量1个碳原子质量×1/12(2)相对原子质量的计算公式 以一种碳原子的质量的1/12 作为基准,其他原子的质量与这一基准的比,称为这种原子的相对原子质量。(1)概念:2. 相对原子质量(Ar)相对原子质量是个比值,单位是 一、符号是1相对原子质量=质子数+中子数为什么不考虑电子数呢?例3.关于相对原子质量的叙述正确的是( )
A. 相对原子质量等于原子质量
B. 相对原子质量以克为单位
相对原子质量以碳12原子质量的1/12
作为基准
D.相对原子质量是一个比值
C D3.相对分子质量(Mr)已知:H:1、O:16、C:12
那么,CO2 、H2O 的相对分子质量是多少呢 ? 1.下列叙述错误的是 ( )
A.任何原子都是由质子、中子、电子三种
粒子 构成的
B.原子核内的质子数和中子数不一定相等
C.原子核比原子小得多,原子里有很大的空
间,电子就在这个空间里作高速的运动
D.跟质子、中子相比,电子质量很小,所以
原 子的质量主要集中在原子核上一、选择题A2.1999年度诺贝尔化学奖获得者哈迈德·泽维尔开创了“飞秒(10-15 S)化学”的新领域,使运用激光光谱技术观测化学反应时分子中原子的运动成为可能,你认为运用该技术不能观测到的是( )
氧分子的不规则运动
氧原子结合成氧分子的过程
氧分子分解成氧原子的过程
氧原子内部的质子、中子、电子的运动D3.科学家曾通过测定古生物遗骸中的碳14含量推断古城年代。碳14原子的核电荷数为6,相对原子质量为14。下列关于碳14原子的说法中,错误的是 ( )
中子数为6 B. 质子数为6
C. 电子数为6 D. 质子数和中子数之和为14 A4.1991年,我国著名化学家张青莲教授与另一位科学家合作,测定了铟(In)元素的相对原子质量新值。铟元素的核电荷数为49,相对原子质量为115。铟原子的质子数为( )
A. 115 B. 49 C. 66 D. 164
5.相对原子质量是 ( )
A.原子质量 B.原子质量的简称
C.原子数量 D.原子质量与一种碳原子
质量的1/12的比值BD6. 原子是由居于原子______的带___电的_______和核外带___电的______构成的。由于原子核所带电量和核外电子电量______,但电性_______,因此原子______电性。
7. 在原子中,____在原子核外不停地运动,_____和_____是决定原子质量的粒子。 二、填空题中心正负电子原子核相等相反不显电子质子中子8. 下列粒子中带正电荷的是 ___ (填序号)
①电子 ②质子 ③中子 ④原子核
⑤原子 ⑥分子9.把分子、原子、质子、电子分别填入下列有关空格中:
氧化汞 __ 是保持氧化汞化学性质的最小粒子,在加热条件下,氧化汞 ___ 分裂成氧 __ 和汞 ___ ,汞 ___ 直接构成金属汞,而两个氧 ___ 构成一个氧 ___ ,许多氧 ___ 构成氧气。氧原子核内有8个带1个单位正电荷的____ ,核外有8个_____做高速运动。② ④分子分子原子原子原子原子分子分子质子电子四、 离子 (一)核外电子排布规律:2.离核越远,能量越高3.每层最多可排2n2个电子4.最外层不超过8 个电子1.核外电子是分层排布的质子数电子层该层电子数原子结构示意图元素金属元素原子:少于4个电子非金属元素原子:多于4个电子 稀有气体元素原子 :8个(He为2个)稳定结构在化学反应中易失电子在化学反应中易得电子练习1.月球土壤含有大量氦3原子,它可能成为未来核能的重要原料。氦3原子核内有2个质子和1个中子。氦3原子结构示意图是( )练习2.下列粒子在化学反应中容易失去电子的是( )NaNa+AlAl3+ClCl-SS2-元素化学性质与最外层电子数关系密切 (在化学变化中,电中性的原子常会得到或失去电子而成为带电荷的微粒,这种带电荷的微粒称为离子。)(二)定义离子是带电荷的原子或原子团(三)分类阳离子阴离子Na+ Mg2+ NH4+ Cl- O2- CO32-原子阳离子阴离子失电子得电子失电子得电子原子中:质子数 电子数(原子不显电性)阳离子中:质子数 电子数(带正电)原子和离子的联系和区别阴离子中:质子数 电子数(带负电)=><(四)离子结构示意图①原子核②原子的质量③核外电子数⑤电子层数④最外层电子数⑥化学性质(五)离子符号的意义: Mg2+一个镁离子带两
个单位的正电荷2表示两个镁离子一个镁离子钠离子Na+氯离子Cl-NaCl由阴阳离子相互作用而形成的化合物(六)离子化合物如:氯化钠 等(八)分子、原子、离子与物质离子构成物质(如:钠原子)分子构成构成构成得到或失去电子原子(如:钠离子)(如:氧原子)(如:铜原子)(如:氧分子)(如:氧气)(如:铜)(如:氯化钠 )
远处闻到花香;
物质的挥发、溶解;
“酒好不怕巷子深”。
......1.氨水能使无色酚酞变红结论1(氨水中的微粒从一只烧杯跑进另一烧杯中,发生化学变化,使无色酚酞变红)2.微粒总在不停地做无规则运动3.微粒之间存在间隙固态固态 液态液态 气态物质状态的变化微观三维模拟动画思考:哪一支注射器内的物质容易被压缩?气体微粒的间隙大于液体微粒的间隙 在固体、液体中,微粒之间的间隙比较小,在气体物质中,微粒之间的间隙比较大。因此,气体较容易被压缩,固体和液体物质不易被压缩。下图如示,一定压强下,气体受热后的变化( 微粒本身没有变化 )物质的“固态、液态、气态的三态”变化实际上就是微粒之间的间隙发生改变的过程。1.物质都是由极其细小的、肉眼看不见的微粒构成的。
2.微粒总在不停地做无规则的运动;温度越高运动速度越快。
3.构成物质的微粒间存在一定的间隙;固体、液体微粒间间隙小,气体微粒间间隙大。知识梳理构成物质的基本粒子有分子、原子和离子二、分子阿佛加德罗(意大利)
提出了分子学说。分子是构成物质的一种微粒。氧气、水等大多数物质是由分子构成,而且它们的分子不同,导致性质不同。(一)定义分子是保持物质化学性质的最小微粒每个水分子约为3×10-26kg,计算一下一滴水(1/20g)中含有水分子的个数为 多少?
答案:1.7×1021 个 分子有一定的质量和体积,但分子很小,
肉眼看不见,不能用天平来称量。分子总在不断运动,分子间有一定间隔。同种分子性质相同,不同种分子性质不同。(二)分子的性质1.分子很小(小)
2.分子不停地运动(动)
3.分子间有空隙(隙)“小东西”三、原子(一)定义:原子是化学变化中的最小微粒原子学说创始人-道尔顿通过移动硅原子构成的文字原子操纵技术(二)性质1. 原子很小
2. 原子不断地运动
3. 原子间有间隙分子与原子的比较在化学变化中,分子可以 再分,而原子不可以再分。原子→分子→物质分子与原子的本质区别:①金属(铜、铁等)
②稀有气体(氦气、氩气等)③部分固态非金属由原子直接构成的物质(金刚石、石墨、磷等 )(三)原子的构成( 汤姆生发现电子 )质子中子电子原子核核外电子原子质子中子一个质子带1个单位正电荷
中子不带电
一个电子带1个单位负电荷1. 几种原子的构成2.核电荷数=质子数=电子数
所以整个原子呈电中性3.原子核在原子中所占的体积很小。电子在核外作高速运动。4. 氢原子: 1个质子、
没有中子、 1个电子。 想一想:1.原子是由哪些粒子构成的?2.原子显电性吗?为什么?例1.原子是( )
不可分割的实心球体
可以构成分子, 也可以直接构成物质
是构成物质的最小微粒
是电中性的微粒,其中组成的各部分
均不显电性B例2.卢瑟福在测定原子构成时做了如下实验:取一极薄的金箔,用一高速运动的a粒子射击,结果发现大多数a粒子通过了金箔,极少数a粒子发生偏转或被弹回。根据上述现象得出的以下结论中,正确的是( )
金原子是实心球体,紧密结合排列
金原子核带正电荷
相对于金原子而言,金原子核体积小,质量大
金原子质量与a粒子质量相当B C (四)原子的质量1. 原子有一定的质量,主要集中在原子核相对原子质量=1个原子质量1个碳原子质量×1/12(2)相对原子质量的计算公式 以一种碳原子的质量的1/12 作为基准,其他原子的质量与这一基准的比,称为这种原子的相对原子质量。(1)概念:2. 相对原子质量(Ar)相对原子质量是个比值,单位是 一、符号是1相对原子质量=质子数+中子数为什么不考虑电子数呢?例3.关于相对原子质量的叙述正确的是( )
A. 相对原子质量等于原子质量
B. 相对原子质量以克为单位
相对原子质量以碳12原子质量的1/12
作为基准
D.相对原子质量是一个比值
C D3.相对分子质量(Mr)已知:H:1、O:16、C:12
那么,CO2 、H2O 的相对分子质量是多少呢 ? 1.下列叙述错误的是 ( )
A.任何原子都是由质子、中子、电子三种
粒子 构成的
B.原子核内的质子数和中子数不一定相等
C.原子核比原子小得多,原子里有很大的空
间,电子就在这个空间里作高速的运动
D.跟质子、中子相比,电子质量很小,所以
原 子的质量主要集中在原子核上一、选择题A2.1999年度诺贝尔化学奖获得者哈迈德·泽维尔开创了“飞秒(10-15 S)化学”的新领域,使运用激光光谱技术观测化学反应时分子中原子的运动成为可能,你认为运用该技术不能观测到的是( )
氧分子的不规则运动
氧原子结合成氧分子的过程
氧分子分解成氧原子的过程
氧原子内部的质子、中子、电子的运动D3.科学家曾通过测定古生物遗骸中的碳14含量推断古城年代。碳14原子的核电荷数为6,相对原子质量为14。下列关于碳14原子的说法中,错误的是 ( )
中子数为6 B. 质子数为6
C. 电子数为6 D. 质子数和中子数之和为14 A4.1991年,我国著名化学家张青莲教授与另一位科学家合作,测定了铟(In)元素的相对原子质量新值。铟元素的核电荷数为49,相对原子质量为115。铟原子的质子数为( )
A. 115 B. 49 C. 66 D. 164
5.相对原子质量是 ( )
A.原子质量 B.原子质量的简称
C.原子数量 D.原子质量与一种碳原子
质量的1/12的比值BD6. 原子是由居于原子______的带___电的_______和核外带___电的______构成的。由于原子核所带电量和核外电子电量______,但电性_______,因此原子______电性。
7. 在原子中,____在原子核外不停地运动,_____和_____是决定原子质量的粒子。 二、填空题中心正负电子原子核相等相反不显电子质子中子8. 下列粒子中带正电荷的是 ___ (填序号)
①电子 ②质子 ③中子 ④原子核
⑤原子 ⑥分子9.把分子、原子、质子、电子分别填入下列有关空格中:
氧化汞 __ 是保持氧化汞化学性质的最小粒子,在加热条件下,氧化汞 ___ 分裂成氧 __ 和汞 ___ ,汞 ___ 直接构成金属汞,而两个氧 ___ 构成一个氧 ___ ,许多氧 ___ 构成氧气。氧原子核内有8个带1个单位正电荷的____ ,核外有8个_____做高速运动。② ④分子分子原子原子原子原子分子分子质子电子四、 离子 (一)核外电子排布规律:2.离核越远,能量越高3.每层最多可排2n2个电子4.最外层不超过8 个电子1.核外电子是分层排布的质子数电子层该层电子数原子结构示意图元素金属元素原子:少于4个电子非金属元素原子:多于4个电子 稀有气体元素原子 :8个(He为2个)稳定结构在化学反应中易失电子在化学反应中易得电子练习1.月球土壤含有大量氦3原子,它可能成为未来核能的重要原料。氦3原子核内有2个质子和1个中子。氦3原子结构示意图是( )练习2.下列粒子在化学反应中容易失去电子的是( )NaNa+AlAl3+ClCl-SS2-元素化学性质与最外层电子数关系密切 (在化学变化中,电中性的原子常会得到或失去电子而成为带电荷的微粒,这种带电荷的微粒称为离子。)(二)定义离子是带电荷的原子或原子团(三)分类阳离子阴离子Na+ Mg2+ NH4+ Cl- O2- CO32-原子阳离子阴离子失电子得电子失电子得电子原子中:质子数 电子数(原子不显电性)阳离子中:质子数 电子数(带正电)原子和离子的联系和区别阴离子中:质子数 电子数(带负电)=><(四)离子结构示意图①原子核②原子的质量③核外电子数⑤电子层数④最外层电子数⑥化学性质(五)离子符号的意义: Mg2+一个镁离子带两
个单位的正电荷2表示两个镁离子一个镁离子钠离子Na+氯离子Cl-NaCl由阴阳离子相互作用而形成的化合物(六)离子化合物如:氯化钠 等(八)分子、原子、离子与物质离子构成物质(如:钠原子)分子构成构成构成得到或失去电子原子(如:钠离子)(如:氧原子)(如:铜原子)(如:氧分子)(如:氧气)(如:铜)(如:氯化钠 )
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
