4.2 化学反应中的质量关系(44张PPT)
文档属性
| 名称 | 4.2 化学反应中的质量关系(44张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-12-17 00:00:00 | ||
图片预览










文档简介
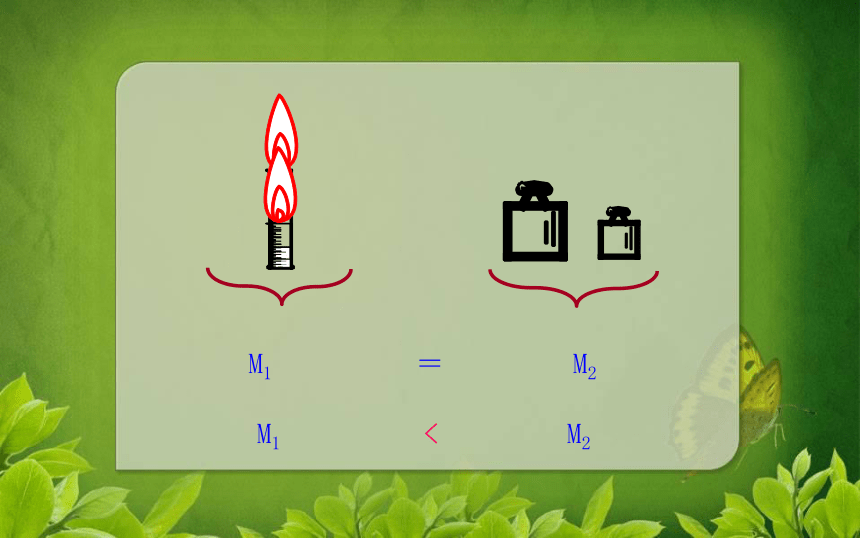
课件44张PPT。复习燃烧?燃烧的条件?爆炸?灭火? 第二节 化学反应中的质量关系 质量守恒定律授课人 唐克保 化学变化发生时,一定有新物质生成,还会伴随着能量的释放或吸收,有时还会发生颜色变化、或生成沉淀、产生气体等现象。那么,在化学变化中物质的质量会发生变化吗?怎样判断化学反应已经发生?课前实验:蜡烛燃烧前后质量测定讨 论1、在实验中,石蜡和氧气反应后情况如何?2、石蜡和氧气反应前后物质的总质量是否改变?请想一想?课前实验小结产生的现象:蜡烛燃烧,逐渐变短,天平发生偏转。蜡烛+氧气→二氧化碳+水 M1 = M2 M1 < M2思考这些物质:火柴、酒精燃烧最后留下什么?铜片在火焰上加热呢?它们的质量有什么变化?○火柴燃烧最后剩下灰烬
○酒精充分燃烧最后连灰烬都没有留下
该化学变化中物质质量变小了吗?○表面变黑,质量变大。
该化学变化中物质质量变大了吗?你猜得着吗?物质发生化学变化前后,总质量到底是增加、减小、还是不变?对物质变化进行定量研究1.提出问题:物质发生变化前后,总质量是否发生改变?参加化学反应的各物质都发生了变化,并有新物质生产。那么,参加反应的各物质质量总和与反应生成的各物质质量总和相比较,是否发生了变化?
2. 猜想与假设:(物质发生化学变化后,其总质量会怎样?)
3. 设计实验方案验证
4. 进行实验探究活动
我们带着这几点来进行实验探究增加?减少?不变?提出问题→作出猜想→设计方案→进行实验→得出结论5.得出结论实验探究实验前,讨论实验步骤。
观察反应物的颜色、状态;
反应时有什么现象发生?
反应前后物质的总质量有没有变化?
完成所附表格。
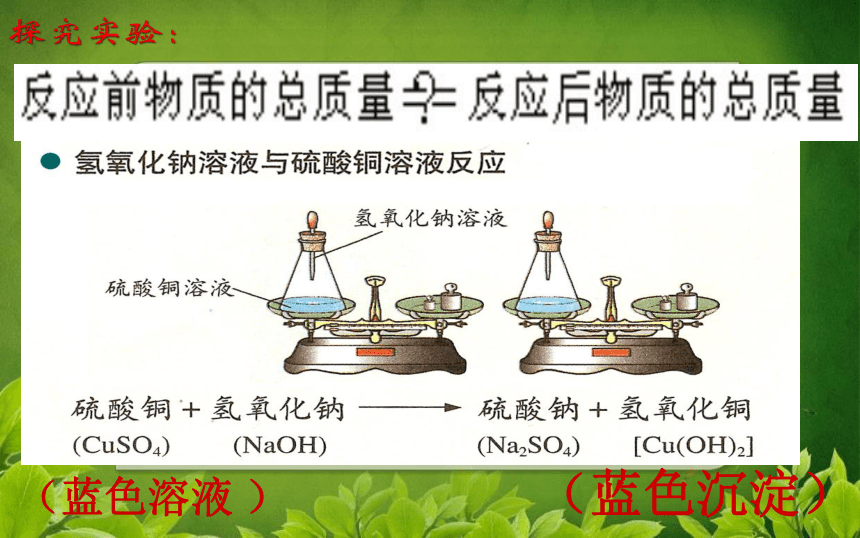
实验后交流讨论。课本P102图4—11氢氧化钠溶液与硫酸铜溶液反应 图4—12碳酸钙与稀盐酸反应 ⑴在锥形瓶中加入蓝色硫酸铜溶液,胶头滴里是氢氧化钠溶液;⑵称量锥形瓶内物质的总质量;为M1。实验1:氢氧化钠溶液跟硫酸铜溶液反应前后质量的测定⑶挤压胶头滴管里的氢氧化钠溶液,使二者反应,观察现象。⑷称量锥形瓶内物质的总质量,为M2.活动与探究一
(蓝色溶液 ) (蓝色沉淀) M1 = M2现象:产生蓝色絮状沉淀;溶液的蓝色逐渐变浅;且天平仍然保持平衡 结论:反应前后,物质的总质量相等CuSO4 NaOH Na2SO4 Cu(OH)2 实验2 石灰石与稀盐酸反应
有气体放出
在锥形瓶中加入适量的石灰石,在试管里装入适量稀盐酸,将其放在在天平左盘里,然后颠倒使其混合反应,观察现象。
实验2演示:盐酸与碳酸钙的反应 M1 M2 M1 M2现象:产生无色气泡。氯化钙+水+二氧化碳碳酸钙+盐酸CaCO3CaCl2HClCO2H2O实验2小结>=质量守恒定律生成的各物质的质量总和 参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。参加反应的各物质的质量总和所有实验证明质量守恒定律 参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。理解质量守恒定律的定义时要注意: 1.质量守恒定律的“守恒”指的是质量守恒,其它
方面如体积等不一定守恒。2.是指“参加反应的各物质” 的质量总和,没有
参加反应的物质不包括在内。如“1g氢气和9g氧气反应生成10g水”是错误的。不是任意数值的简单加和而是各反应物间按一定质量比反应的。 3.“反应生成的物质”仅指该反应过程中新生成的物质
质量,在反应之前已经存在的质量不计算在内。如1g氢气在盛有9g氧气的水中(水的质量为2g)反应生成12g水。4.质量守恒定律只适用于一切化学反应,不涉及物
理变化。如“10g冰加热后变成了10g水蒸气”符合质量守恒定律也是错误的。5.“生成的各物质的质量总和”,应当包括生成的各种
物质,如沉淀、气体等。反思1实验中要注意哪些问题?1)装置气密性良好;
2)用注射器滴加可控制速度,防止反应
速度过快。波义耳的实验(1673年)拉瓦锡的实验(1777年)失败成功至此,质量守恒定律才获得公认。1、化学反应的实质是什么?
拆分 重新组合 聚集
分子-→原子-→新分子-→新物质
变成 构成 化学反应的实质:元素种类变了吗?元素质量变了吗?分子数目变了吗?化学反应前后物质种类呢?分子种类呢?动脑筋不变改变可能改变 为什么“参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和”呢? 你能用物质由微粒构成的观点对质量守恒定律作出解释吗?请以金属镁和氧气的反应为例说明。 Mg O2 Mg O 化学反应是反应物的原子重新组合转变成生成物的过程 2 Mg+O22Mg O点燃原子数:氧原子:2
镁原子:2氧原子:2
镁原子:2相对质量:24×2+16×2=802×(24 +16 )=80参加反应的各物质质量总和反应生成的各物质质量总和化学反应前后原子数目、原子种类原子数目、原子种类都没有改变 思考:某同学定量研究化学反应时发现:木炭燃烧后质量减小了,而铁钉生锈后质量增加了。这些现象与质量守恒定律有矛盾吗?1.木炭燃烧 C+O2 CO2
生成物二氧化碳是一种气体跑到空气中去了,所以质量减少了。点燃2.铁钉之所以会生锈是因为
铁与空气中的氧气发生了缓慢 氧化,所以最后生成的铁锈的质量不仅包括铁的质量还包括参加反应的氧气的质量 原子数目没有增减原子种类没有改变原子质量没有变化化学反应前后质量守恒的原因用微观角度来解释H2O H2 ↑+ O2↑通电结论:化学变化(反应)中,原子
种类、原子数目都不发生改变为什么反应前后质量不变呢?原因分析文字表达式:磷+氧气 五氧化二磷点燃化学反应前后:原子个数不变
原子种类不变
原子质量不变元素种类不变
元素质量不变反应前后物质质量不变原子数目原子质量原子种类元素质量元素种类物质的种类分子的种类可能
改变分子数目化学变化的本质:元素化合价质量守恒定律适用于一切化学反应1. 进行有关的计算 2. 推测一些物质的组成 3. 解释一些实验事实我们可以运用该定律:1、在反应A+B=C+D中,已知2gA和5gB参加了反应,生成了4gC,则有____gD生成。 三.质量守恒定律的简单应用32、 将24.5g氯酸钾加热至完全分解,得到固体质量14.9g,则产生气体 g。
3、加热10g氯酸钾和二氧化锰的混合物,反应后称得残留物的质量总和为9.52g,则生成氧气的质量为 g9.60.48练习与实践判断对错:
1.因为“质量守恒”所以煤燃烧后产生的煤渣的质量一定和所用煤的质量相等 ( )×2.H2和O2形成混合物的质量等于其反应后生成水的质量( )×1、在 A + B —— C 的反应中,5克A和4克B恰好完全反应,求生成的C的质量。
2、在 A + B —— C 的反应中,5克A和4克B充分反应后,剩余1克B,求生成的C的质量。
3、在 A + B —— C 的反应中,5克A和4克B能恰好完全反应,如 5克A和6克B充分反应后,生成C的质量为多少?
9克8克我能行:9克4、已知石蜡是蜡烛的主要成分,蜡烛在空气中完全燃烧后的产物是CO2和H2O,判断石蜡中一定含有_______元素,可能含有___元素。C、HO5、在化学反应2XY2+Y2=2Z中Z的化学式为( )
A、X2Y3 B、XY3
C、X2Y6 D、X2Y4B4.镁带在密闭的容器中加热,其总质量与时间的关系正确的是 ( )B5.汽油、煤油、柴油(主要含碳、氢元素)等燃料都是从石油中提炼出来的。一些人声称可以使“水变燃油”,从而解决世界性的能源问题。你认为这些人的说法正确吗?理由是什么? ×碳、氢点燃2∶1∶28.在一定密闭容器内有X、Y、Z、Q四种物质,在
一定条件下充分反应后,测得反应前后各物质的质
量如下求反应后X的质量____,该反应属于______反应.55分解智者一切求自己,愚者一切求他人。
○酒精充分燃烧最后连灰烬都没有留下
该化学变化中物质质量变小了吗?○表面变黑,质量变大。
该化学变化中物质质量变大了吗?你猜得着吗?物质发生化学变化前后,总质量到底是增加、减小、还是不变?对物质变化进行定量研究1.提出问题:物质发生变化前后,总质量是否发生改变?参加化学反应的各物质都发生了变化,并有新物质生产。那么,参加反应的各物质质量总和与反应生成的各物质质量总和相比较,是否发生了变化?
2. 猜想与假设:(物质发生化学变化后,其总质量会怎样?)
3. 设计实验方案验证
4. 进行实验探究活动
我们带着这几点来进行实验探究增加?减少?不变?提出问题→作出猜想→设计方案→进行实验→得出结论5.得出结论实验探究实验前,讨论实验步骤。
观察反应物的颜色、状态;
反应时有什么现象发生?
反应前后物质的总质量有没有变化?
完成所附表格。
实验后交流讨论。课本P102图4—11氢氧化钠溶液与硫酸铜溶液反应 图4—12碳酸钙与稀盐酸反应 ⑴在锥形瓶中加入蓝色硫酸铜溶液,胶头滴里是氢氧化钠溶液;⑵称量锥形瓶内物质的总质量;为M1。实验1:氢氧化钠溶液跟硫酸铜溶液反应前后质量的测定⑶挤压胶头滴管里的氢氧化钠溶液,使二者反应,观察现象。⑷称量锥形瓶内物质的总质量,为M2.活动与探究一
(蓝色溶液 ) (蓝色沉淀) M1 = M2现象:产生蓝色絮状沉淀;溶液的蓝色逐渐变浅;且天平仍然保持平衡 结论:反应前后,物质的总质量相等CuSO4 NaOH Na2SO4 Cu(OH)2 实验2 石灰石与稀盐酸反应
有气体放出
在锥形瓶中加入适量的石灰石,在试管里装入适量稀盐酸,将其放在在天平左盘里,然后颠倒使其混合反应,观察现象。
实验2演示:盐酸与碳酸钙的反应 M1 M2 M1 M2现象:产生无色气泡。氯化钙+水+二氧化碳碳酸钙+盐酸CaCO3CaCl2HClCO2H2O实验2小结>=质量守恒定律生成的各物质的质量总和 参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。参加反应的各物质的质量总和所有实验证明质量守恒定律 参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。理解质量守恒定律的定义时要注意: 1.质量守恒定律的“守恒”指的是质量守恒,其它
方面如体积等不一定守恒。2.是指“参加反应的各物质” 的质量总和,没有
参加反应的物质不包括在内。如“1g氢气和9g氧气反应生成10g水”是错误的。不是任意数值的简单加和而是各反应物间按一定质量比反应的。 3.“反应生成的物质”仅指该反应过程中新生成的物质
质量,在反应之前已经存在的质量不计算在内。如1g氢气在盛有9g氧气的水中(水的质量为2g)反应生成12g水。4.质量守恒定律只适用于一切化学反应,不涉及物
理变化。如“10g冰加热后变成了10g水蒸气”符合质量守恒定律也是错误的。5.“生成的各物质的质量总和”,应当包括生成的各种
物质,如沉淀、气体等。反思1实验中要注意哪些问题?1)装置气密性良好;
2)用注射器滴加可控制速度,防止反应
速度过快。波义耳的实验(1673年)拉瓦锡的实验(1777年)失败成功至此,质量守恒定律才获得公认。1、化学反应的实质是什么?
拆分 重新组合 聚集
分子-→原子-→新分子-→新物质
变成 构成 化学反应的实质:元素种类变了吗?元素质量变了吗?分子数目变了吗?化学反应前后物质种类呢?分子种类呢?动脑筋不变改变可能改变 为什么“参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和”呢? 你能用物质由微粒构成的观点对质量守恒定律作出解释吗?请以金属镁和氧气的反应为例说明。 Mg O2 Mg O 化学反应是反应物的原子重新组合转变成生成物的过程 2 Mg+O22Mg O点燃原子数:氧原子:2
镁原子:2氧原子:2
镁原子:2相对质量:24×2+16×2=802×(24 +16 )=80参加反应的各物质质量总和反应生成的各物质质量总和化学反应前后原子数目、原子种类原子数目、原子种类都没有改变 思考:某同学定量研究化学反应时发现:木炭燃烧后质量减小了,而铁钉生锈后质量增加了。这些现象与质量守恒定律有矛盾吗?1.木炭燃烧 C+O2 CO2
生成物二氧化碳是一种气体跑到空气中去了,所以质量减少了。点燃2.铁钉之所以会生锈是因为
铁与空气中的氧气发生了缓慢 氧化,所以最后生成的铁锈的质量不仅包括铁的质量还包括参加反应的氧气的质量 原子数目没有增减原子种类没有改变原子质量没有变化化学反应前后质量守恒的原因用微观角度来解释H2O H2 ↑+ O2↑通电结论:化学变化(反应)中,原子
种类、原子数目都不发生改变为什么反应前后质量不变呢?原因分析文字表达式:磷+氧气 五氧化二磷点燃化学反应前后:原子个数不变
原子种类不变
原子质量不变元素种类不变
元素质量不变反应前后物质质量不变原子数目原子质量原子种类元素质量元素种类物质的种类分子的种类可能
改变分子数目化学变化的本质:元素化合价质量守恒定律适用于一切化学反应1. 进行有关的计算 2. 推测一些物质的组成 3. 解释一些实验事实我们可以运用该定律:1、在反应A+B=C+D中,已知2gA和5gB参加了反应,生成了4gC,则有____gD生成。 三.质量守恒定律的简单应用32、 将24.5g氯酸钾加热至完全分解,得到固体质量14.9g,则产生气体 g。
3、加热10g氯酸钾和二氧化锰的混合物,反应后称得残留物的质量总和为9.52g,则生成氧气的质量为 g9.60.48练习与实践判断对错:
1.因为“质量守恒”所以煤燃烧后产生的煤渣的质量一定和所用煤的质量相等 ( )×2.H2和O2形成混合物的质量等于其反应后生成水的质量( )×1、在 A + B —— C 的反应中,5克A和4克B恰好完全反应,求生成的C的质量。
2、在 A + B —— C 的反应中,5克A和4克B充分反应后,剩余1克B,求生成的C的质量。
3、在 A + B —— C 的反应中,5克A和4克B能恰好完全反应,如 5克A和6克B充分反应后,生成C的质量为多少?
9克8克我能行:9克4、已知石蜡是蜡烛的主要成分,蜡烛在空气中完全燃烧后的产物是CO2和H2O,判断石蜡中一定含有_______元素,可能含有___元素。C、HO5、在化学反应2XY2+Y2=2Z中Z的化学式为( )
A、X2Y3 B、XY3
C、X2Y6 D、X2Y4B4.镁带在密闭的容器中加热,其总质量与时间的关系正确的是 ( )B5.汽油、煤油、柴油(主要含碳、氢元素)等燃料都是从石油中提炼出来的。一些人声称可以使“水变燃油”,从而解决世界性的能源问题。你认为这些人的说法正确吗?理由是什么? ×碳、氢点燃2∶1∶28.在一定密闭容器内有X、Y、Z、Q四种物质,在
一定条件下充分反应后,测得反应前后各物质的质
量如下求反应后X的质量____,该反应属于______反应.55分解智者一切求自己,愚者一切求他人。
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
