第一章 第四节 几种重要的盐(2)[上学期]
文档属性
| 名称 | 第一章 第四节 几种重要的盐(2)[上学期] |

|
|
| 格式 | rar | ||
| 文件大小 | 39.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2006-09-12 00:00:00 | ||
图片预览





文档简介
课件24张PPT。第四节 几种重要的盐(第二课时)思考:下列化合物,哪些属于酸? 哪些属于碱?哪些属于盐? 判断化合物类别:
HCl 、NaOH、NaCl、HNO3、Ca(OH)2、Na2CO3、H2SO4、Fe(OH)3、CuSO4、Cu(OH)2 盐的溶解性口诀 ?? K+ 、Na+ 、NH4+ 、NO3- 盐都溶;
盐酸盐(氯化物)有AgCl不溶;
硫酸盐有BaSO4不溶,还有银钙是微溶;
碳酸、磷酸盐,只溶 钾、钠、铵。 可溶性的碱:
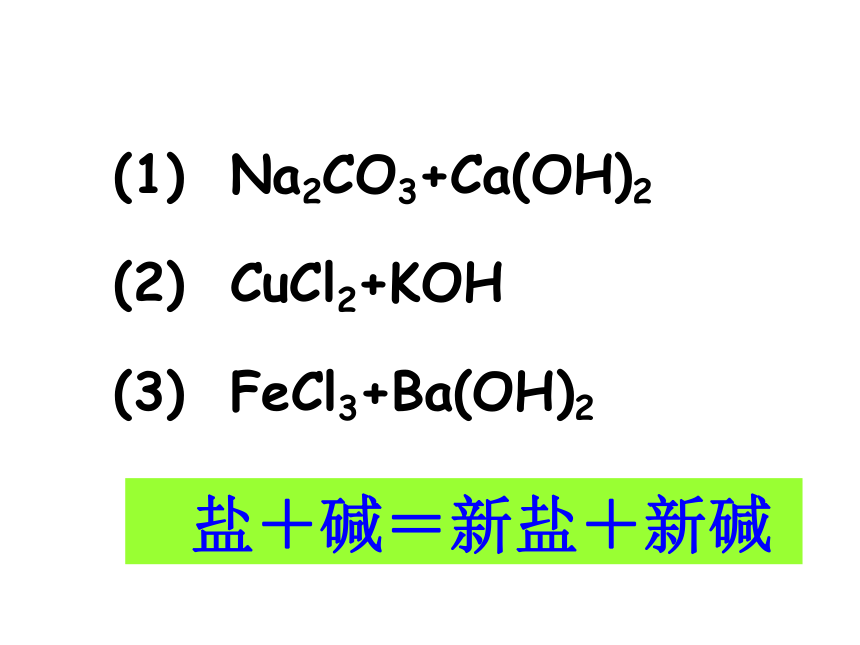
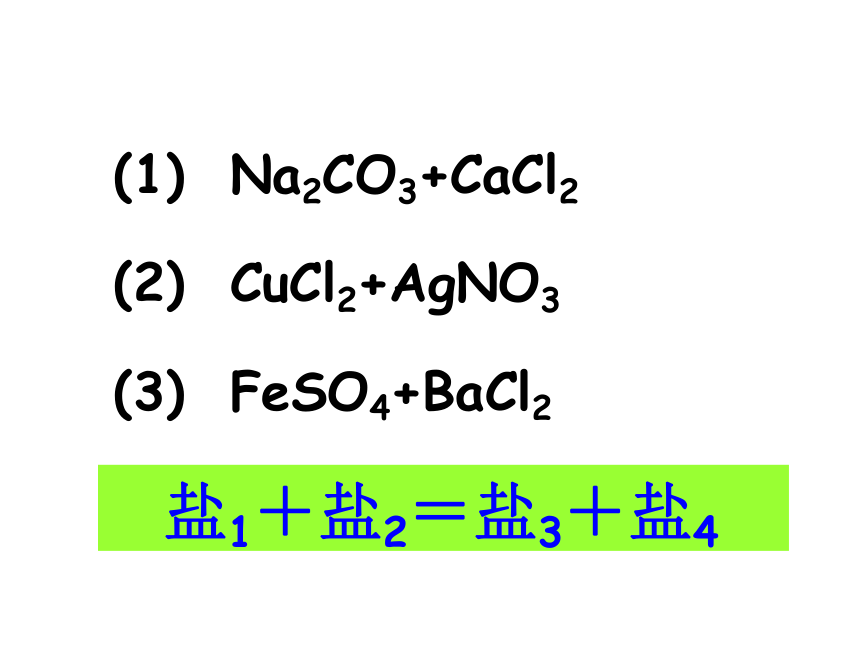
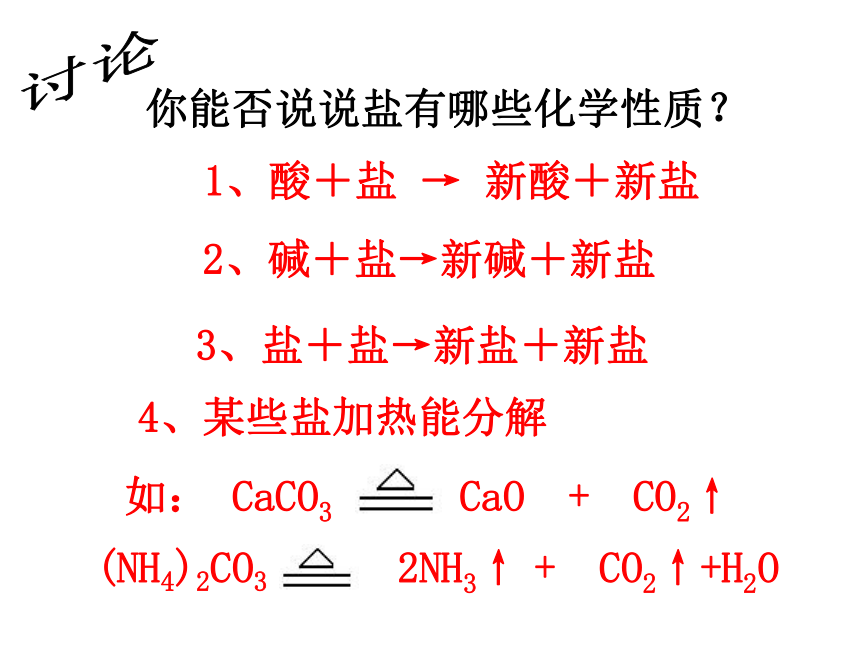
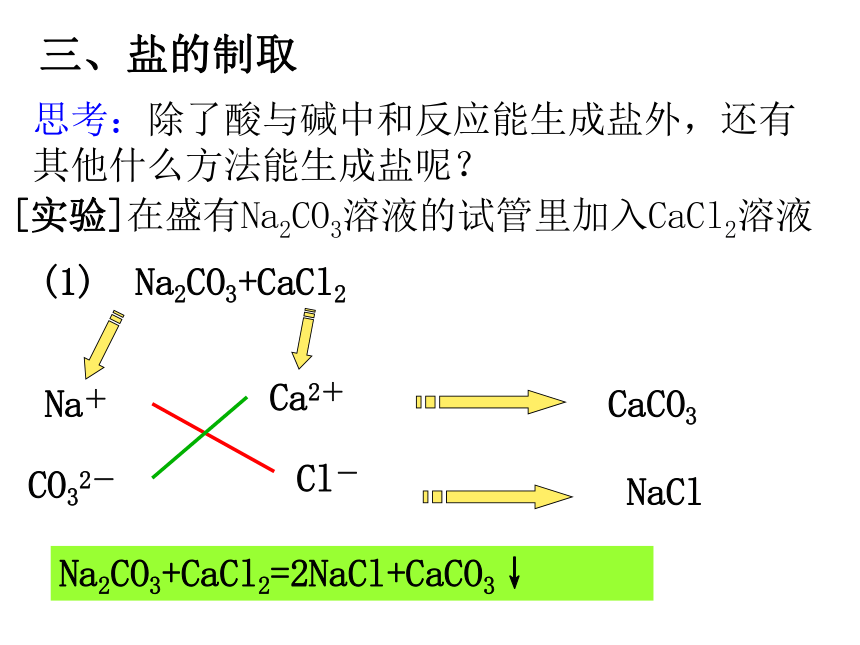
KOH、NaOH、 NH4OH 、Ba(OH) 2不溶性的酸:H2SiO3 书写下列方程式: 盐+酸=新盐+新酸(1) Na2CO3+HCl (2) AgNO3+HCl (3) BaCl2+H2SO4 盐+碱=新盐+新碱(1) Na2CO3+Ca(OH)2(2) CuCl2+KOH (3) FeCl3+Ba(OH)2 盐1+盐2=盐3+盐4(1) Na2CO3+CaCl2(2) CuCl2+AgNO3(3) FeSO4+BaCl2 如: CaCO3 CaO + CO2↑ 你能否说说盐有哪些化学性质?讨论 1、酸+盐 → 新酸+新盐 2、碱+盐→新碱+新盐 3、盐+盐→新盐+新盐4、某些盐加热能分解 (NH4)2CO3 2NH3↑ + CO2↑+H2O(1) Na2CO3+CaCl2 Na+ CO32-Cl-Ca2+CaCO3 NaClNa2CO3+CaCl2=2NaCl+CaCO3↓[实验]在盛有Na2CO3溶液的试管里加入CaCl2溶液思考:除了酸与碱中和反应能生成盐外,还有其他什么方法能生成盐呢?三、盐的制取 复分解反应: 两种化合物互相交换成分生成另外两种化合物的反应。 讨论:中和反应是不是复分解反应? NaOH + HCl Na+ OH-Cl-H+H2O NaClNaOH+HCl=NaCl+H2O中和反应也是复分解反应。复分解反应及发生条件 AB + CD = AD + CB为什么KNO3和NaCl不发生复分解反应?K+ + NO3- + Na+ + Cl- = Na++ NO3- + K+ + Cl- KClNaNO3+金属+酸=盐+氢气
金属氧化物+酸=盐+水
酸+碱=盐+水
酸+盐=新酸+新盐
非金属氧化物+碱=盐+水
碱+盐=新盐+新碱
盐1+盐2= 盐3+盐4想一想:哪些反应可以产生盐?5、来源:
A:天然存在(纯碱)(温度降低析出),如在内蒙古盐湖中提取。
B:化学方法生产
C:侯德榜与制碱(见阅读材料P24) 纯碱工业始创于18世纪,在很长一段时间内制碱技术把持在英、法、德、美等西方发达国家手中。1921年正在美国留学的侯德榜先生为了发展我国的民族工业,应爱国实业家范旭东先生之邀毅然回国,潜心研究制碱技术,成功地摸索和改进了西方的制碱方法,发明了将制碱与制氨结合起来的联合制碱法(又称侯氏制碱法)。侯德榜为纯碱和氮肥工业技术的发展做出了杰出的贡献。“庄稼一枝花,全靠肥当家”化肥:用矿物、空气、水等做原料,经过化学加工精制而成,能为农作物的生长提供养料的一些盐,称为化学肥料,简称为“化肥”。氮肥:给植物生长提供氮元素。NH4+NO3-尿素磷肥:给植物生长提供磷元素。过磷酸钙CaSO4和
Ca(H2PO4)2重过磷酸钙Ca(H2PO4)2钾肥:给植物生长提供钾元素。钾盐:含K+的盐草木灰:主要成分K2CO3思考:在农村,人们常取少量白色粉末状的化肥和消石灰一起放在手掌心搓,通过闻气味来检验是否是氮肥,这是根据什么原理?[活动]
1.向硫酸铵浓溶液中加氢氧化钠溶液,发生什么变化?
2.把湿润的红色石蕊试纸放在试管口,试纸颜色是否发生变化?原因是什么?
有刺激性气体生成(变蓝;气体溶于水,溶液显碱性)思考:如何证明某氮肥是否是氨态氮肥(即是否含NH4+)?NH4+检验:先加碱(NaOH),闻是否产生刺激性气味的气体,或观察气体能否使湿润红色石蕊试纸变蓝。情景:
①细心的农民问我:夏天雷雨过后,田里的庄稼长得特别旺盛。听说你在学校里学过,你能告诉我其中的秘密吗?
②一位老大爷给我讲:70年代刚使用化肥时,生产队里种黄豆,为确保增产,施用了大量尿素。夏天时,黄豆苗生长非常旺盛,农民很高兴。结果,到了秋天,黄豆的结实率很低。相反,漏掉施尿素的地方,黄豆结实却较丰厚,令人哭笑不得。
?
HCl 、NaOH、NaCl、HNO3、Ca(OH)2、Na2CO3、H2SO4、Fe(OH)3、CuSO4、Cu(OH)2 盐的溶解性口诀 ?? K+ 、Na+ 、NH4+ 、NO3- 盐都溶;
盐酸盐(氯化物)有AgCl不溶;
硫酸盐有BaSO4不溶,还有银钙是微溶;
碳酸、磷酸盐,只溶 钾、钠、铵。 可溶性的碱:
KOH、NaOH、 NH4OH 、Ba(OH) 2不溶性的酸:H2SiO3 书写下列方程式: 盐+酸=新盐+新酸(1) Na2CO3+HCl (2) AgNO3+HCl (3) BaCl2+H2SO4 盐+碱=新盐+新碱(1) Na2CO3+Ca(OH)2(2) CuCl2+KOH (3) FeCl3+Ba(OH)2 盐1+盐2=盐3+盐4(1) Na2CO3+CaCl2(2) CuCl2+AgNO3(3) FeSO4+BaCl2 如: CaCO3 CaO + CO2↑ 你能否说说盐有哪些化学性质?讨论 1、酸+盐 → 新酸+新盐 2、碱+盐→新碱+新盐 3、盐+盐→新盐+新盐4、某些盐加热能分解 (NH4)2CO3 2NH3↑ + CO2↑+H2O(1) Na2CO3+CaCl2 Na+ CO32-Cl-Ca2+CaCO3 NaClNa2CO3+CaCl2=2NaCl+CaCO3↓[实验]在盛有Na2CO3溶液的试管里加入CaCl2溶液思考:除了酸与碱中和反应能生成盐外,还有其他什么方法能生成盐呢?三、盐的制取 复分解反应: 两种化合物互相交换成分生成另外两种化合物的反应。 讨论:中和反应是不是复分解反应? NaOH + HCl Na+ OH-Cl-H+H2O NaClNaOH+HCl=NaCl+H2O中和反应也是复分解反应。复分解反应及发生条件 AB + CD = AD + CB为什么KNO3和NaCl不发生复分解反应?K+ + NO3- + Na+ + Cl- = Na++ NO3- + K+ + Cl- KClNaNO3+金属+酸=盐+氢气
金属氧化物+酸=盐+水
酸+碱=盐+水
酸+盐=新酸+新盐
非金属氧化物+碱=盐+水
碱+盐=新盐+新碱
盐1+盐2= 盐3+盐4想一想:哪些反应可以产生盐?5、来源:
A:天然存在(纯碱)(温度降低析出),如在内蒙古盐湖中提取。
B:化学方法生产
C:侯德榜与制碱(见阅读材料P24) 纯碱工业始创于18世纪,在很长一段时间内制碱技术把持在英、法、德、美等西方发达国家手中。1921年正在美国留学的侯德榜先生为了发展我国的民族工业,应爱国实业家范旭东先生之邀毅然回国,潜心研究制碱技术,成功地摸索和改进了西方的制碱方法,发明了将制碱与制氨结合起来的联合制碱法(又称侯氏制碱法)。侯德榜为纯碱和氮肥工业技术的发展做出了杰出的贡献。“庄稼一枝花,全靠肥当家”化肥:用矿物、空气、水等做原料,经过化学加工精制而成,能为农作物的生长提供养料的一些盐,称为化学肥料,简称为“化肥”。氮肥:给植物生长提供氮元素。NH4+NO3-尿素磷肥:给植物生长提供磷元素。过磷酸钙CaSO4和
Ca(H2PO4)2重过磷酸钙Ca(H2PO4)2钾肥:给植物生长提供钾元素。钾盐:含K+的盐草木灰:主要成分K2CO3思考:在农村,人们常取少量白色粉末状的化肥和消石灰一起放在手掌心搓,通过闻气味来检验是否是氮肥,这是根据什么原理?[活动]
1.向硫酸铵浓溶液中加氢氧化钠溶液,发生什么变化?
2.把湿润的红色石蕊试纸放在试管口,试纸颜色是否发生变化?原因是什么?
有刺激性气体生成(变蓝;气体溶于水,溶液显碱性)思考:如何证明某氮肥是否是氨态氮肥(即是否含NH4+)?NH4+检验:先加碱(NaOH),闻是否产生刺激性气味的气体,或观察气体能否使湿润红色石蕊试纸变蓝。情景:
①细心的农民问我:夏天雷雨过后,田里的庄稼长得特别旺盛。听说你在学校里学过,你能告诉我其中的秘密吗?
②一位老大爷给我讲:70年代刚使用化肥时,生产队里种黄豆,为确保增产,施用了大量尿素。夏天时,黄豆苗生长非常旺盛,农民很高兴。结果,到了秋天,黄豆的结实率很低。相反,漏掉施尿素的地方,黄豆结实却较丰厚,令人哭笑不得。
?
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
