几种重要的盐(第2课时)[上学期]
图片预览





文档简介
课件17张PPT。三、盐的制取 实验:在盛有碳酸钠溶液的试管中加入氯化钙溶液,观察实验现象?白色沉淀反应原理Na2CO3溶液
中含有的离子CaCI2溶液
中含有的离子2Na+CO32—Ca2+2CI—Na2CO3+CaCl2 = CaCO3↓+ 2NaCl请同学们分别写出酸与碱、盐与碱、盐与盐反应的化学方程式。 练 习
2NaOH + H2SO4 = Na2SO4 + 2H2OFeCl3 + 3NaOH = Fe(OH)3↓ + 3NaClNa2CO3+CaCl2 = CaCO3↓+ 2NaCl你能找出上述反应类型有什么特点?复分解反应: 两种化合物互相交换成分生成两种新的化合物的反应。 思考:中和反应是否是复分解反应?小结 钾钠铵盐都可溶
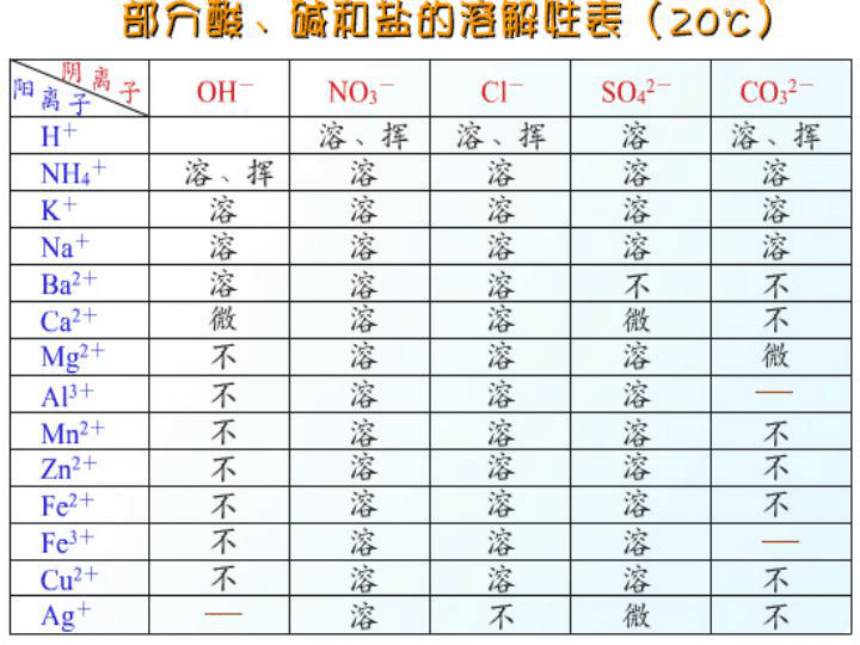
硝酸盐遇水影无踪
盐酸盐不溶氯化银
硫酸盐不溶硫酸钡
溶碱钾钠铵和钡
氢氧化钙微溶水
溶 解 性 口 诀微溶物质:氢氧化钙 硫酸钙
硫酸银 碳酸镁下列物质能发生化学反应吗?为什么?1、CuO+Ba(OH)2= Cu(OH)2 ↓ +BaO
2、SO2+HNO3=
3、2Fe(OH)3+3MgCl2= 2FeCl3+3Mg (OH)2 ↓
4、Na2CO3+CaCl2 = CaCO3 ↓ +2NaCl
5、Na2CO3+2HCl= 2Na Cl +H2CO3
6、 Ba(OH)2+H2SO4= BaSO4 ↓ +2H2 O
7、NaOH+BaCl2= Ba(OH)2+NaCl
8、2NaCl+Cu(NO 3) 2= 2Na NO3+CuCl2 根据酸的共性和碱的共性,以及盐的有关性质,小结能够获得盐的途径有多少?思考比一比,谁想的多! 1、金属+酸——盐+氢气 制取盐的可能途经: 8、盐+盐——新盐+新盐 7、金属+盐——新金属+新盐 6、碱+酸性氧化物——盐+水 5、碱+盐——新碱+新盐 4、酸+盐——新酸+新盐3、酸+碱——盐+水2、酸+金属氧化物——盐+水思考:你能写出获得ZnCl2的途经有 多少?用化学方程式表示。阅读:P26候氏制碱法四、盐与化肥思考1:什么是化肥?化学肥料是用矿物质、空气、水等作原料,经过化学加工精制而成的肥料(简称化肥)。思考2:化肥有哪些类型氮肥:化肥主要含有氮元素的称氮肥。磷肥:化肥主要含有磷元素的称磷肥。
钾肥:化肥主要含有钾元素的称钾肥。复合肥:化肥中含有两种或两种以上主要营养元素的称复合肥。氮肥磷肥钾肥复合肥料(NH4)2SO4NH4HCO3NaNO3NH4ClCa(H2PO4)2k3PO4K2SO4KCl
K2CO3
kNO3
(NH4)3PO4
NH4NO3
读图P27盐和化肥氮 肥铵盐为主,还包括硝酸盐和尿素2NH3+H2SO4=(NH4)2SO4(硫铵) 作用:能促使农作物的茎叶生长茂盛,含有组成叶绿素的重要元素制取:酸与氨气反应制得NH3+H2O+CO2=NH4HCO3(碳铵)氨与碳酸:氨与硫酸:可见:盐的组成中,所含的阳离子不一定都是金属阳离子,也可以是复杂阳离子(带电原子团)铵盐的性质 实验:1、向硫酸铵浓溶液中滴加氢氧化钠溶液,发生了什么变化?产生刺激性气味的气体实验2、把湿润的红色石蕊试纸放在试管口,试纸颜色是否发生变化?变化的原因是什么?使湿润的红色石蕊试纸变蓝(NH4)2SO4+2NaOH= Na2SO4+2H2O+2NH3↑
产物中有氨气产生,氨气是碱性的。 铵盐与碱(强碱),都有能使湿润的红色石蕊试纸变蓝的氨气放出,此法用于铵盐的检验。总 结 练习思考:在农村,人们常取少量白色粉末状的化肥和消石灰一起放在手掌心搓,通过闻气味来检验是否是氮肥,这是根据什么原理?最常用的氮肥:是含氮有机物即人的尿液化 肥:尿素 CO(NH2)2磷 肥作用: 促进农作物要根系发达,增强吸收养份和抗寒抗旱能力,促进作物穗数增多,籽粒饱满等。钾 肥使用注意:长期使用会造成土壤板结,破坏土壤结构。作用:促进农作物生长旺盛,茎杆粗壮,增强抗病虫害能力,促进糖和淀粉的生成。代表物:硫酸钾(K2SO4)、氯化钾(KCl)、草木灰(成份K2CO3)所以需要施一些农家肥料(有机肥)有利于该良土壤结构,提高土壤肥力。
中含有的离子CaCI2溶液
中含有的离子2Na+CO32—Ca2+2CI—Na2CO3+CaCl2 = CaCO3↓+ 2NaCl请同学们分别写出酸与碱、盐与碱、盐与盐反应的化学方程式。 练 习
2NaOH + H2SO4 = Na2SO4 + 2H2OFeCl3 + 3NaOH = Fe(OH)3↓ + 3NaClNa2CO3+CaCl2 = CaCO3↓+ 2NaCl你能找出上述反应类型有什么特点?复分解反应: 两种化合物互相交换成分生成两种新的化合物的反应。 思考:中和反应是否是复分解反应?小结 钾钠铵盐都可溶
硝酸盐遇水影无踪
盐酸盐不溶氯化银
硫酸盐不溶硫酸钡
溶碱钾钠铵和钡
氢氧化钙微溶水
溶 解 性 口 诀微溶物质:氢氧化钙 硫酸钙
硫酸银 碳酸镁下列物质能发生化学反应吗?为什么?1、CuO+Ba(OH)2= Cu(OH)2 ↓ +BaO
2、SO2+HNO3=
3、2Fe(OH)3+3MgCl2= 2FeCl3+3Mg (OH)2 ↓
4、Na2CO3+CaCl2 = CaCO3 ↓ +2NaCl
5、Na2CO3+2HCl= 2Na Cl +H2CO3
6、 Ba(OH)2+H2SO4= BaSO4 ↓ +2H2 O
7、NaOH+BaCl2= Ba(OH)2+NaCl
8、2NaCl+Cu(NO 3) 2= 2Na NO3+CuCl2 根据酸的共性和碱的共性,以及盐的有关性质,小结能够获得盐的途径有多少?思考比一比,谁想的多! 1、金属+酸——盐+氢气 制取盐的可能途经: 8、盐+盐——新盐+新盐 7、金属+盐——新金属+新盐 6、碱+酸性氧化物——盐+水 5、碱+盐——新碱+新盐 4、酸+盐——新酸+新盐3、酸+碱——盐+水2、酸+金属氧化物——盐+水思考:你能写出获得ZnCl2的途经有 多少?用化学方程式表示。阅读:P26候氏制碱法四、盐与化肥思考1:什么是化肥?化学肥料是用矿物质、空气、水等作原料,经过化学加工精制而成的肥料(简称化肥)。思考2:化肥有哪些类型氮肥:化肥主要含有氮元素的称氮肥。磷肥:化肥主要含有磷元素的称磷肥。
钾肥:化肥主要含有钾元素的称钾肥。复合肥:化肥中含有两种或两种以上主要营养元素的称复合肥。氮肥磷肥钾肥复合肥料(NH4)2SO4NH4HCO3NaNO3NH4ClCa(H2PO4)2k3PO4K2SO4KCl
K2CO3
kNO3
(NH4)3PO4
NH4NO3
读图P27盐和化肥氮 肥铵盐为主,还包括硝酸盐和尿素2NH3+H2SO4=(NH4)2SO4(硫铵) 作用:能促使农作物的茎叶生长茂盛,含有组成叶绿素的重要元素制取:酸与氨气反应制得NH3+H2O+CO2=NH4HCO3(碳铵)氨与碳酸:氨与硫酸:可见:盐的组成中,所含的阳离子不一定都是金属阳离子,也可以是复杂阳离子(带电原子团)铵盐的性质 实验:1、向硫酸铵浓溶液中滴加氢氧化钠溶液,发生了什么变化?产生刺激性气味的气体实验2、把湿润的红色石蕊试纸放在试管口,试纸颜色是否发生变化?变化的原因是什么?使湿润的红色石蕊试纸变蓝(NH4)2SO4+2NaOH= Na2SO4+2H2O+2NH3↑
产物中有氨气产生,氨气是碱性的。 铵盐与碱(强碱),都有能使湿润的红色石蕊试纸变蓝的氨气放出,此法用于铵盐的检验。总 结 练习思考:在农村,人们常取少量白色粉末状的化肥和消石灰一起放在手掌心搓,通过闻气味来检验是否是氮肥,这是根据什么原理?最常用的氮肥:是含氮有机物即人的尿液化 肥:尿素 CO(NH2)2磷 肥作用: 促进农作物要根系发达,增强吸收养份和抗寒抗旱能力,促进作物穗数增多,籽粒饱满等。钾 肥使用注意:长期使用会造成土壤板结,破坏土壤结构。作用:促进农作物生长旺盛,茎杆粗壮,增强抗病虫害能力,促进糖和淀粉的生成。代表物:硫酸钾(K2SO4)、氯化钾(KCl)、草木灰(成份K2CO3)所以需要施一些农家肥料(有机肥)有利于该良土壤结构,提高土壤肥力。
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
