盐[上学期]
图片预览






文档简介
课件14张PPT。盐(二)复习:酸、碱各具有哪些通性?一、盐的性质:1、物理性质:碳酸钙、碳酸钠、氯化钙、氯化钠、硫酸钠等几种盐的固体样品,观察这些盐的颜色状态等。结论:常温下盐大多数是固体。下同的盐在水中的溶解性不同。盐溶液溶解性规律:溶碱钾、钠铵和钡,氢氧化钙微溶于水。
钾钠铵盐均可溶,硝酸盐入水影无踪。
盐酸盐不溶银亚汞,硫酸盐不溶钡和铅。
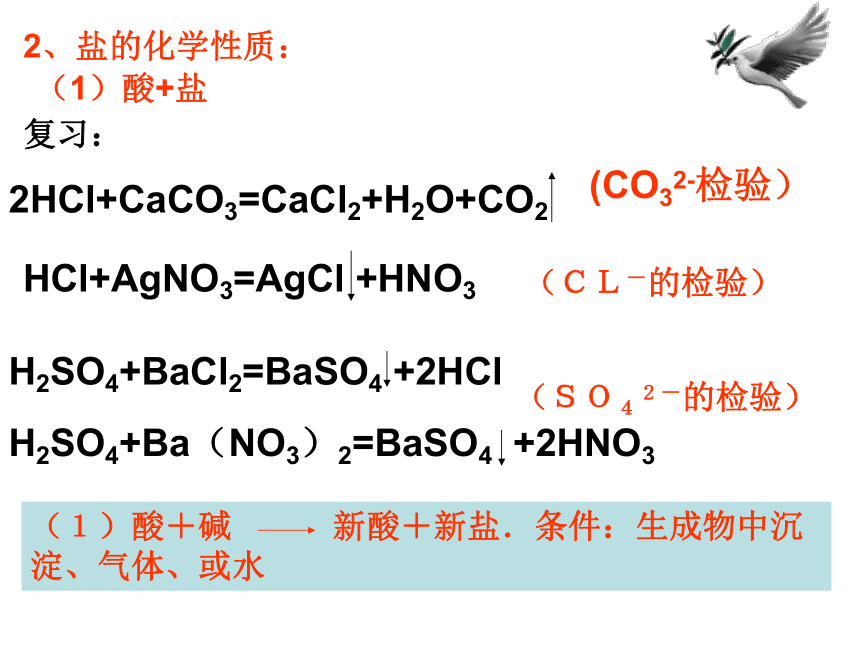
碳酸盐只溶钾钠铵。2、盐的化学性质:(1)酸+盐复习:2HCl+CaCO3=CaCl2+H2O+CO2HCl+AgNO3=AgCl +HNO3H2SO4+BaCl2=BaSO4 +2HClH2SO4+Ba(NO3)2=BaSO4 +2HNO3(CO32-检验)(CL-的检验)(SO42-的检验)(1)酸+碱 新酸+新盐.条件:生成物中沉淀、气体、或水 (2)盐+碱:复习:3NaOH+FeCl3=Fe(OH)3 +3NaCl2KOH+CuSO4=Cu(OH)2+K2SO4Ba(OH)2+CuSO4=BaSO4+Cu(OH)22NaOH+MgCl2=Mg(OH)2 +2NaCl现象:红褐色沉淀。现象:蓝色沉淀。现象:白色、蓝色沉淀。现象:白色沉淀 。(2)盐+碱=新碱+新盐。条件:反应物两者均可溶,生成物中有沉淀。(3)盐+盐实验:在盛有碳酸钠溶液的试管中滴加氯化钙溶液,观察实验现象,写出化学方程式。现象:出现白色沉淀。Na2CO3+CaCl2=CaCO3 +2NaCl实验:将硝酸银溶液滴入盛有氯化钠的溶液中,现象产生白色沉淀,将氯化钡溶液滴入盛有硫酸钠溶液的试管中,现象是产生白色沉淀。NaCl+AgNO3=AgCl +NaNO3Na2SO4+BaCL2=BaS04 +2NaCl(CL-的检验)(SO42-的检验)(3)盐+盐=新盐+新盐。反应物均可溶,生成物中有沉淀。
总结:盐的化学性质(1)盐+酸=新盐+新酸(2)盐+碱=新盐+新碱(3)盐+盐=新盐+新盐例1:下列各组溶液中,不用任何试剂,只用组内溶液互相混合的方法,就能鉴别的一组是( )A、Na2SO4、BaCl2、KNO3、NaCl
B、Na2SO4、Na2CO3、BaCl2、HCl
C、NaOH、Na2SO4、FeCI3、BaCl2
D、NaCl、AgNO3、NaNO3、HClB例2、现有A、B、C、D、E、五瓶无色溶,它们是盐酸、氯化钠、氯化钙,氢氧化钙和碳酸钠。为了确定它们和是哪一种,进行了如下实验,其中观察到如下现象:(1)B跟C两溶液混合,产生白色沉淀
(2)B跟D两溶液混合,产生白色沉淀
(3)B跟E两溶液混合,产生气泡
(4)C溶液能使红色石蕊试纸变蓝分析上述实验现象,推断出A、B、C、D、E、的化学式。二、复分解反应根据盐的三个反应规律,分别写出三个反应的化学方程式。复分解反应:由两种化合物相互交换成分生成新化合物的反应称为复分解反。复分解反应发生的条件:
生成物中有沉淀 、气体、水三者之一生成中和反应是否属于复分解反应。是、因为中和反应中化合物互相交换成分,符合复分解反应条件,生成物中有水是复分解反应。根据下表所列部分碱或盐在水中的溶解性试回答:阴离子阳离子(1)NaNO3 于水,Mg(OH)2 于水。(填溶或不溶)(2)写出Na2CO3溶液和CaCl2溶液反应的化学方程式,该反应的基本类型为什么?练一练:(1)下列各组物质的溶液,不能发生复分解反应的是( )A、盐酸和氢氧化钙 B、碳酸钠和硫酸
C、硝酸银和氯化钡 D、氯化钾和硫酸铜D(2)下列物质的溶液中,即能与氢氧化钡反应又能与盐酸反应的是( )A、蓝矾、B、碳酸钠 C、氯化铁 D、碳酸钙B(3)、向一示知溶液中滴入BACL2溶液,有白色沉淀生成,则原溶液( )A、一定是稀硫酸 B、一定是硝酸银溶液
C、一定是可溶性硫酸盐溶液 D、难以确定D4、下列和物质在同一溶液中能共存的是( )A、氯化钙和盐酸 B、氯化铁和氢氧化钠
C、硫酸镁和氯化钠 D、硝酸银和氯化钾A、C5、在不用指示剂的条件下,欲使含有盐酸的氯化钙溶液由酸性变为中性,应选用的试剂是( )A、澄清石灰水 B、硝酸银溶液
C、石灰石粉末 D、生石灰粉末C6、把下列每组中的两种物质的溶液混合,有沉淀生成,加入足量的稀盐酸,沉淀部分溶解,过滤,滤液呈黄色,则该物质是( )A、氢氧化钠、氯化铁、 B、氢氧化钡、硫酸铜、、
C、氢氧化钡、硫酸铁、 D、碳酸钠、氯化钙C7、一般说来,在盐类中,钾盐、 、 、 都易溶于水,而 盐大多数不溶于水。钠盐钙盐铵盐钡8、两种物质在溶液中相互交换 ,如果有 生成或有 生成或有 放出,那么复分解反应就可以发生,否则不能发生。离子沉淀水气体9、有人误食氯化钡而引起中毒,若及时服用硫酸钠溶液可以解毒,原因是若及时服用碳酸钠溶液液是否可以解毒?BaCl2+Na2SO4=2NaCl+BaSO4下能,原因是Na2CO3+2HCl=2NaCl+H2O+CO210、把含有MgCO3、MgCl2固体的混合物共15.8克加入到100克18.25%的盐酸中,恰好完全反应,同时放出2.2克无色气体,求 1、原混合物中MgCO3的质量分数。
2、反应后所得溶液中溶质的质量分数。
钾钠铵盐均可溶,硝酸盐入水影无踪。
盐酸盐不溶银亚汞,硫酸盐不溶钡和铅。
碳酸盐只溶钾钠铵。2、盐的化学性质:(1)酸+盐复习:2HCl+CaCO3=CaCl2+H2O+CO2HCl+AgNO3=AgCl +HNO3H2SO4+BaCl2=BaSO4 +2HClH2SO4+Ba(NO3)2=BaSO4 +2HNO3(CO32-检验)(CL-的检验)(SO42-的检验)(1)酸+碱 新酸+新盐.条件:生成物中沉淀、气体、或水 (2)盐+碱:复习:3NaOH+FeCl3=Fe(OH)3 +3NaCl2KOH+CuSO4=Cu(OH)2+K2SO4Ba(OH)2+CuSO4=BaSO4+Cu(OH)22NaOH+MgCl2=Mg(OH)2 +2NaCl现象:红褐色沉淀。现象:蓝色沉淀。现象:白色、蓝色沉淀。现象:白色沉淀 。(2)盐+碱=新碱+新盐。条件:反应物两者均可溶,生成物中有沉淀。(3)盐+盐实验:在盛有碳酸钠溶液的试管中滴加氯化钙溶液,观察实验现象,写出化学方程式。现象:出现白色沉淀。Na2CO3+CaCl2=CaCO3 +2NaCl实验:将硝酸银溶液滴入盛有氯化钠的溶液中,现象产生白色沉淀,将氯化钡溶液滴入盛有硫酸钠溶液的试管中,现象是产生白色沉淀。NaCl+AgNO3=AgCl +NaNO3Na2SO4+BaCL2=BaS04 +2NaCl(CL-的检验)(SO42-的检验)(3)盐+盐=新盐+新盐。反应物均可溶,生成物中有沉淀。
总结:盐的化学性质(1)盐+酸=新盐+新酸(2)盐+碱=新盐+新碱(3)盐+盐=新盐+新盐例1:下列各组溶液中,不用任何试剂,只用组内溶液互相混合的方法,就能鉴别的一组是( )A、Na2SO4、BaCl2、KNO3、NaCl
B、Na2SO4、Na2CO3、BaCl2、HCl
C、NaOH、Na2SO4、FeCI3、BaCl2
D、NaCl、AgNO3、NaNO3、HClB例2、现有A、B、C、D、E、五瓶无色溶,它们是盐酸、氯化钠、氯化钙,氢氧化钙和碳酸钠。为了确定它们和是哪一种,进行了如下实验,其中观察到如下现象:(1)B跟C两溶液混合,产生白色沉淀
(2)B跟D两溶液混合,产生白色沉淀
(3)B跟E两溶液混合,产生气泡
(4)C溶液能使红色石蕊试纸变蓝分析上述实验现象,推断出A、B、C、D、E、的化学式。二、复分解反应根据盐的三个反应规律,分别写出三个反应的化学方程式。复分解反应:由两种化合物相互交换成分生成新化合物的反应称为复分解反。复分解反应发生的条件:
生成物中有沉淀 、气体、水三者之一生成中和反应是否属于复分解反应。是、因为中和反应中化合物互相交换成分,符合复分解反应条件,生成物中有水是复分解反应。根据下表所列部分碱或盐在水中的溶解性试回答:阴离子阳离子(1)NaNO3 于水,Mg(OH)2 于水。(填溶或不溶)(2)写出Na2CO3溶液和CaCl2溶液反应的化学方程式,该反应的基本类型为什么?练一练:(1)下列各组物质的溶液,不能发生复分解反应的是( )A、盐酸和氢氧化钙 B、碳酸钠和硫酸
C、硝酸银和氯化钡 D、氯化钾和硫酸铜D(2)下列物质的溶液中,即能与氢氧化钡反应又能与盐酸反应的是( )A、蓝矾、B、碳酸钠 C、氯化铁 D、碳酸钙B(3)、向一示知溶液中滴入BACL2溶液,有白色沉淀生成,则原溶液( )A、一定是稀硫酸 B、一定是硝酸银溶液
C、一定是可溶性硫酸盐溶液 D、难以确定D4、下列和物质在同一溶液中能共存的是( )A、氯化钙和盐酸 B、氯化铁和氢氧化钠
C、硫酸镁和氯化钠 D、硝酸银和氯化钾A、C5、在不用指示剂的条件下,欲使含有盐酸的氯化钙溶液由酸性变为中性,应选用的试剂是( )A、澄清石灰水 B、硝酸银溶液
C、石灰石粉末 D、生石灰粉末C6、把下列每组中的两种物质的溶液混合,有沉淀生成,加入足量的稀盐酸,沉淀部分溶解,过滤,滤液呈黄色,则该物质是( )A、氢氧化钠、氯化铁、 B、氢氧化钡、硫酸铜、、
C、氢氧化钡、硫酸铁、 D、碳酸钠、氯化钙C7、一般说来,在盐类中,钾盐、 、 、 都易溶于水,而 盐大多数不溶于水。钠盐钙盐铵盐钡8、两种物质在溶液中相互交换 ,如果有 生成或有 生成或有 放出,那么复分解反应就可以发生,否则不能发生。离子沉淀水气体9、有人误食氯化钡而引起中毒,若及时服用硫酸钠溶液可以解毒,原因是若及时服用碳酸钠溶液液是否可以解毒?BaCl2+Na2SO4=2NaCl+BaSO4下能,原因是Na2CO3+2HCl=2NaCl+H2O+CO210、把含有MgCO3、MgCl2固体的混合物共15.8克加入到100克18.25%的盐酸中,恰好完全反应,同时放出2.2克无色气体,求 1、原混合物中MgCO3的质量分数。
2、反应后所得溶液中溶质的质量分数。
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
