华师大版八年级上第五章第二节化学方程式[上学期]
文档属性
| 名称 | 华师大版八年级上第五章第二节化学方程式[上学期] |

|
|
| 格式 | rar | ||
| 文件大小 | 2.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 华东师大版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2007-11-06 00:00:00 | ||
图片预览









文档简介
课件32张PPT。化学方程式 第二节【探究活动一】 问:天平的作用有哪些?
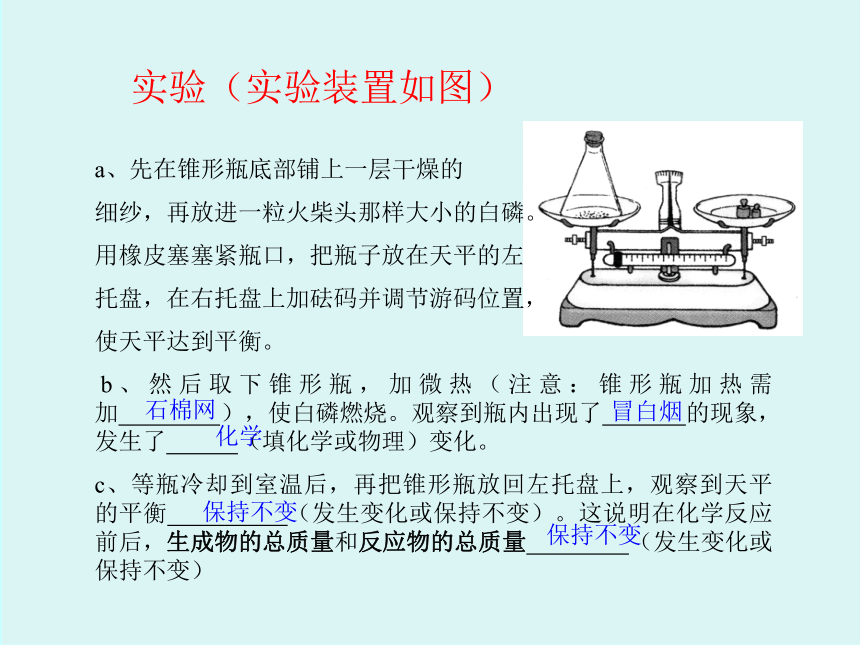
1.称量物体的质量2.比较物体的轻重实验(实验装置如图)a、先在锥形瓶底部铺上一层干燥的
细纱,再放进一粒火柴头那样大小的白磷。
用橡皮塞塞紧瓶口,把瓶子放在天平的左
托盘,在右托盘上加砝码并调节游码位置,
使天平达到平衡。
b、然后取下锥形瓶,加微热(注意:锥形瓶加热需加 ),使白磷燃烧。观察到瓶内出现了 的现象,发生了 (填化学或物理)变化。
c、等瓶冷却到室温后,再把锥形瓶放回左托盘上,观察到天平的平衡 (发生变化或保持不变)。这说明在化学反应前后,生成物的总质量和反应物的总质量 (发生变化或保持不变) 石棉网冒白烟化学保持不变保持不变【探究活动二】 实验: (实验装置如图) a、把盛有无色氢氧化钠(NaOH)溶液的
短试管,小心地放入盛有蓝色硫酸铜(CuSO4)
溶液的锥形瓶里,塞紧瓶塞。再把盛有短试管的
锥形瓶放在天平的左托盘上,在右托盘上加砝码
并调节游码位置,使天平达到平衡。
b、然后拿起锥形瓶并使它倾斜,让短试管中的NaOH溶液倒入CuSO4溶液中,两种溶液充分接触后,可以观察到 现象,发生了 (化学或物理)变化。
c、再把锥形瓶放回左托盘上,观察到天平的平衡 (发生变化或保持不变)说明在化学反应前后,总质量 (发生变化或保持不变)。蓝色沉淀生成化学保持平衡保持平衡通过探究活动一和二你可得到的结论是什么?[板书]:质量守恒定律的宏观含义:生成物总质量=反应物总质量 思考:在化学反应前后,质量守恒的实质是什么【探究活动三】
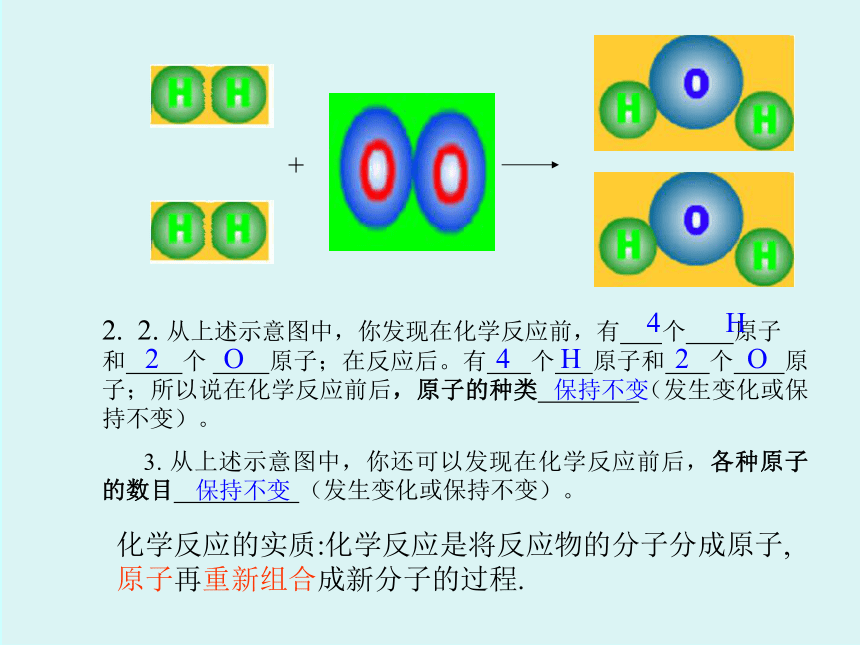
为了进一步从微观角度来认识质量守恒定律,请同学们一起完成下列活动。 1. 试在下表中画出氢气(H2)和氧气(O2)反应生成水分子(H2O)的示意图。 +2. 2. 从上述示意图中,你发现在化学反应前,有 个 原子 和 个 原子;在反应后。有 个 原子和 个 原子;所以说在化学反应前后,原子的种类 (发生变化或保持不变)。
3. 从上述示意图中,你还可以发现在化学反应前后,各种原子的数目 (发生变化或保持不变)。 4H2O4H2O保持不变保持不变化学反应的实质:化学反应是将反应物的分子分成原子,原子再重新组合成新分子的过程.质量守恒定律的解释:反应前后原子种类不变,原子数目没有增减..质量守恒定律
的含义 宏观:生成物总质量=反应物总质量
微观:在化学反应前后原子种类不变(即原子的数目不变,只是进行了重新组合)质量守恒定律的应用: 1解释化学反应过程中的质量变化现象
例:用质量守恒定律解释(1)铁生锈后质量增加, (2)高锰酸钾加热后质量减少了
答:(1)铁生锈后质量增加,是因为铁锈比铁多一种氧元素的质量;(2)高锰酸钾加热后质量减少是因为生成物里氧气的质量没有计算
2推测化学变化中某一物质的元素组成例:物质A在纯氧中燃烧只生成二氧化碳和水,则A物质中一定含有 , 可能含有 .3.可以推测化学变化中某一物质的化学式例:一物质发生化学反应,可表示为
X+2O2 CO2+H2O,则X的化学式可表达为 .◇写出硫在氧气中燃烧的文字表达式S + O2 SO2 点燃硫氧气二氧化硫点燃+ 化 学 方 程 式一、化学方程式 用化学式来表示化学反应的式子叫化学方程式.2、书写原则1、定 义◇以客观事实为依据,反应是真实存在的◇符合质量守恒定律:原子种类无变化,原子个数无增减2、书写原则3、书写步骤写 配 注 等写出反应物和生成物的分子式配平化学方程式注明反应条件,生成物的状态将短线改为等号◇◇◇◇水分解的化学反应方程式 左 (短线连接) 右 反应物分子式 生成物分子式H2OH2+O2水 氢气 + 氧气水分解的化学反应方程式水分解的化学反应方程式 左 (短线连接) 右 反应物分子式 生成物分子式水 氢气 + 氧气H2OH2+O222???水分解的化学反应方程式 左 (短线连接) 右 反应物分子式 生成物分子式水 氢气 + 氧气H2OH2+O222通电水分解的化学反应方程式 左 (短线连接) 右 反应物分子式 生成物分子式水 氢气 + 氧气H2OH2+O222通电 左 (短线连接) 右 反应物分子式 生成物分子式写配平依据配平过程质量守恒定律 分子式前面配上适当的化学计量数使左右两边的每一种元素的原子总数相等
最小公倍数法、观察法、奇偶法等配平方法配注明反应条件,生成物状态注条件符号加热△状态符号气体沉淀将短线改为等号等例题写出下列反应的化学方程式
1、碳在氧气中燃烧
2、磷在氧气中燃烧
3、在硫酸铜(CuSO4 )溶液中加入氢氧化钠(NaOH)溶液1、碳在氧气中燃烧C+O2CO2点燃例题2、磷在氧气中燃烧 磷+氧气 五氧化二磷点燃P+O2P2O5452点燃例题3、在硫酸铜(CuSO4 )溶液中加入氢氧化钠(NaOH)溶液 例题CuSO4+NaOHCu(OH)2+Na2SO42课堂练习1、铁+氧气 四氧化三铁2、甲烷+氧气 水+二氧化碳3、高锰酸钾(KMnO4) 锰酸钾(K2MnO4)+二氧化锰+氧气点燃点燃加热3Fe+O2 Fe3O4点燃CH4+2O2 CO2+2H2O点燃2KMnO4 K2MnO4+MnO2+O2△二、化学方程式的涵义1、表示什么物质参加反应,结果生成什么物质。2、表示各反应物、生成物之间的原子、分子个数之比。3、表示反应物、生成物各物质之间的质量比化学方程式的涵义4P + 5O2 2P2O5
124 160 284点燃1、表示磷和氧气参加反应,结果生成五氧化二磷。2、表示反应物中磷原子、氧分子和生成物中五氧化二磷分子的个数比为4∶5∶2。3、表示124份质量的磷与160份质量的氧气反应生成284份质量的五氧化二磷。质量比为31∶40∶71课堂练习21、根据已学知识判断下列反应方程式是否正确。如有错误,请指出错误之处。
(1)3Fe+2O2 Fe3O4
(2)Mg+O2 MgO2
(3)CH4+O2 CO2+H2O加热点燃点燃全错2、配平下列化学方程式
(1) C + CO2 CO
(2) Al + O2 Al2O3
(3) CuO + C Cu + CO2
(4) C2H2 + O2 H2O + CO2
(5) H2S + O2 S + H2O点燃点燃点燃高温高温课堂练习24 3 22 22 5 2 42 2 2课堂小结化学方程式的书写可归纳为:(以反应“ 氯酸钾 氯化钾+氧气”的化学方程式书写为例)加热左反右生一横线配平以后加一线等号上下注条件箭号标气或沉淀 KClO3 KCl+ O2 2KClO3 2KCl+ 3O2 2KClO3 2 KCl+ 3 O2 2 KClO3 2KCl+ 3 O2MnO2MnO2△△
1.称量物体的质量2.比较物体的轻重实验(实验装置如图)a、先在锥形瓶底部铺上一层干燥的
细纱,再放进一粒火柴头那样大小的白磷。
用橡皮塞塞紧瓶口,把瓶子放在天平的左
托盘,在右托盘上加砝码并调节游码位置,
使天平达到平衡。
b、然后取下锥形瓶,加微热(注意:锥形瓶加热需加 ),使白磷燃烧。观察到瓶内出现了 的现象,发生了 (填化学或物理)变化。
c、等瓶冷却到室温后,再把锥形瓶放回左托盘上,观察到天平的平衡 (发生变化或保持不变)。这说明在化学反应前后,生成物的总质量和反应物的总质量 (发生变化或保持不变) 石棉网冒白烟化学保持不变保持不变【探究活动二】 实验: (实验装置如图) a、把盛有无色氢氧化钠(NaOH)溶液的
短试管,小心地放入盛有蓝色硫酸铜(CuSO4)
溶液的锥形瓶里,塞紧瓶塞。再把盛有短试管的
锥形瓶放在天平的左托盘上,在右托盘上加砝码
并调节游码位置,使天平达到平衡。
b、然后拿起锥形瓶并使它倾斜,让短试管中的NaOH溶液倒入CuSO4溶液中,两种溶液充分接触后,可以观察到 现象,发生了 (化学或物理)变化。
c、再把锥形瓶放回左托盘上,观察到天平的平衡 (发生变化或保持不变)说明在化学反应前后,总质量 (发生变化或保持不变)。蓝色沉淀生成化学保持平衡保持平衡通过探究活动一和二你可得到的结论是什么?[板书]:质量守恒定律的宏观含义:生成物总质量=反应物总质量 思考:在化学反应前后,质量守恒的实质是什么【探究活动三】
为了进一步从微观角度来认识质量守恒定律,请同学们一起完成下列活动。 1. 试在下表中画出氢气(H2)和氧气(O2)反应生成水分子(H2O)的示意图。 +2. 2. 从上述示意图中,你发现在化学反应前,有 个 原子 和 个 原子;在反应后。有 个 原子和 个 原子;所以说在化学反应前后,原子的种类 (发生变化或保持不变)。
3. 从上述示意图中,你还可以发现在化学反应前后,各种原子的数目 (发生变化或保持不变)。 4H2O4H2O保持不变保持不变化学反应的实质:化学反应是将反应物的分子分成原子,原子再重新组合成新分子的过程.质量守恒定律的解释:反应前后原子种类不变,原子数目没有增减..质量守恒定律
的含义 宏观:生成物总质量=反应物总质量
微观:在化学反应前后原子种类不变(即原子的数目不变,只是进行了重新组合)质量守恒定律的应用: 1解释化学反应过程中的质量变化现象
例:用质量守恒定律解释(1)铁生锈后质量增加, (2)高锰酸钾加热后质量减少了
答:(1)铁生锈后质量增加,是因为铁锈比铁多一种氧元素的质量;(2)高锰酸钾加热后质量减少是因为生成物里氧气的质量没有计算
2推测化学变化中某一物质的元素组成例:物质A在纯氧中燃烧只生成二氧化碳和水,则A物质中一定含有 , 可能含有 .3.可以推测化学变化中某一物质的化学式例:一物质发生化学反应,可表示为
X+2O2 CO2+H2O,则X的化学式可表达为 .◇写出硫在氧气中燃烧的文字表达式S + O2 SO2 点燃硫氧气二氧化硫点燃+ 化 学 方 程 式一、化学方程式 用化学式来表示化学反应的式子叫化学方程式.2、书写原则1、定 义◇以客观事实为依据,反应是真实存在的◇符合质量守恒定律:原子种类无变化,原子个数无增减2、书写原则3、书写步骤写 配 注 等写出反应物和生成物的分子式配平化学方程式注明反应条件,生成物的状态将短线改为等号◇◇◇◇水分解的化学反应方程式 左 (短线连接) 右 反应物分子式 生成物分子式H2OH2+O2水 氢气 + 氧气水分解的化学反应方程式水分解的化学反应方程式 左 (短线连接) 右 反应物分子式 生成物分子式水 氢气 + 氧气H2OH2+O222???水分解的化学反应方程式 左 (短线连接) 右 反应物分子式 生成物分子式水 氢气 + 氧气H2OH2+O222通电水分解的化学反应方程式 左 (短线连接) 右 反应物分子式 生成物分子式水 氢气 + 氧气H2OH2+O222通电 左 (短线连接) 右 反应物分子式 生成物分子式写配平依据配平过程质量守恒定律 分子式前面配上适当的化学计量数使左右两边的每一种元素的原子总数相等
最小公倍数法、观察法、奇偶法等配平方法配注明反应条件,生成物状态注条件符号加热△状态符号气体沉淀将短线改为等号等例题写出下列反应的化学方程式
1、碳在氧气中燃烧
2、磷在氧气中燃烧
3、在硫酸铜(CuSO4 )溶液中加入氢氧化钠(NaOH)溶液1、碳在氧气中燃烧C+O2CO2点燃例题2、磷在氧气中燃烧 磷+氧气 五氧化二磷点燃P+O2P2O5452点燃例题3、在硫酸铜(CuSO4 )溶液中加入氢氧化钠(NaOH)溶液 例题CuSO4+NaOHCu(OH)2+Na2SO42课堂练习1、铁+氧气 四氧化三铁2、甲烷+氧气 水+二氧化碳3、高锰酸钾(KMnO4) 锰酸钾(K2MnO4)+二氧化锰+氧气点燃点燃加热3Fe+O2 Fe3O4点燃CH4+2O2 CO2+2H2O点燃2KMnO4 K2MnO4+MnO2+O2△二、化学方程式的涵义1、表示什么物质参加反应,结果生成什么物质。2、表示各反应物、生成物之间的原子、分子个数之比。3、表示反应物、生成物各物质之间的质量比化学方程式的涵义4P + 5O2 2P2O5
124 160 284点燃1、表示磷和氧气参加反应,结果生成五氧化二磷。2、表示反应物中磷原子、氧分子和生成物中五氧化二磷分子的个数比为4∶5∶2。3、表示124份质量的磷与160份质量的氧气反应生成284份质量的五氧化二磷。质量比为31∶40∶71课堂练习21、根据已学知识判断下列反应方程式是否正确。如有错误,请指出错误之处。
(1)3Fe+2O2 Fe3O4
(2)Mg+O2 MgO2
(3)CH4+O2 CO2+H2O加热点燃点燃全错2、配平下列化学方程式
(1) C + CO2 CO
(2) Al + O2 Al2O3
(3) CuO + C Cu + CO2
(4) C2H2 + O2 H2O + CO2
(5) H2S + O2 S + H2O点燃点燃点燃高温高温课堂练习24 3 22 22 5 2 42 2 2课堂小结化学方程式的书写可归纳为:(以反应“ 氯酸钾 氯化钾+氧气”的化学方程式书写为例)加热左反右生一横线配平以后加一线等号上下注条件箭号标气或沉淀 KClO3 KCl+ O2 2KClO3 2KCl+ 3O2 2KClO3 2 KCl+ 3 O2 2 KClO3 2KCl+ 3 O2MnO2MnO2△△
同课章节目录
- 第一章 宇宙的起源与演化
- 1 我们的宇宙
- 2 热大爆炸宇宙模型
- 3 恒星的一生
- 4 星际航行和空间技术
- 第二章 地球的演化和生物圈的形成
- 1 地球的演化
- 2 生命起源
- 3 生物进化
- 4 生态平衡
- 第三章 物质的转化和元素的循环
- 1 物质的转化
- 2 自然界中的碳循环和氧循环
- 3 自然界中的氮循环
- 第四章 健康与保健
- 1 健康、亚健康和疾病
- 2 运动与健康
- 3 免疫与健康
- 4 营养与健康
- 5 卫生与健康
- 6 环境与健康
- 第五章 生物的遗传和变异
- 1 生物的遗传
- 2 生物的变异
- 第六章 能源与社会
- 1 能源和能源的分类
- 2 太阳能的利用
- 3 核能的开发与放射性防护
- 4 新能源与可持续发展
- 第七章 科学与社会发展
- 1 科学就是力量
- 2 科学推动技术发展
- 3 科学技术推动经济增长
- 4 科学技术与可持续发展
