中考复习-溶液[下学期]
图片预览



文档简介
课件14张PPT。1 、认识溶液的概念,理解溶液、溶质、溶剂之关系
2 、能区别饱和溶液和不饱和溶液,了解溶解度的意义并会查阅溶解度表
3、溶液中溶质质量分数的简单计算
初步学习加水稀释时,溶剂的质量计算
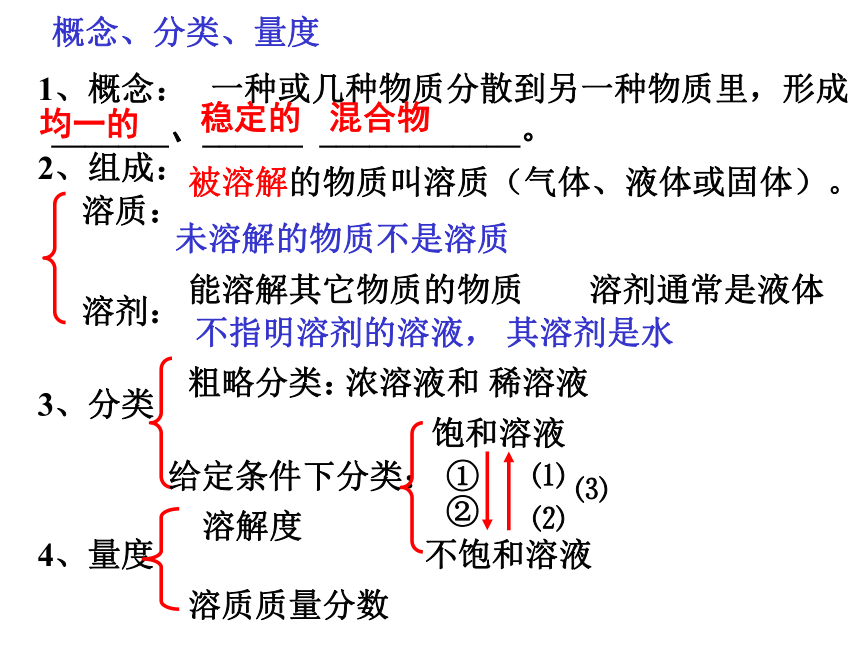
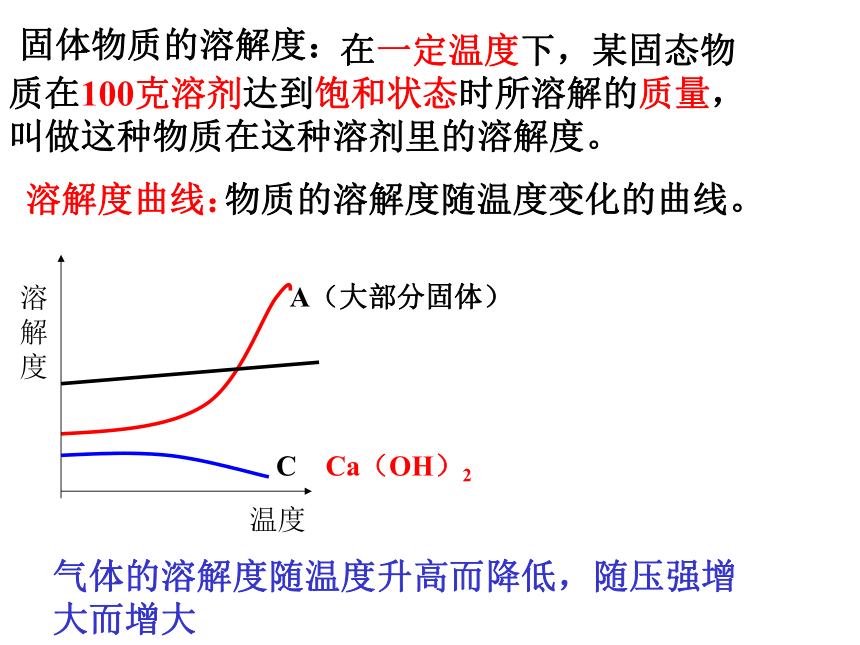
4、初步学会计算含杂质的反应物或生成物的质量分数(杂质不参加反应) 考点扫描第28讲 溶液概念、分类、量度1、概念: 一种或几种物质分散到另一种物质里,形成_______、______ ____________。均一的稳定的混合物2、组成:溶质:溶剂:被溶解的物质叫溶质(气体、液体或固体)。能溶解其它物质的物质溶剂通常是液体不指明溶剂的溶液, 其溶剂是水 未溶解的物质不是溶质3、分类 粗略分类: 浓溶液和 稀溶液给定条件下分类:饱和溶液不饱和溶液①②⑴⑵⑶4、量度溶解度溶质质量分数固体物质的溶解度: 在一定温度下,某固态物质在100克溶剂达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。 溶解度曲线: 物质的溶解度随温度变化的曲线。 A(大部分固体)C Ca(OH)2气体的溶解度随温度升高而降低,随压强增大而增大固体的溶解度曲线图查固体溶解度曲线图:
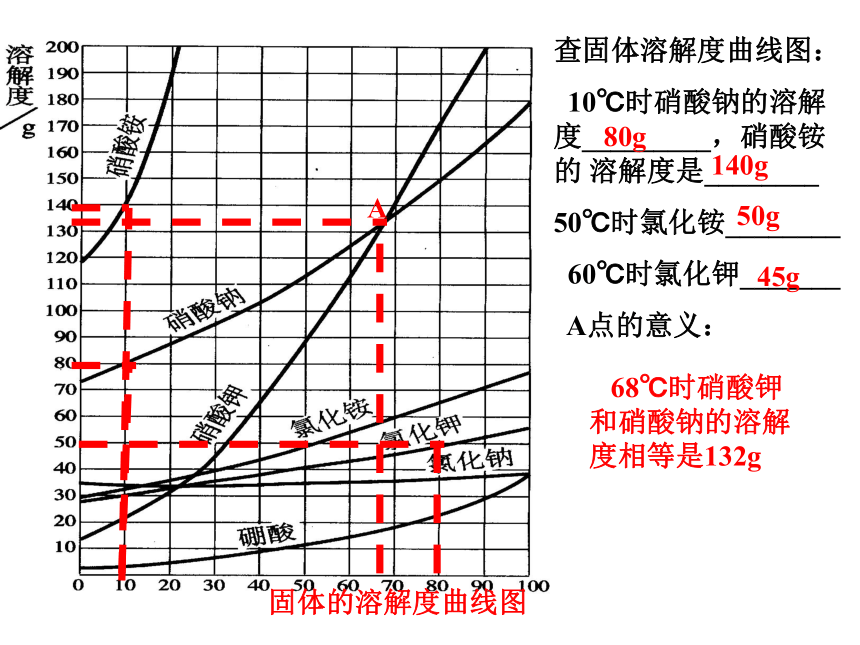
? 10℃时硝酸钠的溶解度_________,硝酸铵的 溶解度是________
50℃时氯化铵________
60℃时氯化钾_______
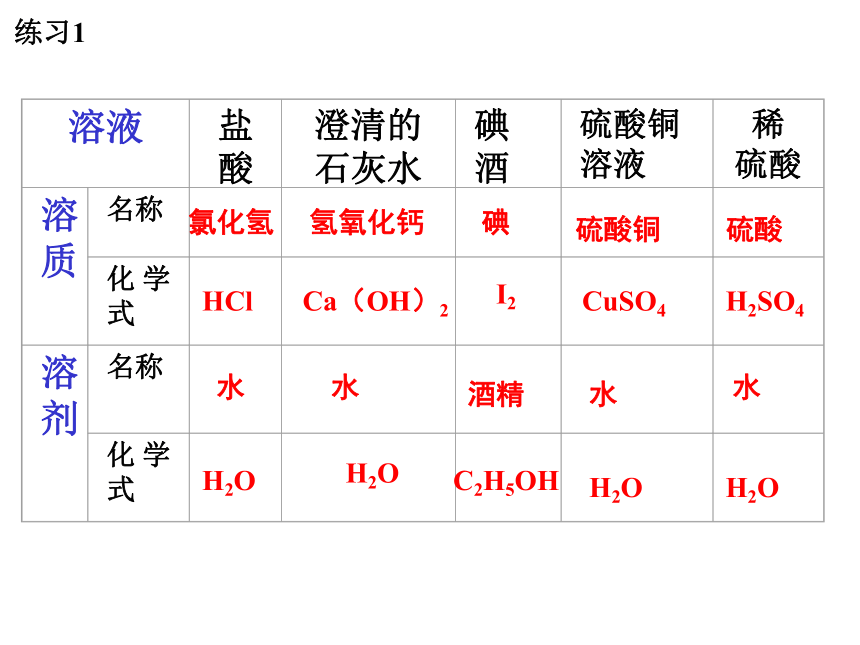
A点的意义:A 68℃时硝酸钾和硝酸钠的溶解度相等是132g80g140g50g45g练习1氯化氢HCl水H2O氢氧化钙Ca(OH)2水H2O碘I2酒精C2H5OH硫酸铜CuSO4水H2O硫酸H2SO4水H2O主要知识点1、溶液质量=溶质质量+溶剂质量 注意:溶质必须是已溶解的,未溶解的不是溶液的一部分 2、溶质的质量分数公式溶质的质量分数=×100%溶液质量=溶质质量÷溶质的质量分数溶质质量=溶液质量×a%3、稀释前后,溶质质量不变 浓溶液质量×a浓%=稀溶液质量×a稀%4、配制过程:计算 、称量 、溶解 溶质的质量分数公式:定义:溶质的质量与溶液的质量之比。推导公式:溶质质量=溶液质量×a%溶质的质量分数(a%)1 计算:算出溶质的质量或体积,溶剂的质量和体积;
2 称量:用天平称取溶质的质量,用量筒量取溶质或溶剂的体积;
3 溶解,在烧杯内溶解配制成一定质量分数的溶液。配制一定质量分数的溶液步骤:溶液的配制过程 把100克98%的浓硫酸稀释成9.8%的稀硫酸,需加水______克,合______毫升。 例1:发生反应的溶液质量反应前各物质的质量总和=反应后溶液质量+气体质量+不溶物(沉淀)质量900900例2:盐酸的标签:500毫升
约590克
Hydrochloric acid
分子式HCl 分子量36.46技术条件
HCl含量 36.0-38.0%
杂质最高含量
…….根据以上标签信息,配制100g溶质的质量分数为15%的稀盐酸,需要溶质的质量分数为36%浓盐酸多少毫升?需加水多少毫升?解:500毫升
约590克
Hydrochloric acid
分子式HCl 分子量36.46技术条件
HCl含量 36.0-38.0%
杂质最高含量
…….5、 设需浓盐酸的质量为m,则
100g×15%=m×36% m=41.7g浓盐酸的体积V=41.7g×=35.3mL加水的质量=100g-41.7g=58.3g
加水的体积为58.3mL1.10克食盐溶于90克水中,求所得溶液的食盐的质量分数?
2.将上述溶液倒出一半到另一烧杯中,求剩余溶液中食盐的质量分数?
3.在剩下溶液中加入10克水,所得溶液的食盐的质量分数为多少?
4.向另一杯中加入5克食盐,食盐的质量分数为多少?
5.若将(1)所得溶液的食盐的质量分数变为原来一半,需加水多少克?(1)10%(2) 10%(3)8.3%(4)18.1%(5)100克练习26.将7克氯化钠加水完全溶解后,继续加水稀释。若以横坐标表示加水质量W克,以纵坐标表示溶液中溶质质量m克,下图所示关系正确的是 ( )D
2 、能区别饱和溶液和不饱和溶液,了解溶解度的意义并会查阅溶解度表
3、溶液中溶质质量分数的简单计算
初步学习加水稀释时,溶剂的质量计算
4、初步学会计算含杂质的反应物或生成物的质量分数(杂质不参加反应) 考点扫描第28讲 溶液概念、分类、量度1、概念: 一种或几种物质分散到另一种物质里,形成_______、______ ____________。均一的稳定的混合物2、组成:溶质:溶剂:被溶解的物质叫溶质(气体、液体或固体)。能溶解其它物质的物质溶剂通常是液体不指明溶剂的溶液, 其溶剂是水 未溶解的物质不是溶质3、分类 粗略分类: 浓溶液和 稀溶液给定条件下分类:饱和溶液不饱和溶液①②⑴⑵⑶4、量度溶解度溶质质量分数固体物质的溶解度: 在一定温度下,某固态物质在100克溶剂达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。 溶解度曲线: 物质的溶解度随温度变化的曲线。 A(大部分固体)C Ca(OH)2气体的溶解度随温度升高而降低,随压强增大而增大固体的溶解度曲线图查固体溶解度曲线图:
? 10℃时硝酸钠的溶解度_________,硝酸铵的 溶解度是________
50℃时氯化铵________
60℃时氯化钾_______
A点的意义:A 68℃时硝酸钾和硝酸钠的溶解度相等是132g80g140g50g45g练习1氯化氢HCl水H2O氢氧化钙Ca(OH)2水H2O碘I2酒精C2H5OH硫酸铜CuSO4水H2O硫酸H2SO4水H2O主要知识点1、溶液质量=溶质质量+溶剂质量 注意:溶质必须是已溶解的,未溶解的不是溶液的一部分 2、溶质的质量分数公式溶质的质量分数=×100%溶液质量=溶质质量÷溶质的质量分数溶质质量=溶液质量×a%3、稀释前后,溶质质量不变 浓溶液质量×a浓%=稀溶液质量×a稀%4、配制过程:计算 、称量 、溶解 溶质的质量分数公式:定义:溶质的质量与溶液的质量之比。推导公式:溶质质量=溶液质量×a%溶质的质量分数(a%)1 计算:算出溶质的质量或体积,溶剂的质量和体积;
2 称量:用天平称取溶质的质量,用量筒量取溶质或溶剂的体积;
3 溶解,在烧杯内溶解配制成一定质量分数的溶液。配制一定质量分数的溶液步骤:溶液的配制过程 把100克98%的浓硫酸稀释成9.8%的稀硫酸,需加水______克,合______毫升。 例1:发生反应的溶液质量反应前各物质的质量总和=反应后溶液质量+气体质量+不溶物(沉淀)质量900900例2:盐酸的标签:500毫升
约590克
Hydrochloric acid
分子式HCl 分子量36.46技术条件
HCl含量 36.0-38.0%
杂质最高含量
…….根据以上标签信息,配制100g溶质的质量分数为15%的稀盐酸,需要溶质的质量分数为36%浓盐酸多少毫升?需加水多少毫升?解:500毫升
约590克
Hydrochloric acid
分子式HCl 分子量36.46技术条件
HCl含量 36.0-38.0%
杂质最高含量
…….5、 设需浓盐酸的质量为m,则
100g×15%=m×36% m=41.7g浓盐酸的体积V=41.7g×=35.3mL加水的质量=100g-41.7g=58.3g
加水的体积为58.3mL1.10克食盐溶于90克水中,求所得溶液的食盐的质量分数?
2.将上述溶液倒出一半到另一烧杯中,求剩余溶液中食盐的质量分数?
3.在剩下溶液中加入10克水,所得溶液的食盐的质量分数为多少?
4.向另一杯中加入5克食盐,食盐的质量分数为多少?
5.若将(1)所得溶液的食盐的质量分数变为原来一半,需加水多少克?(1)10%(2) 10%(3)8.3%(4)18.1%(5)100克练习26.将7克氯化钠加水完全溶解后,继续加水稀释。若以横坐标表示加水质量W克,以纵坐标表示溶液中溶质质量m克,下图所示关系正确的是 ( )D
