物质的结构结构(中考总复习)[下学期]
文档属性
| 名称 | 物质的结构结构(中考总复习)[下学期] |
|
|
| 格式 | rar | ||
| 文件大小 | 828.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2007-03-18 00:00:00 | ||
图片预览









文档简介
课件54张PPT。第七章 物质的结构构成物质的微粒元素物质的分类考试说明145页
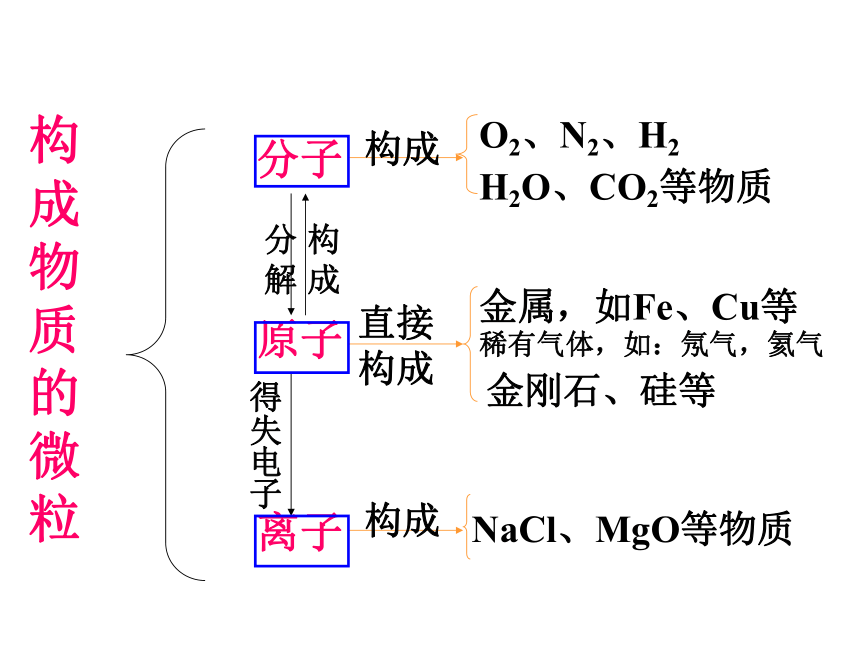
复习导引67页铜 食盐晶体 金刚石二氧化碳模型水 水由______构成 金刚石由______构成 铜由______构成 二氧化碳由___ ___构成 食盐由____ __构成 水分子碳原子铜原子二氧化碳分子钠离子和氯离子分子、原子、离子是三种构成物质的微粒。分子
原子
离子分
解构
成得
失
电
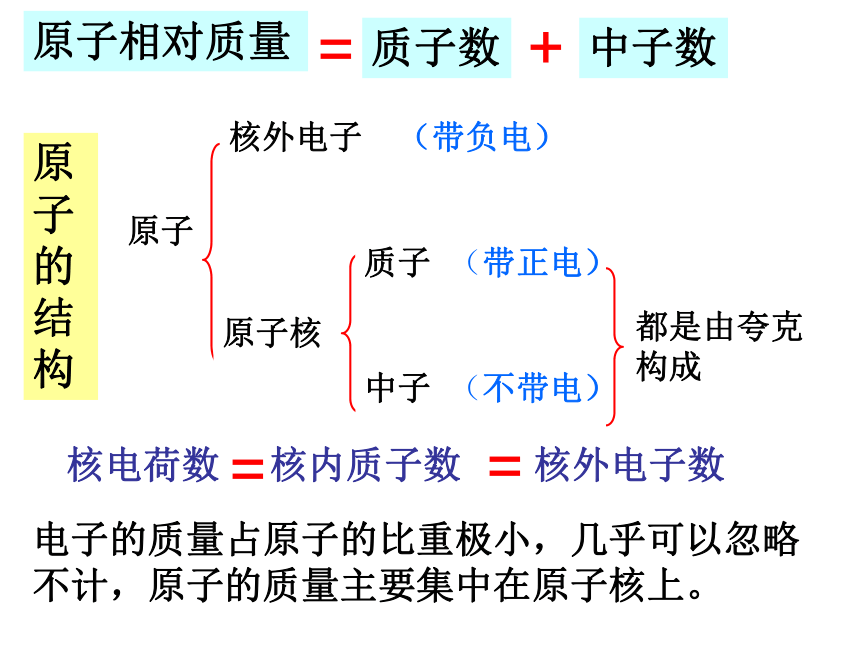
子构成O2、N2、H2
直接构成金属,如Fe、Cu等
构成NaCl、MgO等物质构成物质的微粒H2O、CO2等物质
稀有气体,如:氖气,氦气金刚石、硅等水结成冰后,物理性质是否改变了?水结成冰后,化学性质是否改变了?水结成冰后,水分子是否被拆散?水电解后,生成了氢气和氧气,那么水分子是否发生改变?水电解后,生成了氢气和氧气,那么氢、氧原子是否变成了新的原子?氢、氧原子是否不可再分?分子原子离子构成物质的微粒半径在10-10米数量级,
质量为 1.993n×10-26千克
(n为相对原子质量或相对分子质量 )微粒的大小保持物质化学性质的一种微粒化学变化中的最小微粒带电的原子或原子团分子原子化学反应中破裂相互结合构成纳米材料 以纳米为单位的超级微小颗粒(材料)颗粒直径:(1nm--100nm) 包括金属、非金属、有机、无机和
生物等多种粉末材料。在机械强度、磁、光、声、热等与普通材料不同常见的纳米材料纳米陶瓷韧性好,撞击不破裂 在切削刀具、轴承、汽车发动机部件等诸多方面
都有广泛的应用,并在许多超高温、强腐蚀等苛
刻的环境下起着其他材料不可替代的作用,具有
广阔的应用前景 纳米油墨 色调浓,字迹色泽好 日本等国已有部分纳米二氧化钛的化妆品
问世。紫外线不仅能使肉类食品自动氧化而变
色,而且还会破坏食品中的维生素和芳香化合
物,从而降低食品的营养价值。如用添加
0.1~0.5%的纳米二氧化钛制成的透明塑料包装
材料包装食品,既可以防止紫外线对食品的破
坏作用,还可以使食品保持新鲜。 断裂应力比一般铁材料高12倍纳米铁材料原子(带负电)(带正电)(不带电)都是由夸克构成
核外电子原子核质子中子原子的结构电子的质量占原子的比重极小,几乎可以忽略
不计,原子的质量主要集中在原子核上。核电荷数核外电子数核内质子数==原子相对质量质子数中子数=+1、构成细胞的微粒是 ( )
A、细胞质、细胞膜、细胞核 B、溶质、溶剂
C、分子、原子、离子 D、中子、质子
例3.1985年科学家发现的C60分子是由60个碳原子构成的,它的形状像足球(如图C),因此又叫足球烯(音希)。1991年科学家又发现一种碳的单质——碳纳米管,它是由六边形的碳原子构成的管状大分子(如图D)。下图中,A、B分别是金刚石和石墨的结构示意图。
用你所学到的化学知识回答下列问题:
金刚石、石墨、足球烯、碳纳米管物理性质有较大差异的原因是什么?
答:________________。
原子之间的排列(结构)不同1、原子结构模型的建立与修正一切物质都是由最小的不能再分的粒子——原子构成。
原子模型:原子是坚实的、不可再分的实心球。道尔顿原子模型(1803年)——实心球模型原子并不是构成物质的最小微粒 ——汤姆生发现了电子(1897年)电子是种带负电、有一定质量的微粒,普遍存在于各种原子之中。
汤姆生原子模型:原子是一个平均分布着正电荷的粒子,其中镶嵌着许多电子,中和了电荷,从而形成了中性原子。.汤姆生原子模型(1904年)——汤姆生模型 电子在原子核外空间的一定轨道上分层绕核做高速的圆周运动。.波尔原子模型(1913年)——分层模型.电子云模型(1927年—1935年) 道尔顿原子模型(1803年)——实心球模型.汤姆生原子模型(1904年)——汤姆生模型 .波尔原子模型(1913年)——分层模型.电子云模型(1927年—1935年) 3、2004年诺贝尔物理学奖颁给了美国的三位科学家格罗斯、波利茨、威乐茨克,他们对有关原子核内夸克之间存在的强作用力的研究方面作出了管理重要的理论发现。有关夸克的说法,不正确的是( )
A夸克是目前原子核中发现的最小粒子
B、质子和中子都是由夸克构成
C、不是所有分子中都存在夸克粒子
D、夸克研究是一个科学研究的热点C4、最接近原子实际的原子结构模型是( )
A、汤姆森模型 B、卢瑟福模型
C、波尔分层模型 D、电子云模型D5、在化学变化中可分的微粒是 ( )
A、原子 B、分子 C、质子 D、原子核B2.物质、元素、分子、原子的区别与联系 微观粒子
(讲种类、讲个数) 宏观概念
(只讲种类、不讲个数)2、(1)组成人体的主要元素有: 。(2)组成地球的主要元素有:
。 (3)重要化肥的有效元素有:
。 氧 硅 铝 铁 氧 碳 氢 氮氮、磷、钾例1:元素符号的意义② 元素符号Fe代表什么意义?① 用元素符号表示1个碳原子、3个氮原子、2个钙原子C3N2Ca1、表示铁元素2、表示一个铁原子3、表示物质铁(铁单质)练一练下列各个2表示的意义
2H2 2Cl 2Mg2+
2NO3 Ba
+2-分析化学式“H2O” 给你传递了多少信息 ①水②水是由氢氧两种元素组成③一个水分子④每个水分子是由2个氢原子1个氧原子构成宏观微观例2:自第十一届奥运会以来,历届奥运会都要举行颇为隆重的“火炬接力”,火炬的可燃物为丁烷(化学式C4H10),它燃烧时,火苗高且亮,在白天,二百米以外也能清晰可见,下列关于丁烷的叙述正确的是( )
①丁烷是由碳、氢两种元素组成的
②丁烷是由丁烷分子构成的
③丁烷分子是由碳、氢两种元素组成的
④丁烷由4个碳原子和10个氢原子组成
⑤丁烷分子是由碳原子和氧原子构成的根据化学式计算组成物质的元素的质量比 b
根据化学式计算组成物质的某元素的质量分数 b10、原子核内有6个质子和6个中子的一种碳原子的质量为x克,另一种元素R的原子质量为y克.则R的相对原子质量为( )
A.y克 B.12x/y克 C.y/x D.12y/x18、100克含碳酸钙(CaCO3)90%的石灰石中,所含钙元素的质量为 ( )
A、90克 B、36克 C、18克 D、12.5克B练习:(3)会根据化学式进行简单的计算1、某元素的相对原子质量为 24,化合价为+2价,那么其氧化物中的含氧质量分数为( )
A.12% B.24% C.30% D.60%40%(3)会根据化学式进行简单的计算2、骨质疏松症是由人体缺钙引起的,可服用补钙剂来治疗。乳酸钙(CaC6H10O6 ? 5H2O)是一种常见的补钙剂。市售乳酸钙片剂,每片含乳酸钙200mg,一个成年缺钙病人每天服用20片可达到补钙目的
计算:(计算结果保留整数)
(1)乳酸钙中各元素的质量比
(2)乳酸钙中钙元素的质量分数
(3)该成年缺钙病人改用牛奶(每100ml牛奶中含钙>=1.04g)来补钙每天至少需喝多少ml牛奶13%50ml1、经检测一份尿样中含尿素CO(NH2)2 的质量分数为2%,假定其他成分不含氮,求:此尿样中氮元素的质量分数;尿素在尿样中的质量分数尿素中含氮元素的质量分数×6。常见元素的化合价 7。原子团的化合价例3:化合价与化学式之间的应用(1)用化合价写出简单的化学式已知氮的化合价有-3、0、+1、+2、+3、+4、+5,试着写出氮与氢元素或氮与氧元素形成的化合物NH3、N2O、NO、N2O3、NO2、N2O5、(2)根据化学式推断元素的化合价1、新型的净水剂铁酸钠(Na2FeO4)中,铁元素的化合价为 ----------( )
A. 6价 B.+5价 C.+3价 D.十2价A+6价机动车驾驶员严禁酒后驾车,交警常用装有重铬酸钾(K2Cr2O7)的仪器检测司机是否酒后驾车,因为酒中的乙醇分子可以使橙红色重铬酸钾变为绿色硫酸铬,重铬酸钾(K2Cr2O7)中铬元素的化合价是( )
A、+3 B、+5 C、+6 D、+7已知某元素R只有一种化合价,其氯化物的化学式为RCl3那么其氧化物的化学式为 。
CO2二氧化碳这种物质(1个)二氧化碳分子二氧化碳由碳元素和氧元素组成(1个)二氧化碳分子由(2个)氧原子和(1个)碳原子构成二氧化碳的相对分子质量为:12+2×16=44三、常见的物质分类请你写出各类分类的依据例4:物质的分类1、(天津市2004年)美国和日本的三位科学家以导电有机高分子材料的研究成果,荣获了2000年度诺贝尔化学奖。在其相关技术中,用碘来掺杂聚合物,使其导电能力增加107倍,具有金属般的导电能力。碘(I2)属于--------------------( )
A.非金属单质 B.混合物 C.化合物 D.金属单质A例4:物质的分类2、根据下列模型,分别写出A、B、C、D分别属于哪一类物质A、_______B、________C、_______D、______。化合物混合物单质混合物例5:混合物的分离操作和粗盐的提纯过程1.(’04山东)用足量的含不溶性固体杂质(其含量不详)的粗盐,经提纯后配制一定溶质质量分数的NaCl溶液,实验操作有 ①称量 ②过滤 ③蒸发结晶 ④计算 ⑤溶解 ⑥干燥。其先后顺序正确的是 ( )
A、④⑤②③⑤①⑥
B.④⑤②③①⑥⑤
C.⑤②③⑥④①⑤
D.④①⑤②③⑥⑤C例5:混合物的分离操作和粗盐的提纯过程2.粗盐提纯实验中,必须用到的一组仪器是 ( )
(A)量筒、酒精灯、漏斗;玻璃棒
(B)烧杯,漏斗、坩埚、玻璃棒
(C)烧杯、酒精灯、玻璃棒、漏斗、蒸发皿
(D)铁架台、烧杯、胶头滴管、酒精灯C结构和组成决定性质,性质决定用途和制取33.物质的分类标准有多种,标准可以是物质的组成、性质、用途……。请根据所学知识,依据物质所具有的某种性质,自拟两种分类标准,对以下物质进行分类,每类至少包括三种物质(填化学式)氢气、氧气、一氧化碳、二氧化碳、二氧化硫(棕红色、有毒)、水、碳。
分类标准一:_____________________ ___,
包括物质____________ ___;
分类标准二:_____________________ _,
包括物质_____________ ___。
2、右图为精制粗盐的示意图,回答 (1)写出仪器名称① __________②______________
(2)漏斗中的液面应 __________(填“高”或“低”)于滤纸边缘
(3)蒸发滤液时,玻璃棒起的作用是 _________,图中玻璃棒的作用是______________
(4)粗盐提纯时正确顺序是( )
A、溶解、蒸发、过滤
B、过滤,蒸发
C、溶解、过滤、冷却
D、溶解、过滤、蒸发
复习导引67页铜 食盐晶体 金刚石二氧化碳模型水 水由______构成 金刚石由______构成 铜由______构成 二氧化碳由___ ___构成 食盐由____ __构成 水分子碳原子铜原子二氧化碳分子钠离子和氯离子分子、原子、离子是三种构成物质的微粒。分子
原子
离子分
解构
成得
失
电
子构成O2、N2、H2
直接构成金属,如Fe、Cu等
构成NaCl、MgO等物质构成物质的微粒H2O、CO2等物质
稀有气体,如:氖气,氦气金刚石、硅等水结成冰后,物理性质是否改变了?水结成冰后,化学性质是否改变了?水结成冰后,水分子是否被拆散?水电解后,生成了氢气和氧气,那么水分子是否发生改变?水电解后,生成了氢气和氧气,那么氢、氧原子是否变成了新的原子?氢、氧原子是否不可再分?分子原子离子构成物质的微粒半径在10-10米数量级,
质量为 1.993n×10-26千克
(n为相对原子质量或相对分子质量 )微粒的大小保持物质化学性质的一种微粒化学变化中的最小微粒带电的原子或原子团分子原子化学反应中破裂相互结合构成纳米材料 以纳米为单位的超级微小颗粒(材料)颗粒直径:(1nm--100nm) 包括金属、非金属、有机、无机和
生物等多种粉末材料。在机械强度、磁、光、声、热等与普通材料不同常见的纳米材料纳米陶瓷韧性好,撞击不破裂 在切削刀具、轴承、汽车发动机部件等诸多方面
都有广泛的应用,并在许多超高温、强腐蚀等苛
刻的环境下起着其他材料不可替代的作用,具有
广阔的应用前景 纳米油墨 色调浓,字迹色泽好 日本等国已有部分纳米二氧化钛的化妆品
问世。紫外线不仅能使肉类食品自动氧化而变
色,而且还会破坏食品中的维生素和芳香化合
物,从而降低食品的营养价值。如用添加
0.1~0.5%的纳米二氧化钛制成的透明塑料包装
材料包装食品,既可以防止紫外线对食品的破
坏作用,还可以使食品保持新鲜。 断裂应力比一般铁材料高12倍纳米铁材料原子(带负电)(带正电)(不带电)都是由夸克构成
核外电子原子核质子中子原子的结构电子的质量占原子的比重极小,几乎可以忽略
不计,原子的质量主要集中在原子核上。核电荷数核外电子数核内质子数==原子相对质量质子数中子数=+1、构成细胞的微粒是 ( )
A、细胞质、细胞膜、细胞核 B、溶质、溶剂
C、分子、原子、离子 D、中子、质子
例3.1985年科学家发现的C60分子是由60个碳原子构成的,它的形状像足球(如图C),因此又叫足球烯(音希)。1991年科学家又发现一种碳的单质——碳纳米管,它是由六边形的碳原子构成的管状大分子(如图D)。下图中,A、B分别是金刚石和石墨的结构示意图。
用你所学到的化学知识回答下列问题:
金刚石、石墨、足球烯、碳纳米管物理性质有较大差异的原因是什么?
答:________________。
原子之间的排列(结构)不同1、原子结构模型的建立与修正一切物质都是由最小的不能再分的粒子——原子构成。
原子模型:原子是坚实的、不可再分的实心球。道尔顿原子模型(1803年)——实心球模型原子并不是构成物质的最小微粒 ——汤姆生发现了电子(1897年)电子是种带负电、有一定质量的微粒,普遍存在于各种原子之中。
汤姆生原子模型:原子是一个平均分布着正电荷的粒子,其中镶嵌着许多电子,中和了电荷,从而形成了中性原子。.汤姆生原子模型(1904年)——汤姆生模型 电子在原子核外空间的一定轨道上分层绕核做高速的圆周运动。.波尔原子模型(1913年)——分层模型.电子云模型(1927年—1935年) 道尔顿原子模型(1803年)——实心球模型.汤姆生原子模型(1904年)——汤姆生模型 .波尔原子模型(1913年)——分层模型.电子云模型(1927年—1935年) 3、2004年诺贝尔物理学奖颁给了美国的三位科学家格罗斯、波利茨、威乐茨克,他们对有关原子核内夸克之间存在的强作用力的研究方面作出了管理重要的理论发现。有关夸克的说法,不正确的是( )
A夸克是目前原子核中发现的最小粒子
B、质子和中子都是由夸克构成
C、不是所有分子中都存在夸克粒子
D、夸克研究是一个科学研究的热点C4、最接近原子实际的原子结构模型是( )
A、汤姆森模型 B、卢瑟福模型
C、波尔分层模型 D、电子云模型D5、在化学变化中可分的微粒是 ( )
A、原子 B、分子 C、质子 D、原子核B2.物质、元素、分子、原子的区别与联系 微观粒子
(讲种类、讲个数) 宏观概念
(只讲种类、不讲个数)2、(1)组成人体的主要元素有: 。(2)组成地球的主要元素有:
。 (3)重要化肥的有效元素有:
。 氧 硅 铝 铁 氧 碳 氢 氮氮、磷、钾例1:元素符号的意义② 元素符号Fe代表什么意义?① 用元素符号表示1个碳原子、3个氮原子、2个钙原子C3N2Ca1、表示铁元素2、表示一个铁原子3、表示物质铁(铁单质)练一练下列各个2表示的意义
2H2 2Cl 2Mg2+
2NO3 Ba
+2-分析化学式“H2O” 给你传递了多少信息 ①水②水是由氢氧两种元素组成③一个水分子④每个水分子是由2个氢原子1个氧原子构成宏观微观例2:自第十一届奥运会以来,历届奥运会都要举行颇为隆重的“火炬接力”,火炬的可燃物为丁烷(化学式C4H10),它燃烧时,火苗高且亮,在白天,二百米以外也能清晰可见,下列关于丁烷的叙述正确的是( )
①丁烷是由碳、氢两种元素组成的
②丁烷是由丁烷分子构成的
③丁烷分子是由碳、氢两种元素组成的
④丁烷由4个碳原子和10个氢原子组成
⑤丁烷分子是由碳原子和氧原子构成的根据化学式计算组成物质的元素的质量比 b
根据化学式计算组成物质的某元素的质量分数 b10、原子核内有6个质子和6个中子的一种碳原子的质量为x克,另一种元素R的原子质量为y克.则R的相对原子质量为( )
A.y克 B.12x/y克 C.y/x D.12y/x18、100克含碳酸钙(CaCO3)90%的石灰石中,所含钙元素的质量为 ( )
A、90克 B、36克 C、18克 D、12.5克B练习:(3)会根据化学式进行简单的计算1、某元素的相对原子质量为 24,化合价为+2价,那么其氧化物中的含氧质量分数为( )
A.12% B.24% C.30% D.60%40%(3)会根据化学式进行简单的计算2、骨质疏松症是由人体缺钙引起的,可服用补钙剂来治疗。乳酸钙(CaC6H10O6 ? 5H2O)是一种常见的补钙剂。市售乳酸钙片剂,每片含乳酸钙200mg,一个成年缺钙病人每天服用20片可达到补钙目的
计算:(计算结果保留整数)
(1)乳酸钙中各元素的质量比
(2)乳酸钙中钙元素的质量分数
(3)该成年缺钙病人改用牛奶(每100ml牛奶中含钙>=1.04g)来补钙每天至少需喝多少ml牛奶13%50ml1、经检测一份尿样中含尿素CO(NH2)2 的质量分数为2%,假定其他成分不含氮,求:此尿样中氮元素的质量分数;尿素在尿样中的质量分数尿素中含氮元素的质量分数×6。常见元素的化合价 7。原子团的化合价例3:化合价与化学式之间的应用(1)用化合价写出简单的化学式已知氮的化合价有-3、0、+1、+2、+3、+4、+5,试着写出氮与氢元素或氮与氧元素形成的化合物NH3、N2O、NO、N2O3、NO2、N2O5、(2)根据化学式推断元素的化合价1、新型的净水剂铁酸钠(Na2FeO4)中,铁元素的化合价为 ----------( )
A. 6价 B.+5价 C.+3价 D.十2价A+6价机动车驾驶员严禁酒后驾车,交警常用装有重铬酸钾(K2Cr2O7)的仪器检测司机是否酒后驾车,因为酒中的乙醇分子可以使橙红色重铬酸钾变为绿色硫酸铬,重铬酸钾(K2Cr2O7)中铬元素的化合价是( )
A、+3 B、+5 C、+6 D、+7已知某元素R只有一种化合价,其氯化物的化学式为RCl3那么其氧化物的化学式为 。
CO2二氧化碳这种物质(1个)二氧化碳分子二氧化碳由碳元素和氧元素组成(1个)二氧化碳分子由(2个)氧原子和(1个)碳原子构成二氧化碳的相对分子质量为:12+2×16=44三、常见的物质分类请你写出各类分类的依据例4:物质的分类1、(天津市2004年)美国和日本的三位科学家以导电有机高分子材料的研究成果,荣获了2000年度诺贝尔化学奖。在其相关技术中,用碘来掺杂聚合物,使其导电能力增加107倍,具有金属般的导电能力。碘(I2)属于--------------------( )
A.非金属单质 B.混合物 C.化合物 D.金属单质A例4:物质的分类2、根据下列模型,分别写出A、B、C、D分别属于哪一类物质A、_______B、________C、_______D、______。化合物混合物单质混合物例5:混合物的分离操作和粗盐的提纯过程1.(’04山东)用足量的含不溶性固体杂质(其含量不详)的粗盐,经提纯后配制一定溶质质量分数的NaCl溶液,实验操作有 ①称量 ②过滤 ③蒸发结晶 ④计算 ⑤溶解 ⑥干燥。其先后顺序正确的是 ( )
A、④⑤②③⑤①⑥
B.④⑤②③①⑥⑤
C.⑤②③⑥④①⑤
D.④①⑤②③⑥⑤C例5:混合物的分离操作和粗盐的提纯过程2.粗盐提纯实验中,必须用到的一组仪器是 ( )
(A)量筒、酒精灯、漏斗;玻璃棒
(B)烧杯,漏斗、坩埚、玻璃棒
(C)烧杯、酒精灯、玻璃棒、漏斗、蒸发皿
(D)铁架台、烧杯、胶头滴管、酒精灯C结构和组成决定性质,性质决定用途和制取33.物质的分类标准有多种,标准可以是物质的组成、性质、用途……。请根据所学知识,依据物质所具有的某种性质,自拟两种分类标准,对以下物质进行分类,每类至少包括三种物质(填化学式)氢气、氧气、一氧化碳、二氧化碳、二氧化硫(棕红色、有毒)、水、碳。
分类标准一:_____________________ ___,
包括物质____________ ___;
分类标准二:_____________________ _,
包括物质_____________ ___。
2、右图为精制粗盐的示意图,回答 (1)写出仪器名称① __________②______________
(2)漏斗中的液面应 __________(填“高”或“低”)于滤纸边缘
(3)蒸发滤液时,玻璃棒起的作用是 _________,图中玻璃棒的作用是______________
(4)粗盐提纯时正确顺序是( )
A、溶解、蒸发、过滤
B、过滤,蒸发
C、溶解、过滤、冷却
D、溶解、过滤、蒸发
