碱的通性[下学期]
图片预览






文档简介
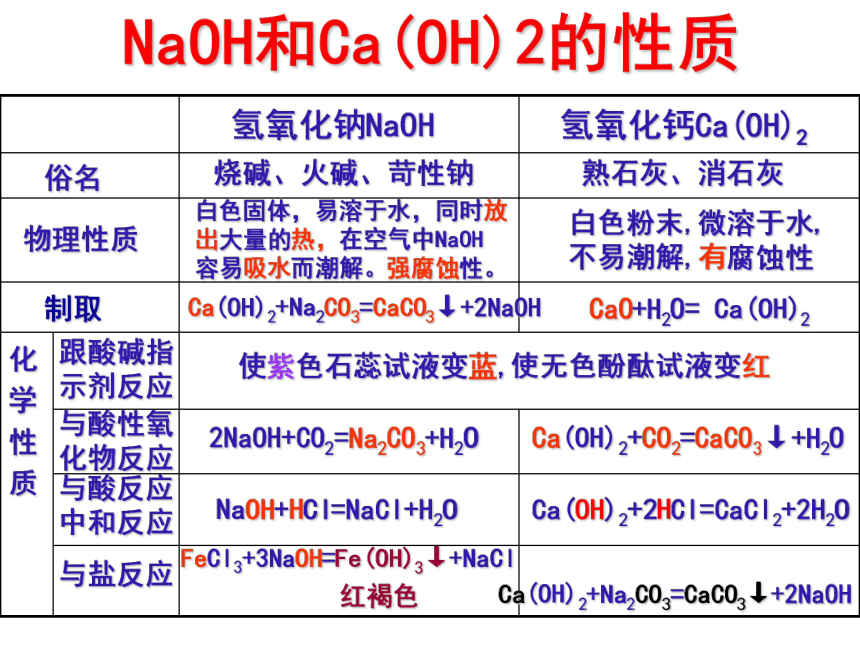
课件17张PPT。探索碱的性质第3课时碱的通性NaOH和Ca(OH)2的性质 氢氧化钠NaOH 氢氧化钙Ca(OH)2俗名 物理性质 跟酸碱指示剂反应烧碱、火碱、苛性钠 熟石灰、消石灰 白色固体,易溶于水,同时放出大量的热,在空气中NaOH 容易吸水而潮解。强腐蚀性。 白色粉末,微溶于水,不易潮解,有腐蚀性 使紫色石蕊试液变蓝,使无色酚酞试液变红 与酸性氧化物反应 2NaOH+CO2=Na2CO3+H2O Ca(OH)2+CO2=CaCO3↓+H2O 与酸反应
中和反应NaOH+HCl=NaCl+H2O Ca(OH)2+2HCl=CaCl2+2H2O 与盐反应FeCl3+3NaOH=Fe(OH)3↓+NaCl
红褐色 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH化
学
性
质制取CaO+H2O= Ca(OH)2Ca(OH)2+Na2CO3=CaCO3↓+2NaOH碱 的 通 性1. 碱可与酸碱指示剂作用:
2. 碱+ 非金属氧化物→盐+水
3.碱+酸→盐+水
4. 碱+某些 盐→新碱+新盐可溶可溶可溶可溶可 溶可溶性碱能使石蕊试液变蓝,酚酞试液变红。2NaOH+SO2=Na2SO3+H2ONaOH+HCl=NaCl+H2O2NaOH+CuCl2=Cu(OH)2↓+2NaClCa(OH)2+CO2=CaCO3↓+H2OCa(OH)2+H2SO4=CaSO4+2H2OCa(OH)2+Na2CO3=CaCO3↓+2NaOHCu(OH)2能使指示剂变色吗?NaOH+CO能反应吗?KOH+BaCl2.Ca(OH)2+CuCO3能反应吗?电离时生成阴离子都是OH-,
一般可溶性碱具有以上四条通性大多难溶碱一般只与酸反应:难溶性碱的性质Fe(OH)3+3HCl ==FeCl3+3H2O难溶性碱:CuO+H2O=Cu(OH)2 错,CuO不溶于水可溶性碱:CaO+ H2O =Ca(OH)2
Na2O + H2O = 2NaOH 错,可溶碱受热不分解2.碱的通性指的是可溶碱而言.不溶碱
一般只跟酸反应3.碱一般不能与金属氧化物反应,酸一
般不能与非金属氧化物反应 4.不溶碱受热易分解;可溶碱受热不分解.5.碱有通性是因为溶液中的阴离子都是氢氧根离子 强调:1.碱与盐反应反应物均要可溶碱的通性是指可溶性碱而言以Ba(OH)2为例,分别写出它与SO3、CO2、H2SO4、HCl和CuSO4、Fe2(SO4)2的反应。Ba(OH)2+SO3==BaSO4↓+H2OBa(OH)2+CO2==BaCO3↓+H2OBa(OH)2+2HNO3==Ba(NO3)2+2H2OBa(OH)2+H2SO4==BaSO4↓+2H2OBa(OH)2+CuSO4==BaSO4↓+Cu(OH)2↓3Ba(OH)2+Fe2(SO4)3==3BaSO4↓+2Fe(OH)3↓白色沉淀既有白色沉淀,又有蓝色沉淀既有白色沉淀,又有红褐色沉淀反应无现象 氨水(化学式为NH3·H2O)为无色透明或微带黄色的液体,溶解度很大,是一种弱碱(pH值10左右),易挥发,有腐蚀性,对人有刺激性;它的电离方程式:NH3.H2O = NH4++ OH-,请根据碱的通性写出它的性质:氨水特性1.可溶碱与酸碱指示剂作用:
2.可溶碱+大多非金属氧化物→
3.碱+酸→盐+水
4.可溶碱+某些可溶盐→新碱+新盐氨水可使石蕊试液变蓝,酚酞试液变红.NH3.H2O+HCl==NH4Cl+H2O3NH3.H2O+FeCl3==Fe(OH)3↓+3NH4Cl思考?能与二氧化碳反应生成碳酸氢铵,请写出化学方程式;有人称它为“气肥”,你知道是为什么吗?NH3·H2O + CO2 = NH4HCO31.下列物质的溶液中跟盐酸.二氧化碳.碳酸钠都能发生化学反应的是( )
(A)NaOH (B)Ba(OH)2 (C)BaCl2 (D)H2SO42.只用酚酞一种指示剂就能鉴别的一组溶液是( )
A.NaOH、HCl、NaCl B.NaOH、BaCl2、NaNO3
C.NaOH、NaCl、MgCl2 D.NaOH、KOH、HCl AC3.下列关于碱的性质的叙述中,错误的是( )
A.碱溶液中滴入紫色石蕊试液变蓝色。
B.非金属氧化物都能跟碱反应生成盐和水。
C.非金属氧化物跟碱反应生成盐和水,但不是中和反应
D.碱溶液只能跟某些盐发生反应。BB4.下列物质中,既能与氢氧化钙溶液反应,又能与盐酸反应的是( )
A.碳酸钠 B.二氧化碳 C.氧化铜 D.氢氧化钠A6.下列可用于鉴别NaOH、BaCl2、HCl三瓶无色溶液的一种试剂是( ) A、硫酸铜溶液
B、氢氧化铜固体 C、硝酸银溶液 D、酚酞试液A5.下列性质中,可以确定某物质属于碱的是( )
A.能是酚酞试液变红色 B.PH>7的溶液
C.能跟酸发生反应生成盐和水 D.水溶液能导电
E.电离时生成的阴离子全部是氢氧根离子D7.可一次将AgNO3、Na2CO3、MgCl2三种无色溶液区别开来的试剂是( )
A.HNO3溶液 B.NaCl溶液 C.Na2SO4溶液 D.稀盐酸DB8.下列叙述中不正确的是( )
A.酸和碱一定都含有氢元素,但酸不一定含氧元素
B.硫酸氢钠在水溶液中可电离出H+,并且其水溶液可使紫色石蕊试液显红色,所以硫酸氢钠也是一种酸
C.碱溶液能使酚酞变红,但能使酚酞变红溶液不一定是碱溶液
D.含氧化合物可能不是氧化物 9.我校初中自然科学实验室所用的化学药品,很多是易燃、易爆、有毒、有腐蚀性的。在使用时,一定要严格遵照有关规定和操作规程,确保安全。现有下图所示四种图标,请你找出适合贴在存放氢氧化钠、氢氧化钾等浓碱药品橱上的图标( ) 10.溶液的碱性强弱跟溶液中OH-数量有关,一定体积的溶液中OH-数量越多,则溶液碱性越强,10%的NaOH溶液(密度为1.1g/cm3)与10%的KOH溶液(密度是1.1g/cm3)相比较,碱性更强的是( )
A.NaOH B.KOH C.一样强 D.无法比较DA稀硫酸或
稀盐酸氢氧化钙或
氢氧化钡氯化钡或
硝酸钙溶液12.为了证明长期暴露在空气中的氢氧化钠溶液已经部分变质,实验前请选用三种不同物质类别的试剂.Na2CO3+2HCl=
2NaCl+H2O+CO2↑Ca(OH)2+Na2CO3=
CaCO3↓+2NaOHBaCl2+Na2CO3=
BaCO3↓+2NaCl11.分别将下列各组内的二种物质同时放入水中,得到无色透明溶液的是( ) A.FeCl3.KOH B.K2SO4.BaCl2 C.CuSO4.HCl D.Na2SO4.NaNO3D13,我国古代纺织常用氢氧化钾做漂洗的洗涤剂:前人用贝壳(主要成份是碳酸钙)煅烧后的固体与草木灰(主要成份是碳酸钾)在水中相互作用,便可得到氢氧化钾,写出上述反应方程式并注明反应类型:CaO+H2O=Ca(OH)2Ca(OH)2+K2CO3=CaCO3↓+2KOH分解反应化合反应复分解反应14.如图,广口瓶中盛有气体X,胶头滴管中盛有液体Y,若挤压胶头滴管使液体滴入瓶中,振荡,一段时间可见小球膨胀起来,那么当X为CO2,那么Y为 ;当Y为水,则X应为 . NaOH等碱性溶液HCl.NH3等易溶气体不可,生成氢氧化钠,影响对氢氧化钠的确定不正确,两者混合物也可不正确,碳酸钠也呈碱性碳酸钠向滤液中滴酚酞(或石蕊)试液15.小刚在化学实验室发现,盛放NaOH溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末。小刚叫来小军和小红,共同探究这种白色粉末的成分。他们依据所学的化学知识,对这种白色粉末的成分作了如下猜想:① 可能是NaOH; ② 可能是Na2CO3; ③ 可能是NaOH与Na2CO3的混合物。
(1)小刚取少量白色粉末,滴加稀盐酸,有气体生成。由此小刚认为白色粉末是Na2CO3。请判断小刚所得结论是否正确,并简述理由。_______________________________。
(2)小军取少量白色粉末溶于水,向所得溶液中滴加酚酞试液,溶液变为红色。由此小军认为白色粉末是NaOH。请判断小刚所得结论是否正确,并简述理由。_______________________.
(3)小红取少量白色粉末溶于水,向所得溶液中滴加BaCl2试液,有白色沉淀产生。由此判断白色粉末中含有________。为了验证猜想③,小红继续向溶液中滴加BaCl2试液至不再产生沉淀,然后过滤。你认为她接下来还应进行的实验是___________________________;
在小红所做的实验中,若把BaCl2溶液换成Ba(OH)2溶液是否可行?请简述理由。___________________________________。17.某校化学兴趣小组的同学做制取难溶性的氢氧化铜Cu(OH)2
的实验。(1)在盛有黑色氧化铜粉末的试管中加入稀硫酸,其反应化学方程式是 。
(2)上述反应后,再向试管中加氢氧化钠溶液,制得氢氧化铜,其反应化学方程式是 。现在甲、乙两同学分别做该实验,实验结束,看到不同的现象。甲同学看到了蓝色絮状沉淀;而乙同学看到均是蓝色溶液。你认为实验成功的是 同学。试分析另一位同学所看到现象的原因是 .CuO +H2SO4==CuSO4 +H2O甲 乙同学实验一时加入的稀硫酸太多,使得实验二中的氢氧化钠溶液无法与CuSO4反应16.现有①氯化钠. ②氯化镁. ③氢氧化钠. ④氯化铁四种溶液,不另用任何试剂,仅用观察法和溶液之间的相互反应就可以将其区分出来,则鉴别出来的先后顺序是 .④ ③ ② ①H2SO4NaOHMgCl220.某溶液由NaOH.HCl.H2SO4和MgCl2中的一种或几种组成,向该溶液中滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2 溶
液体积的关系如右图所示,
请你从图中获得的信息来
分析,该溶液中不可能存
在的物质是 ;
肯定存在的物质是 .HCl18.请你根据碱的两种不同性质,设计实验来证明溶液呈碱性 , .19.欲制取少量NaOH,下列各组试剂可选用的一组是( ) A.NaCl.Cu(OH)2 B.NaNO3.Ba(OH)2 C.Na2CO3.Ca(OH)2 D.Na2SO4.Mg(OH)2石蕊(或酚酞)CuSO4(或FeCl3)C再见!
中和反应NaOH+HCl=NaCl+H2O Ca(OH)2+2HCl=CaCl2+2H2O 与盐反应FeCl3+3NaOH=Fe(OH)3↓+NaCl
红褐色 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH化
学
性
质制取CaO+H2O= Ca(OH)2Ca(OH)2+Na2CO3=CaCO3↓+2NaOH碱 的 通 性1. 碱可与酸碱指示剂作用:
2. 碱+ 非金属氧化物→盐+水
3.碱+酸→盐+水
4. 碱+某些 盐→新碱+新盐可溶可溶可溶可溶可 溶可溶性碱能使石蕊试液变蓝,酚酞试液变红。2NaOH+SO2=Na2SO3+H2ONaOH+HCl=NaCl+H2O2NaOH+CuCl2=Cu(OH)2↓+2NaClCa(OH)2+CO2=CaCO3↓+H2OCa(OH)2+H2SO4=CaSO4+2H2OCa(OH)2+Na2CO3=CaCO3↓+2NaOHCu(OH)2能使指示剂变色吗?NaOH+CO能反应吗?KOH+BaCl2.Ca(OH)2+CuCO3能反应吗?电离时生成阴离子都是OH-,
一般可溶性碱具有以上四条通性大多难溶碱一般只与酸反应:难溶性碱的性质Fe(OH)3+3HCl ==FeCl3+3H2O难溶性碱:CuO+H2O=Cu(OH)2 错,CuO不溶于水可溶性碱:CaO+ H2O =Ca(OH)2
Na2O + H2O = 2NaOH 错,可溶碱受热不分解2.碱的通性指的是可溶碱而言.不溶碱
一般只跟酸反应3.碱一般不能与金属氧化物反应,酸一
般不能与非金属氧化物反应 4.不溶碱受热易分解;可溶碱受热不分解.5.碱有通性是因为溶液中的阴离子都是氢氧根离子 强调:1.碱与盐反应反应物均要可溶碱的通性是指可溶性碱而言以Ba(OH)2为例,分别写出它与SO3、CO2、H2SO4、HCl和CuSO4、Fe2(SO4)2的反应。Ba(OH)2+SO3==BaSO4↓+H2OBa(OH)2+CO2==BaCO3↓+H2OBa(OH)2+2HNO3==Ba(NO3)2+2H2OBa(OH)2+H2SO4==BaSO4↓+2H2OBa(OH)2+CuSO4==BaSO4↓+Cu(OH)2↓3Ba(OH)2+Fe2(SO4)3==3BaSO4↓+2Fe(OH)3↓白色沉淀既有白色沉淀,又有蓝色沉淀既有白色沉淀,又有红褐色沉淀反应无现象 氨水(化学式为NH3·H2O)为无色透明或微带黄色的液体,溶解度很大,是一种弱碱(pH值10左右),易挥发,有腐蚀性,对人有刺激性;它的电离方程式:NH3.H2O = NH4++ OH-,请根据碱的通性写出它的性质:氨水特性1.可溶碱与酸碱指示剂作用:
2.可溶碱+大多非金属氧化物→
3.碱+酸→盐+水
4.可溶碱+某些可溶盐→新碱+新盐氨水可使石蕊试液变蓝,酚酞试液变红.NH3.H2O+HCl==NH4Cl+H2O3NH3.H2O+FeCl3==Fe(OH)3↓+3NH4Cl思考?能与二氧化碳反应生成碳酸氢铵,请写出化学方程式;有人称它为“气肥”,你知道是为什么吗?NH3·H2O + CO2 = NH4HCO31.下列物质的溶液中跟盐酸.二氧化碳.碳酸钠都能发生化学反应的是( )
(A)NaOH (B)Ba(OH)2 (C)BaCl2 (D)H2SO42.只用酚酞一种指示剂就能鉴别的一组溶液是( )
A.NaOH、HCl、NaCl B.NaOH、BaCl2、NaNO3
C.NaOH、NaCl、MgCl2 D.NaOH、KOH、HCl AC3.下列关于碱的性质的叙述中,错误的是( )
A.碱溶液中滴入紫色石蕊试液变蓝色。
B.非金属氧化物都能跟碱反应生成盐和水。
C.非金属氧化物跟碱反应生成盐和水,但不是中和反应
D.碱溶液只能跟某些盐发生反应。BB4.下列物质中,既能与氢氧化钙溶液反应,又能与盐酸反应的是( )
A.碳酸钠 B.二氧化碳 C.氧化铜 D.氢氧化钠A6.下列可用于鉴别NaOH、BaCl2、HCl三瓶无色溶液的一种试剂是( ) A、硫酸铜溶液
B、氢氧化铜固体 C、硝酸银溶液 D、酚酞试液A5.下列性质中,可以确定某物质属于碱的是( )
A.能是酚酞试液变红色 B.PH>7的溶液
C.能跟酸发生反应生成盐和水 D.水溶液能导电
E.电离时生成的阴离子全部是氢氧根离子D7.可一次将AgNO3、Na2CO3、MgCl2三种无色溶液区别开来的试剂是( )
A.HNO3溶液 B.NaCl溶液 C.Na2SO4溶液 D.稀盐酸DB8.下列叙述中不正确的是( )
A.酸和碱一定都含有氢元素,但酸不一定含氧元素
B.硫酸氢钠在水溶液中可电离出H+,并且其水溶液可使紫色石蕊试液显红色,所以硫酸氢钠也是一种酸
C.碱溶液能使酚酞变红,但能使酚酞变红溶液不一定是碱溶液
D.含氧化合物可能不是氧化物 9.我校初中自然科学实验室所用的化学药品,很多是易燃、易爆、有毒、有腐蚀性的。在使用时,一定要严格遵照有关规定和操作规程,确保安全。现有下图所示四种图标,请你找出适合贴在存放氢氧化钠、氢氧化钾等浓碱药品橱上的图标( ) 10.溶液的碱性强弱跟溶液中OH-数量有关,一定体积的溶液中OH-数量越多,则溶液碱性越强,10%的NaOH溶液(密度为1.1g/cm3)与10%的KOH溶液(密度是1.1g/cm3)相比较,碱性更强的是( )
A.NaOH B.KOH C.一样强 D.无法比较DA稀硫酸或
稀盐酸氢氧化钙或
氢氧化钡氯化钡或
硝酸钙溶液12.为了证明长期暴露在空气中的氢氧化钠溶液已经部分变质,实验前请选用三种不同物质类别的试剂.Na2CO3+2HCl=
2NaCl+H2O+CO2↑Ca(OH)2+Na2CO3=
CaCO3↓+2NaOHBaCl2+Na2CO3=
BaCO3↓+2NaCl11.分别将下列各组内的二种物质同时放入水中,得到无色透明溶液的是( ) A.FeCl3.KOH B.K2SO4.BaCl2 C.CuSO4.HCl D.Na2SO4.NaNO3D13,我国古代纺织常用氢氧化钾做漂洗的洗涤剂:前人用贝壳(主要成份是碳酸钙)煅烧后的固体与草木灰(主要成份是碳酸钾)在水中相互作用,便可得到氢氧化钾,写出上述反应方程式并注明反应类型:CaO+H2O=Ca(OH)2Ca(OH)2+K2CO3=CaCO3↓+2KOH分解反应化合反应复分解反应14.如图,广口瓶中盛有气体X,胶头滴管中盛有液体Y,若挤压胶头滴管使液体滴入瓶中,振荡,一段时间可见小球膨胀起来,那么当X为CO2,那么Y为 ;当Y为水,则X应为 . NaOH等碱性溶液HCl.NH3等易溶气体不可,生成氢氧化钠,影响对氢氧化钠的确定不正确,两者混合物也可不正确,碳酸钠也呈碱性碳酸钠向滤液中滴酚酞(或石蕊)试液15.小刚在化学实验室发现,盛放NaOH溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末。小刚叫来小军和小红,共同探究这种白色粉末的成分。他们依据所学的化学知识,对这种白色粉末的成分作了如下猜想:① 可能是NaOH; ② 可能是Na2CO3; ③ 可能是NaOH与Na2CO3的混合物。
(1)小刚取少量白色粉末,滴加稀盐酸,有气体生成。由此小刚认为白色粉末是Na2CO3。请判断小刚所得结论是否正确,并简述理由。_______________________________。
(2)小军取少量白色粉末溶于水,向所得溶液中滴加酚酞试液,溶液变为红色。由此小军认为白色粉末是NaOH。请判断小刚所得结论是否正确,并简述理由。_______________________.
(3)小红取少量白色粉末溶于水,向所得溶液中滴加BaCl2试液,有白色沉淀产生。由此判断白色粉末中含有________。为了验证猜想③,小红继续向溶液中滴加BaCl2试液至不再产生沉淀,然后过滤。你认为她接下来还应进行的实验是___________________________;
在小红所做的实验中,若把BaCl2溶液换成Ba(OH)2溶液是否可行?请简述理由。___________________________________。17.某校化学兴趣小组的同学做制取难溶性的氢氧化铜Cu(OH)2
的实验。(1)在盛有黑色氧化铜粉末的试管中加入稀硫酸,其反应化学方程式是 。
(2)上述反应后,再向试管中加氢氧化钠溶液,制得氢氧化铜,其反应化学方程式是 。现在甲、乙两同学分别做该实验,实验结束,看到不同的现象。甲同学看到了蓝色絮状沉淀;而乙同学看到均是蓝色溶液。你认为实验成功的是 同学。试分析另一位同学所看到现象的原因是 .CuO +H2SO4==CuSO4 +H2O甲 乙同学实验一时加入的稀硫酸太多,使得实验二中的氢氧化钠溶液无法与CuSO4反应16.现有①氯化钠. ②氯化镁. ③氢氧化钠. ④氯化铁四种溶液,不另用任何试剂,仅用观察法和溶液之间的相互反应就可以将其区分出来,则鉴别出来的先后顺序是 .④ ③ ② ①H2SO4NaOHMgCl220.某溶液由NaOH.HCl.H2SO4和MgCl2中的一种或几种组成,向该溶液中滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2 溶
液体积的关系如右图所示,
请你从图中获得的信息来
分析,该溶液中不可能存
在的物质是 ;
肯定存在的物质是 .HCl18.请你根据碱的两种不同性质,设计实验来证明溶液呈碱性 , .19.欲制取少量NaOH,下列各组试剂可选用的一组是( ) A.NaCl.Cu(OH)2 B.NaNO3.Ba(OH)2 C.Na2CO3.Ca(OH)2 D.Na2SO4.Mg(OH)2石蕊(或酚酞)CuSO4(或FeCl3)C再见!
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
