中考专题复习:物质的鉴别[下学期]
图片预览






文档简介
课件14张PPT。物质的鉴别复习目标1、掌握物质的鉴别方法及能进一步进行物质鉴别;
2、掌握鉴别物质的步骤;
3、注意语言表达的规范性。[课前基础练习]
1、如何鉴定氯酸钾含有氯元素和氧元素?
2、如何证明某一溶液是盐酸溶液?
1)滴加 ,如果 ,则原溶液为酸或加入
产生 的为酸。
2)取样品滴加 产生 ,原溶液中有Cl-溶液为盐酸。
3、如何区别失去标鉴的盐酸溶液和硫酸溶液?
取样品滴加 ,产生 的原物质是H2SO4,则另一种为盐酸。(注:不能用AgNO3鉴别;因为Ag2SO4微溶)石蕊变红色可燃性气体Zn或Fe等金属AgNO3和HNO3白色沉淀BaCl2溶液不溶于稀硝酸的沉淀物质鉴别方法:
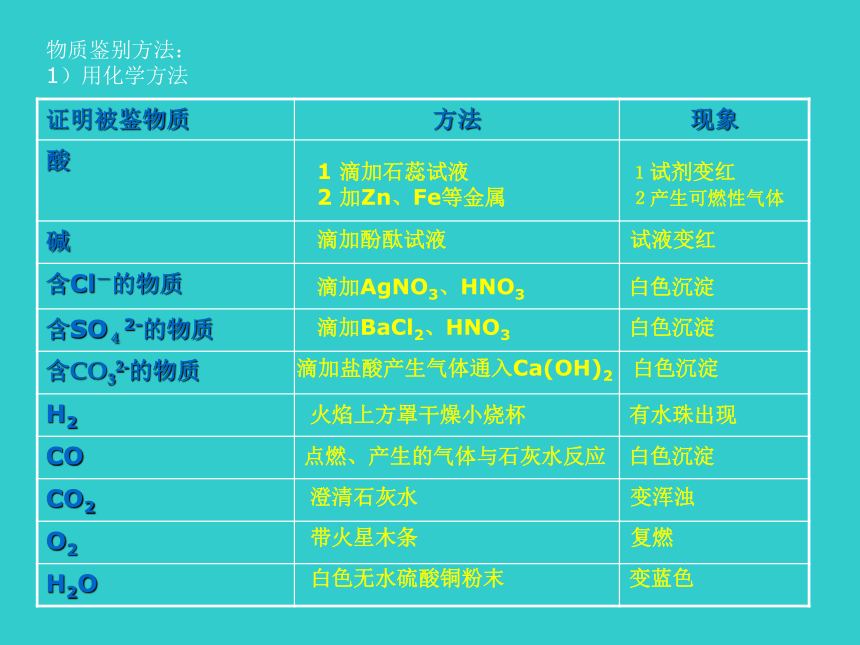
1)用化学方法1 滴加石蕊试液 1试剂变红
2 加Zn、Fe等金属 2产生可燃性气体滴加酚酞试液 试液变红滴加AgNO3、HNO3 白色沉淀滴加BaCl2、HNO3 白色沉淀滴加盐酸产生气体通入Ca(OH)2 白色沉淀火焰上方罩干燥小烧杯 有水珠出现点燃、产生的气体与石灰水反应 白色沉淀澄清石灰水 变浑浊带火星木条 复燃 白色无水硫酸铜粉末 变蓝色(2)用物理方法:
⑴蓝 色 溶 液——
⑵黄 色 溶 液——
⑶蓝色不溶物——
⑷红褐色不溶物——
⑸白色不溶物——
⑹打开盛液体的瓶盖出现白雾的是——
⑺片状白色固体露置在空气中潮解的是——
⑻黑色粉末——
⑼红色粉末——
⑽红色光亮的金属——
⑾溶于水产生大量热——BaSO4、AgCl、BaCO3、CaCO3、Mg(OH)2NaOH浓H2SO4、CaO等CuSO4FeCl3Cu(OH)2Fe(OH)3浓盐酸CuO、MnO2、CFe2O3Cu例1 现有四瓶无标签溶液,已知分别是NaCl、Na2CO3、NaNO3、Na2SO4,如何鉴别它们?法一:1)取四种溶液少量于试管中,分别滴加BaCl2溶液,
若产生白色沉淀的原物质是Na2CO3、 Na2SO4。无
现象的原物质是NaCl、NaNO3
2)在沉淀中加稀HNO3,沉淀溶解并产生气体的原物
质是Na2CO3,无现象的原物质是Na2SO4
3)在第一实验中无现象的两溶液重新取样品加入
AgNO3、HNO3,产生白色沉淀,则原物质是NaCl、
NaNO3
法二:1)取样品加入硝酸,有气体产生的是Na2 CO3、对另
三支没有明显现象的试管中滴加BaCl2,产生白色沉淀
的原物质是Na2SO4
2)另二种未知溶液重新取样品滴加AgNO3、HNO3,
产生白色沉淀的原物质是NaCl,无现象的原物质是硝
酸钠
注意:
(1)叙述的方法,通过现象,判断得出物质,而不是某某物质反应,产生现象;
(2)如果一开始加入AgNO3溶液,应注意Ag2SO4是微溶物质,可能引起溶液的浑浊,而不能将Na2SO4与Na2CO3、NaCl区别出来;
(3)表达要用“看到××的现象,说明原物质是××。”
例2 如何鉴别失去标鉴的H2SO4、HCl、
Na2SO4、NaCl溶液?法一:1)取样品,滴加紫色石蕊试液,使溶液变红
色的原物质是酸,另两种无现象的原物质为盐.
2)重新取样品,滴加BaCl2溶液,酸中产生
白色沉淀的是H2SO4 ,无现象的原物质是盐
酸,盐中出现白色沉淀的是Na2SO4,无现象
的是NaCl.
法二:上述滴加试剂的顺序调换.例3 用一种试剂,如何区别?
①稀盐酸、NaOH、NaCl溶液
②AgNO3、Na2CO3、Na2SO4溶液
③NaOH、Ba(OH)2、H2SO4溶液
④Na2CO3、CaO、CaCO3固体粉末。(4)用水。能溶解的是Na2CO3;与水反应并放热的是CaO;不能溶解的是CaCO3。(1)用紫色石蕊试液。显红色的是稀盐酸;显蓝色的是NaOH;
不变色(紫色)的是NaCl。(2)用盐酸。有白色沉淀产生的是AgNO3;有无色气体产生的
是Na2CO3;无明显变化的是Na2SO4。(3)用Na2CO3溶液。无明显变化的是 NaOH;有白色沉淀产生的是Ba(OH)2;有气体产生的是H2SO4。例4 ①K2CO3、BaCl2、NaCl、浓盐酸
②CuSO4、NaOH、MgCl2、NaCl
上述二组失去标鉴的无色溶液,不用任何试剂如何鉴别?(1)打开瓶盖,看到有白雾的是浓盐酸,另三种各取少量,分别滴加浓盐酸,产生气体的是K2CO3,另二种取少量滴加K2CO3 ,有沉淀产生的是BaCl2,剩下的是NaCl。(2)蓝色溶液是CuSO4,另三种各取少量滴加CuSO4 溶液,有蓝色沉淀的是NaOH,另二种加NaOH,有白色沉淀的是MgCl2,无明显反应的是NaCl。例5 Na2CO3、BaCl2、HCl、NaCl四种溶液,不用任何试剂,能否鉴别出来?分析:无色白白无色例6 有一包粉末,由BaCl2、Na2CO3、Na2SO4、 CaCO3、CuSO4中的一种或几种组成,为鉴定其成份,做如下实验:
1)将该粉末溶于足量的水中,发现下层有白色不溶物,上层溶液无色澄清;
2)过滤后滴加足量的稀HNO3,发现白色不溶物部分溶解。
则该混合物的组成可能为 。答案:
(1) BaCl2、Na2SO4、 CaCO3;
(2) BaCl2、Na2CO3、Na2SO4;
(3) BaCl2、Na2CO3、Na2SO4、 CaCO3。小结:
1、掌握基本现象是寻找解题突破口的关键;
2、当用一种试剂鉴别几种物质时,一般用到紫色石蕊,Na2CO3、稀HCl、稀H2SO4、Ba(OH)2、水等;
3、当不用任何试剂时,先尝试用物理方法看颜色、闻气味),再用两两混合的方法。思考题: A、B、C是初中常见的三种化合物,它们各由两种元素组成,甲、乙、丙是三种常见的单质。这些化合物和单质之间存在如下变化的关系:
单质乙
1)若单质甲为黑色固体,单质丙为红色金属。则:单质甲为
;写出化合物B和化合物C反应的化学方程
式 。
2)若关系图中:“化合物A→化合物B”上的单质甲改为单质乙,“化合物A+单质丙”里的单质丙改为一种其它化合物X,其余不变。则化合物X为 。碳H2O
2、掌握鉴别物质的步骤;
3、注意语言表达的规范性。[课前基础练习]
1、如何鉴定氯酸钾含有氯元素和氧元素?
2、如何证明某一溶液是盐酸溶液?
1)滴加 ,如果 ,则原溶液为酸或加入
产生 的为酸。
2)取样品滴加 产生 ,原溶液中有Cl-溶液为盐酸。
3、如何区别失去标鉴的盐酸溶液和硫酸溶液?
取样品滴加 ,产生 的原物质是H2SO4,则另一种为盐酸。(注:不能用AgNO3鉴别;因为Ag2SO4微溶)石蕊变红色可燃性气体Zn或Fe等金属AgNO3和HNO3白色沉淀BaCl2溶液不溶于稀硝酸的沉淀物质鉴别方法:
1)用化学方法1 滴加石蕊试液 1试剂变红
2 加Zn、Fe等金属 2产生可燃性气体滴加酚酞试液 试液变红滴加AgNO3、HNO3 白色沉淀滴加BaCl2、HNO3 白色沉淀滴加盐酸产生气体通入Ca(OH)2 白色沉淀火焰上方罩干燥小烧杯 有水珠出现点燃、产生的气体与石灰水反应 白色沉淀澄清石灰水 变浑浊带火星木条 复燃 白色无水硫酸铜粉末 变蓝色(2)用物理方法:
⑴蓝 色 溶 液——
⑵黄 色 溶 液——
⑶蓝色不溶物——
⑷红褐色不溶物——
⑸白色不溶物——
⑹打开盛液体的瓶盖出现白雾的是——
⑺片状白色固体露置在空气中潮解的是——
⑻黑色粉末——
⑼红色粉末——
⑽红色光亮的金属——
⑾溶于水产生大量热——BaSO4、AgCl、BaCO3、CaCO3、Mg(OH)2NaOH浓H2SO4、CaO等CuSO4FeCl3Cu(OH)2Fe(OH)3浓盐酸CuO、MnO2、CFe2O3Cu例1 现有四瓶无标签溶液,已知分别是NaCl、Na2CO3、NaNO3、Na2SO4,如何鉴别它们?法一:1)取四种溶液少量于试管中,分别滴加BaCl2溶液,
若产生白色沉淀的原物质是Na2CO3、 Na2SO4。无
现象的原物质是NaCl、NaNO3
2)在沉淀中加稀HNO3,沉淀溶解并产生气体的原物
质是Na2CO3,无现象的原物质是Na2SO4
3)在第一实验中无现象的两溶液重新取样品加入
AgNO3、HNO3,产生白色沉淀,则原物质是NaCl、
NaNO3
法二:1)取样品加入硝酸,有气体产生的是Na2 CO3、对另
三支没有明显现象的试管中滴加BaCl2,产生白色沉淀
的原物质是Na2SO4
2)另二种未知溶液重新取样品滴加AgNO3、HNO3,
产生白色沉淀的原物质是NaCl,无现象的原物质是硝
酸钠
注意:
(1)叙述的方法,通过现象,判断得出物质,而不是某某物质反应,产生现象;
(2)如果一开始加入AgNO3溶液,应注意Ag2SO4是微溶物质,可能引起溶液的浑浊,而不能将Na2SO4与Na2CO3、NaCl区别出来;
(3)表达要用“看到××的现象,说明原物质是××。”
例2 如何鉴别失去标鉴的H2SO4、HCl、
Na2SO4、NaCl溶液?法一:1)取样品,滴加紫色石蕊试液,使溶液变红
色的原物质是酸,另两种无现象的原物质为盐.
2)重新取样品,滴加BaCl2溶液,酸中产生
白色沉淀的是H2SO4 ,无现象的原物质是盐
酸,盐中出现白色沉淀的是Na2SO4,无现象
的是NaCl.
法二:上述滴加试剂的顺序调换.例3 用一种试剂,如何区别?
①稀盐酸、NaOH、NaCl溶液
②AgNO3、Na2CO3、Na2SO4溶液
③NaOH、Ba(OH)2、H2SO4溶液
④Na2CO3、CaO、CaCO3固体粉末。(4)用水。能溶解的是Na2CO3;与水反应并放热的是CaO;不能溶解的是CaCO3。(1)用紫色石蕊试液。显红色的是稀盐酸;显蓝色的是NaOH;
不变色(紫色)的是NaCl。(2)用盐酸。有白色沉淀产生的是AgNO3;有无色气体产生的
是Na2CO3;无明显变化的是Na2SO4。(3)用Na2CO3溶液。无明显变化的是 NaOH;有白色沉淀产生的是Ba(OH)2;有气体产生的是H2SO4。例4 ①K2CO3、BaCl2、NaCl、浓盐酸
②CuSO4、NaOH、MgCl2、NaCl
上述二组失去标鉴的无色溶液,不用任何试剂如何鉴别?(1)打开瓶盖,看到有白雾的是浓盐酸,另三种各取少量,分别滴加浓盐酸,产生气体的是K2CO3,另二种取少量滴加K2CO3 ,有沉淀产生的是BaCl2,剩下的是NaCl。(2)蓝色溶液是CuSO4,另三种各取少量滴加CuSO4 溶液,有蓝色沉淀的是NaOH,另二种加NaOH,有白色沉淀的是MgCl2,无明显反应的是NaCl。例5 Na2CO3、BaCl2、HCl、NaCl四种溶液,不用任何试剂,能否鉴别出来?分析:无色白白无色例6 有一包粉末,由BaCl2、Na2CO3、Na2SO4、 CaCO3、CuSO4中的一种或几种组成,为鉴定其成份,做如下实验:
1)将该粉末溶于足量的水中,发现下层有白色不溶物,上层溶液无色澄清;
2)过滤后滴加足量的稀HNO3,发现白色不溶物部分溶解。
则该混合物的组成可能为 。答案:
(1) BaCl2、Na2SO4、 CaCO3;
(2) BaCl2、Na2CO3、Na2SO4;
(3) BaCl2、Na2CO3、Na2SO4、 CaCO3。小结:
1、掌握基本现象是寻找解题突破口的关键;
2、当用一种试剂鉴别几种物质时,一般用到紫色石蕊,Na2CO3、稀HCl、稀H2SO4、Ba(OH)2、水等;
3、当不用任何试剂时,先尝试用物理方法看颜色、闻气味),再用两两混合的方法。思考题: A、B、C是初中常见的三种化合物,它们各由两种元素组成,甲、乙、丙是三种常见的单质。这些化合物和单质之间存在如下变化的关系:
单质乙
1)若单质甲为黑色固体,单质丙为红色金属。则:单质甲为
;写出化合物B和化合物C反应的化学方程
式 。
2)若关系图中:“化合物A→化合物B”上的单质甲改为单质乙,“化合物A+单质丙”里的单质丙改为一种其它化合物X,其余不变。则化合物X为 。碳H2O
