溶液概念复习[下学期]
图片预览





文档简介
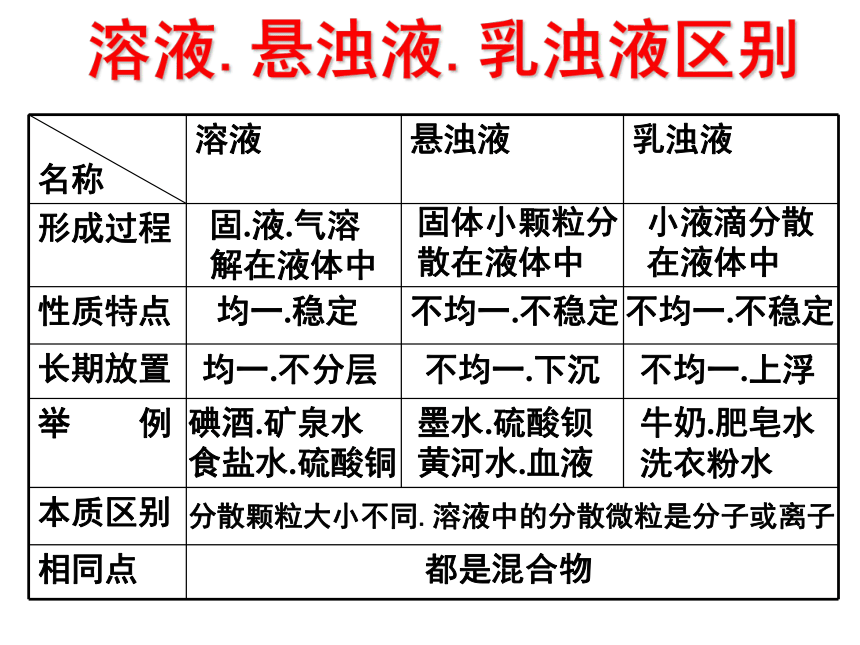
课件22张PPT。溶液复习课之一溶液和饱和溶液固.液.气溶解在液体中固体小颗粒分散在液体中小液滴分散在液体中均一.稳定不均一.不稳定不均一.不稳定均一.不分层不均一.下沉不均一.上浮溶液.悬浊液.乳浊液区别碘酒.矿泉水
食盐水.硫酸铜墨水.硫酸钡
黄河水.血液牛奶.肥皂水
洗衣粉水分散颗粒大小不同.溶液中的分散微粒是分子或离子都是混合物 一种或几种物质分散到另一种物质
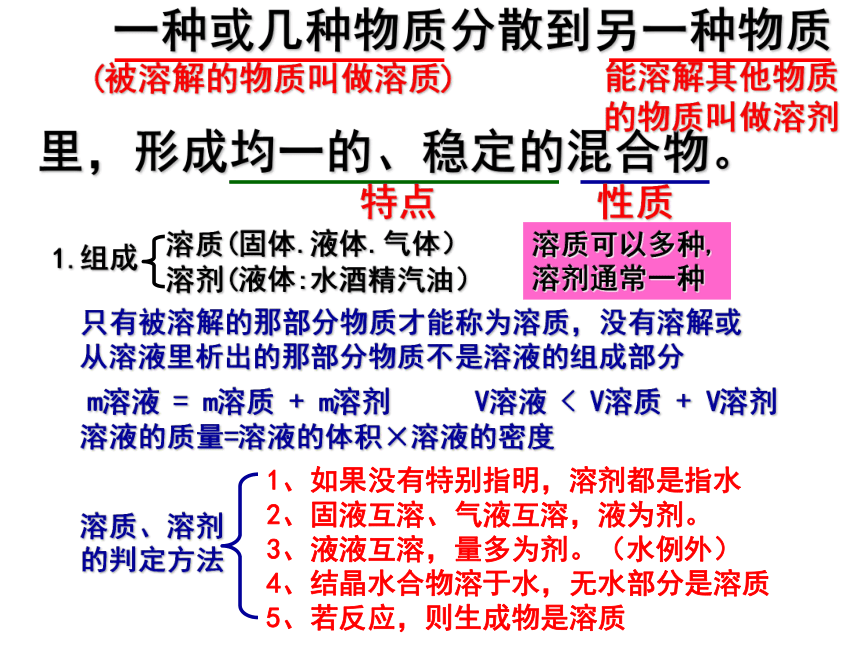
里,形成均一的、稳定的混合物。(被溶解的物质叫做溶质)能溶解其他物质的物质叫做溶剂特点性质1.组成溶质(固体.液体.气体)溶剂(液体:水酒精汽油)溶质可以多种,溶剂通常一种m溶液 = m溶质 + m溶剂V溶液 < V溶质 + V溶剂只有被溶解的那部分物质才能称为溶质,没有溶解或从溶液里析出的那部分物质不是溶液的组成部分溶液的质量=溶液的体积×溶液的密度溶质、溶剂的判定方法1、如果没有特别指明,溶剂都是指水
2、固液互溶、气液互溶,液为剂。
3、液液互溶,量多为剂。(水例外)
4、结晶水合物溶于水,无水部分是溶质
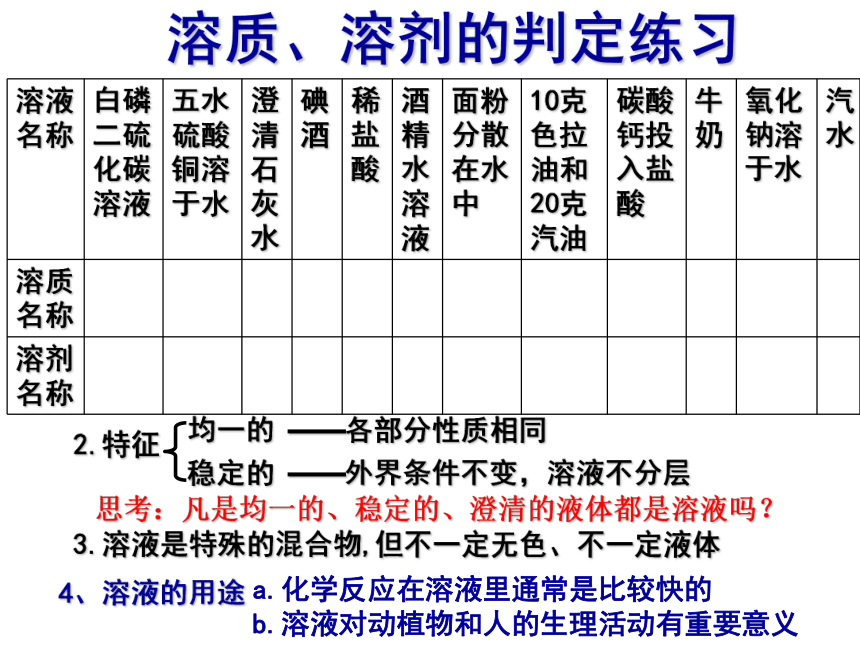
5、若反应,则生成物是溶质溶质、溶剂的判定练习 2.特征均一的思考:凡是均一的、稳定的、澄清的液体都是溶液吗?稳定的——各部分性质相同——外界条件不变,溶液不分层3.溶液是特殊的混合物,但不一定无色、不一定液体a.化学反应在溶液里通常是比较快的
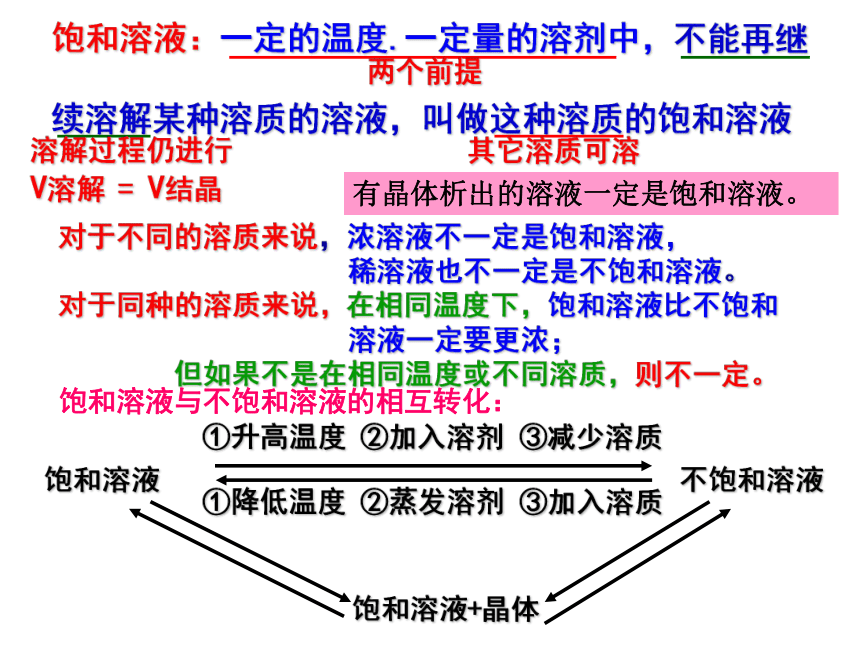
b.溶液对动植物和人的生理活动有重要意义4、溶液的用途升高不变降低5、溶解过程常伴随温度变化洗涤餐具的方法:只用冷水,只用热水,在冷水中加几滴洗涤剂,在热水中加几滴洗涤剂,上述那种方法洗涤最干净? 饱和溶液:一定的温度.一定量的溶剂中,不能再继
续溶解某种溶质的溶液,叫做这种溶质的饱和溶液两个前提其它溶质可溶溶解过程仍进行V溶解 = V结晶对于不同的溶质来说,浓溶液不一定是饱和溶液,
稀溶液也不一定是不饱和溶液。 对于同种的溶质来说,在相同温度下,饱和溶液比不饱和
溶液一定要更浓;
但如果不是在相同温度或不同溶质,则不一定。饱和溶液与不饱和溶液的相互转化:①降低温度 ②蒸发溶剂 ③加入溶质饱和溶液 不饱和溶液①升高温度 ②加入溶剂 ③减少溶质有晶体析出的溶液一定是饱和溶液。饱和溶液+晶体1、溶解性:(定性)
一种物质在另一种物质里的溶解能力的大小2、溶解度:(定量)
在一定温度下,某固态物质在100克溶剂里达到饱和状态时所溶解的克数,叫做这种溶质在这种溶剂里的溶解度思考:30℃时,硝酸钾的溶解度是45.8g,它表示什么意义?①在30℃时, 45.8g硝酸钾溶解到100克的水中,恰好达到饱和状态 ②在30℃时,100克的水中最多能溶解45.8g硝酸钾溶质.溶剂的性质(内因—决定因素)4、溶解性影响因素:温度(外因——影响因素)3、溶解度与溶解性的对应关系(室温20OC)溶解性的分类:易溶、 可溶、 微溶、 难溶>10g1g~10g0.01g~1g<0.01g溶解度:大多数固体物质的溶解度(如KNO3、NH4O3、NaNO3等)随温度的升高而增大。
少数固体物质的溶解度(如NaCl、KCl、NH4Cl等)随温度的升高变化不大。
极少数固体物质的溶解度(如Ca(OH)2等)随温度的升高反而减小。气体物质溶解度随温度升高而减少,随压强增大而增大。(1)图象上的点的含义:曲线上的点(恰好饱和).曲线下方的点(不饱和).曲线上方的点(饱和+晶体)
(2)曲线的坡度的含义:(1)曲线越徒峭,溶解度受温度影响越大,饱和溶液降温析出的晶体就越多。
(2)曲线越平缓,溶解度受温度影响越小,饱和溶液降温析出的晶体就越少。6.溶解度曲线:5.气体溶解度:标准大气压下,一定温度时,某气体在 1体积水中达到饱和状态时所溶解的体积数(无单位)混合物的分离:过滤和结晶一、过滤:(1)适用范围:难溶性固体与液体之间的分离。
(2)操作的注意事项:“三靠两低,一贴紧”二、结晶:(1)适用范围:可溶物与液体之间的分离。 降温结晶:冷却热饱和溶液;适用于溶解度受温度影响大的可溶物(如:KNO3)与液体之间的分离。蒸发结晶:蒸发溶剂;适用于溶解度温度影响小的可溶物(如:NaCl)与液体之间的分离(3)蒸发操作中的注意事项:当蒸发皿中出现较多量固体时就停止加热。思考:粗盐提纯实验中,主要步骤有哪些?每一步中玻璃棒的作用分别是什么?(2)分类溶解 过滤 蒸发结晶 洗涤烘干搅拌.加速溶解引流搅拌.使受热均匀转移结晶物溶液配制(一)固体溶质与水步骤:1、计算;2、称量与量取; 3、溶解。(二)浓溶液加水稀释步骤:1、计算; 2、量取;3、稀释。 一、判断题:
1、物质溶于水时,常使溶液的温度发生改变
2、升高温度可以使接近饱和的石灰水变成饱和溶液3、凡是均一稳定的液体就是溶液 4、溶液一定是无色透明的混合物 5、食盐水和汽水混合得到的还是溶液 6、果汁能溶于水,果汁是溶质7、m克氯化钠和n克水混全振荡形成的溶液质量等于或 少于(m+n)克。8、溶液是一种固体溶解在水中形成的;9、有固体溶质与溶液共存时的溶液一定是该温度下该固体溶液的饱和溶液
10、在饱和溶液中再加入任何物质都不可能溶解。11、75%的医用酒精消毒液,溶剂是酒精1、实验室现有相同体积且无污染的饱和食盐水和蒸馏水各一瓶,如何将它们区别出来?(1)尝味道(2)测密度(3)加少量食盐(4)测液体的沸点(盐水的沸点比水高)(5)加热蒸发,有固体析出的是食盐2、含有蔗糖晶体的溶液A,从冰霜里取出放置一段时间后,晶体慢慢消失,形成溶液B。对于溶液A和B,一定处于饱和状态的是 ,其中溶液溶质质量分数较大的是 。4、在配制一定质量的食盐溶液是要使食盐尽快溶解可以采用哪些方法?原理是什么?3、在一定温度下,向某溶液中加入少量该物质,振荡后加入的物质质量并不见少,则原溶液是 溶液,再将该混合加热,未溶解的物质全溶解,这说明 。 氯化钠注射液
【规格】100ml 0.9g
【注意】使用前发现溶液中有絮状物、瓶身细微破裂等均不可使用.
【贮藏】密封保存5、病人在医院接受静脉注射或滴注时,常用到生理盐水即氯化钠注射液。右图是某药业公司生产的氯化钠注射液包装标签上的部分文字,请回答:(1)该注射液里的溶质_____;(2)常温下,一瓶合格的氯化钠注射液密封放置一段时间后,是6、饱和溶液降温时 析出晶体,析出晶体后的溶液 是该温度下该溶质的饱和溶液(填“一定”或“不一定”)7、吃火锅时,我们虽然没往锅内继续放盐,但汤越吃越咸,这是因为( )
A.汤的上部淡下部咸 B. 汤内盐的质量分数随着水份的蒸发而增大 C. 汤内锅底的盐没溶解 D. 其它原因否会出现浑浊现象.为什么? 8、下列有关溶液的说法中,正确的是( ) A、不饱和溶液转化为饱和溶液,其溶质的质量分数一定增大 B、饱和溶液中析出晶体后,溶质质量分数一定减小 C、温度不变,某饱和溶液中溶质质量分数一定不变 D、降温时,饱和溶液可能不析出晶体 9、粗盐的杂质主要是氯化镁(能溶于水)。工业上常把粗盐粉碎后用饱和食盐水浸洗,再过滤出食盐。对这一过程认识正确的是( )
A浸洗前后,被浸洗的粗盐中的氯化镁的含量基本不变
B浸洗前后,食盐水中氯化钠的质量基本不变
C浸洗后,食盐水中氯化钠的质量分数增大
D浸洗用的饱和食盐水可以无数次地使用下去10.在一定温度下,将一瓶接近饱和的硝酸钾溶液转变为饱和溶液,可采取的方法是:1升高温度 2降低温度
3温度不变条件下加入适量的硝酸钾晶体
4温度不变的情况下加入适量的水
5恒温蒸发一部分水
6倒出一些硝酸钾溶液。正确的是( )
A 1,3,5 B 2,3,5,C 2,3,6 D 1,3,411.物质的溶解度与下列因素无关的是( )1溶剂性质 2温度高低 3溶质性质 4溶质和溶剂的质量 5溶液的总质量 6气体的压强的大小
A 1,2,4,5 B 2,3,5,6 C 只有4,5 D 2,3,4,513.将20℃时的氯化铵饱和溶液升温至50℃(不考虑水分的蒸发),一定发生改变的是 ( )
A.氯化铵的溶解度 B.溶液的质量
C.溶质的质量分数 D.溶质的质量12、有两瓶硝酸钾溶液,一瓶为饱和溶液(溶质的质量分数为40%),另一瓶为10%的溶液,下列实验操作中,无法区分这两种溶液的是 ( )
A.加一定量的水 B.加入少量硝酸钾晶体
C.略降低温度 D.t℃时,蒸发少量水 14.室温下,向一定质量的NaCl溶液中加入10 g NaCl固体,充分搅拌后,尚有部分固体未溶解,再加入10g水后,剩余固体全部溶解。下列判断正确的是
A.加水前一定是饱和溶液? B.加水前可能是饱和溶液?
C.加水后一定是饱和溶液? D.加水后可能是饱和溶液 15.某温度下,溶质质量分数为26%、密度为ρ的食盐水一杯,倒出半杯后,剩下食盐水的质量分数和密度分别为( )
A. 26% , 1/2ρ B. 13% ,ρ
C. 26% , ρ D. 13% , 1/2ρ16.将不饱和溶液变为饱和溶液,最可靠的方法是( )
A升高温度 B降低温度 C加入溶质 D倒出溶剂A.③④①②⑤ B.①②③④⑤ C.④⑤①②③ D.②①④③⑤17.配制一定溶质质量分数的氯化钠溶液的一些操作步骤见下图。正确的操作顺序是( )18.指出下列各句的含义及判断是非:
1、20℃时,10克食盐溶解在100克水中,所以20℃时食盐的溶解度是10克
2、20℃时,100克饱和食盐溶液里含有10克食盐,所以20℃时食盐的溶解度是10克。
3、在20℃时,100克水里最多溶解33.3克氯化铵,则氯化铵的溶解度是33.3克
4、100克硝酸钾饱和溶液里含硝酸钾24克,则硝酸钾的溶解度是2419.烧开水时,加热不久在锅底会出现大量的气泡,这说明气体的溶解度随温度的升高而_______,打开汽水瓶盖时,有大量的气泡从瓶口逸出,这是因为 .20.某温度下,将120克的硝酸钾饱和溶液蒸干,得到20克硝酸钾,则该温度下硝酸钾的溶解度为( ) A. 20 B. 16.7克 C. 16.7 D. 20克 21.A图表示硝酸钾和氢氧化钙的溶解度随温度变化的情况。B图中甲、乙试管分别盛有硝酸钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体。向烧杯中加入一种物质后,甲试管中固体减少,乙试管中的固体增加,则加入的物质不可能是
A.浓硫酸 B.氢氧化钠 C.氧化钙 D.氯化钠22.下列混合物分离,可用冷却热饱和溶液法分离的是( )
A.混有泥沙的粗盐 B.混有少量食盐的硝酸钾
C.混有少量水的酒精 D.悬浮在池塘水中的小颗粒23.从海水中提取食盐通常采用 方法。而冬天北方的盐湖中有纯碱晶体析出,这是因为 。abcC1C224根据右图回答下列问题:
(1)a.b两点的意义分别是什么?
(2)C.C1.C2三点表示溶液的状态及意义是什么?
(3)采用降温结晶.蒸发结晶.升温结晶的物质分别是什么?
(4)当温度 时,SB>SA>SC;当温度 时,C饱和溶液的质量分数大于A饱和溶液的质量分数.
(5)t40C时,相同质量的A.B.C饱和溶液降温至t10C,析出晶体的质量大小顺序为 .(6)若A中含B,B中含A,C中含A,分别如何提纯?
(7)若将t30C的A饱和溶液升温至t40C或降温至t20C,则A点如何移动?质量分数如何变化?
(8)ABC中属于易溶的是什么?再见滤纸紧贴漏斗滤纸边缘比
漏斗口稍低滤液液面低于
滤纸的边缘烧杯嘴靠玻璃棒玻璃棒靠
三层滤纸漏斗末端靠
烧杯内壁
食盐水.硫酸铜墨水.硫酸钡
黄河水.血液牛奶.肥皂水
洗衣粉水分散颗粒大小不同.溶液中的分散微粒是分子或离子都是混合物 一种或几种物质分散到另一种物质
里,形成均一的、稳定的混合物。(被溶解的物质叫做溶质)能溶解其他物质的物质叫做溶剂特点性质1.组成溶质(固体.液体.气体)溶剂(液体:水酒精汽油)溶质可以多种,溶剂通常一种m溶液 = m溶质 + m溶剂V溶液 < V溶质 + V溶剂只有被溶解的那部分物质才能称为溶质,没有溶解或从溶液里析出的那部分物质不是溶液的组成部分溶液的质量=溶液的体积×溶液的密度溶质、溶剂的判定方法1、如果没有特别指明,溶剂都是指水
2、固液互溶、气液互溶,液为剂。
3、液液互溶,量多为剂。(水例外)
4、结晶水合物溶于水,无水部分是溶质
5、若反应,则生成物是溶质溶质、溶剂的判定练习 2.特征均一的思考:凡是均一的、稳定的、澄清的液体都是溶液吗?稳定的——各部分性质相同——外界条件不变,溶液不分层3.溶液是特殊的混合物,但不一定无色、不一定液体a.化学反应在溶液里通常是比较快的
b.溶液对动植物和人的生理活动有重要意义4、溶液的用途升高不变降低5、溶解过程常伴随温度变化洗涤餐具的方法:只用冷水,只用热水,在冷水中加几滴洗涤剂,在热水中加几滴洗涤剂,上述那种方法洗涤最干净? 饱和溶液:一定的温度.一定量的溶剂中,不能再继
续溶解某种溶质的溶液,叫做这种溶质的饱和溶液两个前提其它溶质可溶溶解过程仍进行V溶解 = V结晶对于不同的溶质来说,浓溶液不一定是饱和溶液,
稀溶液也不一定是不饱和溶液。 对于同种的溶质来说,在相同温度下,饱和溶液比不饱和
溶液一定要更浓;
但如果不是在相同温度或不同溶质,则不一定。饱和溶液与不饱和溶液的相互转化:①降低温度 ②蒸发溶剂 ③加入溶质饱和溶液 不饱和溶液①升高温度 ②加入溶剂 ③减少溶质有晶体析出的溶液一定是饱和溶液。饱和溶液+晶体1、溶解性:(定性)
一种物质在另一种物质里的溶解能力的大小2、溶解度:(定量)
在一定温度下,某固态物质在100克溶剂里达到饱和状态时所溶解的克数,叫做这种溶质在这种溶剂里的溶解度思考:30℃时,硝酸钾的溶解度是45.8g,它表示什么意义?①在30℃时, 45.8g硝酸钾溶解到100克的水中,恰好达到饱和状态 ②在30℃时,100克的水中最多能溶解45.8g硝酸钾溶质.溶剂的性质(内因—决定因素)4、溶解性影响因素:温度(外因——影响因素)3、溶解度与溶解性的对应关系(室温20OC)溶解性的分类:易溶、 可溶、 微溶、 难溶>10g1g~10g0.01g~1g<0.01g溶解度:大多数固体物质的溶解度(如KNO3、NH4O3、NaNO3等)随温度的升高而增大。
少数固体物质的溶解度(如NaCl、KCl、NH4Cl等)随温度的升高变化不大。
极少数固体物质的溶解度(如Ca(OH)2等)随温度的升高反而减小。气体物质溶解度随温度升高而减少,随压强增大而增大。(1)图象上的点的含义:曲线上的点(恰好饱和).曲线下方的点(不饱和).曲线上方的点(饱和+晶体)
(2)曲线的坡度的含义:(1)曲线越徒峭,溶解度受温度影响越大,饱和溶液降温析出的晶体就越多。
(2)曲线越平缓,溶解度受温度影响越小,饱和溶液降温析出的晶体就越少。6.溶解度曲线:5.气体溶解度:标准大气压下,一定温度时,某气体在 1体积水中达到饱和状态时所溶解的体积数(无单位)混合物的分离:过滤和结晶一、过滤:(1)适用范围:难溶性固体与液体之间的分离。
(2)操作的注意事项:“三靠两低,一贴紧”二、结晶:(1)适用范围:可溶物与液体之间的分离。 降温结晶:冷却热饱和溶液;适用于溶解度受温度影响大的可溶物(如:KNO3)与液体之间的分离。蒸发结晶:蒸发溶剂;适用于溶解度温度影响小的可溶物(如:NaCl)与液体之间的分离(3)蒸发操作中的注意事项:当蒸发皿中出现较多量固体时就停止加热。思考:粗盐提纯实验中,主要步骤有哪些?每一步中玻璃棒的作用分别是什么?(2)分类溶解 过滤 蒸发结晶 洗涤烘干搅拌.加速溶解引流搅拌.使受热均匀转移结晶物溶液配制(一)固体溶质与水步骤:1、计算;2、称量与量取; 3、溶解。(二)浓溶液加水稀释步骤:1、计算; 2、量取;3、稀释。 一、判断题:
1、物质溶于水时,常使溶液的温度发生改变
2、升高温度可以使接近饱和的石灰水变成饱和溶液3、凡是均一稳定的液体就是溶液 4、溶液一定是无色透明的混合物 5、食盐水和汽水混合得到的还是溶液 6、果汁能溶于水,果汁是溶质7、m克氯化钠和n克水混全振荡形成的溶液质量等于或 少于(m+n)克。8、溶液是一种固体溶解在水中形成的;9、有固体溶质与溶液共存时的溶液一定是该温度下该固体溶液的饱和溶液
10、在饱和溶液中再加入任何物质都不可能溶解。11、75%的医用酒精消毒液,溶剂是酒精1、实验室现有相同体积且无污染的饱和食盐水和蒸馏水各一瓶,如何将它们区别出来?(1)尝味道(2)测密度(3)加少量食盐(4)测液体的沸点(盐水的沸点比水高)(5)加热蒸发,有固体析出的是食盐2、含有蔗糖晶体的溶液A,从冰霜里取出放置一段时间后,晶体慢慢消失,形成溶液B。对于溶液A和B,一定处于饱和状态的是 ,其中溶液溶质质量分数较大的是 。4、在配制一定质量的食盐溶液是要使食盐尽快溶解可以采用哪些方法?原理是什么?3、在一定温度下,向某溶液中加入少量该物质,振荡后加入的物质质量并不见少,则原溶液是 溶液,再将该混合加热,未溶解的物质全溶解,这说明 。 氯化钠注射液
【规格】100ml 0.9g
【注意】使用前发现溶液中有絮状物、瓶身细微破裂等均不可使用.
【贮藏】密封保存5、病人在医院接受静脉注射或滴注时,常用到生理盐水即氯化钠注射液。右图是某药业公司生产的氯化钠注射液包装标签上的部分文字,请回答:(1)该注射液里的溶质_____;(2)常温下,一瓶合格的氯化钠注射液密封放置一段时间后,是6、饱和溶液降温时 析出晶体,析出晶体后的溶液 是该温度下该溶质的饱和溶液(填“一定”或“不一定”)7、吃火锅时,我们虽然没往锅内继续放盐,但汤越吃越咸,这是因为( )
A.汤的上部淡下部咸 B. 汤内盐的质量分数随着水份的蒸发而增大 C. 汤内锅底的盐没溶解 D. 其它原因否会出现浑浊现象.为什么? 8、下列有关溶液的说法中,正确的是( ) A、不饱和溶液转化为饱和溶液,其溶质的质量分数一定增大 B、饱和溶液中析出晶体后,溶质质量分数一定减小 C、温度不变,某饱和溶液中溶质质量分数一定不变 D、降温时,饱和溶液可能不析出晶体 9、粗盐的杂质主要是氯化镁(能溶于水)。工业上常把粗盐粉碎后用饱和食盐水浸洗,再过滤出食盐。对这一过程认识正确的是( )
A浸洗前后,被浸洗的粗盐中的氯化镁的含量基本不变
B浸洗前后,食盐水中氯化钠的质量基本不变
C浸洗后,食盐水中氯化钠的质量分数增大
D浸洗用的饱和食盐水可以无数次地使用下去10.在一定温度下,将一瓶接近饱和的硝酸钾溶液转变为饱和溶液,可采取的方法是:1升高温度 2降低温度
3温度不变条件下加入适量的硝酸钾晶体
4温度不变的情况下加入适量的水
5恒温蒸发一部分水
6倒出一些硝酸钾溶液。正确的是( )
A 1,3,5 B 2,3,5,C 2,3,6 D 1,3,411.物质的溶解度与下列因素无关的是( )1溶剂性质 2温度高低 3溶质性质 4溶质和溶剂的质量 5溶液的总质量 6气体的压强的大小
A 1,2,4,5 B 2,3,5,6 C 只有4,5 D 2,3,4,513.将20℃时的氯化铵饱和溶液升温至50℃(不考虑水分的蒸发),一定发生改变的是 ( )
A.氯化铵的溶解度 B.溶液的质量
C.溶质的质量分数 D.溶质的质量12、有两瓶硝酸钾溶液,一瓶为饱和溶液(溶质的质量分数为40%),另一瓶为10%的溶液,下列实验操作中,无法区分这两种溶液的是 ( )
A.加一定量的水 B.加入少量硝酸钾晶体
C.略降低温度 D.t℃时,蒸发少量水 14.室温下,向一定质量的NaCl溶液中加入10 g NaCl固体,充分搅拌后,尚有部分固体未溶解,再加入10g水后,剩余固体全部溶解。下列判断正确的是
A.加水前一定是饱和溶液? B.加水前可能是饱和溶液?
C.加水后一定是饱和溶液? D.加水后可能是饱和溶液 15.某温度下,溶质质量分数为26%、密度为ρ的食盐水一杯,倒出半杯后,剩下食盐水的质量分数和密度分别为( )
A. 26% , 1/2ρ B. 13% ,ρ
C. 26% , ρ D. 13% , 1/2ρ16.将不饱和溶液变为饱和溶液,最可靠的方法是( )
A升高温度 B降低温度 C加入溶质 D倒出溶剂A.③④①②⑤ B.①②③④⑤ C.④⑤①②③ D.②①④③⑤17.配制一定溶质质量分数的氯化钠溶液的一些操作步骤见下图。正确的操作顺序是( )18.指出下列各句的含义及判断是非:
1、20℃时,10克食盐溶解在100克水中,所以20℃时食盐的溶解度是10克
2、20℃时,100克饱和食盐溶液里含有10克食盐,所以20℃时食盐的溶解度是10克。
3、在20℃时,100克水里最多溶解33.3克氯化铵,则氯化铵的溶解度是33.3克
4、100克硝酸钾饱和溶液里含硝酸钾24克,则硝酸钾的溶解度是2419.烧开水时,加热不久在锅底会出现大量的气泡,这说明气体的溶解度随温度的升高而_______,打开汽水瓶盖时,有大量的气泡从瓶口逸出,这是因为 .20.某温度下,将120克的硝酸钾饱和溶液蒸干,得到20克硝酸钾,则该温度下硝酸钾的溶解度为( ) A. 20 B. 16.7克 C. 16.7 D. 20克 21.A图表示硝酸钾和氢氧化钙的溶解度随温度变化的情况。B图中甲、乙试管分别盛有硝酸钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体。向烧杯中加入一种物质后,甲试管中固体减少,乙试管中的固体增加,则加入的物质不可能是
A.浓硫酸 B.氢氧化钠 C.氧化钙 D.氯化钠22.下列混合物分离,可用冷却热饱和溶液法分离的是( )
A.混有泥沙的粗盐 B.混有少量食盐的硝酸钾
C.混有少量水的酒精 D.悬浮在池塘水中的小颗粒23.从海水中提取食盐通常采用 方法。而冬天北方的盐湖中有纯碱晶体析出,这是因为 。abcC1C224根据右图回答下列问题:
(1)a.b两点的意义分别是什么?
(2)C.C1.C2三点表示溶液的状态及意义是什么?
(3)采用降温结晶.蒸发结晶.升温结晶的物质分别是什么?
(4)当温度 时,SB>SA>SC;当温度 时,C饱和溶液的质量分数大于A饱和溶液的质量分数.
(5)t40C时,相同质量的A.B.C饱和溶液降温至t10C,析出晶体的质量大小顺序为 .(6)若A中含B,B中含A,C中含A,分别如何提纯?
(7)若将t30C的A饱和溶液升温至t40C或降温至t20C,则A点如何移动?质量分数如何变化?
(8)ABC中属于易溶的是什么?再见滤纸紧贴漏斗滤纸边缘比
漏斗口稍低滤液液面低于
滤纸的边缘烧杯嘴靠玻璃棒玻璃棒靠
三层滤纸漏斗末端靠
烧杯内壁
同课章节目录
- 第1章 水和水的溶液
- 第1节 地球上的水
- 第2节 水的组成
- 第3节 水的浮力
- 第4节 物质在水中的分散状况
- 第5节 物质的溶解
- 第6节 物质的分离
- 第7节 水资源的利用、开发和保护
- 第2章 天气与气候
- 第1节 大气层
- 第2节 气温
- 第3节 大气的压强
- 第4节 风和降水
- 第5节 天气预报
- 第6节 气候和影响气候的因素
- 第7节 我国的气候特征与主要气象灾害
- 第3章 生命活动的调节
- 第1节 植物生命活动的调节
- 第2节 人体的激素调节
- 第3节 神经调节
- 第4节 动物的行为
- 第5节 体温的控制
- 第4章 电路探秘
- 第1节 电荷与电流
- 第2节 电流的测量
- 第3节 物质的导电性与电阻
- 第4节 变阻器
- 第5节 电压的测量
- 第6节 电流与电压、电阻的关系
- 第7节 电路分析与应用
- 研究性学习课题
- 一 测定本地区的“酸雨”情况及分析原因
- 二 太阳黑子活动与本地区降水的关系
- 三 训练小动物建立某种条件反射
- 四 调查在自然界或生命活动中的电现象
