第一章溶液复习,练习课[上学期]
图片预览








文档简介
课件20张PPT。1.下列说法中正确的是( )
A. 100g水中最多能溶解某物质40g,则该物质的溶解度为40g
B. 4℃时,溶质N的饱和溶液120g中含N 20g,所以4℃时,溶质N的溶解度为20g
C. 一定温度下,物质M的饱和溶液100g中含M物质30g,则物质M在该温度时的溶解度为30g
D. 20℃时,50g水中溶有溶质P 20g,则物质P在20℃时的溶解度为40gB2.下列关于饱和溶液的说法中,错误的是( )
A.在温度不变时,硝酸钾饱和溶液不能再溶解硝酸钾晶体
B.改变条件可以使不饱和溶液变成饱和溶液
C.室温下,与固体溶质共存的溶液一定是这种溶质的饱和溶液
D.在温度升高时,某物质的饱和溶液一定能继续溶解该物质D3.下列有关溶液的说法中,正确的是 ( )
A、不饱和溶液转化为饱和溶液,其溶质的质量分数一定增大
B、饱和溶液不蒸发溶剂而析出晶体后,溶液的溶质质量分数一定减小
C、只要温度不变,某饱和溶液中溶质的质量分数一定不变
D、降温时,饱和溶液肯定不析出晶体B4.在一个大萝卜上挖个坑,向其中注入饱和食盐水,一定时间后将食盐水倒出,在相同的温度下,发现倒出的溶液还能溶解少量的食盐,这说明倒出的溶液 ( )
A.是饱和溶液
B.是不饱和溶液
C.氯化钠溶解度升高
D.氯化钠溶解度降低 B5.将两杯20℃时的食盐饱和溶液,甲为500g,乙为1000g,在温度不变的情况下分别蒸发掉15g水,析出的食盐晶体的质量( )
甲=乙 B. 甲<乙
C. 甲>乙 D. 无法判断A6.20℃时,将某硝酸钾溶液,第一次蒸发掉10g水,冷却到原来的温度,析出晶体0g,第二次蒸发掉10g水,冷却到原温度,析出晶体3g,第三次蒸发掉10g水,冷却到原温度,析出晶体质量为( )
A. 等于3g B. 不等于3g
C. 大于或等于3g D. 小于或等于3gC7. 下列说法中正确的是( )
A. 溶液一定是无色、稳定的混合物
B. 100毫升酒精和100毫升水混合在一起,体积等于200毫升
C. 在同一温度下,氯化钠饱和溶液比不饱和溶液浓
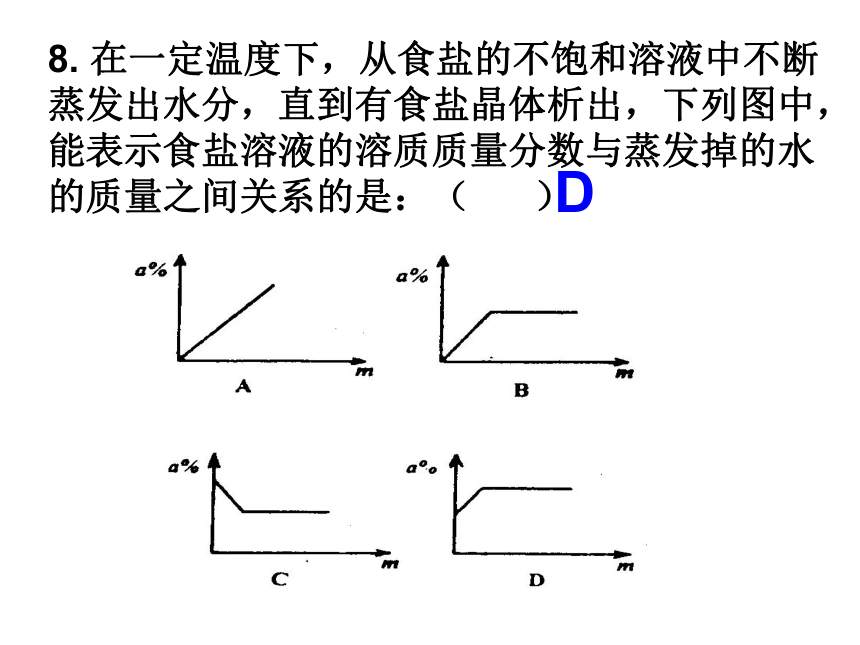
D. 任何物质的溶解度都随着温度的升高而增大C8. 在一定温度下,从食盐的不饱和溶液中不断蒸发出水分,直到有食盐晶体析出,下列图中,能表示食盐溶液的溶质质量分数与蒸发掉的水的质量之间关系的是:( )D9. 下列说法中,不正确的是( )
A. 从溶液中析出的晶体都含有结晶水
B. 浓溶液不一定是饱和溶液,稀溶液不一定是不饱和溶液
C. 同温时,同种物质的饱和溶液的溶质的质量分数一定大于不饱和溶液的溶质质量分数
D. 溶解度曲线上的任意一点都表示某温度时,某物质在100克溶剂中达到饱和时所溶解的质量A10. 下列关于溶解度的说法,不正确的是( )
A. 相同条件下,不同物质的溶解度一般是不同的
B. 相同条件下,物质的溶解度随溶剂的量的增减而变化
C. 同一物质的溶解度,随温度的变化而变化
D. 气体的溶解度随温度的升高而减小,多数固体物质的溶解度随温度的升高而增大B11.20℃时,把某物质的溶液分成质量相等的两份,其中一份蒸发掉25克水达到饱和,另一份加入15克溶质也达到饱和,则时,有关该物质的结论正确的是( )
A. 该物质是一种难溶物
B. 该物质溶液质量分数的最大值为37.5%
C. 20℃时,该物质的溶解度为60克
D. 将其饱和溶液中溶质的质量分数增大一倍,可采用蒸发溶剂的方法C12. 计算1.5升质量分数为98%的浓硫酸(密度为1.84 克/厘米3)所含溶质的质量时,下列算式中正确的是( )ABCDD13. 把在“粗盐提纯”实验中玻璃棒的作用或用法,按要求填在横线上:
(1)粗盐溶解时,玻璃棒的用法是________,作用是________;
(2)过滤食盐水时,玻璃棒的用法是________,作用是________;
(3)滤液蒸发时,玻璃棒的用法是________,作用是________。搅拌加速粗盐溶解搅拌使液体均匀受热
防止液体飞溅引流引流14. 已知医用碘酒中碘的质量分数为2% ,10克碘可配制这种碘酒________克,156.8克酒精可配制这种碘酒________克。15. 配制一定质量、一定溶质质量分数的食盐水的实验步骤为_______、_______、_______。
500160计算称量溶解16.在下列叙述中的横线上,填上适宜分离操作的编号:
A.蒸发结晶法 B.降温结晶法(冷却热饱和溶液) C.过滤法;D.蒸馏法
⑴食盐水中混有泥沙,欲从中分离出食盐,
应先 再 ;
⑵硝酸钾中混有少量氯化钠, 用 ;
⑶将酒精溶液中的酒精和水分离开,应用 ;
⑷欲从含有泥沙的水里得到较纯净的水,
应用 ;CABDC17.某固体物质的溶解度曲线如图所示,根据图回答如下问题:
⑴图中B点的意义:表示该物质在t3℃时,每100g溶剂和S1 g溶质形成不饱和溶液。A点的意义: 。
此溶液的溶质质量分数的表达式 。每100g溶剂和S2 g溶质形成饱和溶液。S2/(100+S2)⑵若A、B两点的溶液在保持温度不变的情况下各加20克水,A点的溶解度将 (填“增大”、“减小”、或“不变”);
A、B的溶质质量分数 (填“前者大”、“后者大”或“相等”)。
⑶当温度降低时,A点变动后溶液的质量分数与原来比较 ( )
(填“增大”、“减小”或“不变”)。
⑷若使M点的(100+S1)g溶液成为饱和溶液的方法:降温至 ℃;不变前者大减小t118.20℃时,食盐的溶解度为36克,在20℃时将100克食盐放入250克水中,充分搅拌,所得溶液的质量分数为多少?19.一定温度下质量分数为a%的硝酸钾溶液,将其分成两份,一份等温蒸发10g水,得0.5g晶体;另一份等温蒸发12.5g水得1.5g晶体,该温度下硝酸钾的溶解度为多少?20、将30℃时某物质的溶液100克,分成质量相等的两份,向其中的一份加入5克该溶质,溶液恰好达到饱和,将另一份冷却到20℃,溶液也恰好达到饱和,此饱和溶液的质量分数为20%,求该物质在30℃时的溶解度?
A. 100g水中最多能溶解某物质40g,则该物质的溶解度为40g
B. 4℃时,溶质N的饱和溶液120g中含N 20g,所以4℃时,溶质N的溶解度为20g
C. 一定温度下,物质M的饱和溶液100g中含M物质30g,则物质M在该温度时的溶解度为30g
D. 20℃时,50g水中溶有溶质P 20g,则物质P在20℃时的溶解度为40gB2.下列关于饱和溶液的说法中,错误的是( )
A.在温度不变时,硝酸钾饱和溶液不能再溶解硝酸钾晶体
B.改变条件可以使不饱和溶液变成饱和溶液
C.室温下,与固体溶质共存的溶液一定是这种溶质的饱和溶液
D.在温度升高时,某物质的饱和溶液一定能继续溶解该物质D3.下列有关溶液的说法中,正确的是 ( )
A、不饱和溶液转化为饱和溶液,其溶质的质量分数一定增大
B、饱和溶液不蒸发溶剂而析出晶体后,溶液的溶质质量分数一定减小
C、只要温度不变,某饱和溶液中溶质的质量分数一定不变
D、降温时,饱和溶液肯定不析出晶体B4.在一个大萝卜上挖个坑,向其中注入饱和食盐水,一定时间后将食盐水倒出,在相同的温度下,发现倒出的溶液还能溶解少量的食盐,这说明倒出的溶液 ( )
A.是饱和溶液
B.是不饱和溶液
C.氯化钠溶解度升高
D.氯化钠溶解度降低 B5.将两杯20℃时的食盐饱和溶液,甲为500g,乙为1000g,在温度不变的情况下分别蒸发掉15g水,析出的食盐晶体的质量( )
甲=乙 B. 甲<乙
C. 甲>乙 D. 无法判断A6.20℃时,将某硝酸钾溶液,第一次蒸发掉10g水,冷却到原来的温度,析出晶体0g,第二次蒸发掉10g水,冷却到原温度,析出晶体3g,第三次蒸发掉10g水,冷却到原温度,析出晶体质量为( )
A. 等于3g B. 不等于3g
C. 大于或等于3g D. 小于或等于3gC7. 下列说法中正确的是( )
A. 溶液一定是无色、稳定的混合物
B. 100毫升酒精和100毫升水混合在一起,体积等于200毫升
C. 在同一温度下,氯化钠饱和溶液比不饱和溶液浓
D. 任何物质的溶解度都随着温度的升高而增大C8. 在一定温度下,从食盐的不饱和溶液中不断蒸发出水分,直到有食盐晶体析出,下列图中,能表示食盐溶液的溶质质量分数与蒸发掉的水的质量之间关系的是:( )D9. 下列说法中,不正确的是( )
A. 从溶液中析出的晶体都含有结晶水
B. 浓溶液不一定是饱和溶液,稀溶液不一定是不饱和溶液
C. 同温时,同种物质的饱和溶液的溶质的质量分数一定大于不饱和溶液的溶质质量分数
D. 溶解度曲线上的任意一点都表示某温度时,某物质在100克溶剂中达到饱和时所溶解的质量A10. 下列关于溶解度的说法,不正确的是( )
A. 相同条件下,不同物质的溶解度一般是不同的
B. 相同条件下,物质的溶解度随溶剂的量的增减而变化
C. 同一物质的溶解度,随温度的变化而变化
D. 气体的溶解度随温度的升高而减小,多数固体物质的溶解度随温度的升高而增大B11.20℃时,把某物质的溶液分成质量相等的两份,其中一份蒸发掉25克水达到饱和,另一份加入15克溶质也达到饱和,则时,有关该物质的结论正确的是( )
A. 该物质是一种难溶物
B. 该物质溶液质量分数的最大值为37.5%
C. 20℃时,该物质的溶解度为60克
D. 将其饱和溶液中溶质的质量分数增大一倍,可采用蒸发溶剂的方法C12. 计算1.5升质量分数为98%的浓硫酸(密度为1.84 克/厘米3)所含溶质的质量时,下列算式中正确的是( )ABCDD13. 把在“粗盐提纯”实验中玻璃棒的作用或用法,按要求填在横线上:
(1)粗盐溶解时,玻璃棒的用法是________,作用是________;
(2)过滤食盐水时,玻璃棒的用法是________,作用是________;
(3)滤液蒸发时,玻璃棒的用法是________,作用是________。搅拌加速粗盐溶解搅拌使液体均匀受热
防止液体飞溅引流引流14. 已知医用碘酒中碘的质量分数为2% ,10克碘可配制这种碘酒________克,156.8克酒精可配制这种碘酒________克。15. 配制一定质量、一定溶质质量分数的食盐水的实验步骤为_______、_______、_______。
500160计算称量溶解16.在下列叙述中的横线上,填上适宜分离操作的编号:
A.蒸发结晶法 B.降温结晶法(冷却热饱和溶液) C.过滤法;D.蒸馏法
⑴食盐水中混有泥沙,欲从中分离出食盐,
应先 再 ;
⑵硝酸钾中混有少量氯化钠, 用 ;
⑶将酒精溶液中的酒精和水分离开,应用 ;
⑷欲从含有泥沙的水里得到较纯净的水,
应用 ;CABDC17.某固体物质的溶解度曲线如图所示,根据图回答如下问题:
⑴图中B点的意义:表示该物质在t3℃时,每100g溶剂和S1 g溶质形成不饱和溶液。A点的意义: 。
此溶液的溶质质量分数的表达式 。每100g溶剂和S2 g溶质形成饱和溶液。S2/(100+S2)⑵若A、B两点的溶液在保持温度不变的情况下各加20克水,A点的溶解度将 (填“增大”、“减小”、或“不变”);
A、B的溶质质量分数 (填“前者大”、“后者大”或“相等”)。
⑶当温度降低时,A点变动后溶液的质量分数与原来比较 ( )
(填“增大”、“减小”或“不变”)。
⑷若使M点的(100+S1)g溶液成为饱和溶液的方法:降温至 ℃;不变前者大减小t118.20℃时,食盐的溶解度为36克,在20℃时将100克食盐放入250克水中,充分搅拌,所得溶液的质量分数为多少?19.一定温度下质量分数为a%的硝酸钾溶液,将其分成两份,一份等温蒸发10g水,得0.5g晶体;另一份等温蒸发12.5g水得1.5g晶体,该温度下硝酸钾的溶解度为多少?20、将30℃时某物质的溶液100克,分成质量相等的两份,向其中的一份加入5克该溶质,溶液恰好达到饱和,将另一份冷却到20℃,溶液也恰好达到饱和,此饱和溶液的质量分数为20%,求该物质在30℃时的溶解度?
同课章节目录
- 第1章 水和水的溶液
- 第1节 地球上的水
- 第2节 水的组成
- 第3节 水的浮力
- 第4节 物质在水中的分散状况
- 第5节 物质的溶解
- 第6节 物质的分离
- 第7节 水资源的利用、开发和保护
- 第2章 天气与气候
- 第1节 大气层
- 第2节 气温
- 第3节 大气的压强
- 第4节 风和降水
- 第5节 天气预报
- 第6节 气候和影响气候的因素
- 第7节 我国的气候特征与主要气象灾害
- 第3章 生命活动的调节
- 第1节 植物生命活动的调节
- 第2节 人体的激素调节
- 第3节 神经调节
- 第4节 动物的行为
- 第5节 体温的控制
- 第4章 电路探秘
- 第1节 电荷与电流
- 第2节 电流的测量
- 第3节 物质的导电性与电阻
- 第4节 变阻器
- 第5节 电压的测量
- 第6节 电流与电压、电阻的关系
- 第7节 电路分析与应用
- 研究性学习课题
- 一 测定本地区的“酸雨”情况及分析原因
- 二 太阳黑子活动与本地区降水的关系
- 三 训练小动物建立某种条件反射
- 四 调查在自然界或生命活动中的电现象
