物质转化规律的典型例题[上学期]
图片预览





文档简介
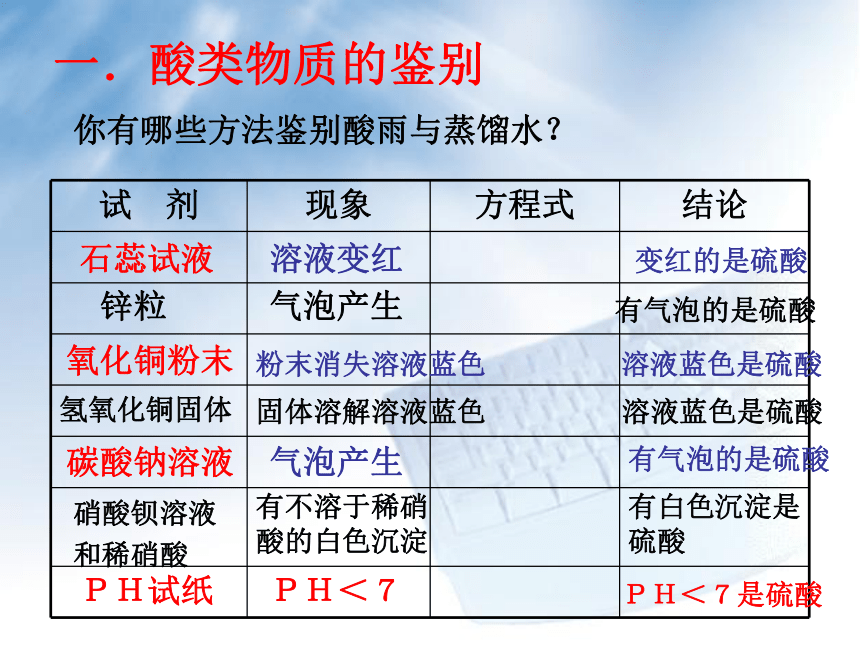
课件21张PPT。物质的转化规律练习一.酸类物质的鉴别你有哪些方法鉴别酸雨与蒸馏水?石蕊试液溶液变红变红的是硫酸锌粒气泡产生有气泡的是硫酸氧化铜粉末粉末消失溶液蓝色溶液蓝色是硫酸氢氧化铜固体固体溶解溶液蓝色溶液蓝色是硫酸碳酸钠溶液气泡产生有气泡的是硫酸硝酸钡溶液
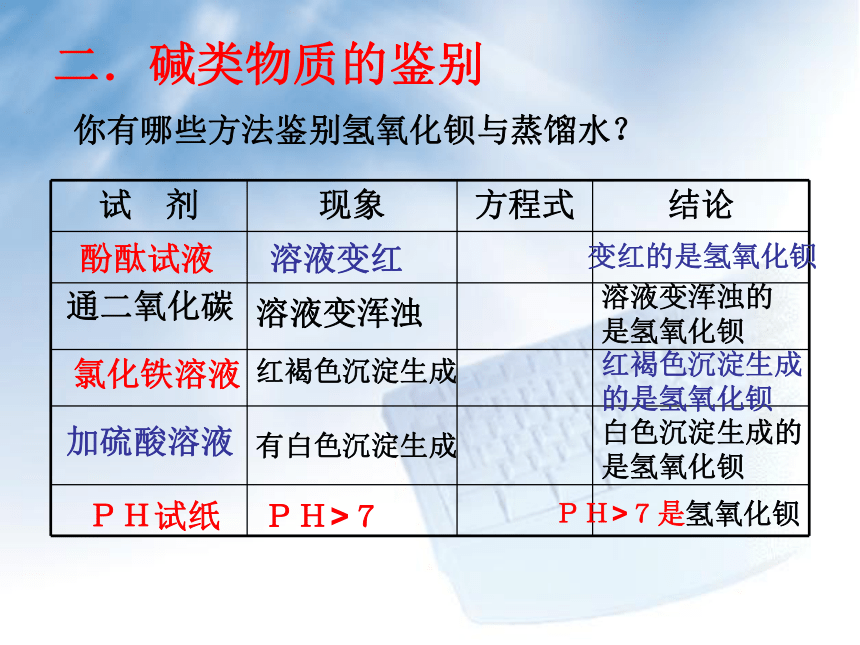
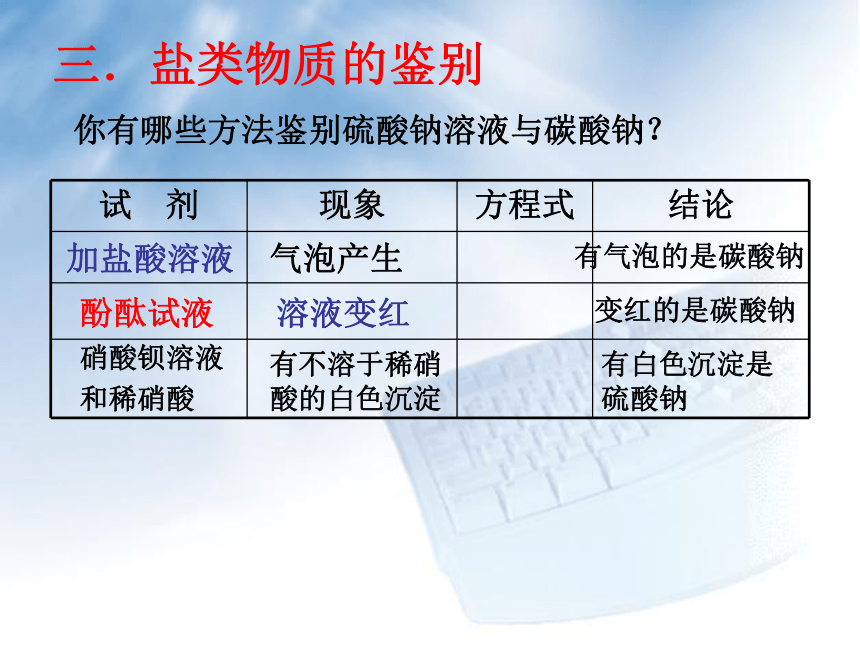
和稀硝酸有不溶于稀硝酸的白色沉淀有白色沉淀是硫酸PH试纸PH<7PH<7是硫酸二.碱类物质的鉴别你有哪些方法鉴别氢氧化钡与蒸馏水?酚酞试液溶液变红变红的是氢氧化钡通二氧化碳溶液变浑浊溶液变浑浊的是氢氧化钡氯化铁溶液红褐色沉淀生成红褐色沉淀生成的是氢氧化钡加硫酸溶液有白色沉淀生成白色沉淀生成的是氢氧化钡PH试纸PH>7PH>7是氢氧化钡三.盐类物质的鉴别你有哪些方法鉴别硫酸钠溶液与碳酸钠?加盐酸溶液气泡产生有气泡的是碳酸钠酚酞试液溶液变红变红的是碳酸钠硝酸钡溶液
和稀硝酸有不溶于稀硝酸的白色沉淀有白色沉淀是硫酸钠例现有盐酸、氢氧化钙、碳酸钠三种溶液,请你从中选择两种溶液,用化学方法进行鉴别。要求:①选择试剂时,同类物质只能用一次;②每次鉴别一次完成;③有微溶生成的不按沉淀处理。请回答:
(1)你认为鉴别方法最多的两种溶液是:
(2)鉴别上述任意两种溶液,你所选择的试剂分别是:
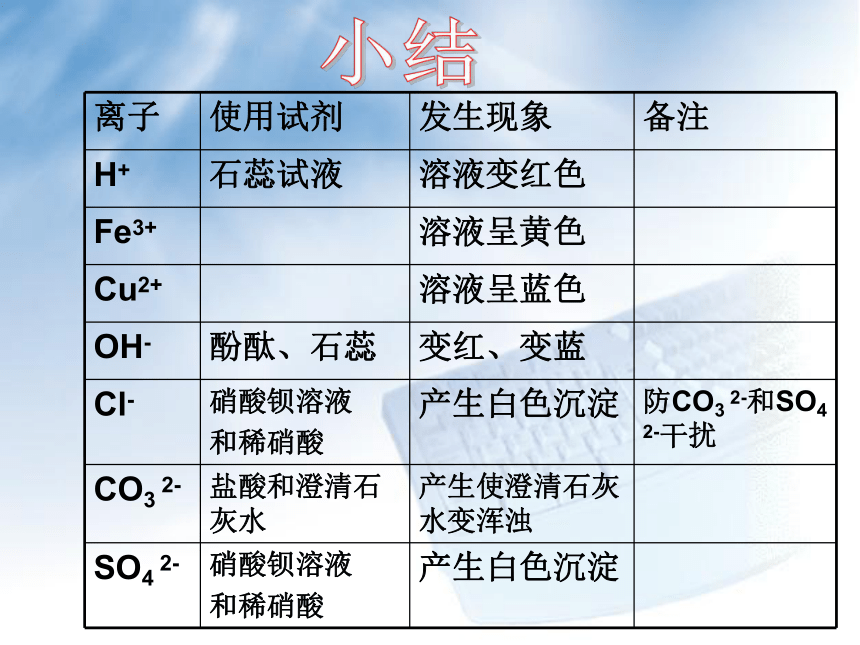
(3)填写上述任意一种试剂鉴别这两种溶液的实验报告小结四.除杂题的方法和原则1.除杂方法(1)过滤法:即通过过滤,除去不溶性杂质。如粗盐精制。(2)结晶法:当两种固体物质的溶解度相差很大时。如硝酸钾中混有少量食盐。(3)溶解法:将杂质用化学方法溶解。如铜粉中混有少量的铁粉。(4)沉淀法:加入某种试剂,跟杂质反应形成沉淀,滤去沉淀,即可除去杂质。(5)化气法:加入某种试剂,跟杂质反应,化为气体逸出,即可除去杂质。(6)加热法:通过加热,使杂质分解,从而除去杂质。(7)吸收法:用某种物质做吸收剂,把杂质吸收。如制取氢气中常混有水蒸气和氯化氢,用氢氧化钠来吸收HCl,用浓硫酸来吸收水蒸气。1.除杂题的原则(1)除杂时,所选用的试剂不能跟被提纯的物质反应。(2)除杂时,要防止在被提纯的物质中引入新的杂质。(3)还有考虑除杂后便于分离。五.分离题的解题思路分离方法物理方法化学方法过滤冷却热饱和溶液蒸发结晶用于分离溶解性不同的物质。用于分离溶解度受温度影响不同的物质。将溶质从溶液中分离出来。先采用除杂的方法将一种成分转化,利用溶解性差异将物质分开后,再分别复原为原物质。六.如何判断常见溶液中的离子能否大量共存。(1)在酸、碱、盐溶液的相互反应中,两种离子能直接结合成难溶物质,则这种离子就不能大量共存。(2)两种离子能结合成水,则H+和OH-不能共存。(3)两种离子能结合成水,则H+和OH-不能共存。例1.有三种阳离子H+、Cu2+、Ba2+中的两种离子和NO3-、Cl-、OH-、CO32-四种阴离子中的两种离子,在溶液中大量含有的四种离子应该是___________。Cu2+ 、 Ba2+ 、 NO3-、Cl-2.欲除去下列物质中括号内的少量杂质,分别写出所加试剂和发生的化学方程式。
NaCl(Na2CO3) HNO3(HCl)
Na2SO4(Na2CO3) HCl(H2SO4)HC 、 AgNO3 、 H2SO4、BaCl试一试:1.除去下列括号内杂质,用化学方程式表示。
硝酸钠(氯化钠)、烧碱(纯碱)、汞(铜)
2.某硝酸钠溶液中混有少量氯化钠、硫酸钠、碳酸钠杂质,仅提供三种药品:硝酸银溶液、氯化钡溶液和稀盐酸。请设计合理的顺序将杂质逐一除去。
3.含有少量水蒸气、一氧化碳、二氧化碳的氮气,欲得到纯净的氮气,可使混合气体先后通过足量的_________,再通过_______________,最后通过____________。4.在分开盛放的A、B两溶液中,共含有钠离子、铜离子、钡离子、镁离子、氢氧根离子、硝酸根离子、硫酸根离子,两溶液中所含离子各不相同,已知A溶液里含三种阳离子和两种阴离子,其余在B溶液里,则B溶液里所含离子应该是__________。
5.某工厂的废渣中混有少量的锌和氧化铜与大量废盐酸接触能形成污水,产生公害,若向污水中撒入铁粉,且反应后铁粉有剩余,此时污水中一定含有的金属离子是______________。钡离子和氢氧根离子锌离子和亚铁离子六.推断题。有四种失去标签的无色溶液,其物质分别是碳酸钾、盐酸、硝酸银、氯化钡中的一种。现将其随意编号为A、B、C、D,并分别取少量两两混合实验。有关实验现象如下所示。试推断出A、B、C、D分别是什么?1.表格型统计2.密码型1.有A、B、C三种物质,已知A为钠盐,B为盐酸盐,C为碱。将它们分别溶于水后各取少量进行两两混合实验。其结果如下:
(1)A+B—无明显现象
(2)B+C——产生蓝色沉淀
(3)A+C——产生不溶于稀硝酸的白色沉淀
由此推断A、B、C的化学式分别是_____3.框图型分别取少量钾盐和钙盐B分别溶于水,均得到无色透明溶液。有关实验操作和结果如图所示。推断A、B的化学式。A溶液B溶液C溶液白色沉淀C硝酸银溶液加稀盐酸无色溶液白色沉淀B溶液无色气体F澄清石灰水白色沉淀D加稀硝酸沉淀不溶解 有一种钠盐A和一种可溶性钙盐B组成的固体混合物,按下列步骤实验:混合物溶于水,恰好完全反应,过滤白色沉淀无色溶液加稀盐酸氯化钙溶液二氧化碳加硝酸银溶液硝酸钠溶液氯化银沉淀推断出A、B的化学式。4.连线型如图所示,编号1-6代表六中物质,它们分别是硫酸铜溶液、铁、石灰水、碳酸钾溶液、氯化钡溶液,凡连线两端的物质都能反应,根据图中关系确定方框内的物质。
和稀硝酸有不溶于稀硝酸的白色沉淀有白色沉淀是硫酸PH试纸PH<7PH<7是硫酸二.碱类物质的鉴别你有哪些方法鉴别氢氧化钡与蒸馏水?酚酞试液溶液变红变红的是氢氧化钡通二氧化碳溶液变浑浊溶液变浑浊的是氢氧化钡氯化铁溶液红褐色沉淀生成红褐色沉淀生成的是氢氧化钡加硫酸溶液有白色沉淀生成白色沉淀生成的是氢氧化钡PH试纸PH>7PH>7是氢氧化钡三.盐类物质的鉴别你有哪些方法鉴别硫酸钠溶液与碳酸钠?加盐酸溶液气泡产生有气泡的是碳酸钠酚酞试液溶液变红变红的是碳酸钠硝酸钡溶液
和稀硝酸有不溶于稀硝酸的白色沉淀有白色沉淀是硫酸钠例现有盐酸、氢氧化钙、碳酸钠三种溶液,请你从中选择两种溶液,用化学方法进行鉴别。要求:①选择试剂时,同类物质只能用一次;②每次鉴别一次完成;③有微溶生成的不按沉淀处理。请回答:
(1)你认为鉴别方法最多的两种溶液是:
(2)鉴别上述任意两种溶液,你所选择的试剂分别是:
(3)填写上述任意一种试剂鉴别这两种溶液的实验报告小结四.除杂题的方法和原则1.除杂方法(1)过滤法:即通过过滤,除去不溶性杂质。如粗盐精制。(2)结晶法:当两种固体物质的溶解度相差很大时。如硝酸钾中混有少量食盐。(3)溶解法:将杂质用化学方法溶解。如铜粉中混有少量的铁粉。(4)沉淀法:加入某种试剂,跟杂质反应形成沉淀,滤去沉淀,即可除去杂质。(5)化气法:加入某种试剂,跟杂质反应,化为气体逸出,即可除去杂质。(6)加热法:通过加热,使杂质分解,从而除去杂质。(7)吸收法:用某种物质做吸收剂,把杂质吸收。如制取氢气中常混有水蒸气和氯化氢,用氢氧化钠来吸收HCl,用浓硫酸来吸收水蒸气。1.除杂题的原则(1)除杂时,所选用的试剂不能跟被提纯的物质反应。(2)除杂时,要防止在被提纯的物质中引入新的杂质。(3)还有考虑除杂后便于分离。五.分离题的解题思路分离方法物理方法化学方法过滤冷却热饱和溶液蒸发结晶用于分离溶解性不同的物质。用于分离溶解度受温度影响不同的物质。将溶质从溶液中分离出来。先采用除杂的方法将一种成分转化,利用溶解性差异将物质分开后,再分别复原为原物质。六.如何判断常见溶液中的离子能否大量共存。(1)在酸、碱、盐溶液的相互反应中,两种离子能直接结合成难溶物质,则这种离子就不能大量共存。(2)两种离子能结合成水,则H+和OH-不能共存。(3)两种离子能结合成水,则H+和OH-不能共存。例1.有三种阳离子H+、Cu2+、Ba2+中的两种离子和NO3-、Cl-、OH-、CO32-四种阴离子中的两种离子,在溶液中大量含有的四种离子应该是___________。Cu2+ 、 Ba2+ 、 NO3-、Cl-2.欲除去下列物质中括号内的少量杂质,分别写出所加试剂和发生的化学方程式。
NaCl(Na2CO3) HNO3(HCl)
Na2SO4(Na2CO3) HCl(H2SO4)HC 、 AgNO3 、 H2SO4、BaCl试一试:1.除去下列括号内杂质,用化学方程式表示。
硝酸钠(氯化钠)、烧碱(纯碱)、汞(铜)
2.某硝酸钠溶液中混有少量氯化钠、硫酸钠、碳酸钠杂质,仅提供三种药品:硝酸银溶液、氯化钡溶液和稀盐酸。请设计合理的顺序将杂质逐一除去。
3.含有少量水蒸气、一氧化碳、二氧化碳的氮气,欲得到纯净的氮气,可使混合气体先后通过足量的_________,再通过_______________,最后通过____________。4.在分开盛放的A、B两溶液中,共含有钠离子、铜离子、钡离子、镁离子、氢氧根离子、硝酸根离子、硫酸根离子,两溶液中所含离子各不相同,已知A溶液里含三种阳离子和两种阴离子,其余在B溶液里,则B溶液里所含离子应该是__________。
5.某工厂的废渣中混有少量的锌和氧化铜与大量废盐酸接触能形成污水,产生公害,若向污水中撒入铁粉,且反应后铁粉有剩余,此时污水中一定含有的金属离子是______________。钡离子和氢氧根离子锌离子和亚铁离子六.推断题。有四种失去标签的无色溶液,其物质分别是碳酸钾、盐酸、硝酸银、氯化钡中的一种。现将其随意编号为A、B、C、D,并分别取少量两两混合实验。有关实验现象如下所示。试推断出A、B、C、D分别是什么?1.表格型统计2.密码型1.有A、B、C三种物质,已知A为钠盐,B为盐酸盐,C为碱。将它们分别溶于水后各取少量进行两两混合实验。其结果如下:
(1)A+B—无明显现象
(2)B+C——产生蓝色沉淀
(3)A+C——产生不溶于稀硝酸的白色沉淀
由此推断A、B、C的化学式分别是_____3.框图型分别取少量钾盐和钙盐B分别溶于水,均得到无色透明溶液。有关实验操作和结果如图所示。推断A、B的化学式。A溶液B溶液C溶液白色沉淀C硝酸银溶液加稀盐酸无色溶液白色沉淀B溶液无色气体F澄清石灰水白色沉淀D加稀硝酸沉淀不溶解 有一种钠盐A和一种可溶性钙盐B组成的固体混合物,按下列步骤实验:混合物溶于水,恰好完全反应,过滤白色沉淀无色溶液加稀盐酸氯化钙溶液二氧化碳加硝酸银溶液硝酸钠溶液氯化银沉淀推断出A、B的化学式。4.连线型如图所示,编号1-6代表六中物质,它们分别是硫酸铜溶液、铁、石灰水、碳酸钾溶液、氯化钡溶液,凡连线两端的物质都能反应,根据图中关系确定方框内的物质。
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
