科学[上学期]
图片预览










文档简介
课件60张PPT。科学
九年级上册
北京市京源学校 孙清亚第一章 金属
第二章 酸、碱、盐 第二章 酸碱盐
第一节 溶液的酸碱性
第二节 酸
第三节 碱 中和反应
第四节 盐
第五节 溶解度 溶质的质量分数课标要求:
1、说出某些重要的盐的性质(如:食
盐、纯碱、小苏打、碳酸钙等)
2、了解酸和碱的主要性质,举例说明酸
和碱在日常生活中的用途和对人类的
影响,会测定溶液的酸碱性,了解强
酸、强碱的使用注意事项
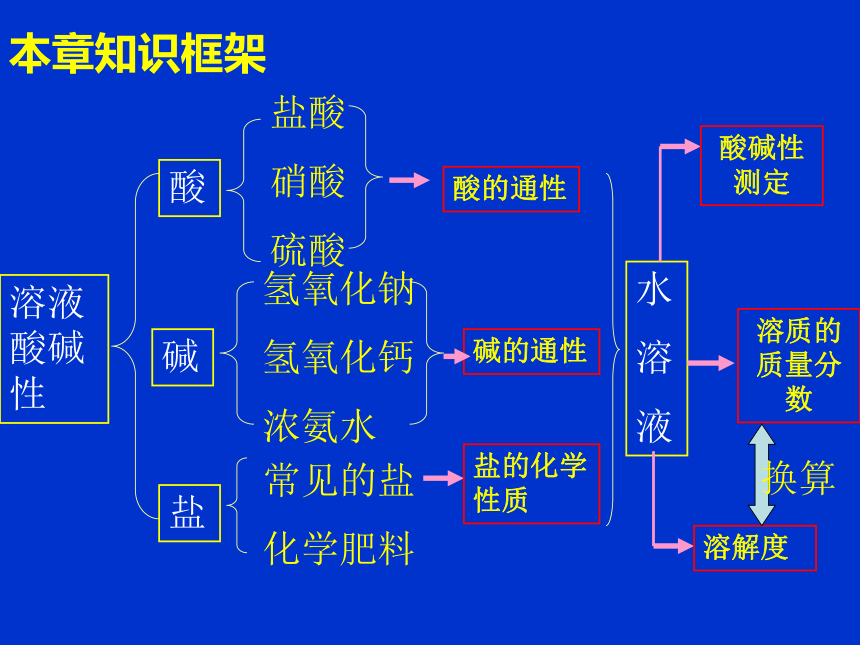
3、说出中和反应的特点 本章知识框架 酸溶液酸碱性盐酸
硝酸
硫酸碱盐氢氧化钠
氢氧化钙
浓氨水常见的盐
化学肥料
酸的通性碱的通性盐的化学性质 水
溶
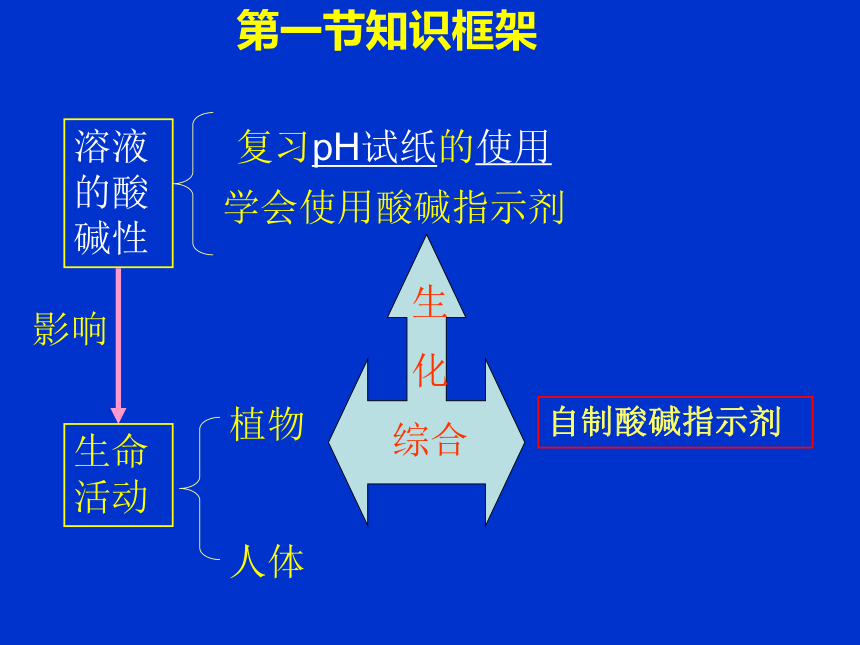
液酸碱性测定溶质的质量分数溶解度换算 第二章 酸碱盐 第一节 溶液的酸碱性 第一节知识框架 溶液的酸碱性生命活动复习pH试纸的使用自制酸碱指示剂学会使用酸碱指示剂植物
人体影响生
化
综合第一节教学建议 魔术引入:雨落叶出红花开导入建议:第一节教学建议 1、复习pH试纸的使用方法—学生演示 2、本节课的试剂可以由学生自带与实验室准备相结合 3、酸碱指示剂的使用-自制酸碱指示剂 方法见课本26页(可以改为家庭小实验) 4、石蕊试纸的使用 红色石蕊试纸----检验碱溶液 蓝色石蕊试纸----检验酸溶液 过程建议:pH与人体健康人体体液的pH是7.35~7.45时正常;
人体体液的pH<7.35时,处于亚健康状况;
人体体液的pH=6.9时,变成植物人;
人体体液的pH是6.85~6.45时死亡。知识浏览——溶液的酸碱性认识酸性和碱性溶液酸碱度)pH试纸、测定溶液的pH溶液酸碱性与生命活动的关系酸碱指示剂、检验溶液的酸碱性拓展视野:自制酸碱批示剂关于本节设计思想的说明 本节从对溶液酸碱性的认识入手,最主要体现的科学思想是自然界普遍联系,物质相互作用的思想,这同时也是应在本节教学中始终坚持的观点和理念。本节内容,在前一章学习了金属的有关知识后,为学习几类重要的化合物——酸、碱和盐做个铺垫。 第二章 酸碱盐 第二节 酸 第二节知识框架 常见的酸浓硫酸的特性盐酸
硫酸
硝酸物理性质化学性质物理性质化学性质物理性质化学性质使用安全稀酸主要性质跟指示剂的反应
跟金属的反应
跟金属氧化物的反应
跟碱的反应
跟盐的反应探究
活动稀释方法事故处理第二节教学建议 导入建议: 对日常生活中见过或认为是酸的物品性质的讨论开始引入第二节教学建议 1、 浓硫酸特性---先教方法再操作 可以补充演示吸水性、脱水性1、2和水入浓硫酸的危险 2、腐蚀性,用时一定要注意安全 3、稀酸的主要性质的实验探究和归纳总结,设计课堂活动 4、盐酸“毁容”两公里马路(图) 5、金属活动性顺序表再应用 过程建议:稀释浓硫酸清华一学生硫酸烧伤5头熊 清华一学生硫酸烧伤5头熊 清纯少女惨遭浓硫酸毁容 只因成绩好遭妒忌 盐酸“毁容”两公里马路(图) 硫酸的用途 第二节教学建议 1、 浓硫酸特性---先教方法再操作 可以补充演示吸水性、脱水性1、2和水入浓硫酸的危险 2、腐蚀性,盐酸“毁容”两公里马路(图)用时一定要注意安全 3、稀酸的主要性质的实验探究和归纳总结,设计课堂活动 4、依据课本探究 5、金属活动性顺序表再应用 过程建议2:关于本节设计思想的说明 本节首先从学生已知的对酸的表面的、可能并不科学的认识开始,引导他们通过自己的观察、体验和有一定规律的实验,进一步认识化学中的酸类物质。主要体现的科学思想是物质相互作用及物质的一般性与特殊性关系问题。本节的内容与后面两节内容共同完成学生对酸碱盐的认识,使学生了解研究一类物质性质的科学方法。依据课本探究酸的化学性质结论:
1. 稀酸与含OH-的物质反应时,有什么共同特点?
2. 稀酸可以与哪些金属发生反应,不能与哪些金属发生反应?
3. 稀硫酸与含Ba2+的物质发生反应时,有什么共同特点?
4.稀酸与含CO32-的物质发生反应时,有什么共同特点? 依据课本探究酸的化学性质讨论:
1. 在做酸和碱反应的实验时,为什么要先滴加酚酞试液?与不加酚酞试液进行比较。
2. 将你对归纳总结中问题的看法与其他同学进行交流。
依据课本探究酸的化学性质归纳酸的通性:
跟指示剂的反应
跟金属的反应
跟金属氧化物的反应
跟碱的反应
跟盐的反应关于本节设计思想的说明 本节首先从学生已知的对酸的表面的、可能并不科学的认识开始,引导他们通过自己的观察、体验和有一定规律的实验,进一步认识化学中的酸类物质。主要体现的科学思想是物质相互作用及物质的一般性与特殊性关系问题。本节的内容与后面两节内容共同完成学生对酸碱盐的认识,使学生了解研究一类物质性质的科学方法。 第二章 酸碱盐 第三节 碱 中和反应 第三节知识框架 常见的碱氢氧化钠
氢氧化钙
浓氨水物理性质化学性质物理性质化学性质物理性质化学性质碱的主要化学性质跟指示剂的反应
跟非金属氧化物
的反应
跟酸的反应
跟盐的反应化学方程式书写中和反应第三节教学建议 导入建议: 对日常生活中见过或认为是碱的物品性质的讨论开始引入第三节教学建议 1、 氢氧化钠的腐蚀性---20%氢氧化钠泡鸡爪 2、碱的主要性质的实验探究和归纳总结,设计课堂活动 3、酸和碱的应用—小课题研究:列举身边的酸碱 过程建议:氢氧化钠有腐蚀性 复分解反应Cu(OH)2+2HClHCl+AgNO3CuCl2+2H2O=AgCl↓+HNO3= 像这类由两种化合物相互交换成分,生成另外两种化合物的反应,叫做复分解反应AB + CD = AD + CBA DA D A D A D A DAD复分解反应的特征AB + CD = AD + CBB CB CB CB CBC+ CB复分解反应的特征复分解反应发生的条件Cu(OH)2 + 2HCl = CuCl2 + 2H2O HCl + AgNO3 = AgCl ↓ + HNO3 CaCO3+2HCl=CaCl2+H2O+CO2↑H2OH2OH2O↓↓↓↑↑↑ 有难溶的物质(如BaSO4、AgCl)或难电离的物质(如H2O)或挥发性的物质(如CO2)生成,只要具备上述条件之一,这类反应就能发生。复分解反应发生的条件 第二章 酸碱盐 第四节 盐 第四节知识框架 自然界中的盐明矾
硝酸钾
氯化钠
硫酸铜
碳酸钙
盐溶液的主要化学性质跟某些金属的反应
跟酸的反应
跟碱的反应
跟盐的反应化学方程式书写化学肥料第四节教学建议 导入建议: 对日常生活中见过或认为是盐的物品性质的讨论开始引入第四节教学建议 1、 碱的主要性质的实验探究和归纳总结,设计课堂活动 2、盐的应用—小课题研究:列举身边的酸碱盐 3、单质氧化物酸碱盐之间的转化 4、 认识化学肥料的现实意义过程建议:化学肥料肥料化学肥料农家肥料:如厩肥、人粪尿、绿肥等。氮肥磷肥钾肥复合肥料微量元素肥料对比化学肥料和农家肥料的一些特点缺氮的棉花氮肥能促使作物的茎、叶生长茂盛,叶色浓绿。铵态氮肥不宜和碱性物质混合施用!铵盐跟碱起反应,生成氨气,使肥料失效。磷肥促进作物提早成熟,穗粒增多,子粒饱满。缺钾的大豆缺钾的甘蓝钾肥能促使作物生长健壮,茎杆粗硬,增强对虫害和倒伏的抵抗能力。 复合肥料是含有两种或两种以上营养元素的化肥,如磷酸二氢铵、硝酸钾等。 微量元素肥料主要有硼肥、锰肥、铜肥、锌肥、钼肥等,施用的量很少。植物缺乏这些微量元素,就会影响生长发育,减弱抗病能力。对比化学肥料和农家肥料的一些特点第二章 酸、碱、盐 重新整合第五节 溶解度 溶质的质量分数同种溶质在不同的溶 剂中的溶解能力不同不同的溶质在同种溶 剂中的溶解能力不同溶解性物质的溶解度易溶 、可溶 、 微溶 、 难(不)溶 固体的溶解度气体的溶解度影响因素(温度) 影响因素 (温度、压强)表示方法表示方法评价建议评价内容
(1)对科学探究(过程、方法和能力)的评价
(2)对科学知识与技能的评价
(3)对科学态度、情感与价值观的评价
(4)对科学、技术与社会关系认识的评价
评价建议评价方法
科学课程(7?9年级)采用的评价方法主要有连续观察与面谈、实践活动、书面测试、个人成长记录等方法。评价建议命题原则
基础性
发展性
开放性
探究性
实践性
综合性评价建议命题趋势
强调科学知识的应用;
突出环境保护及其他人类所关心的共同问题;
注重化学、物理、生物等学科知识的综合
加强实验考查
开始重视研究性学习和学生的创新能力
注重图表中相关数据的应用 为学生的有效学习 而系统设计教学2004年7月
盐、纯碱、小苏打、碳酸钙等)
2、了解酸和碱的主要性质,举例说明酸
和碱在日常生活中的用途和对人类的
影响,会测定溶液的酸碱性,了解强
酸、强碱的使用注意事项
3、说出中和反应的特点 本章知识框架 酸溶液酸碱性盐酸
硝酸
硫酸碱盐氢氧化钠
氢氧化钙
浓氨水常见的盐
化学肥料
酸的通性碱的通性盐的化学性质 水
溶
液酸碱性测定溶质的质量分数溶解度换算 第二章 酸碱盐 第一节 溶液的酸碱性 第一节知识框架 溶液的酸碱性生命活动复习pH试纸的使用自制酸碱指示剂学会使用酸碱指示剂植物
人体影响生
化
综合第一节教学建议 魔术引入:雨落叶出红花开导入建议:第一节教学建议 1、复习pH试纸的使用方法—学生演示 2、本节课的试剂可以由学生自带与实验室准备相结合 3、酸碱指示剂的使用-自制酸碱指示剂 方法见课本26页(可以改为家庭小实验) 4、石蕊试纸的使用 红色石蕊试纸----检验碱溶液 蓝色石蕊试纸----检验酸溶液 过程建议:pH与人体健康人体体液的pH是7.35~7.45时正常;
人体体液的pH<7.35时,处于亚健康状况;
人体体液的pH=6.9时,变成植物人;
人体体液的pH是6.85~6.45时死亡。知识浏览——溶液的酸碱性认识酸性和碱性溶液酸碱度)pH试纸、测定溶液的pH溶液酸碱性与生命活动的关系酸碱指示剂、检验溶液的酸碱性拓展视野:自制酸碱批示剂关于本节设计思想的说明 本节从对溶液酸碱性的认识入手,最主要体现的科学思想是自然界普遍联系,物质相互作用的思想,这同时也是应在本节教学中始终坚持的观点和理念。本节内容,在前一章学习了金属的有关知识后,为学习几类重要的化合物——酸、碱和盐做个铺垫。 第二章 酸碱盐 第二节 酸 第二节知识框架 常见的酸浓硫酸的特性盐酸
硫酸
硝酸物理性质化学性质物理性质化学性质物理性质化学性质使用安全稀酸主要性质跟指示剂的反应
跟金属的反应
跟金属氧化物的反应
跟碱的反应
跟盐的反应探究
活动稀释方法事故处理第二节教学建议 导入建议: 对日常生活中见过或认为是酸的物品性质的讨论开始引入第二节教学建议 1、 浓硫酸特性---先教方法再操作 可以补充演示吸水性、脱水性1、2和水入浓硫酸的危险 2、腐蚀性,用时一定要注意安全 3、稀酸的主要性质的实验探究和归纳总结,设计课堂活动 4、盐酸“毁容”两公里马路(图) 5、金属活动性顺序表再应用 过程建议:稀释浓硫酸清华一学生硫酸烧伤5头熊 清华一学生硫酸烧伤5头熊 清纯少女惨遭浓硫酸毁容 只因成绩好遭妒忌 盐酸“毁容”两公里马路(图) 硫酸的用途 第二节教学建议 1、 浓硫酸特性---先教方法再操作 可以补充演示吸水性、脱水性1、2和水入浓硫酸的危险 2、腐蚀性,盐酸“毁容”两公里马路(图)用时一定要注意安全 3、稀酸的主要性质的实验探究和归纳总结,设计课堂活动 4、依据课本探究 5、金属活动性顺序表再应用 过程建议2:关于本节设计思想的说明 本节首先从学生已知的对酸的表面的、可能并不科学的认识开始,引导他们通过自己的观察、体验和有一定规律的实验,进一步认识化学中的酸类物质。主要体现的科学思想是物质相互作用及物质的一般性与特殊性关系问题。本节的内容与后面两节内容共同完成学生对酸碱盐的认识,使学生了解研究一类物质性质的科学方法。依据课本探究酸的化学性质结论:
1. 稀酸与含OH-的物质反应时,有什么共同特点?
2. 稀酸可以与哪些金属发生反应,不能与哪些金属发生反应?
3. 稀硫酸与含Ba2+的物质发生反应时,有什么共同特点?
4.稀酸与含CO32-的物质发生反应时,有什么共同特点? 依据课本探究酸的化学性质讨论:
1. 在做酸和碱反应的实验时,为什么要先滴加酚酞试液?与不加酚酞试液进行比较。
2. 将你对归纳总结中问题的看法与其他同学进行交流。
依据课本探究酸的化学性质归纳酸的通性:
跟指示剂的反应
跟金属的反应
跟金属氧化物的反应
跟碱的反应
跟盐的反应关于本节设计思想的说明 本节首先从学生已知的对酸的表面的、可能并不科学的认识开始,引导他们通过自己的观察、体验和有一定规律的实验,进一步认识化学中的酸类物质。主要体现的科学思想是物质相互作用及物质的一般性与特殊性关系问题。本节的内容与后面两节内容共同完成学生对酸碱盐的认识,使学生了解研究一类物质性质的科学方法。 第二章 酸碱盐 第三节 碱 中和反应 第三节知识框架 常见的碱氢氧化钠
氢氧化钙
浓氨水物理性质化学性质物理性质化学性质物理性质化学性质碱的主要化学性质跟指示剂的反应
跟非金属氧化物
的反应
跟酸的反应
跟盐的反应化学方程式书写中和反应第三节教学建议 导入建议: 对日常生活中见过或认为是碱的物品性质的讨论开始引入第三节教学建议 1、 氢氧化钠的腐蚀性---20%氢氧化钠泡鸡爪 2、碱的主要性质的实验探究和归纳总结,设计课堂活动 3、酸和碱的应用—小课题研究:列举身边的酸碱 过程建议:氢氧化钠有腐蚀性 复分解反应Cu(OH)2+2HClHCl+AgNO3CuCl2+2H2O=AgCl↓+HNO3= 像这类由两种化合物相互交换成分,生成另外两种化合物的反应,叫做复分解反应AB + CD = AD + CBA DA D A D A D A DAD复分解反应的特征AB + CD = AD + CBB CB CB CB CBC+ CB复分解反应的特征复分解反应发生的条件Cu(OH)2 + 2HCl = CuCl2 + 2H2O HCl + AgNO3 = AgCl ↓ + HNO3 CaCO3+2HCl=CaCl2+H2O+CO2↑H2OH2OH2O↓↓↓↑↑↑ 有难溶的物质(如BaSO4、AgCl)或难电离的物质(如H2O)或挥发性的物质(如CO2)生成,只要具备上述条件之一,这类反应就能发生。复分解反应发生的条件 第二章 酸碱盐 第四节 盐 第四节知识框架 自然界中的盐明矾
硝酸钾
氯化钠
硫酸铜
碳酸钙
盐溶液的主要化学性质跟某些金属的反应
跟酸的反应
跟碱的反应
跟盐的反应化学方程式书写化学肥料第四节教学建议 导入建议: 对日常生活中见过或认为是盐的物品性质的讨论开始引入第四节教学建议 1、 碱的主要性质的实验探究和归纳总结,设计课堂活动 2、盐的应用—小课题研究:列举身边的酸碱盐 3、单质氧化物酸碱盐之间的转化 4、 认识化学肥料的现实意义过程建议:化学肥料肥料化学肥料农家肥料:如厩肥、人粪尿、绿肥等。氮肥磷肥钾肥复合肥料微量元素肥料对比化学肥料和农家肥料的一些特点缺氮的棉花氮肥能促使作物的茎、叶生长茂盛,叶色浓绿。铵态氮肥不宜和碱性物质混合施用!铵盐跟碱起反应,生成氨气,使肥料失效。磷肥促进作物提早成熟,穗粒增多,子粒饱满。缺钾的大豆缺钾的甘蓝钾肥能促使作物生长健壮,茎杆粗硬,增强对虫害和倒伏的抵抗能力。 复合肥料是含有两种或两种以上营养元素的化肥,如磷酸二氢铵、硝酸钾等。 微量元素肥料主要有硼肥、锰肥、铜肥、锌肥、钼肥等,施用的量很少。植物缺乏这些微量元素,就会影响生长发育,减弱抗病能力。对比化学肥料和农家肥料的一些特点第二章 酸、碱、盐 重新整合第五节 溶解度 溶质的质量分数同种溶质在不同的溶 剂中的溶解能力不同不同的溶质在同种溶 剂中的溶解能力不同溶解性物质的溶解度易溶 、可溶 、 微溶 、 难(不)溶 固体的溶解度气体的溶解度影响因素(温度) 影响因素 (温度、压强)表示方法表示方法评价建议评价内容
(1)对科学探究(过程、方法和能力)的评价
(2)对科学知识与技能的评价
(3)对科学态度、情感与价值观的评价
(4)对科学、技术与社会关系认识的评价
评价建议评价方法
科学课程(7?9年级)采用的评价方法主要有连续观察与面谈、实践活动、书面测试、个人成长记录等方法。评价建议命题原则
基础性
发展性
开放性
探究性
实践性
综合性评价建议命题趋势
强调科学知识的应用;
突出环境保护及其他人类所关心的共同问题;
注重化学、物理、生物等学科知识的综合
加强实验考查
开始重视研究性学习和学生的创新能力
注重图表中相关数据的应用 为学生的有效学习 而系统设计教学2004年7月
同课章节目录
