浙教版九年级上第二章第2节 物质的转化规律(第二课)[下学期]
文档属性
| 名称 | 浙教版九年级上第二章第2节 物质的转化规律(第二课)[下学期] |

|
|
| 格式 | rar | ||
| 文件大小 | 363.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2007-09-22 00:00:00 | ||
图片预览




文档简介
课件19张PPT。(第二课时)科学第五册第二章第二节物质转化规律第2课时金属化合物与金属单质 (三)金属冶炼引入:在自然界里仅有少数金属是以游离态(单质)的形式存在的,大多数金属是以化合态的形式存在。 金属冶炼就是要把金属从化合态变成游离态。常用的方法: 碳、一氧化碳、氢气等还原剂与金属氧化物在高温下的反应。实验五:、木炭还原氧化铜
1、将干燥的氧化铜和碳研磨成粉末,以5:1的比例均匀混合。木炭粉是黑色,粉末
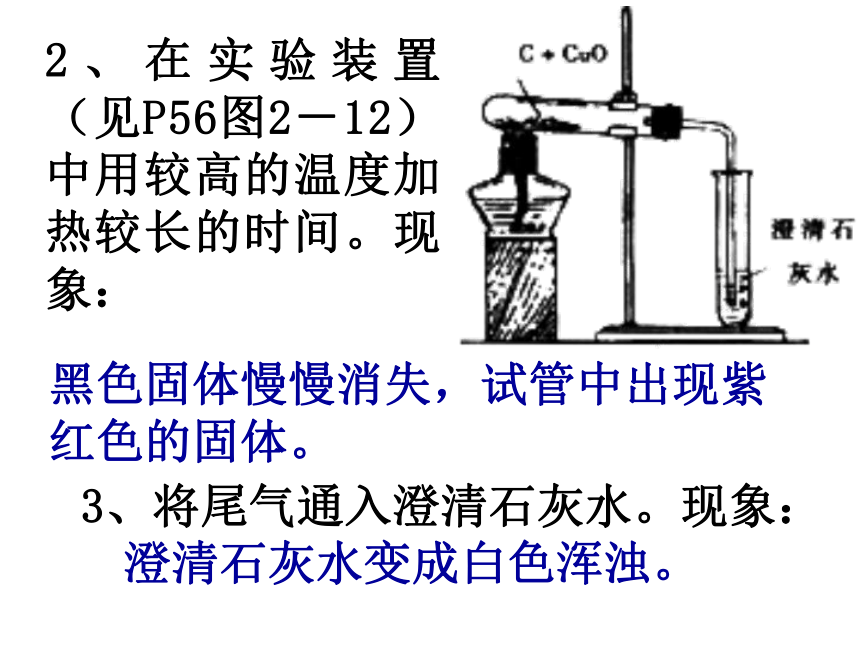
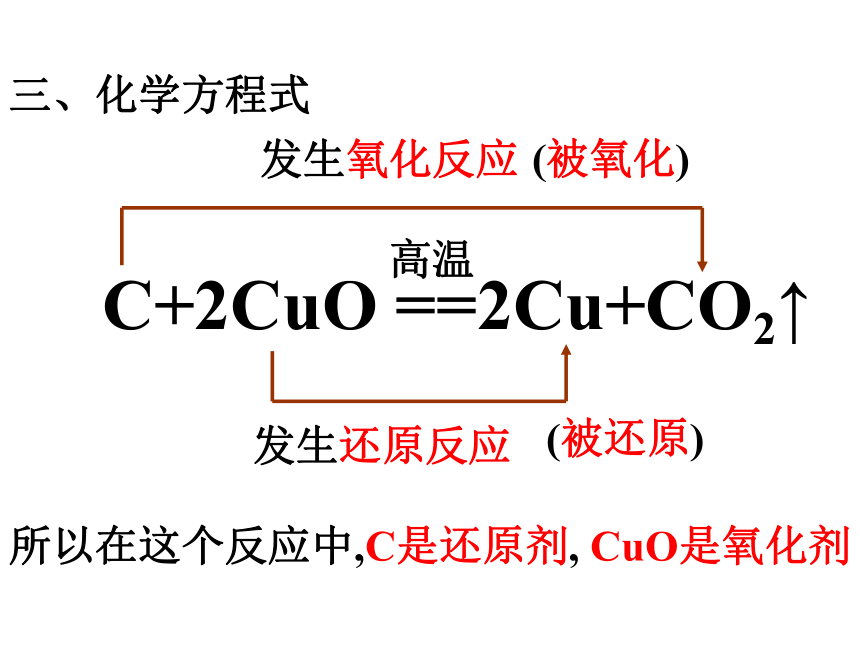
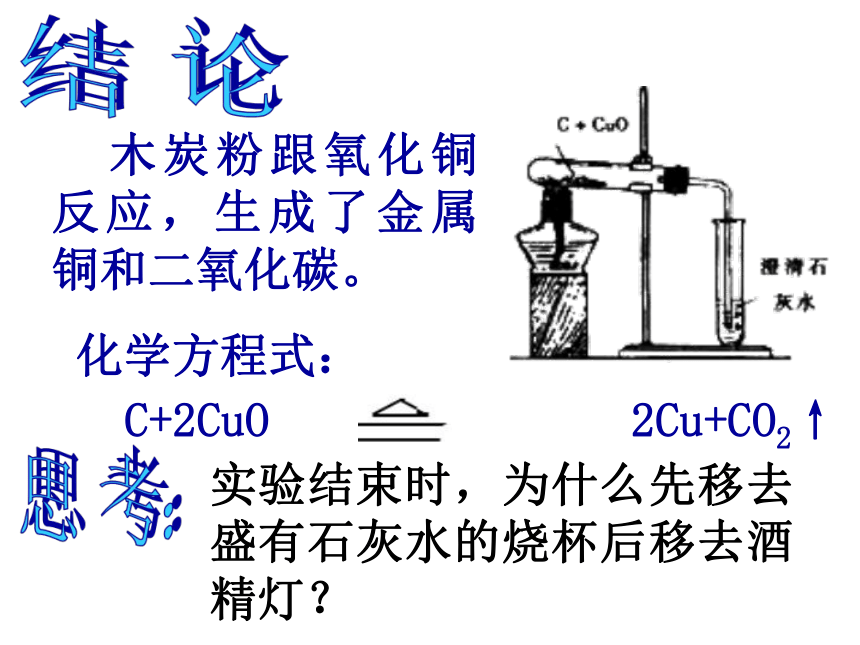
氧化铜是一种黑色固体。二、说出观察到的实验现象3、将尾气通入澄清石灰水。现象:黑色固体慢慢消失,试管中出现紫红色的固体。2、在实验装置(见P56图2-12)中用较高的温度加热较长的时间。现象:澄清石灰水变成白色浑浊。发生氧化反应所以在这个反应中,C是还原剂, CuO是氧化剂CuO是氧化剂(被氧化)(被还原)发生还原反应三、化学方程式 木炭粉跟氧化铜反应,生成了金属铜和二氧化碳。结 论实验结束时,为什么先移去盛有石灰水的烧杯后移去酒精灯??化学方程式: C+2CuO 2Cu+CO2↑思 考: 其他的一些副反应的化学方程式:
1、碳——一氧化碳;
2、一氧化碳还原氧化铜。 C+CO2 2CO
CO+CuO Cu+CO2实验六:步骤:
1、? 观察孔雀石颜 色:化学名:化学式:碱式碳酸铜Cu2(OH)2CO3是一种绿色的固体 2、? 把少量孔雀石粉末置于大试管内,用酒精灯加热约15分钟,用湿润的pH试纸贴在试管壁上观察颜色的变化,测定气体的水溶液pH大约是多少?现象:湿润的PH试纸变成浅红色,气体水溶液的PH约为6。3、孔雀石加热时有什么变化?绿色固体慢慢变成黑色固体。试管内壁出现小水滴,试管口冒出“白气”。结 论: 孔雀石加热时生成氧化铜、水和二氧化碳。1、? 化学反应方程式: Cu2(OH)2CO3 CuO+H2O+CO2↑ 4、待大试管的产物冷却后,如P57图2-13所示,通入氢气,过一会儿再给氧化铜加热。
现象: 1、黑色氧化铜变成光亮紫红色的金属铜。氢气还原氧化铜2、试管内壁出现小水滴,试管口冒出“白气“。结论:氢气和氧化铜在高温下反应生成金属铜和水。 H2+CuO Cu+ H2O1、盛放氧化铜的试管口为什么需略向下倾斜?防止反应生成的水倒流。 问题思考3、实验停止以后,为什么还要继续通入氢气,直到试管冷却为止?2、为什么要先通一会儿氢气,再加热.氧化铜?防止氢气与空气混合加热时试管内爆炸。防止灼热的铜被空气中的氧气重新氧化成氧化铜。由氧化铜制取铜,除氢气外,还可以用其他的什么方法吗?也可以用碳或一氧化碳 问题思考怎样把铁矿石炼成铁呢?思考铁矿石观察现象: 加热前:氧化铁粉末是一种
红棕色的固体。结论: 加热后:红棕色的固体变成黑色的粉末。澄清的石灰水变浑浊 CO和Fe2O3高温反应生成铁和二氧化碳。化学反应方程式:Fe2O3+3CO 2 Fe+ 3CO2 一氧化碳是一种有毒气体,剩余的CO应该如何处理?思考此实验应在通风橱内进行,也可将多余的CO导入火焰中燃烧。
1、将干燥的氧化铜和碳研磨成粉末,以5:1的比例均匀混合。木炭粉是黑色,粉末
氧化铜是一种黑色固体。二、说出观察到的实验现象3、将尾气通入澄清石灰水。现象:黑色固体慢慢消失,试管中出现紫红色的固体。2、在实验装置(见P56图2-12)中用较高的温度加热较长的时间。现象:澄清石灰水变成白色浑浊。发生氧化反应所以在这个反应中,C是还原剂, CuO是氧化剂CuO是氧化剂(被氧化)(被还原)发生还原反应三、化学方程式 木炭粉跟氧化铜反应,生成了金属铜和二氧化碳。结 论实验结束时,为什么先移去盛有石灰水的烧杯后移去酒精灯??化学方程式: C+2CuO 2Cu+CO2↑思 考: 其他的一些副反应的化学方程式:
1、碳——一氧化碳;
2、一氧化碳还原氧化铜。 C+CO2 2CO
CO+CuO Cu+CO2实验六:步骤:
1、? 观察孔雀石颜 色:化学名:化学式:碱式碳酸铜Cu2(OH)2CO3是一种绿色的固体 2、? 把少量孔雀石粉末置于大试管内,用酒精灯加热约15分钟,用湿润的pH试纸贴在试管壁上观察颜色的变化,测定气体的水溶液pH大约是多少?现象:湿润的PH试纸变成浅红色,气体水溶液的PH约为6。3、孔雀石加热时有什么变化?绿色固体慢慢变成黑色固体。试管内壁出现小水滴,试管口冒出“白气”。结 论: 孔雀石加热时生成氧化铜、水和二氧化碳。1、? 化学反应方程式: Cu2(OH)2CO3 CuO+H2O+CO2↑ 4、待大试管的产物冷却后,如P57图2-13所示,通入氢气,过一会儿再给氧化铜加热。
现象: 1、黑色氧化铜变成光亮紫红色的金属铜。氢气还原氧化铜2、试管内壁出现小水滴,试管口冒出“白气“。结论:氢气和氧化铜在高温下反应生成金属铜和水。 H2+CuO Cu+ H2O1、盛放氧化铜的试管口为什么需略向下倾斜?防止反应生成的水倒流。 问题思考3、实验停止以后,为什么还要继续通入氢气,直到试管冷却为止?2、为什么要先通一会儿氢气,再加热.氧化铜?防止氢气与空气混合加热时试管内爆炸。防止灼热的铜被空气中的氧气重新氧化成氧化铜。由氧化铜制取铜,除氢气外,还可以用其他的什么方法吗?也可以用碳或一氧化碳 问题思考怎样把铁矿石炼成铁呢?思考铁矿石观察现象: 加热前:氧化铁粉末是一种
红棕色的固体。结论: 加热后:红棕色的固体变成黑色的粉末。澄清的石灰水变浑浊 CO和Fe2O3高温反应生成铁和二氧化碳。化学反应方程式:Fe2O3+3CO 2 Fe+ 3CO2 一氧化碳是一种有毒气体,剩余的CO应该如何处理?思考此实验应在通风橱内进行,也可将多余的CO导入火焰中燃烧。
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
