物质的转化规律[上学期]
图片预览









文档简介
(共47张PPT)
科学家常利用物质与物质之间的反应,制造出许多新的物质,使物质世界更加丰富多彩。那么,哪些种类的物质之间可以发生化学反应?物质之间的反应遵循怎样的规律呢?
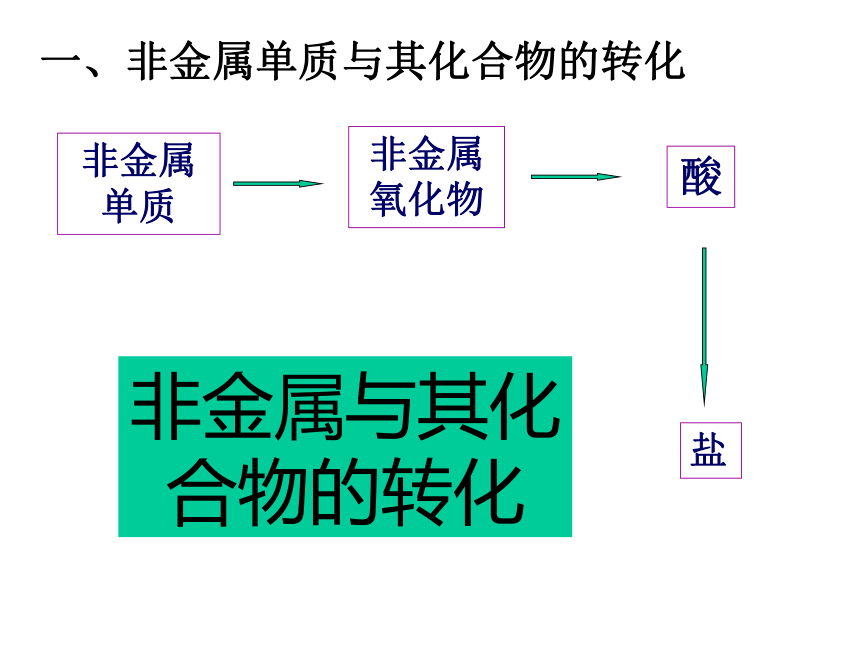
非金属单质
非金属氧化物
酸
盐
非金属与其化合物的转化
一、非金属单质与其化合物的转化
硫和氧气的反应
一、非金属单质与其化合物的转化
1、取一药匙硫黄,观察其外观: ____________________________。
2、将硫黄放到燃烧匙中,在酒精灯上点燃硫黄,观察现象:____________________。
3.把燃烧着的硫黄放进盛的氧气的集气瓶内,观察现象:______________________。
用化学方程式:
硫和氧气的反应
淡黄色粉末状固体
微弱的淡蓝色火焰
明亮的蓝紫色火焰
S + O2 ==== SO2
点燃
SO2+2NaOH=Na2SO3+H2O
SO2的处理:
你知道其他非金属在空气和氧气燃烧能转化成相应的氧化物?
SO2+H2O=H2SO3
SO3+H2O=H2SO4
某些非金属氧化物能转化成相应的酸
现象:通入二氧化碳的烧杯中,紫色石蕊试液变红色。
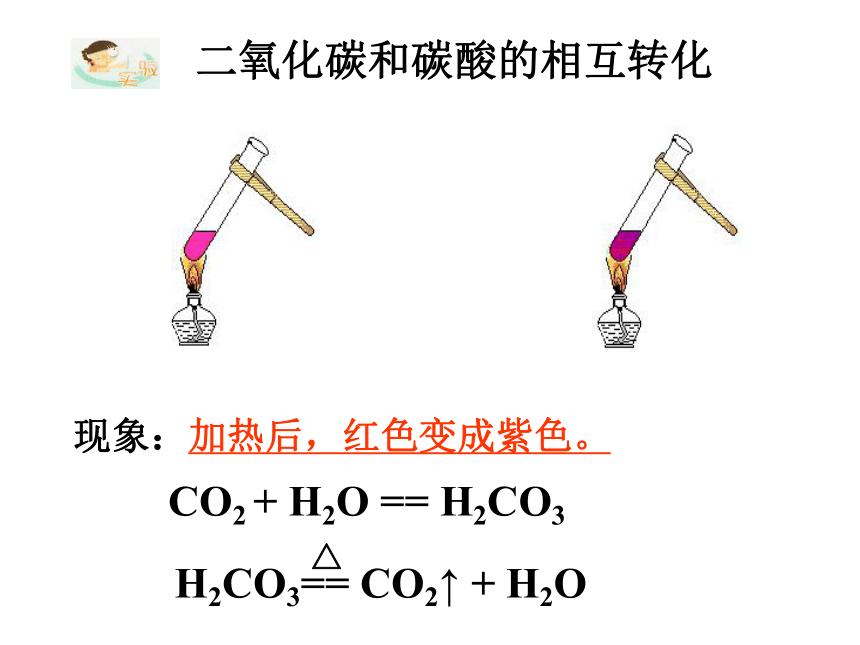
二氧化碳和碳酸的相互转化
现象:加热后,红色变成紫色。
二氧化碳和碳酸的相互转化
CO2 + H2O == H2CO3
H2CO3== CO2↑ + H2O
△
C→CO2→H2CO3
怎样用化学方程式表示下列物质的转化?
C+O2===CO2
CO2+H2O===H2CO3
点燃
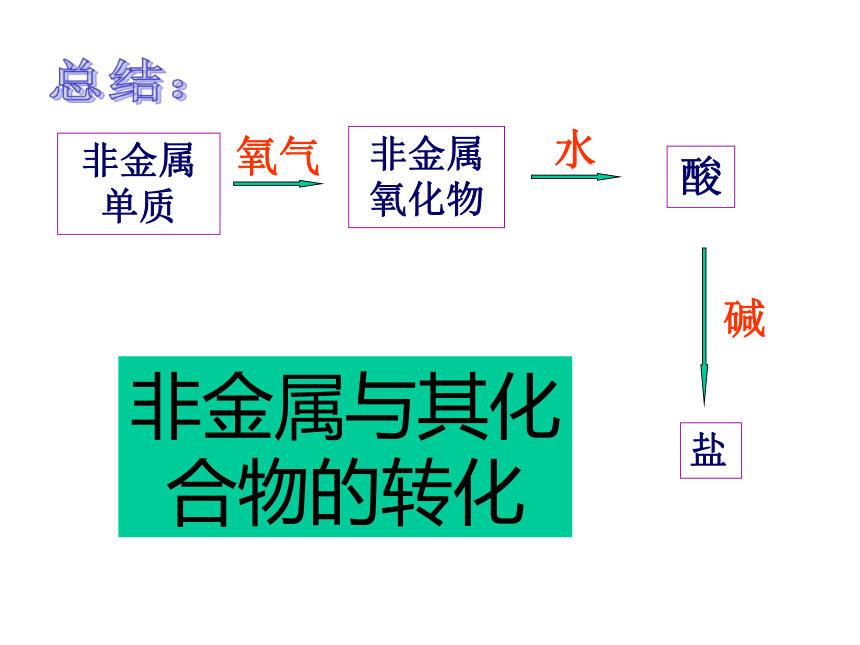
非金属单质
非金属氧化物
酸
盐
非金属与其化合物的转化
氧气
水
碱
返回
铁和硫的反应
二、金属单质与其化合物的转化
2、用磁铁接近混合物,你看到什么现象:___________________。
3、将混合物放进试管内,用酒精灯加热,有什么现象:__________________。
5、生成物外观如何?_____________。
磁铁能否吸引生成物?____________。
6、用化学方程式: ________________________。
铁粉被吸出
生成黑色固体
黑色固体
不能吸引
Fe + S ==== FeS
点燃
铁和硫的反应
跳跃
在蒸发皿中放1小块生石灰,加水,搅拌,有什么现象?
__________________________________。
用化学方程式表示:
变成白色粉末,放出大量热
CaO + H2O = Ca(OH)2
生石灰和水的反应
怎样用化学方程式表示下列物质的转化?
Ca→CaO→Ca(OH)2
1、金属单质 + 非金属单质→ 盐
2、金属氧化物 + 水→ 碱
(只有4种:CaO Na2O K2O BaO )
金属单质与其化合物的转化规律
方铅矿
赤铁矿
孔雀石
自然界中有现成的铁吗?
三、金属的冶炼
三、金属的冶炼
1、定义: 把金属从化合态变成游离态叫金属
的冶炼。
2、常用方法:碳等还原剂与金属氧化物在高
温下反应,碳能夺取金属氧化
物的氧,得到游离态的金属。
碳与氧化铜反应
返回
⑴加热一段时间后,发现试管壁出现:
_____________________________
⑵澄清石灰水变:____________,
说明_________________________________。
⑶木炭跟氧化铜反应,生成了____和__________。
⑷化学方程式:
C + 2CuO === 2 Cu + CO2 ↑
高温
红色物质
变浑浊
产生的气体是二氧化碳
铜
二氧化碳
碳与氧化铜反应
跳跃
碳与二氧化碳反应
C + CO2 ====
高温
2
CO
注意:这个反应要除尾气。用点燃的方法除尾气
一氧化碳冶炼金属
CO + CuO ==
Cu + CO2
△
孔雀石受热分解
返回
氢气还原氧化铜
1、观察孔雀石(主要成份为碱式碳酸铜)的颜色:____________________。
2、加热后,用湿润的PH试纸贴在试管壁上,观察颜色的变化:_______________。测定的PH值大约是多少?______________。
3、孔雀石在加热时有什么变化?___________。
4、化学方程式:
绿色固体变黑
浅红色
6
绿色固体
Cu2(OH)2CO3 === 2CuO + H2O + CO2↑
△
跳跃
5、如图,通入氢气后,过一会给氧化铜加热。试管中的变化:____________________。
试管口有什么生成?____________________。
6、反应完成后停止加热,继续通入氢气,直到试管冷却。化学方程式:
黑色变红色
水珠生成
H2 + CuO === Cu + H2O
△
氢气还原氧化铜
实验中的注意问题:
装置上:
1、试管口略向下倾斜。
2、导管要伸到试管底部。
操作上:
1、实验前,氢气先通,酒精灯后点。
2、实验完毕后,酒精灯先熄,氢气后撤。
(口诀:氢、灯、灯、氢)
1、由氧化铜制取铜,还可用其它什么方法?
⑴用稀硫酸和锌反应,生成氢气。再与氧化铜反应。
⑵用稀硫酸和氧化铜反应,生成硫酸铜,再用Zn置换。
2、为什么在氢气还原氧化铜实验开始时,要先通氢气后给氧化铜加热?
防止试管中氢气不纯,加热时发生爆炸。
3、铜在空气加热时容易氧化变成氧化铜,你在操作中要注意什么?
反应完成后停止加热,继续通入氢气,直到试管冷却
一氧化碳还原氧化铁
返回
一氧化碳还原氧化铁
观察发生的现象:
_______________
化学方程式:
(这个反应是炼铁的原理)
红棕色变黑色
注意:这个反应要除尾气。用点燃的方法除尾气
3CO +Fe2O3 === 2Fe + 3CO2
高温
跳跃
金属冶炼的原理:
与还原剂共热
C、H2、CO
金属氧化物
→
游离态金属
1、还原法
2、置换法
活泼金属
比盐中金属活泼
金属盐溶液
→
游离态金属
书写:碳、一氧化碳和氢气和金属氧化物的反应等重要的化学方程式。
---含氧化合物里的氧被夺取的反应,叫做还原反应,
---碳、氢气和一氧化碳等能从氧化铜、氧化铁中夺取氧的能力叫做还原性
---具有还原性的物质可做还原剂
H2 + CuO Cu + H2O
氧化反应 还原反应
还原剂(被氧化) 氧化剂(被还原)
从得失
氧的角度:
得 氧 失 氧
从化合价
升降角度:
升 价 降 价
从电子得
失的角度:
失电子 得电子
第三课时:
第3课时
四、有关纯度物质的计
算和化合物的相互转化
计算:有关纯度问题的计算
例题:100吨含Fe2O3的质量分数为85%的铁矿石中,可炼出含铁的质量分数为96%的生铁多少吨?
方法一:根据化学方程式计算
1、写出相关的化学方程式
2、在化学方程式下标上题目中已知质量的物质的相对分子质量和实际质量,同时标出需要球的物质的相对分子质量
3、列式
4、求解
解:
设:可炼出含铁的质量分数为96%的生铁的质量为M
Fe2O3 + 3CO
2Fe + 3CO2
高温
160
112
100t×85%
M×96%
160
112
100t×85%
M×96%
M=62t
答:可炼出生铁的质量为62t
方法二:根据元素质量守恒思想计算,
铁矿石中的铁的质量= 生铁中铁的质量
解:铁矿石中含Fe2O3的质量为:
100t× 85%=85t
铁的质量为:85t× ×100%
=85t × ×100%
=59.5t
炼出生铁的质量为:59.5t÷96%=62t
答:炼出的生铁的质量为62t.
2Fe
Fe2O3
112
160
习题1:用2000吨含Fe2O375%的铁矿石,最多可以炼出多少吨铁?
习题2:铁的氧化物2.32g,被CO还原后,只剩下1.68g铁,求铁的氧化物的化学式。
解析:反应后,固体质量减轻是由于铁的氧化物失氧所致。
解:设铁的氧化物化学式为FexOy,则:
FexOy + yCO xFe + yCO2 56x+16y 56x
2.32g 1.68g
( 56x+16y ) ∶56x = 2.32g∶1.68g
故:x∶y=3∶4
即所求铁的氧化物化学式为Fe3O4
五、化合物之间的相互转换:
例如:1熟石灰的制备及粉刷后的转化可用下式表示:
CaCO3 CaO Ca(OH)2 CaCO3
你能写出转化的化学反应方程式吗?
CaCO3 CaO+ CO2↑
CaO + H2O == Ca(OH)2
Ca(OH)2+ CO2 == CaCO3↓+ H2O
2、溶洞和钟乳石是怎样形成的呢?
石灰石主要成分是碳酸钙CaCO3
溶洞原理:
在自然界里,含有碳酸钙的石灰石岩层遇到溶有二氧化碳的水时,不溶水的碳酸钙就会变成可溶性的碳酸氢钙〖Ca(HCO3)2〗而被地下水带走,在长年累月的作用下会慢慢地形成溶洞。
CaCO3 +CO2+ H2O = Ca(HCO3)2
钟乳石的形成原理:
当含有碳酸氢钙的地下水从溶洞顶渗出,一滴一滴落下来时,由于水分蒸发,水里的碳酸氢钙又会变成碳酸钙而沉积下来,附在洞顶的石壁上,年深日久,洞顶就垂下乳状石条,这就石钟乳石。滴落地洞底的水也发生着同样的变化,形成了向上生长的石笋。钟乳石和石笋慢慢伸长连在一起成了石柱。
Ca(HCO3)2 CaCO3↓+H2O +CO2↑
实验:观察鸡蛋在稀盐酸溶液中的各种现象,并做科学的解释。
现象:1、鸡蛋下沉后慢慢地上浮。接近液面时,几乎是静止不动。
2、鸡蛋浸到容器底后鸡蛋壳表面就有大量气泡冒出,同时鸡蛋浮起来,不久,看到有白色泡沫物质从鸡蛋里跑出,白色泡沫越来越多,随着气流量流到了烧杯的外面。
3、最后,鸡蛋壳完全消失了,变成了一个由膜包着的无壳鸡蛋,而沉在容器的底部。
讨论:1、鸡蛋下沉后慢慢地上浮的原因可能是什么?
刚放入时鸡蛋重力大于浮力,下沉到底部;下沉时, CaCO3和HCI反应放出CO2,形成气泡附着在蛋壳表面,浮力将鸡蛋托起,鸡蛋受到的浮力大于重力,鸡蛋上浮。
接近液面, CO2气泡破裂,浮力减少,但液面下的蛋壳产生的大量气泡而产生的浮力远大于减少的浮力。这时浮力等于重力,所以接近液面,几乎静止不动。
2、接近液面时,几乎是静止不动。
3、最后,鸡蛋壳完全消失了,变成了一个由膜包着的无壳鸡蛋,而沉在容器的底部,为什么?
这时气泡消失,重力大于浮力而沉在容器的底部。
思考:从上面的实验你能懂得什么?
第4课时
五、利用物质转化的规
律寻找物质制取的途径
科学家常利用物质与物质之间的反应,制造出许多新的物质,使物质世界更加丰富多彩。那么,哪些种类的物质之间可以发生化学反应?物质之间的反应遵循怎样的规律呢?
非金属单质
非金属氧化物
酸
盐
非金属与其化合物的转化
一、非金属单质与其化合物的转化
硫和氧气的反应
一、非金属单质与其化合物的转化
1、取一药匙硫黄,观察其外观: ____________________________。
2、将硫黄放到燃烧匙中,在酒精灯上点燃硫黄,观察现象:____________________。
3.把燃烧着的硫黄放进盛的氧气的集气瓶内,观察现象:______________________。
用化学方程式:
硫和氧气的反应
淡黄色粉末状固体
微弱的淡蓝色火焰
明亮的蓝紫色火焰
S + O2 ==== SO2
点燃
SO2+2NaOH=Na2SO3+H2O
SO2的处理:
你知道其他非金属在空气和氧气燃烧能转化成相应的氧化物?
SO2+H2O=H2SO3
SO3+H2O=H2SO4
某些非金属氧化物能转化成相应的酸
现象:通入二氧化碳的烧杯中,紫色石蕊试液变红色。
二氧化碳和碳酸的相互转化
现象:加热后,红色变成紫色。
二氧化碳和碳酸的相互转化
CO2 + H2O == H2CO3
H2CO3== CO2↑ + H2O
△
C→CO2→H2CO3
怎样用化学方程式表示下列物质的转化?
C+O2===CO2
CO2+H2O===H2CO3
点燃
非金属单质
非金属氧化物
酸
盐
非金属与其化合物的转化
氧气
水
碱
返回
铁和硫的反应
二、金属单质与其化合物的转化
2、用磁铁接近混合物,你看到什么现象:___________________。
3、将混合物放进试管内,用酒精灯加热,有什么现象:__________________。
5、生成物外观如何?_____________。
磁铁能否吸引生成物?____________。
6、用化学方程式: ________________________。
铁粉被吸出
生成黑色固体
黑色固体
不能吸引
Fe + S ==== FeS
点燃
铁和硫的反应
跳跃
在蒸发皿中放1小块生石灰,加水,搅拌,有什么现象?
__________________________________。
用化学方程式表示:
变成白色粉末,放出大量热
CaO + H2O = Ca(OH)2
生石灰和水的反应
怎样用化学方程式表示下列物质的转化?
Ca→CaO→Ca(OH)2
1、金属单质 + 非金属单质→ 盐
2、金属氧化物 + 水→ 碱
(只有4种:CaO Na2O K2O BaO )
金属单质与其化合物的转化规律
方铅矿
赤铁矿
孔雀石
自然界中有现成的铁吗?
三、金属的冶炼
三、金属的冶炼
1、定义: 把金属从化合态变成游离态叫金属
的冶炼。
2、常用方法:碳等还原剂与金属氧化物在高
温下反应,碳能夺取金属氧化
物的氧,得到游离态的金属。
碳与氧化铜反应
返回
⑴加热一段时间后,发现试管壁出现:
_____________________________
⑵澄清石灰水变:____________,
说明_________________________________。
⑶木炭跟氧化铜反应,生成了____和__________。
⑷化学方程式:
C + 2CuO === 2 Cu + CO2 ↑
高温
红色物质
变浑浊
产生的气体是二氧化碳
铜
二氧化碳
碳与氧化铜反应
跳跃
碳与二氧化碳反应
C + CO2 ====
高温
2
CO
注意:这个反应要除尾气。用点燃的方法除尾气
一氧化碳冶炼金属
CO + CuO ==
Cu + CO2
△
孔雀石受热分解
返回
氢气还原氧化铜
1、观察孔雀石(主要成份为碱式碳酸铜)的颜色:____________________。
2、加热后,用湿润的PH试纸贴在试管壁上,观察颜色的变化:_______________。测定的PH值大约是多少?______________。
3、孔雀石在加热时有什么变化?___________。
4、化学方程式:
绿色固体变黑
浅红色
6
绿色固体
Cu2(OH)2CO3 === 2CuO + H2O + CO2↑
△
跳跃
5、如图,通入氢气后,过一会给氧化铜加热。试管中的变化:____________________。
试管口有什么生成?____________________。
6、反应完成后停止加热,继续通入氢气,直到试管冷却。化学方程式:
黑色变红色
水珠生成
H2 + CuO === Cu + H2O
△
氢气还原氧化铜
实验中的注意问题:
装置上:
1、试管口略向下倾斜。
2、导管要伸到试管底部。
操作上:
1、实验前,氢气先通,酒精灯后点。
2、实验完毕后,酒精灯先熄,氢气后撤。
(口诀:氢、灯、灯、氢)
1、由氧化铜制取铜,还可用其它什么方法?
⑴用稀硫酸和锌反应,生成氢气。再与氧化铜反应。
⑵用稀硫酸和氧化铜反应,生成硫酸铜,再用Zn置换。
2、为什么在氢气还原氧化铜实验开始时,要先通氢气后给氧化铜加热?
防止试管中氢气不纯,加热时发生爆炸。
3、铜在空气加热时容易氧化变成氧化铜,你在操作中要注意什么?
反应完成后停止加热,继续通入氢气,直到试管冷却
一氧化碳还原氧化铁
返回
一氧化碳还原氧化铁
观察发生的现象:
_______________
化学方程式:
(这个反应是炼铁的原理)
红棕色变黑色
注意:这个反应要除尾气。用点燃的方法除尾气
3CO +Fe2O3 === 2Fe + 3CO2
高温
跳跃
金属冶炼的原理:
与还原剂共热
C、H2、CO
金属氧化物
→
游离态金属
1、还原法
2、置换法
活泼金属
比盐中金属活泼
金属盐溶液
→
游离态金属
书写:碳、一氧化碳和氢气和金属氧化物的反应等重要的化学方程式。
---含氧化合物里的氧被夺取的反应,叫做还原反应,
---碳、氢气和一氧化碳等能从氧化铜、氧化铁中夺取氧的能力叫做还原性
---具有还原性的物质可做还原剂
H2 + CuO Cu + H2O
氧化反应 还原反应
还原剂(被氧化) 氧化剂(被还原)
从得失
氧的角度:
得 氧 失 氧
从化合价
升降角度:
升 价 降 价
从电子得
失的角度:
失电子 得电子
第三课时:
第3课时
四、有关纯度物质的计
算和化合物的相互转化
计算:有关纯度问题的计算
例题:100吨含Fe2O3的质量分数为85%的铁矿石中,可炼出含铁的质量分数为96%的生铁多少吨?
方法一:根据化学方程式计算
1、写出相关的化学方程式
2、在化学方程式下标上题目中已知质量的物质的相对分子质量和实际质量,同时标出需要球的物质的相对分子质量
3、列式
4、求解
解:
设:可炼出含铁的质量分数为96%的生铁的质量为M
Fe2O3 + 3CO
2Fe + 3CO2
高温
160
112
100t×85%
M×96%
160
112
100t×85%
M×96%
M=62t
答:可炼出生铁的质量为62t
方法二:根据元素质量守恒思想计算,
铁矿石中的铁的质量= 生铁中铁的质量
解:铁矿石中含Fe2O3的质量为:
100t× 85%=85t
铁的质量为:85t× ×100%
=85t × ×100%
=59.5t
炼出生铁的质量为:59.5t÷96%=62t
答:炼出的生铁的质量为62t.
2Fe
Fe2O3
112
160
习题1:用2000吨含Fe2O375%的铁矿石,最多可以炼出多少吨铁?
习题2:铁的氧化物2.32g,被CO还原后,只剩下1.68g铁,求铁的氧化物的化学式。
解析:反应后,固体质量减轻是由于铁的氧化物失氧所致。
解:设铁的氧化物化学式为FexOy,则:
FexOy + yCO xFe + yCO2 56x+16y 56x
2.32g 1.68g
( 56x+16y ) ∶56x = 2.32g∶1.68g
故:x∶y=3∶4
即所求铁的氧化物化学式为Fe3O4
五、化合物之间的相互转换:
例如:1熟石灰的制备及粉刷后的转化可用下式表示:
CaCO3 CaO Ca(OH)2 CaCO3
你能写出转化的化学反应方程式吗?
CaCO3 CaO+ CO2↑
CaO + H2O == Ca(OH)2
Ca(OH)2+ CO2 == CaCO3↓+ H2O
2、溶洞和钟乳石是怎样形成的呢?
石灰石主要成分是碳酸钙CaCO3
溶洞原理:
在自然界里,含有碳酸钙的石灰石岩层遇到溶有二氧化碳的水时,不溶水的碳酸钙就会变成可溶性的碳酸氢钙〖Ca(HCO3)2〗而被地下水带走,在长年累月的作用下会慢慢地形成溶洞。
CaCO3 +CO2+ H2O = Ca(HCO3)2
钟乳石的形成原理:
当含有碳酸氢钙的地下水从溶洞顶渗出,一滴一滴落下来时,由于水分蒸发,水里的碳酸氢钙又会变成碳酸钙而沉积下来,附在洞顶的石壁上,年深日久,洞顶就垂下乳状石条,这就石钟乳石。滴落地洞底的水也发生着同样的变化,形成了向上生长的石笋。钟乳石和石笋慢慢伸长连在一起成了石柱。
Ca(HCO3)2 CaCO3↓+H2O +CO2↑
实验:观察鸡蛋在稀盐酸溶液中的各种现象,并做科学的解释。
现象:1、鸡蛋下沉后慢慢地上浮。接近液面时,几乎是静止不动。
2、鸡蛋浸到容器底后鸡蛋壳表面就有大量气泡冒出,同时鸡蛋浮起来,不久,看到有白色泡沫物质从鸡蛋里跑出,白色泡沫越来越多,随着气流量流到了烧杯的外面。
3、最后,鸡蛋壳完全消失了,变成了一个由膜包着的无壳鸡蛋,而沉在容器的底部。
讨论:1、鸡蛋下沉后慢慢地上浮的原因可能是什么?
刚放入时鸡蛋重力大于浮力,下沉到底部;下沉时, CaCO3和HCI反应放出CO2,形成气泡附着在蛋壳表面,浮力将鸡蛋托起,鸡蛋受到的浮力大于重力,鸡蛋上浮。
接近液面, CO2气泡破裂,浮力减少,但液面下的蛋壳产生的大量气泡而产生的浮力远大于减少的浮力。这时浮力等于重力,所以接近液面,几乎静止不动。
2、接近液面时,几乎是静止不动。
3、最后,鸡蛋壳完全消失了,变成了一个由膜包着的无壳鸡蛋,而沉在容器的底部,为什么?
这时气泡消失,重力大于浮力而沉在容器的底部。
思考:从上面的实验你能懂得什么?
第4课时
五、利用物质转化的规
律寻找物质制取的途径
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
