物质之间的相互转化[上学期]
图片预览









文档简介
课件35张PPT。第二节 物质之间的相互转换用化学方程式表示以下变化: S + O2 --------
P + O2 --------
C + O2 --------
H2 + O2 -------
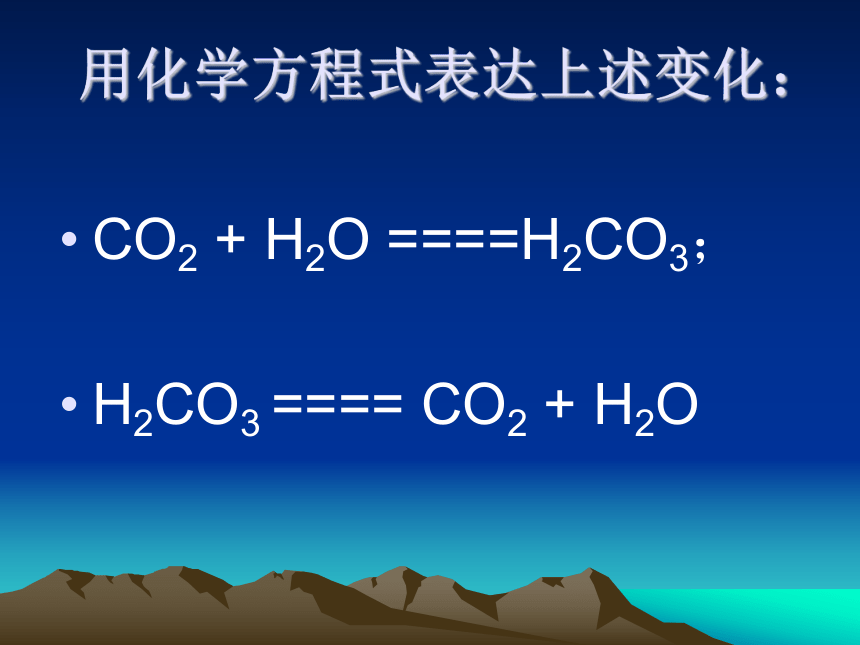
小结反应规律:1.非金属+氧气 非金属氧化物一、非金属单质与其化合物的转化实验(二) 蒸馏水的变化取2杯蒸馏水,向其中1杯蒸馏水中吹气或通CO2,然后,分别向2只烧杯中滴加几滴石蕊试液,比较2只烧杯中液体出现的现象并加以说明。用化学方程式表达上述变化: CO2 + H2O ====H2CO3;
H2CO3 ==== CO2 + H2O
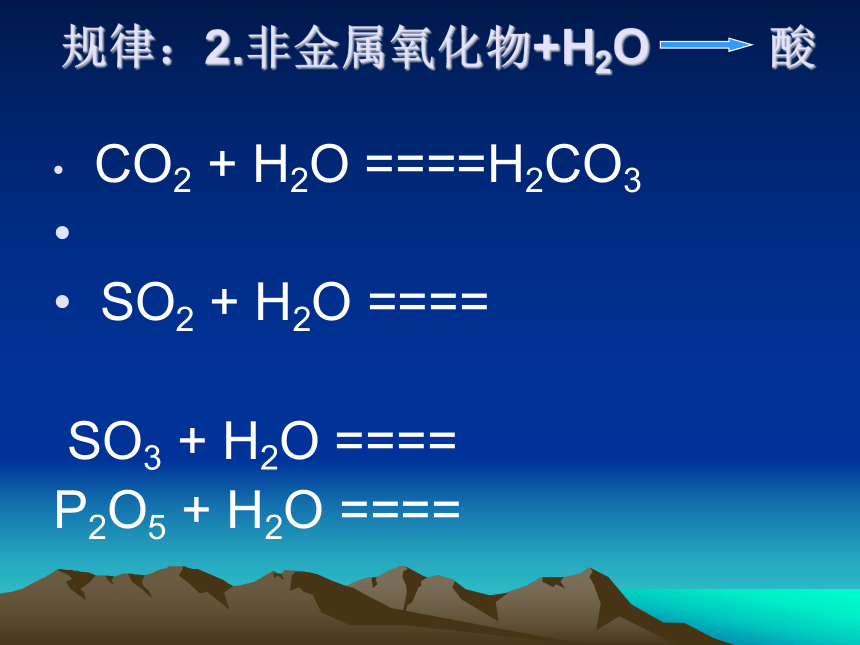
规律:2.非金属氧化物+H2O 酸 CO2 + H2O ====H2CO3
SO2 + H2O ====
SO3 + H2O ====
P2O5 + H2O ==== 二、金属单质与其化合物的转化实验(三): Fe和S的反应(一)游离态金属 化合态金属Fe + S =======FeS完成: Na + Cl2=======
Fe + Cl2 =======△点燃规律:1.金属和非金属(不包括 氧气)反应生成盐。
1.金属+非金属(除氧气) 盐规律:2.金属+氧气 金属氧化物回忆: Fe +O2 ====
Mg +O2 ====
Al + O2 ====
Cu + O2 ====
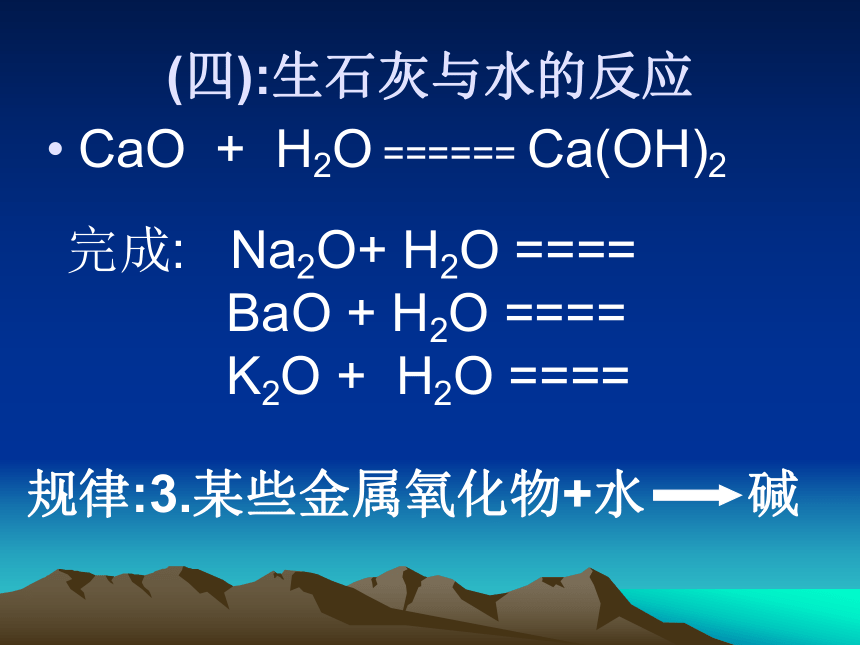
Na + O2 ==== (四):生石灰与水的反应CaO + H2O ====== Ca(OH)2完成: Na2O+ H2O ====
BaO + H2O ====
K2O + H2O ====规律:3.某些金属氧化物+水 碱 讨论:用化学方程式表示下列转化: Ca CaO Ca(OH)2Ca + O2 ====== CaO
CaO + H2O ====== Ca(OH)2 C + 2CuO ==== 2Cu + CO2↑完成: C + Fe2O3 ====
C + ZnO ====高温△规律:
炭+金属氧化物 金属+二氧化碳写出变化的反应式:Cu2(OH)2CO3 ========
2CuO+ CO2↑+H2O 加热 化 合 态 金 属
游 离 态 金 属1.氢气2. 炭3.一氧化碳 思考:要将赤铁矿(主要成分为 Fe2O3)冶炼成生铁(主要成分为铁),你有哪些方法?哪种方法制得的铁最纯?请写出化学方程式。3C + 2Fe2O3 ====4Fe +3CO2↑
3CO + Fe2O3 ====2Fe +3CO2↑
3H2 + Fe2O3 ====2Fe +3H2O↑高温高温高温1.单质.化合物之间的相互转化写出下列转化的化学方程式,并注各物质的类别。
Ca CaO Ca(OH)2 CaCO3 Ca CaO Ca(OH)2 CaCO3
金属 金属氧化物 碱 盐2Ca + O2 === 2CaO CaO + H2O===Ca(OH)2Ca(OH)2+ CO2===CaCO3 ↓+ H2O写出下列转化的化学方程式,并注各物质的类别。
C CO2 H2CO3 CaCO3 C CO2 H2CO3 CaCO3
非金属 非金属氧化物 酸 盐C + O2 ===CO2CO2 + H2O ===H2CO3H2CO3+Ca(OH)2==CaCO3↓ +H2O点燃 指出酸的共性,以硫酸为例各写出一条化学方程式。1. 酸 + 指示剂 2. 酸 + 活泼金属 盐 + 氢气Fe + H2SO4 === FeSO4 + H2↑3. 酸 + 金属氧化物 盐 + 水 H2SO4 + CuO === CuSO4 + H2O 4. 酸 + 碱 盐 + 水H2SO4+ 2NaOH==Na2SO4+ 2H2O5. 酸 + 盐 新酸 + 新盐H2SO4+ BaCl2==BaSO4 ↓+ 2HCl指出碱的共性,以氢氧化钠为例各写出一条化学方程式。1.碱 + 指示剂2.碱 + 非金属 盐 + 水2NaOH + SO2 == Na2SO3 + H2O3.碱 + 酸 盐 + 水Ba(OH)2+H2SO4==BaSO4↓+ H2O4.碱 + 盐 新碱 + 新盐2NaOH + CuSO4=Cu(OH)2↓+Na2SO4 补充说出金属的性质,并用一条化学方程式表示。1.金属 + 非金属(除氧气) 盐 Fe + S =======FeS2.金属 + 盐 新金属 + 新盐Fe + CuSO4 === FeSO4 + Cu议一议1、熟石灰是如何制取的?粉刷利用的石灰浆日子久后转变成了什么物质?你可用家中的什么物质去鉴定。熟石灰的制备及粉刷后的转化可用下式表示:
CaCO3 CaO Ca(OH)2 CaCO3
制备 粉刷时转化(鉴定用醋酸)2、研究金华的双龙洞和兰溪的地下长河及洞内的钟乳石、石笋和石柱是如何形成的?石灰岩溶洞的形成与石笋、石柱、钟乳石的形成:
CaCO3 + H2O +CO2 ===Ca(HCO3)2
Ca(HCO3)2==== CaCO3 + H2O +CO2 盐盐+水酸+盐碱+盐盐+盐金
属
+
盐盐+氢气化合物的相互转化关系1、两条纵线A B2、四条横线c3、四条交叉线D4、两条弯线幻灯片 8应用之一:查找各类物质的主要的化学性质。
如:1、酸
2、碱
3、盐
4、氧化物四条横线:
1、金属 + 非金属 ===== 盐
2、金属氧化物 + 非金属氧化物 =====盐
3、酸 + 碱 === 盐 + 水
4、盐 + 盐 === 盐 + 盐 2Na +Cl2==2NaClCaO +SiO2 ====CaSiO3H2SO4 +2NaOH ===Na2SO4 +2H2OAgNO3 + NaCl ===AgCl +NaNO3四条交叉线:
金属氧化物 + 酸 === 盐 + 水
非金属氧化物 + 碱 ==== 盐 + 水
酸 + 盐 === 新酸 + 新盐
碱 + 盐 === 新碱 + 新盐CuO + H2SO4===CuSO4 + H2OCO2 +2 NaOH ===Na2CO3 + H2O2NaOH + CuSO4 ===Cu(OH)2 + Na2SO4HCl+ AgNO3===HNO3 + AgCl两条弯线:
金属 + 盐 ===== 金属 + 盐
金属 + 酸 ===== 盐 + 氢气Fe + CuSO4 ====Cu + FeSO4Zn + H2SO4 ====ZnSO4 + H23、下列物质不能由氧化物直接与水反应制取的是( )
A、H2CO3 B、H2SO4 C、Fe(OH)3 D、NaOH
4、下列盐不能用金属与稀酸直接反应制得的是( )
A、MgCl2 B、Fe2(SO4)3 C、 FeCl2 D、Al2(SO4)3
5、下列各组物质中,不能发生反应的是( )
A、盐酸与碳酸钠 B、硝酸银与氯化钠溶液
C、硝酸钾与氯化钠 D、氢氧化钾与硝酸
6、下列各组物质相互混合,加入足量的稀盐酸,最终还有白色 沉 淀产生的是( )
A、氢氧化钠和硫酸铜 B、硝酸钡与硫酸钠
C、碳酸钠与氢氧化钙 D、氯化铁与氢氧化钡
CBCB物质鉴别方法:
1)用化学方法1 滴加石蕊试液 1试剂变红
2 加Zn、Fe等金属 2产生可燃性气体滴加酚酞试液 试液变红滴加AgNO3、HNO3 白色沉淀滴加BaCl2、HNO3 白色沉淀滴加盐酸产生气体通入Ca(OH)2 白色沉淀火焰上方罩干燥小烧杯 有水珠出现点燃、产生的气体与石灰水反应 白色沉淀澄清石灰水 变浑浊带火星木条 复燃 白色无水硫酸铜粉末 变蓝色(2)用物理方法:
⑴蓝 色 溶 液——
⑵黄 色 溶 液——
⑶蓝色不溶物——
⑷红褐色不溶物——
⑸白色不溶物——
⑹打开盛液体的瓶盖出现白雾的是——
⑺片状白色固体露置在空气中潮解的是——
⑻黑色粉末——
⑼红色粉末——
⑽红色光亮的金属——
⑾溶于水产生大量热——BaSO4、AgCl、BaCO3、CaCO3、Mg(OH)2NaOH浓H2SO4、CaO等CuSO4FeCl3Cu(OH)2Fe(OH)3浓盐酸CuO、MnO2、CFe2O3Cu再见
P + O2 --------
C + O2 --------
H2 + O2 -------
小结反应规律:1.非金属+氧气 非金属氧化物一、非金属单质与其化合物的转化实验(二) 蒸馏水的变化取2杯蒸馏水,向其中1杯蒸馏水中吹气或通CO2,然后,分别向2只烧杯中滴加几滴石蕊试液,比较2只烧杯中液体出现的现象并加以说明。用化学方程式表达上述变化: CO2 + H2O ====H2CO3;
H2CO3 ==== CO2 + H2O
规律:2.非金属氧化物+H2O 酸 CO2 + H2O ====H2CO3
SO2 + H2O ====
SO3 + H2O ====
P2O5 + H2O ==== 二、金属单质与其化合物的转化实验(三): Fe和S的反应(一)游离态金属 化合态金属Fe + S =======FeS完成: Na + Cl2=======
Fe + Cl2 =======△点燃规律:1.金属和非金属(不包括 氧气)反应生成盐。
1.金属+非金属(除氧气) 盐规律:2.金属+氧气 金属氧化物回忆: Fe +O2 ====
Mg +O2 ====
Al + O2 ====
Cu + O2 ====
Na + O2 ==== (四):生石灰与水的反应CaO + H2O ====== Ca(OH)2完成: Na2O+ H2O ====
BaO + H2O ====
K2O + H2O ====规律:3.某些金属氧化物+水 碱 讨论:用化学方程式表示下列转化: Ca CaO Ca(OH)2Ca + O2 ====== CaO
CaO + H2O ====== Ca(OH)2 C + 2CuO ==== 2Cu + CO2↑完成: C + Fe2O3 ====
C + ZnO ====高温△规律:
炭+金属氧化物 金属+二氧化碳写出变化的反应式:Cu2(OH)2CO3 ========
2CuO+ CO2↑+H2O 加热 化 合 态 金 属
游 离 态 金 属1.氢气2. 炭3.一氧化碳 思考:要将赤铁矿(主要成分为 Fe2O3)冶炼成生铁(主要成分为铁),你有哪些方法?哪种方法制得的铁最纯?请写出化学方程式。3C + 2Fe2O3 ====4Fe +3CO2↑
3CO + Fe2O3 ====2Fe +3CO2↑
3H2 + Fe2O3 ====2Fe +3H2O↑高温高温高温1.单质.化合物之间的相互转化写出下列转化的化学方程式,并注各物质的类别。
Ca CaO Ca(OH)2 CaCO3 Ca CaO Ca(OH)2 CaCO3
金属 金属氧化物 碱 盐2Ca + O2 === 2CaO CaO + H2O===Ca(OH)2Ca(OH)2+ CO2===CaCO3 ↓+ H2O写出下列转化的化学方程式,并注各物质的类别。
C CO2 H2CO3 CaCO3 C CO2 H2CO3 CaCO3
非金属 非金属氧化物 酸 盐C + O2 ===CO2CO2 + H2O ===H2CO3H2CO3+Ca(OH)2==CaCO3↓ +H2O点燃 指出酸的共性,以硫酸为例各写出一条化学方程式。1. 酸 + 指示剂 2. 酸 + 活泼金属 盐 + 氢气Fe + H2SO4 === FeSO4 + H2↑3. 酸 + 金属氧化物 盐 + 水 H2SO4 + CuO === CuSO4 + H2O 4. 酸 + 碱 盐 + 水H2SO4+ 2NaOH==Na2SO4+ 2H2O5. 酸 + 盐 新酸 + 新盐H2SO4+ BaCl2==BaSO4 ↓+ 2HCl指出碱的共性,以氢氧化钠为例各写出一条化学方程式。1.碱 + 指示剂2.碱 + 非金属 盐 + 水2NaOH + SO2 == Na2SO3 + H2O3.碱 + 酸 盐 + 水Ba(OH)2+H2SO4==BaSO4↓+ H2O4.碱 + 盐 新碱 + 新盐2NaOH + CuSO4=Cu(OH)2↓+Na2SO4 补充说出金属的性质,并用一条化学方程式表示。1.金属 + 非金属(除氧气) 盐 Fe + S =======FeS2.金属 + 盐 新金属 + 新盐Fe + CuSO4 === FeSO4 + Cu议一议1、熟石灰是如何制取的?粉刷利用的石灰浆日子久后转变成了什么物质?你可用家中的什么物质去鉴定。熟石灰的制备及粉刷后的转化可用下式表示:
CaCO3 CaO Ca(OH)2 CaCO3
制备 粉刷时转化(鉴定用醋酸)2、研究金华的双龙洞和兰溪的地下长河及洞内的钟乳石、石笋和石柱是如何形成的?石灰岩溶洞的形成与石笋、石柱、钟乳石的形成:
CaCO3 + H2O +CO2 ===Ca(HCO3)2
Ca(HCO3)2==== CaCO3 + H2O +CO2 盐盐+水酸+盐碱+盐盐+盐金
属
+
盐盐+氢气化合物的相互转化关系1、两条纵线A B2、四条横线c3、四条交叉线D4、两条弯线幻灯片 8应用之一:查找各类物质的主要的化学性质。
如:1、酸
2、碱
3、盐
4、氧化物四条横线:
1、金属 + 非金属 ===== 盐
2、金属氧化物 + 非金属氧化物 =====盐
3、酸 + 碱 === 盐 + 水
4、盐 + 盐 === 盐 + 盐 2Na +Cl2==2NaClCaO +SiO2 ====CaSiO3H2SO4 +2NaOH ===Na2SO4 +2H2OAgNO3 + NaCl ===AgCl +NaNO3四条交叉线:
金属氧化物 + 酸 === 盐 + 水
非金属氧化物 + 碱 ==== 盐 + 水
酸 + 盐 === 新酸 + 新盐
碱 + 盐 === 新碱 + 新盐CuO + H2SO4===CuSO4 + H2OCO2 +2 NaOH ===Na2CO3 + H2O2NaOH + CuSO4 ===Cu(OH)2 + Na2SO4HCl+ AgNO3===HNO3 + AgCl两条弯线:
金属 + 盐 ===== 金属 + 盐
金属 + 酸 ===== 盐 + 氢气Fe + CuSO4 ====Cu + FeSO4Zn + H2SO4 ====ZnSO4 + H23、下列物质不能由氧化物直接与水反应制取的是( )
A、H2CO3 B、H2SO4 C、Fe(OH)3 D、NaOH
4、下列盐不能用金属与稀酸直接反应制得的是( )
A、MgCl2 B、Fe2(SO4)3 C、 FeCl2 D、Al2(SO4)3
5、下列各组物质中,不能发生反应的是( )
A、盐酸与碳酸钠 B、硝酸银与氯化钠溶液
C、硝酸钾与氯化钠 D、氢氧化钾与硝酸
6、下列各组物质相互混合,加入足量的稀盐酸,最终还有白色 沉 淀产生的是( )
A、氢氧化钠和硫酸铜 B、硝酸钡与硫酸钠
C、碳酸钠与氢氧化钙 D、氯化铁与氢氧化钡
CBCB物质鉴别方法:
1)用化学方法1 滴加石蕊试液 1试剂变红
2 加Zn、Fe等金属 2产生可燃性气体滴加酚酞试液 试液变红滴加AgNO3、HNO3 白色沉淀滴加BaCl2、HNO3 白色沉淀滴加盐酸产生气体通入Ca(OH)2 白色沉淀火焰上方罩干燥小烧杯 有水珠出现点燃、产生的气体与石灰水反应 白色沉淀澄清石灰水 变浑浊带火星木条 复燃 白色无水硫酸铜粉末 变蓝色(2)用物理方法:
⑴蓝 色 溶 液——
⑵黄 色 溶 液——
⑶蓝色不溶物——
⑷红褐色不溶物——
⑸白色不溶物——
⑹打开盛液体的瓶盖出现白雾的是——
⑺片状白色固体露置在空气中潮解的是——
⑻黑色粉末——
⑼红色粉末——
⑽红色光亮的金属——
⑾溶于水产生大量热——BaSO4、AgCl、BaCO3、CaCO3、Mg(OH)2NaOH浓H2SO4、CaO等CuSO4FeCl3Cu(OH)2Fe(OH)3浓盐酸CuO、MnO2、CFe2O3Cu再见
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
