课题 2 金属的化学性质课件(共26张PPT)
文档属性
| 名称 | 课题 2 金属的化学性质课件(共26张PPT) |  | |
| 格式 | zip | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-01-22 16:32:20 | ||
图片预览








文档简介
课件26张PPT。金属的化学性质【学习目标】
1.学会镁、铝、铁、铜等常见金属与氧 气、与酸溶液的反应。
2.在探究中理解金属活动性顺序,并作简单的应用。
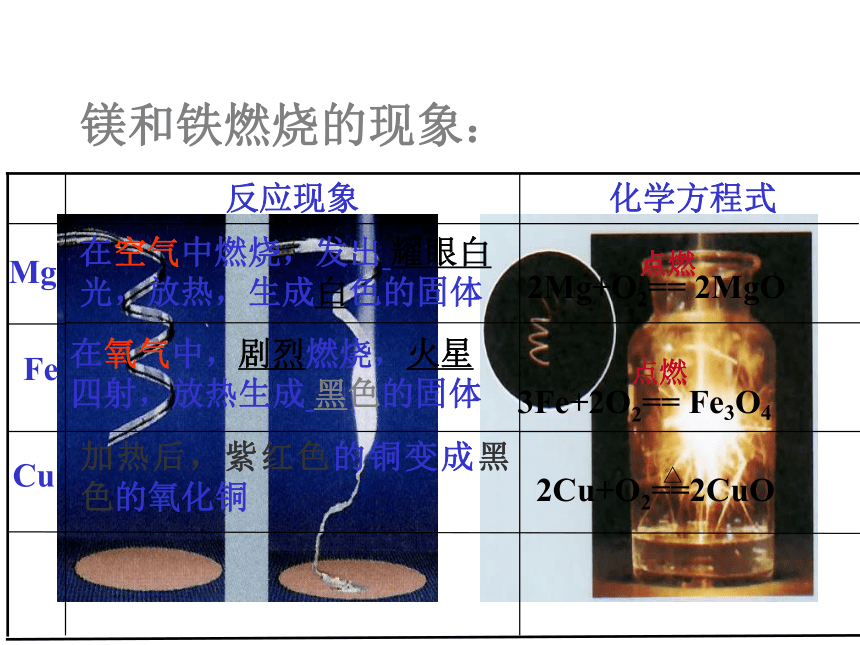
3.会将所学化学知识用于解决生活的实际问题。你都知道哪些金属可以和氧气反应?反应时伴随怎样的现象?化学方程式如何书写?举例说明...... 金属与氧气的反应回顾镁和铁燃烧的现象:△探究金属铝与氧气的反应1.不同的金属与氧气的反应条件 .2. 反应条件的不同,说明金属的活泼程度 .(该性质称作 )不同不同“金属活动性”实验结论一:镁、铝等在常温下就能与氧气反应;
铁、铜等在高温下能与氧气反应;
金即使在高温时也不与氧气反应。镁、铝较活泼,铁、铜次之,金最不活泼。 铝在空气中与氧气反应,其表面生成一层致密的氧化铝(Al2O3)薄膜,阻止铝进一步氧化,因此,铝具有很好的抗腐蚀性能。1、铝的活动性比铁强,可是通常看见铁生锈而没有看到铝生锈,为什么?应不要把铝制品表面的氧化物保护膜清洗掉。2、在清洗铝制品时应注意些什么?我会应用: 实验探究二:金属与酸的反应思考:
(1)是否所有金属能与稀酸(稀盐酸或稀硫酸)反应?
(2)反应剧烈程度有无差异? Mg Zn Fe Cu 实验步骤及注意事项:
1、向4支试管中分别装入Cu、Fe、Zn、Mg金属
(药品用量:金属铜和镁用镊子各取一片;锌粒用药匙取3—5粒; 铁钉一个,注意铁钉圆头朝下滑落试管)
2、向上述试管中各注入约2ml
稀盐酸 或稀硫酸
(注意做到口挨口倾倒液体药
品,防止洒落)
3、观察、在学案上记录实验现象。讨论交流:从你的探究中,你的发现或收获?金属稀酸1、__________能与稀盐酸或稀硫酸反应,放出气体,而___却不能。
2、铁、镁、锌与稀盐酸或稀硫酸反应时剧烈程度不同。___反应最剧烈其次是____,然后是____。能否与酸反应,反应剧烈程度都与金属活动性强弱有关。实验结论二:Mg、Zn、FeCu镁锌铁趣味小实验空中点鞭炮情景再现排在越 面的元素,金属活泼性越强;
排在 之前的金属是较活泼的金属,能跟稀
硫酸一类的稀酸反应,生成氢气;
金属活动性顺序表所含信息:前氢单质化合物化合物单质小结:
这种由一种单质与一种化合物反应,生成了另一种单质和另一种化合物的反应叫做置换反应。讨论: 对于以上的反应,从反应物和生成物的类别角度分析,有何特点?
Mg + 2HCl = MgCl2 + H2 ↑
Zn + 2HCl = ZnCl2 + H2 ↑
Fe + 2HCl = FeCl2 + H2 ↑A + BC = AC + B一、金属的化学性质:
1、与氧气反应
(金属越活泼,反应越容易,越剧烈)
2、氢前金属与稀盐酸(稀硫酸)反应
(金属越活泼,反应越容易,越剧烈)
二、金属活动顺序及其应用
(判断金属能否在酸溶液中发生置换反应) 学完本课题我学到了为了谋取暴利,市场上假冒的商品随处可见。不法商常常把黄铜(铜锌合金)饰品冒充黄金以高价出卖,很多顾客上当受骗。1、下列反应中,有单质出现,但不属于置换反应的是( )A.Cu+2AgNO3=Cu(NO3)2+2Ag
B.2Al+3H2SO4=A12(SO4)3+3H2↑
C.2Mg+CO2 2MgO+C
D.2Na2O2+2CO2=2Na2CO3+O2D达标测评(基础题)2.社会上一些不法分子以铜锌合金(金黄色,俗称黄铜)假冒黄金进行诈骗活动。为鉴别黄铜和黄金,以下方法可行且简便的是( )(不定项)
A. 观察颜色 B. 在空气中加热
C. 加稀硫酸 D. 磁铁吸引 B C3.下列物质放入稀硫酸中,不能反应的是 ( ) A.A1 B.Cu C.Fe D.Zn
4.下列化学方程式正确的是( )
A.4Fe+3O2=2Fe2O3
B.Fe+H2SO4=FeSO4+H2↑
C.2Fe+6HCl=2FeCl3+H2↑
D.Fe+3CuSO4=Fe2(SO4)3+3CuBB5. 出土的古文物中,金器保存完好,铜器表面有锈迹,而铁器锈迹斑斑。这表明金.铜.铁的金属活动性从强到弱的顺序是( )
A.金.铜.铁 B.铁.金.铜
C.铁.铜.金 D.铜.金.铁C 能力提高
6.下表中不同的金属被开发和利用的年代不同,从化学反应的角度看,决定这一年代先后顺序的关键因素是( )
K 、Ca、 Na、 Mg 、Al 、Zn 、Fe、 Sn、 Pb、(H) 、Cu 、Hg 、Ag 、Pt 、Au约200年前约6000年前约6000年前AA.金属的活动性 B.金属的导电性
C.金属的延展性 D.地壳中金属元素的含量约2500年前7.等质量的稀硫酸分别与足量的镁铁锌三种金属反应,下列图像能正确生产氢气质量与反应时间之间关系的是( )
B
1.学会镁、铝、铁、铜等常见金属与氧 气、与酸溶液的反应。
2.在探究中理解金属活动性顺序,并作简单的应用。
3.会将所学化学知识用于解决生活的实际问题。你都知道哪些金属可以和氧气反应?反应时伴随怎样的现象?化学方程式如何书写?举例说明...... 金属与氧气的反应回顾镁和铁燃烧的现象:△探究金属铝与氧气的反应1.不同的金属与氧气的反应条件 .2. 反应条件的不同,说明金属的活泼程度 .(该性质称作 )不同不同“金属活动性”实验结论一:镁、铝等在常温下就能与氧气反应;
铁、铜等在高温下能与氧气反应;
金即使在高温时也不与氧气反应。镁、铝较活泼,铁、铜次之,金最不活泼。 铝在空气中与氧气反应,其表面生成一层致密的氧化铝(Al2O3)薄膜,阻止铝进一步氧化,因此,铝具有很好的抗腐蚀性能。1、铝的活动性比铁强,可是通常看见铁生锈而没有看到铝生锈,为什么?应不要把铝制品表面的氧化物保护膜清洗掉。2、在清洗铝制品时应注意些什么?我会应用: 实验探究二:金属与酸的反应思考:
(1)是否所有金属能与稀酸(稀盐酸或稀硫酸)反应?
(2)反应剧烈程度有无差异? Mg Zn Fe Cu 实验步骤及注意事项:
1、向4支试管中分别装入Cu、Fe、Zn、Mg金属
(药品用量:金属铜和镁用镊子各取一片;锌粒用药匙取3—5粒; 铁钉一个,注意铁钉圆头朝下滑落试管)
2、向上述试管中各注入约2ml
稀盐酸 或稀硫酸
(注意做到口挨口倾倒液体药
品,防止洒落)
3、观察、在学案上记录实验现象。讨论交流:从你的探究中,你的发现或收获?金属稀酸1、__________能与稀盐酸或稀硫酸反应,放出气体,而___却不能。
2、铁、镁、锌与稀盐酸或稀硫酸反应时剧烈程度不同。___反应最剧烈其次是____,然后是____。能否与酸反应,反应剧烈程度都与金属活动性强弱有关。实验结论二:Mg、Zn、FeCu镁锌铁趣味小实验空中点鞭炮情景再现排在越 面的元素,金属活泼性越强;
排在 之前的金属是较活泼的金属,能跟稀
硫酸一类的稀酸反应,生成氢气;
金属活动性顺序表所含信息:前氢单质化合物化合物单质小结:
这种由一种单质与一种化合物反应,生成了另一种单质和另一种化合物的反应叫做置换反应。讨论: 对于以上的反应,从反应物和生成物的类别角度分析,有何特点?
Mg + 2HCl = MgCl2 + H2 ↑
Zn + 2HCl = ZnCl2 + H2 ↑
Fe + 2HCl = FeCl2 + H2 ↑A + BC = AC + B一、金属的化学性质:
1、与氧气反应
(金属越活泼,反应越容易,越剧烈)
2、氢前金属与稀盐酸(稀硫酸)反应
(金属越活泼,反应越容易,越剧烈)
二、金属活动顺序及其应用
(判断金属能否在酸溶液中发生置换反应) 学完本课题我学到了为了谋取暴利,市场上假冒的商品随处可见。不法商常常把黄铜(铜锌合金)饰品冒充黄金以高价出卖,很多顾客上当受骗。1、下列反应中,有单质出现,但不属于置换反应的是( )A.Cu+2AgNO3=Cu(NO3)2+2Ag
B.2Al+3H2SO4=A12(SO4)3+3H2↑
C.2Mg+CO2 2MgO+C
D.2Na2O2+2CO2=2Na2CO3+O2D达标测评(基础题)2.社会上一些不法分子以铜锌合金(金黄色,俗称黄铜)假冒黄金进行诈骗活动。为鉴别黄铜和黄金,以下方法可行且简便的是( )(不定项)
A. 观察颜色 B. 在空气中加热
C. 加稀硫酸 D. 磁铁吸引 B C3.下列物质放入稀硫酸中,不能反应的是 ( ) A.A1 B.Cu C.Fe D.Zn
4.下列化学方程式正确的是( )
A.4Fe+3O2=2Fe2O3
B.Fe+H2SO4=FeSO4+H2↑
C.2Fe+6HCl=2FeCl3+H2↑
D.Fe+3CuSO4=Fe2(SO4)3+3CuBB5. 出土的古文物中,金器保存完好,铜器表面有锈迹,而铁器锈迹斑斑。这表明金.铜.铁的金属活动性从强到弱的顺序是( )
A.金.铜.铁 B.铁.金.铜
C.铁.铜.金 D.铜.金.铁C 能力提高
6.下表中不同的金属被开发和利用的年代不同,从化学反应的角度看,决定这一年代先后顺序的关键因素是( )
K 、Ca、 Na、 Mg 、Al 、Zn 、Fe、 Sn、 Pb、(H) 、Cu 、Hg 、Ag 、Pt 、Au约200年前约6000年前约6000年前AA.金属的活动性 B.金属的导电性
C.金属的延展性 D.地壳中金属元素的含量约2500年前7.等质量的稀硫酸分别与足量的镁铁锌三种金属反应,下列图像能正确生产氢气质量与反应时间之间关系的是( )
B
同课章节目录
