2018年春九年级鲁教版化学下册同步习题:第七单元 第二节 碱及其性质
文档属性
| 名称 | 2018年春九年级鲁教版化学下册同步习题:第七单元 第二节 碱及其性质 |

|
|
| 格式 | zip | ||
| 文件大小 | 623.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-01-24 00:00:00 | ||
图片预览




文档简介
第二节 碱及其性质
第1课时 常见的碱
01 知识管理
1.氢氧化钠
俗 称:________、________、________。
性 质:________色固体,________溶于水,溶解时放热,有________性,可作干燥剂。暴露在空气中容易吸收空气中的水蒸气而逐渐________,并且能与________反应而导致变质。
注 意:氢氧化钠固体具有吸水性,但氢氧化钠溶液不具有吸水性;氢氧化钠只能干燥不能与其反应的气体,如CO2、SO2等气体就不能用氢氧化钠干燥。
贮 存:________保存。
安全处理:若不慎将氢氧化钠沾到皮肤上,应立即用大量的________冲洗,然后涂上________溶液。
2.氢氧化钙
俗 称:________、________。
性 质:________色粉末状固体,________溶于水,其水溶液称石灰水,有腐蚀性。
制 备:(1)煅烧石灰石获得生石灰:________________________________;
(2)生石灰和水发生反应制得氢氧化钙:________________________________。
知识点拨:氢氧化钙、氧化钙、碳酸钙之间的关系:
02 基础题
1.(2017·上海)氢氧化钙的俗称( )
A.烧碱 B.纯碱
C.熟石灰 D.石灰石
2.下列物质属于碱类的是( )
A.苛性钠 B.食醋
C.生石灰 D.纯碱
3.下列几组物质按酸、碱、盐顺序排列的是( )
A.KNO3、NaOH、HCl
B.Ca(OH)2、HCl、NaCl
C.H2SO4、Na2CO3、Ba(OH)2
D.HNO3、KOH、CuSO4
4.物质的性质决定它的用途,还决定了它的保存方法。固体NaOH具有以下性质:①白色片状固体;②有腐蚀性;③易吸收水分而潮解;④易溶于水,溶解放热;⑤能与空气中的二氧化碳反应。实验室中必须将它密封保存的主要原因是( )
A.①② B.①②③ C.②③④ D.③⑤
5.(2016·舟山)化学反应常伴随能量的变化,如图所示,在
装有水的烧杯中放入一定质量的生石灰固体,反应片刻后可观察到玻璃管中的有色液体柱将________(填“上升”“下降”或“不变”),请写出反应后所得溶液中溶质
的化学式________。
6.如图是小庆同学归纳的几种含钙化合物的知识网络图,请根据该图回答:
(1)属于碱的是________。
(2)可作食品干燥剂的是________。
(3)写出图中涉及的任意一个反应的化学方程式:____________________________。
03 中档题
7.有一种“即热即食型食品”适合外出旅游时使用,其内层用铝箔包装食品,外层则是包装两种化学物质。使用预留在外的开关,使两种物质发生化学反应,此时便可以对食品进行加热,这两种化学物质最适合的选择是( )
A.熟石灰与水 B.生石灰与水
C.食盐与水 D.浓硫酸与水
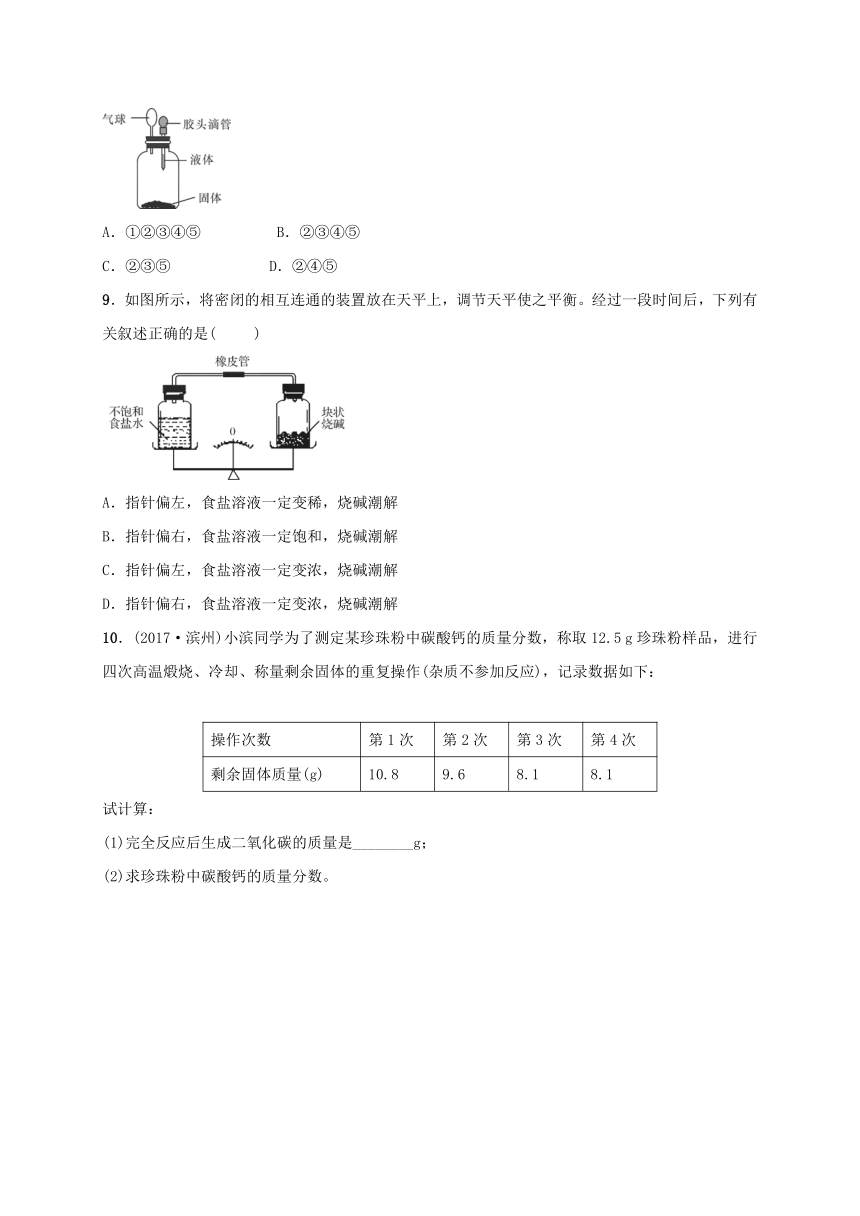
8.要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )
①硝酸铵和水;②铁和稀硫酸;③固体氢氧化钠和水;④生石灰和水;⑤石灰石和稀盐酸
A.①②③④⑤ B.②③④⑤
C.②③⑤ D.②④⑤
9.如图所示,将密闭的相互连通的装置放在天平上,调节天平使之平衡。经过一段时间后,下列有关叙述正确的是( )
A.指针偏左,食盐溶液一定变稀,烧碱潮解
B.指针偏右,食盐溶液一定饱和,烧碱潮解
C.指针偏左,食盐溶液一定变浓,烧碱潮解
D.指针偏右,食盐溶液一定变浓,烧碱潮解
10.(2017·滨州)小滨同学为了测定某珍珠粉中碳酸钙的质量分数,称取12.5 g珍珠粉样品,进行四次高温煅烧、冷却、称量剩余固体的重复操作(杂质不参加反应),记录数据如下:
操作次数
第1次
第2次
第3次
第4次
剩余固体质量(g)
10.8
9.6
8.1
8.1
试计算:
(1)完全反应后生成二氧化碳的质量是________g;
(2)求珍珠粉中碳酸钙的质量分数。
04 实验突破
11.(2016·巴中)生石灰常用作食品干燥剂,其包装上除了表明主要成分为生石灰外,还提醒了人们注意不可食用、不可浸水、不可开袋、儿童勿碰。甲、乙两同学想知道刚从食品袋中取出的生石灰的成分,进行了如下探究 (提示:氢氧化钙和稀盐酸反应无现象):
【提出问题】生石灰干燥剂中含有哪些物质?
【猜想与假设】猜想Ⅰ:含有氧化钙(CaO)、氢氧化钙[Ca(OH)2];
猜想Ⅱ:含有氧化钙(CaO)、碳酸钙(CaCO3);
猜想Ⅲ:含有氧化钙(CaO)、氢氧化钙[(Ca(OH)2)]、碳酸钙CaCO3。
【活动与探究】甲、乙两同学为了验证猜想,进行如下实验:
甲同学实验:取少量样品于试管中,加入适量的水充分反应后,再滴加几滴无色酚酞试液,可观察到溶液呈红色(碱溶液中滴加无色酚酞试液,溶液会变成红色)。
乙同学实验:取少量样品于试管中,加入足量的稀盐酸,有无色无味气体产生,该气体能使澄清石灰水变浑浊。
【结论与反思】
(1)猜想________(填“Ⅰ”“Ⅱ”或“Ⅲ”)错误。
(2)甲同学实验中发生反应的方程式:________________________________。
(3)乙同学检验气体的方程式:________________________________。
(4)乙同学认为甲同学的实验是多余的,因为_________________________________。
【拓展应用】甲、乙最终无法确定该生石灰干燥剂的成分,实验失败,丙同学认为可以通过定量实验来确定,在定量实验时,一定要用到的实验操作是________。
第2课时 碱的化学性质
01 知识管理
1.碱的化学性质
化学性质:(1)氢氧化钠溶液和氢氧化钙溶液都能使紫色石蕊试液变________色,使无色酚酞试液变________色。
(2)氢氧化钠和氢氧化钙都能与二氧化碳反应,反应的化学方程式分别为________________________________ 、________________________________。
(3)氢氧化钠和氢氧化钙都能与氯化铜溶液反应,反应的化学方程式分别为________________________________、________________________________。
(4)氢氧化钙能与碳酸钠溶液反应,反应的化学方程式为________________________________。
2.碱的通性
通 性:由于碱溶液中的阴离子都是 ________,所以碱具有相似的化学性质,即碱具有通性。
(1)都能使紫色石蕊试液变________,使无色酚酞试液变________。
(2)非金属氧化物+碱―→________+________。
(3)盐+碱―→________+________。
易错警示:(1)不溶性的碱[如Cu(OH)2等]在水中不会解离出氢氧根离子,不能使紫色石蕊试液和无色酚酞试液变色。
(2)并不是所有的非金属氧化物都能与碱反应,如一氧化碳等。
方法归纳:鉴别氢氧化钠溶液和氢氧化钙溶液的方法:(1)通入二氧化碳,产生沉淀的是氢氧化钙溶液;(2)滴加碳酸钠溶液,产生沉淀的是氢氧化钙溶液。
02 基础题
1.氢氧化钠溶液和氢氧化钙溶液具有相似的化学性质,其本质原因是( )
A.都能与指示剂作用
B.都能解离出氢氧根离子
C.都能解离出金属阳离子
D.都含有氢元素和氧元素
2.下列试剂不能区分稀盐酸和澄清石灰水的是( )
A.酚酞试液 B.食盐水
C.二氧化碳 D.碳酸钠溶液
3.已知氢氧化钾(KOH)可溶于水,其化学性质与氢氧化钠相似。下列对氢氧化钾的化学性质叙述错误的是( )
A.能与二氧化碳反应
B.能与硫酸铜溶液反应
C.能使无色酚酞试液变成红色
D.能与氯化钾溶液反应
4.四个烧杯中分别盛有下列物质,向烧杯中通入CO2,无明显现象的是( )
A.NaOH稀溶液 B.紫色石蕊试液
C.澄清石灰水 D.燃烧的蜡烛
5.(2016·自贡)归纳总结是学习化学的一种方法。请结合某同学对碱的四点化学性质的归纳图完成下列问题(箭头上方的物质是指与碱反应的物质)。
(1)碱溶液能使无色酚酞溶液变________。
(2)氢氧化钠暴露在空气中变质的化学方程式为________________________________,所以氢氧化钠必须________保存。
(3)碱溶液有相似的化学性质,是因为碱溶液中都含有__________(填化学符号)。
(4)利用氢氧化钙与盐反应的性质,可以除去氢氧化钠溶液中少量的氢氧化钙杂质,请写出反应的化学方程式:_____________________________________________。
03 中档题
6.研究氢氧化钠性质实验中的部分实验及现象记录如下,其中现象不合理的是( )
选项
实验
现象
A
将氢氧化钠固体放在表面皿上,放置一会儿
固体受潮,逐渐溶解
B
向盛有氢氧化钠溶液的试管中滴入无色酚酞试液
溶液变红
C
向盛有氢氧化钠溶液的试管中加入一根头发丝,加热煮沸2~3 min
头发丝无任何变化
D
向盛有氢氧化钠溶液的试管中滴加硫酸铜溶液
有蓝色沉淀生成
7.下列物质中,与CO2、CuCl2溶液、Na2CO3溶液都能发生反应,且都有明显现象的是( )
A.NaOH B.Ca(OH)2
C.H2SO4 D.HCl
8.(2017·潍坊)下列验证“CO2与NaOH溶液反应”的装置中,不能观察到明显现象的是(装置气密性均良好)( )
A B
C D
9.学习了氢氧化钠的性质之后,知道氢氧化钠溶液中含有H2O、Na+、OH-,能使无色酚酞溶液变红色,某科技小组想进一步探究是哪一种粒子使无色酚酞溶液变红色。
【提出猜想】猜想①:可能是H2O;猜想②:可能是Na+ ;猜想③:可能是OH-。
【实验验证】
实验操作
实验现象
结论
①用试管取少量蒸馏水,滴入1~2滴无色酚酞溶液,振荡
试管内溶液仍为无色
水分子不能使无色酚酞溶液变红色
②用试管取少量氯化钠溶液,滴入1~2滴无色酚酞溶液,振荡
_________________________
_________________________
③用试管取少量氢氧化钠溶液,滴 入1~2滴无色酚酞溶液,振荡
__________________________________________________
________________________________________________________________________
【讨论反思】有同学认为猜想①不需要实验验证就可以排除,你认为该同学的理由是________________________________________________________________________。
10.(2017·德阳)某校化学课外活动小组的同学在实验室的一次探究性活动中,他们将50 g氢氧化钠溶液与50 g硫酸铜溶液混合恰好完全反应,得到9.8 g沉淀,请你计算氢氧化钠溶液中溶质的质量分数。
04 实验突破
11.某化学兴趣小组同学为了探究实验室中的氢氧化钠固体是否变质,进行了有关实验。请你与他们一起完成以下探究活动:
【猜想】
猜想Ⅰ:没有变质;
猜想Ⅱ:已经变质。
【实验和推断】
(1)加入的适量A溶液是____________________(填名称),若现象a为有气泡产生,则说明氢氧化钠已经变质。
(2)若现象b为________________________,说明氢氧化钠没有变质。
【反思】
氢氧化钠的保存方法是________(填“A”或“B”)。
A.密封保存 B.不需密封保存
参考答案
第1课时 常见的碱
知识管理
1.烧碱 火碱 苛性钠 白 易 吸水 溶解 CO2 密封 水 硼酸 2.熟石灰 消石灰 白 微 (1)CaCO3CaO+CO2↑ (2)CaO+H2O===Ca(OH)2
基础题
1.C 2.A 3.D 4.D 5.上升 Ca(OH)2 6.(1) Ca(OH)2 (2)CaO (3)CaO+H2O===Ca(OH)2(其他合理答案均可)
中档题
7.B 8.B 9.D
10.(1) 4.4
(2)解:设珍珠粉样品中碳酸钙的质量为x。
CaCO3CaO+CO2↑
100 44
x 4.4 g
= x=10 g
珍珠粉中碳酸钙的质量分数为×100%=80%
答:珍珠粉中碳酸钙的质量分数为80%。
实验突破
11.(1)Ⅰ (2)CaO+H2O===Ca(OH)2 (3)CO2+Ca(OH)2===CaCO3↓+H2O (4)在有氧化钙的情况下,无法检验是否含有氢氧化钙 称量
第2课时 碱的化学性质
知识管理
1.(1)蓝 红 (2)2NaOH+CO2===Na2CO3+H2O Ca(OH) 2 +CO2===CaCO3↓+H2O (3)2NaOH+CuCl2===2NaCl+Cu(OH)2↓ Ca(OH)2+CuCl2===CaCl2+Cu(OH)2↓ (4)Ca(OH)2+Na2CO3===CaCO3↓+2NaOH 2.OH- (1)蓝 红 (2)盐 水 (3)新盐 新碱
基础题
1.B 2.B 3.D 4.A 5.(1)红色 (2)2NaOH+CO2===Na2CO3+H2O 密封 (3)OH- (4)Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
中档题
6.C 7.B 8.A 9.【实验验证】 试管内溶液仍为无色 Na+不能使无色酚酞溶液变红色 试管内溶液变为红色 OH-能使无色酚酞溶液变红色 【讨论反思】 酚酞试液本身就含有水分子,且氯化钠溶液中含有水,实验②就能同时验证水和钠离子对酚酞变色的影响
10.解:设氢氧化钠的质量为x。
CuSO4+2NaOH===Na2SO4+Cu(OH)2↓
80 98
x 9.8 g
= x=8 g
氢氧化钠溶液中溶质的质量分数为×100%=16%
答:氢氧化钠溶液中溶质的质量分数为16%。
实验突破
11.(1)稀盐酸(或稀硫酸等) (2)无明显现象(或无气泡产生) 【反思】A
第1课时 常见的碱
01 知识管理
1.氢氧化钠
俗 称:________、________、________。
性 质:________色固体,________溶于水,溶解时放热,有________性,可作干燥剂。暴露在空气中容易吸收空气中的水蒸气而逐渐________,并且能与________反应而导致变质。
注 意:氢氧化钠固体具有吸水性,但氢氧化钠溶液不具有吸水性;氢氧化钠只能干燥不能与其反应的气体,如CO2、SO2等气体就不能用氢氧化钠干燥。
贮 存:________保存。
安全处理:若不慎将氢氧化钠沾到皮肤上,应立即用大量的________冲洗,然后涂上________溶液。
2.氢氧化钙
俗 称:________、________。
性 质:________色粉末状固体,________溶于水,其水溶液称石灰水,有腐蚀性。
制 备:(1)煅烧石灰石获得生石灰:________________________________;
(2)生石灰和水发生反应制得氢氧化钙:________________________________。
知识点拨:氢氧化钙、氧化钙、碳酸钙之间的关系:
02 基础题
1.(2017·上海)氢氧化钙的俗称( )
A.烧碱 B.纯碱
C.熟石灰 D.石灰石
2.下列物质属于碱类的是( )
A.苛性钠 B.食醋
C.生石灰 D.纯碱
3.下列几组物质按酸、碱、盐顺序排列的是( )
A.KNO3、NaOH、HCl
B.Ca(OH)2、HCl、NaCl
C.H2SO4、Na2CO3、Ba(OH)2
D.HNO3、KOH、CuSO4
4.物质的性质决定它的用途,还决定了它的保存方法。固体NaOH具有以下性质:①白色片状固体;②有腐蚀性;③易吸收水分而潮解;④易溶于水,溶解放热;⑤能与空气中的二氧化碳反应。实验室中必须将它密封保存的主要原因是( )
A.①② B.①②③ C.②③④ D.③⑤
5.(2016·舟山)化学反应常伴随能量的变化,如图所示,在
装有水的烧杯中放入一定质量的生石灰固体,反应片刻后可观察到玻璃管中的有色液体柱将________(填“上升”“下降”或“不变”),请写出反应后所得溶液中溶质
的化学式________。
6.如图是小庆同学归纳的几种含钙化合物的知识网络图,请根据该图回答:
(1)属于碱的是________。
(2)可作食品干燥剂的是________。
(3)写出图中涉及的任意一个反应的化学方程式:____________________________。
03 中档题
7.有一种“即热即食型食品”适合外出旅游时使用,其内层用铝箔包装食品,外层则是包装两种化学物质。使用预留在外的开关,使两种物质发生化学反应,此时便可以对食品进行加热,这两种化学物质最适合的选择是( )
A.熟石灰与水 B.生石灰与水
C.食盐与水 D.浓硫酸与水
8.要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )
①硝酸铵和水;②铁和稀硫酸;③固体氢氧化钠和水;④生石灰和水;⑤石灰石和稀盐酸
A.①②③④⑤ B.②③④⑤
C.②③⑤ D.②④⑤
9.如图所示,将密闭的相互连通的装置放在天平上,调节天平使之平衡。经过一段时间后,下列有关叙述正确的是( )
A.指针偏左,食盐溶液一定变稀,烧碱潮解
B.指针偏右,食盐溶液一定饱和,烧碱潮解
C.指针偏左,食盐溶液一定变浓,烧碱潮解
D.指针偏右,食盐溶液一定变浓,烧碱潮解
10.(2017·滨州)小滨同学为了测定某珍珠粉中碳酸钙的质量分数,称取12.5 g珍珠粉样品,进行四次高温煅烧、冷却、称量剩余固体的重复操作(杂质不参加反应),记录数据如下:
操作次数
第1次
第2次
第3次
第4次
剩余固体质量(g)
10.8
9.6
8.1
8.1
试计算:
(1)完全反应后生成二氧化碳的质量是________g;
(2)求珍珠粉中碳酸钙的质量分数。
04 实验突破
11.(2016·巴中)生石灰常用作食品干燥剂,其包装上除了表明主要成分为生石灰外,还提醒了人们注意不可食用、不可浸水、不可开袋、儿童勿碰。甲、乙两同学想知道刚从食品袋中取出的生石灰的成分,进行了如下探究 (提示:氢氧化钙和稀盐酸反应无现象):
【提出问题】生石灰干燥剂中含有哪些物质?
【猜想与假设】猜想Ⅰ:含有氧化钙(CaO)、氢氧化钙[Ca(OH)2];
猜想Ⅱ:含有氧化钙(CaO)、碳酸钙(CaCO3);
猜想Ⅲ:含有氧化钙(CaO)、氢氧化钙[(Ca(OH)2)]、碳酸钙CaCO3。
【活动与探究】甲、乙两同学为了验证猜想,进行如下实验:
甲同学实验:取少量样品于试管中,加入适量的水充分反应后,再滴加几滴无色酚酞试液,可观察到溶液呈红色(碱溶液中滴加无色酚酞试液,溶液会变成红色)。
乙同学实验:取少量样品于试管中,加入足量的稀盐酸,有无色无味气体产生,该气体能使澄清石灰水变浑浊。
【结论与反思】
(1)猜想________(填“Ⅰ”“Ⅱ”或“Ⅲ”)错误。
(2)甲同学实验中发生反应的方程式:________________________________。
(3)乙同学检验气体的方程式:________________________________。
(4)乙同学认为甲同学的实验是多余的,因为_________________________________。
【拓展应用】甲、乙最终无法确定该生石灰干燥剂的成分,实验失败,丙同学认为可以通过定量实验来确定,在定量实验时,一定要用到的实验操作是________。
第2课时 碱的化学性质
01 知识管理
1.碱的化学性质
化学性质:(1)氢氧化钠溶液和氢氧化钙溶液都能使紫色石蕊试液变________色,使无色酚酞试液变________色。
(2)氢氧化钠和氢氧化钙都能与二氧化碳反应,反应的化学方程式分别为________________________________ 、________________________________。
(3)氢氧化钠和氢氧化钙都能与氯化铜溶液反应,反应的化学方程式分别为________________________________、________________________________。
(4)氢氧化钙能与碳酸钠溶液反应,反应的化学方程式为________________________________。
2.碱的通性
通 性:由于碱溶液中的阴离子都是 ________,所以碱具有相似的化学性质,即碱具有通性。
(1)都能使紫色石蕊试液变________,使无色酚酞试液变________。
(2)非金属氧化物+碱―→________+________。
(3)盐+碱―→________+________。
易错警示:(1)不溶性的碱[如Cu(OH)2等]在水中不会解离出氢氧根离子,不能使紫色石蕊试液和无色酚酞试液变色。
(2)并不是所有的非金属氧化物都能与碱反应,如一氧化碳等。
方法归纳:鉴别氢氧化钠溶液和氢氧化钙溶液的方法:(1)通入二氧化碳,产生沉淀的是氢氧化钙溶液;(2)滴加碳酸钠溶液,产生沉淀的是氢氧化钙溶液。
02 基础题
1.氢氧化钠溶液和氢氧化钙溶液具有相似的化学性质,其本质原因是( )
A.都能与指示剂作用
B.都能解离出氢氧根离子
C.都能解离出金属阳离子
D.都含有氢元素和氧元素
2.下列试剂不能区分稀盐酸和澄清石灰水的是( )
A.酚酞试液 B.食盐水
C.二氧化碳 D.碳酸钠溶液
3.已知氢氧化钾(KOH)可溶于水,其化学性质与氢氧化钠相似。下列对氢氧化钾的化学性质叙述错误的是( )
A.能与二氧化碳反应
B.能与硫酸铜溶液反应
C.能使无色酚酞试液变成红色
D.能与氯化钾溶液反应
4.四个烧杯中分别盛有下列物质,向烧杯中通入CO2,无明显现象的是( )
A.NaOH稀溶液 B.紫色石蕊试液
C.澄清石灰水 D.燃烧的蜡烛
5.(2016·自贡)归纳总结是学习化学的一种方法。请结合某同学对碱的四点化学性质的归纳图完成下列问题(箭头上方的物质是指与碱反应的物质)。
(1)碱溶液能使无色酚酞溶液变________。
(2)氢氧化钠暴露在空气中变质的化学方程式为________________________________,所以氢氧化钠必须________保存。
(3)碱溶液有相似的化学性质,是因为碱溶液中都含有__________(填化学符号)。
(4)利用氢氧化钙与盐反应的性质,可以除去氢氧化钠溶液中少量的氢氧化钙杂质,请写出反应的化学方程式:_____________________________________________。
03 中档题
6.研究氢氧化钠性质实验中的部分实验及现象记录如下,其中现象不合理的是( )
选项
实验
现象
A
将氢氧化钠固体放在表面皿上,放置一会儿
固体受潮,逐渐溶解
B
向盛有氢氧化钠溶液的试管中滴入无色酚酞试液
溶液变红
C
向盛有氢氧化钠溶液的试管中加入一根头发丝,加热煮沸2~3 min
头发丝无任何变化
D
向盛有氢氧化钠溶液的试管中滴加硫酸铜溶液
有蓝色沉淀生成
7.下列物质中,与CO2、CuCl2溶液、Na2CO3溶液都能发生反应,且都有明显现象的是( )
A.NaOH B.Ca(OH)2
C.H2SO4 D.HCl
8.(2017·潍坊)下列验证“CO2与NaOH溶液反应”的装置中,不能观察到明显现象的是(装置气密性均良好)( )
A B
C D
9.学习了氢氧化钠的性质之后,知道氢氧化钠溶液中含有H2O、Na+、OH-,能使无色酚酞溶液变红色,某科技小组想进一步探究是哪一种粒子使无色酚酞溶液变红色。
【提出猜想】猜想①:可能是H2O;猜想②:可能是Na+ ;猜想③:可能是OH-。
【实验验证】
实验操作
实验现象
结论
①用试管取少量蒸馏水,滴入1~2滴无色酚酞溶液,振荡
试管内溶液仍为无色
水分子不能使无色酚酞溶液变红色
②用试管取少量氯化钠溶液,滴入1~2滴无色酚酞溶液,振荡
_________________________
_________________________
③用试管取少量氢氧化钠溶液,滴 入1~2滴无色酚酞溶液,振荡
__________________________________________________
________________________________________________________________________
【讨论反思】有同学认为猜想①不需要实验验证就可以排除,你认为该同学的理由是________________________________________________________________________。
10.(2017·德阳)某校化学课外活动小组的同学在实验室的一次探究性活动中,他们将50 g氢氧化钠溶液与50 g硫酸铜溶液混合恰好完全反应,得到9.8 g沉淀,请你计算氢氧化钠溶液中溶质的质量分数。
04 实验突破
11.某化学兴趣小组同学为了探究实验室中的氢氧化钠固体是否变质,进行了有关实验。请你与他们一起完成以下探究活动:
【猜想】
猜想Ⅰ:没有变质;
猜想Ⅱ:已经变质。
【实验和推断】
(1)加入的适量A溶液是____________________(填名称),若现象a为有气泡产生,则说明氢氧化钠已经变质。
(2)若现象b为________________________,说明氢氧化钠没有变质。
【反思】
氢氧化钠的保存方法是________(填“A”或“B”)。
A.密封保存 B.不需密封保存
参考答案
第1课时 常见的碱
知识管理
1.烧碱 火碱 苛性钠 白 易 吸水 溶解 CO2 密封 水 硼酸 2.熟石灰 消石灰 白 微 (1)CaCO3CaO+CO2↑ (2)CaO+H2O===Ca(OH)2
基础题
1.C 2.A 3.D 4.D 5.上升 Ca(OH)2 6.(1) Ca(OH)2 (2)CaO (3)CaO+H2O===Ca(OH)2(其他合理答案均可)
中档题
7.B 8.B 9.D
10.(1) 4.4
(2)解:设珍珠粉样品中碳酸钙的质量为x。
CaCO3CaO+CO2↑
100 44
x 4.4 g
= x=10 g
珍珠粉中碳酸钙的质量分数为×100%=80%
答:珍珠粉中碳酸钙的质量分数为80%。
实验突破
11.(1)Ⅰ (2)CaO+H2O===Ca(OH)2 (3)CO2+Ca(OH)2===CaCO3↓+H2O (4)在有氧化钙的情况下,无法检验是否含有氢氧化钙 称量
第2课时 碱的化学性质
知识管理
1.(1)蓝 红 (2)2NaOH+CO2===Na2CO3+H2O Ca(OH) 2 +CO2===CaCO3↓+H2O (3)2NaOH+CuCl2===2NaCl+Cu(OH)2↓ Ca(OH)2+CuCl2===CaCl2+Cu(OH)2↓ (4)Ca(OH)2+Na2CO3===CaCO3↓+2NaOH 2.OH- (1)蓝 红 (2)盐 水 (3)新盐 新碱
基础题
1.B 2.B 3.D 4.A 5.(1)红色 (2)2NaOH+CO2===Na2CO3+H2O 密封 (3)OH- (4)Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
中档题
6.C 7.B 8.A 9.【实验验证】 试管内溶液仍为无色 Na+不能使无色酚酞溶液变红色 试管内溶液变为红色 OH-能使无色酚酞溶液变红色 【讨论反思】 酚酞试液本身就含有水分子,且氯化钠溶液中含有水,实验②就能同时验证水和钠离子对酚酞变色的影响
10.解:设氢氧化钠的质量为x。
CuSO4+2NaOH===Na2SO4+Cu(OH)2↓
80 98
x 9.8 g
= x=8 g
氢氧化钠溶液中溶质的质量分数为×100%=16%
答:氢氧化钠溶液中溶质的质量分数为16%。
实验突破
11.(1)稀盐酸(或稀硫酸等) (2)无明显现象(或无气泡产生) 【反思】A
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
