化学用语化学量[下学期]
图片预览






文档简介
课件26张PPT。1 、物质的组成:化学式和化合价
2 、元素周期表的简单结构和意义
3、常见元素名称和符号、化学式、化学方程式
4、计算:物质的相对分子质量(式量)、元素的质量比、元素的质量分数考点扫描 第25讲
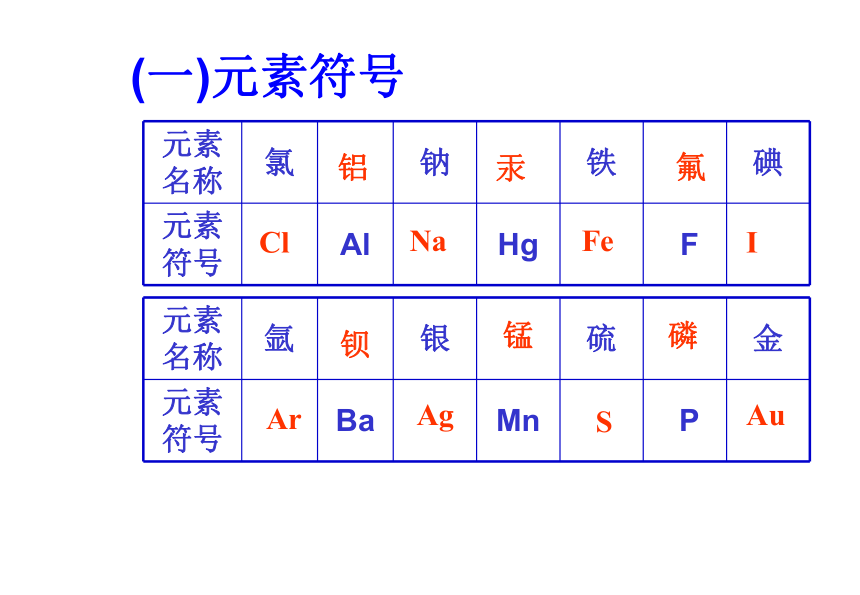
化学用语化学量(一)元素符号Cl铝Na汞Fe氟IAr钡Ag锰S磷Au氢氦锂铍硼 碳氮氧氟氖 钠镁铝硅磷 硫氯氩请写出质子数1——18各元素名称和符号按金属活动性顺序由强到弱默写元素名称和符号钾钙钠镁铝 锌铁锡铅 氢 铜汞银铂金默写常见元素化合价口诀H He Li Be B C N O F Ne Na Mg Al Si P S Cl ArK Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au用于反映不同元素间化合的原子个数关系的数。表示方法:元素的化合价标在元素符号的正上方 。(二)化合价与化学式“+”号不能省略。H2O O3 Ca(OH)2 Ca10(PO4)6OH)2+1 -20+2 -2 +1请标出下列物质中各元素的化合价+2 +5 -2 -2 1+2-1+1-2+1+1+6-20注意:标化合价的方式与离子表示的方法不同,
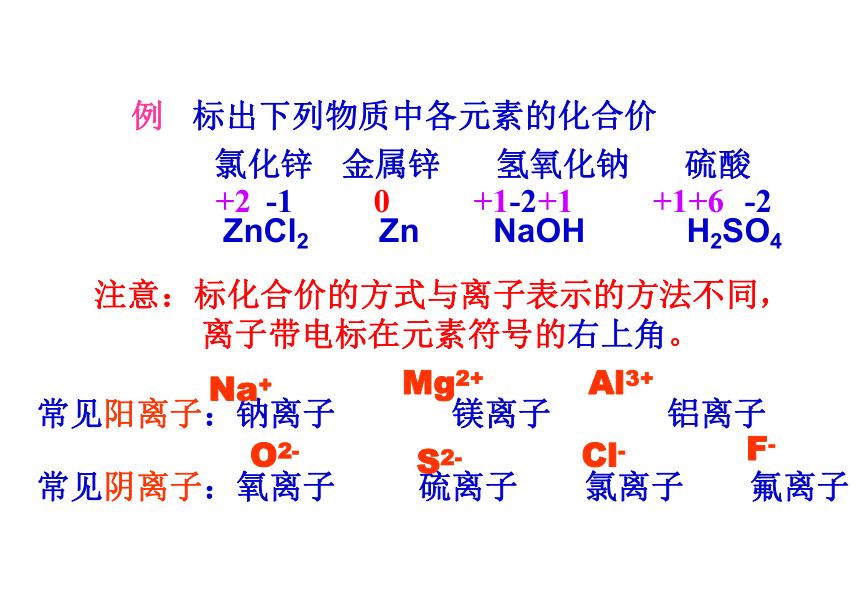
离子带电标在元素符号的右上角。常见阳离子:钠离子 镁离子 铝离子Na+Mg2+Al3+常见阴离子:氧离子 硫离子 氯离子 氟离子O2-S2-Cl-F-例 标出下列物质中各元素的化合价
氯化锌 金属锌 氢氧化钠 硫酸
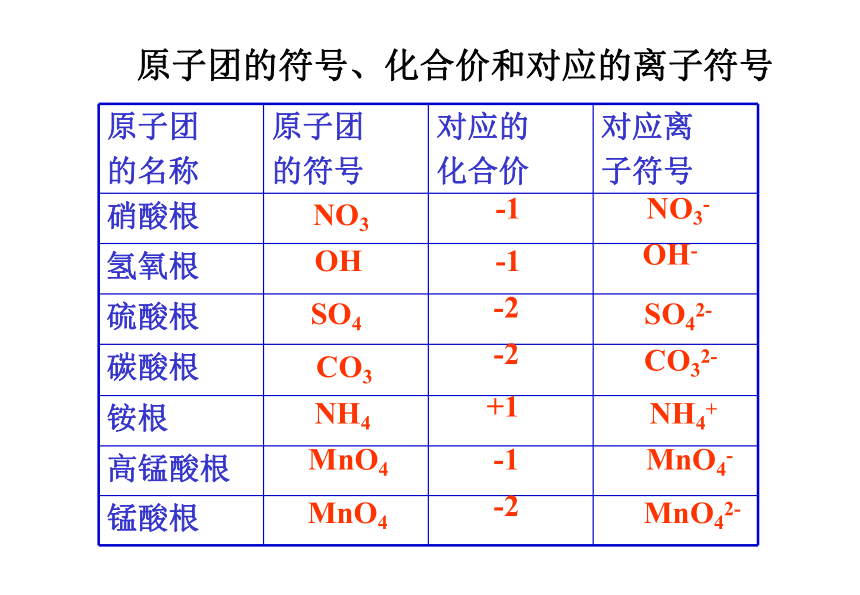
ZnCl2 Zn NaOH H2SO4+1价:钾钠银铵氢, +2价:钡钙镁铜汞锌 二、三铁,二、四碳 三铝四硅五价磷, 氟氯溴碘-1价氧是-2要记清 氢氧根、硝酸根(OH、NO3 )-1价 硫酸根、碳酸根(SO4 、CO3 )-2价, 化合物各元素化合价代数和为零, 单质元素化合价是零。 注:+ 2价的铁叫“亚铁”; 硫、氧、氯有多种价常见元素化合价口诀原子团的符号、化合价和对应的离子符号NO3OHSO4CO3NH4MnO4MnO4-1-1-2-2+1-1-2NO3-OH-SO42-CO32-NH4+MnO4-MnO42-根据化合价写化学式交叉法确定化学式:正价在前负价后,约简化合价,交叉。 (1) 写出 +3 价磷的氧化物的化学式例: 已知磷有两种氧化物,其中磷的化合价分别为 +3 和 +5 ,写出这两种磷的氧化物的化学式。P O+3 -223验证: +3×2 + (-2)×3=0P O+5 -225验证: +5×2 + (-2)×5=0 (2) 写出 +5 价磷的氧化物的化学式P2 O3P2 O5例 试确定碘酸钾(KIO3)中碘元素的化合价K I O3 -2 X +1 1+ X +(-2)×3=0 X= +5 解:继续原则:化合物中,正、负化合价代 数和为零。求元素的化合价方法:设要标价元素的化合价为X, 根据口诀标出其他元素化合价, 列方程求解。 设碘元素的化合价为X,则 化学式H2OCO2Fe3O4MnO2SO2P2O5Al2O3CaOCH4Fe2(SO4)3NaOH(NH4)2SO4Na2CO3C2H5OHKMnO4K2MnO4(三)三种微粒符号的表示方法HNH2O2S3N23O2-F-Na+Mg2+Al3+S2-Cl-(四)不同位置上数字的含义 2氮原子一个氮分子由两个氮原子构成3个水分子一个水分子中含有2个氢原子一个镁离子带有两个单位的正电荷3个硫离子一个硫离子带有两个单位的负电荷5个镁离子不同位置上数字的含义 KMnO4+7F0NH4-32个硫酸根一个硫酸根中含有4个氧原子高锰酸钾中锰元素的化合价为+7价氟元素的化合价为0价铵根中氮元素的化合价为-3价氮原子的原子核内的质子数为7Ax By 相对分子质量= (五)根据化学式的计算a x + byA元素 : B元素 = a x : byA%=A的相对原子质量×XAx By的相对分子质量×100%A元素的质量=物质的质量×A元素的质量分数某物质的化学式Ax By,A、B的相对原子质量为a、b1、元素种类和一个分子中原子个数3323491015410C:H:O= 12:3:8N:H:O=7:1:12C:H= 21:2C:H:O= 6:1:8C:H:O:N= 24:5:32:142、相对分子质量(式量)2(1 ×2 + 16×2) =NH4NO3的相对分子质量= 14 +4+14+16×3=80CuSO4·5H2O的相对分子质量= 64+32+16×4+5(2+16)=25068相对分子质量(式量)= 相对原子质量总和Ca( OH)2相对分子质量= 40+(16 + 1)×2=742H2 O2相对分子质量= 例:维生素C(化学式为C6H8O6)主要存在于蔬菜和水果中,它能促进人体和生长发育,增强人体对疾病的抵抗力,近来年发现维生素C还有防癌作用,则维生素________(填“是”或“不是”)氧化物,________(填“是”或“不是”)有机物;它由______种元素组成,其相对分子质量_______,各元素的原子个数比C:H:O=________, 碳元素的质量分数为_______________,缺少维生素C可以引发 ______________病,通过平衡膳食,多吃__________________________可补充维生素C。不是是40.9%31769:1:12质量比坏血病新鲜蔬菜和水果六、质量守恒定律: 参加化学反应的各物质质量总和,等于反应后生成的各物质质量总和。在一切化学反应中,反应前后元素的种类、原子的种类、各类原子的数目和原子的质量都不变。⑴2X + 3O2 =2H2O+2SO2,则X的化学式是____H2S⑵ 4.6g某化合物在氧气里燃烧生成8.8g二氧化碳和5.4g水,则参加反应的O2的质量为______该物质一定含有的元素是________ 解:参加反应的O2质量=8.8g+5.4g-4.6g=9.6g 5.4g水中含O=5.4g ×—— =4.8g 9.6g碳、氢和氧元素天平平衡2HCl——H2 H2SO4——H2
73 2 98 2
73克 2 73克 1.5天平平衡条件:
左边加入质量-气体质量=右边加入质量-气体质量 右左化学方程式及反应类型(1) 双氧水和二氧化锰的混合H2O2H2O+O222MnO2(2) 加热高锰酸钾KMnO4K2MnO4+MnO2+O22(3)锌和稀硫酸反应Zn+H2SO4ZnSO4+H2(4)氢气还原氧化铜H2+CuOCu+H2O(分解反应)(分解反应)(置换反应)(置换反应)(5)铁丝在氧气中燃烧Fe+O2Fe3O432点燃(6)白磷在空气中燃烧P+O2P2O5254点燃(化合反应)(化合反应)题型1 概念的理解应用1、决定元素种类的是原子的( )
A、中子数 B、质子数 C、电子数 D、最外层电子数
2、我国将启动一项涉及千家万户营养健康问题的“补铁工程”。卫生部已批准以酱油为食物载体,逐步开展“补铁工程”。这里
的铁指的是( )
A、分子 B、原子 C、元素 D、单质
3、在人体和地壳所含的元素中,质量分数最大的是( )
A、氮 B、氧 C、碳 D、氢 热点题型例析BCB题型2 用分子、原子、元素描述物质组成、构成4、2005年在某些国家和我国一些地区的有些食品中发现了对人体有害的苏丹红Ⅰ号。对苏丹红Ⅰ号(化学式为C16H12N2O)的叙述,不正确的是( )
A、是一种有机化合物 B、由四种元素组成
C、每个分子中含有31个原子
D、这种物质中,碳、氧两种元素的质量比为16:1
5、下列叙述中,正确的是( )
A、二氧化碳分子是由一个碳原子和一个氧分子构成的
B、不同元素的原子的核电荷数一定不同
C、核外电子排布相同的粒子一定属于同种元素
D、原子是保持物质化学性质的最小粒子DB选择题、CBCAP99-100答案5、71 36:5:16:14 19.7% 6、D 7、A 8、3N Al nH2O 2Fe3+9、质子数(核电荷数) 中子数10、⑴二氧化碳 ⑵1个二氧化碳分子由1个碳原子和2个氧原子构成⑶二氧化碳由碳元素和氧元素组成 ⑷1个二氧化碳分子⑸二氧化碳的式量为4411、B知能巧练:ABC4、31 48:3:7:4 5、 A 6、C 7、 C 9、 B8、③ ① ④ ②+3P101答案10、⑴2 10 ⑵CH4+2O2 = CO2+2H20点燃11、⑴NH4NO3=N2O↑+2H2O ⑵ - 3 +5 +1 12、⑴同一周期中,元素原子的半径随质子数(原子序数)增加而减小 ⑵同一主族元素原子的半径随质子数(原子序数)增加而增大 (七)原子、离子结构示意图画出氖原子结构示意图画出氧离子结构示意图画出铝离子结构示意图
2 、元素周期表的简单结构和意义
3、常见元素名称和符号、化学式、化学方程式
4、计算:物质的相对分子质量(式量)、元素的质量比、元素的质量分数考点扫描 第25讲
化学用语化学量(一)元素符号Cl铝Na汞Fe氟IAr钡Ag锰S磷Au氢氦锂铍硼 碳氮氧氟氖 钠镁铝硅磷 硫氯氩请写出质子数1——18各元素名称和符号按金属活动性顺序由强到弱默写元素名称和符号钾钙钠镁铝 锌铁锡铅 氢 铜汞银铂金默写常见元素化合价口诀H He Li Be B C N O F Ne Na Mg Al Si P S Cl ArK Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au用于反映不同元素间化合的原子个数关系的数。表示方法:元素的化合价标在元素符号的正上方 。(二)化合价与化学式“+”号不能省略。H2O O3 Ca(OH)2 Ca10(PO4)6OH)2+1 -20+2 -2 +1请标出下列物质中各元素的化合价+2 +5 -2 -2 1+2-1+1-2+1+1+6-20注意:标化合价的方式与离子表示的方法不同,
离子带电标在元素符号的右上角。常见阳离子:钠离子 镁离子 铝离子Na+Mg2+Al3+常见阴离子:氧离子 硫离子 氯离子 氟离子O2-S2-Cl-F-例 标出下列物质中各元素的化合价
氯化锌 金属锌 氢氧化钠 硫酸
ZnCl2 Zn NaOH H2SO4+1价:钾钠银铵氢, +2价:钡钙镁铜汞锌 二、三铁,二、四碳 三铝四硅五价磷, 氟氯溴碘-1价氧是-2要记清 氢氧根、硝酸根(OH、NO3 )-1价 硫酸根、碳酸根(SO4 、CO3 )-2价, 化合物各元素化合价代数和为零, 单质元素化合价是零。 注:+ 2价的铁叫“亚铁”; 硫、氧、氯有多种价常见元素化合价口诀原子团的符号、化合价和对应的离子符号NO3OHSO4CO3NH4MnO4MnO4-1-1-2-2+1-1-2NO3-OH-SO42-CO32-NH4+MnO4-MnO42-根据化合价写化学式交叉法确定化学式:正价在前负价后,约简化合价,交叉。 (1) 写出 +3 价磷的氧化物的化学式例: 已知磷有两种氧化物,其中磷的化合价分别为 +3 和 +5 ,写出这两种磷的氧化物的化学式。P O+3 -223验证: +3×2 + (-2)×3=0P O+5 -225验证: +5×2 + (-2)×5=0 (2) 写出 +5 价磷的氧化物的化学式P2 O3P2 O5例 试确定碘酸钾(KIO3)中碘元素的化合价K I O3 -2 X +1 1+ X +(-2)×3=0 X= +5 解:继续原则:化合物中,正、负化合价代 数和为零。求元素的化合价方法:设要标价元素的化合价为X, 根据口诀标出其他元素化合价, 列方程求解。 设碘元素的化合价为X,则 化学式H2OCO2Fe3O4MnO2SO2P2O5Al2O3CaOCH4Fe2(SO4)3NaOH(NH4)2SO4Na2CO3C2H5OHKMnO4K2MnO4(三)三种微粒符号的表示方法HNH2O2S3N23O2-F-Na+Mg2+Al3+S2-Cl-(四)不同位置上数字的含义 2氮原子一个氮分子由两个氮原子构成3个水分子一个水分子中含有2个氢原子一个镁离子带有两个单位的正电荷3个硫离子一个硫离子带有两个单位的负电荷5个镁离子不同位置上数字的含义 KMnO4+7F0NH4-32个硫酸根一个硫酸根中含有4个氧原子高锰酸钾中锰元素的化合价为+7价氟元素的化合价为0价铵根中氮元素的化合价为-3价氮原子的原子核内的质子数为7Ax By 相对分子质量= (五)根据化学式的计算a x + byA元素 : B元素 = a x : byA%=A的相对原子质量×XAx By的相对分子质量×100%A元素的质量=物质的质量×A元素的质量分数某物质的化学式Ax By,A、B的相对原子质量为a、b1、元素种类和一个分子中原子个数3323491015410C:H:O= 12:3:8N:H:O=7:1:12C:H= 21:2C:H:O= 6:1:8C:H:O:N= 24:5:32:142、相对分子质量(式量)2(1 ×2 + 16×2) =NH4NO3的相对分子质量= 14 +4+14+16×3=80CuSO4·5H2O的相对分子质量= 64+32+16×4+5(2+16)=25068相对分子质量(式量)= 相对原子质量总和Ca( OH)2相对分子质量= 40+(16 + 1)×2=742H2 O2相对分子质量= 例:维生素C(化学式为C6H8O6)主要存在于蔬菜和水果中,它能促进人体和生长发育,增强人体对疾病的抵抗力,近来年发现维生素C还有防癌作用,则维生素________(填“是”或“不是”)氧化物,________(填“是”或“不是”)有机物;它由______种元素组成,其相对分子质量_______,各元素的原子个数比C:H:O=________, 碳元素的质量分数为_______________,缺少维生素C可以引发 ______________病,通过平衡膳食,多吃__________________________可补充维生素C。不是是40.9%31769:1:12质量比坏血病新鲜蔬菜和水果六、质量守恒定律: 参加化学反应的各物质质量总和,等于反应后生成的各物质质量总和。在一切化学反应中,反应前后元素的种类、原子的种类、各类原子的数目和原子的质量都不变。⑴2X + 3O2 =2H2O+2SO2,则X的化学式是____H2S⑵ 4.6g某化合物在氧气里燃烧生成8.8g二氧化碳和5.4g水,则参加反应的O2的质量为______该物质一定含有的元素是________ 解:参加反应的O2质量=8.8g+5.4g-4.6g=9.6g 5.4g水中含O=5.4g ×—— =4.8g 9.6g碳、氢和氧元素天平平衡2HCl——H2 H2SO4——H2
73 2 98 2
73克 2 73克 1.5天平平衡条件:
左边加入质量-气体质量=右边加入质量-气体质量 右左化学方程式及反应类型(1) 双氧水和二氧化锰的混合H2O2H2O+O222MnO2(2) 加热高锰酸钾KMnO4K2MnO4+MnO2+O22(3)锌和稀硫酸反应Zn+H2SO4ZnSO4+H2(4)氢气还原氧化铜H2+CuOCu+H2O(分解反应)(分解反应)(置换反应)(置换反应)(5)铁丝在氧气中燃烧Fe+O2Fe3O432点燃(6)白磷在空气中燃烧P+O2P2O5254点燃(化合反应)(化合反应)题型1 概念的理解应用1、决定元素种类的是原子的( )
A、中子数 B、质子数 C、电子数 D、最外层电子数
2、我国将启动一项涉及千家万户营养健康问题的“补铁工程”。卫生部已批准以酱油为食物载体,逐步开展“补铁工程”。这里
的铁指的是( )
A、分子 B、原子 C、元素 D、单质
3、在人体和地壳所含的元素中,质量分数最大的是( )
A、氮 B、氧 C、碳 D、氢 热点题型例析BCB题型2 用分子、原子、元素描述物质组成、构成4、2005年在某些国家和我国一些地区的有些食品中发现了对人体有害的苏丹红Ⅰ号。对苏丹红Ⅰ号(化学式为C16H12N2O)的叙述,不正确的是( )
A、是一种有机化合物 B、由四种元素组成
C、每个分子中含有31个原子
D、这种物质中,碳、氧两种元素的质量比为16:1
5、下列叙述中,正确的是( )
A、二氧化碳分子是由一个碳原子和一个氧分子构成的
B、不同元素的原子的核电荷数一定不同
C、核外电子排布相同的粒子一定属于同种元素
D、原子是保持物质化学性质的最小粒子DB选择题、CBCAP99-100答案5、71 36:5:16:14 19.7% 6、D 7、A 8、3N Al nH2O 2Fe3+9、质子数(核电荷数) 中子数10、⑴二氧化碳 ⑵1个二氧化碳分子由1个碳原子和2个氧原子构成⑶二氧化碳由碳元素和氧元素组成 ⑷1个二氧化碳分子⑸二氧化碳的式量为4411、B知能巧练:ABC4、31 48:3:7:4 5、 A 6、C 7、 C 9、 B8、③ ① ④ ②+3P101答案10、⑴2 10 ⑵CH4+2O2 = CO2+2H20点燃11、⑴NH4NO3=N2O↑+2H2O ⑵ - 3 +5 +1 12、⑴同一周期中,元素原子的半径随质子数(原子序数)增加而减小 ⑵同一主族元素原子的半径随质子数(原子序数)增加而增大 (七)原子、离子结构示意图画出氖原子结构示意图画出氧离子结构示意图画出铝离子结构示意图
