化学练习1[上下学期通用]
图片预览




文档简介
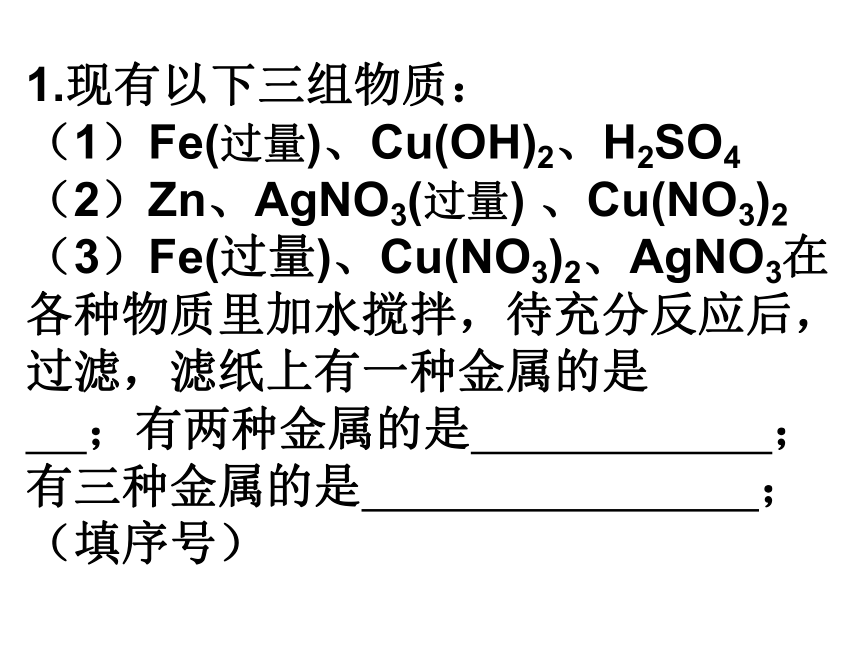
课件10张PPT。1.现有以下三组物质:
(1)Fe(过量)、Cu(OH)2、H2SO4 (2)Zn、AgNO3(过量) 、Cu(NO3)2
(3)Fe(过量)、Cu(NO3)2、AgNO3在各种物质里加水搅拌,待充分反应后,过滤,滤纸上有一种金属的是 ;有两种金属的是 ;有三种金属的是 ;(填序号)2.有失去标签的硝酸钾、碳酸钠、硝酸银、硝酸钙和稀盐酸五瓶溶液。将其任意编号:A、B、C、D、E,进行两两混合,其现象如下表:
(1)试推断并写出五种溶液中溶质的化学式。
A ,B ,C ,D ,E 。
(2)写出有关反应的化学方程式。
A+E . B+E . 3.现有稀盐酸、稀硫酸、氢氧化钡、碳酸钠4瓶失去标签的溶液,分别编号为A、B、C、D。每次取少量溶液两两混合,所观察到的现象记录在下表中(“—”表示无明显现象;“↓”表示有沉淀生成;“↑”表示有气体生成)。由此推断4瓶溶液中的溶质的化学式分别为:
A. ;B. ;C. ;D.
写出上述实验过程的有关反应方程式:
A+B: C+D: . 1、硫在氧气中燃烧,火焰的颜色是 ,在空气中燃烧时火焰的颜色是 向通有CO2气体的蒸馏水中加入几滴石蕊试液,溶液会呈 _色原因是 _____
2、检验酒精中是否含有微量的水,可将 投入酒精中,若 证明酒精里含有水,化学方程式是 。
3、用试管取适量碳酸钠溶液,向试管中滴加酚酞试液,现象: 可见,碳酸钠的水溶液呈 性。
4、写出下列物质的化学式:
纯碱 生石灰 石灰石 甲烷 某化工场排放的污水中,常溶有某些对人体有害的物质。通过目测,初步认为可能含有Fe3+、Ba2+、Na+、OH-、CI-、CO32-、SO42-;为了进一步确认,进行实验检测:
(1)取污水仔细观察,呈无色、透明、均一状态。
(2)向取样的污水中,滴入稀硫酸,有大量白色沉淀产生,再加稀硝酸,白色沉淀不消失。
(3)用pH试纸测定污水的pH值,试纸显深蓝色。由此可知,该污水中,肯定含有离子是 。肯定没有的离子是 ,可能含有的离子是 。有一包白色粉末,可能由氯化银、碳酸钠、氢氧化镁、氯化钡、硫酸钠和硝酸钾中的某几种组成。为了鉴定其成分,实验如下:
(1)将少量粉末放入足量水中,搅拌、静置、过滤、得白色沉淀和无色滤液。
(2)向所得沉淀中加入足量稀硝酸,沉淀全部溶解,但无气体产生。
(3)向滤液中滴加硝酸银溶液,有白色沉淀生成,加入足量稀硝酸,沉淀不溶解。试根据以上现象推断该白色粉末中一定含有 ;一定没有 ;可能含有 .(填化学式)1.18.6克NaOH和Na2CO3的混合物中加入100克稀盐酸刚好反应,产生气体4.4克。求:
⑴18.6克混合物中含Na2CO3多少。
⑵所加盐酸溶液的质量分数是多少。
⑶反应后所得溶液的质量分数又是多少。2、酸碱盐的溶解性的:溶的打“√”不溶的打“╳”
NaOH CuSO4 KNO3 CaCO3
BaSO4 AgNO3 Cu(OH)2 FeCl3 BaCO3 Na2SO4 Na2CO3 MgCl2
KCl Ca(OH)2 Al2(SO4)3 ZnSO4 FeSO4 CuSO4 AgCl Mg(OH)21、各举一例:
化合反应: ; 分解反应: ;
置换反应: ; 复分解反应: ; 2、写出下列能反应的化学方式 ①用盐酸除铁锈 ②铜和稀硫酸酸制氢气 ③用氢氧化铝的药品中和胃酸 ④氢氧化钠放在空气中变质 ⑤铁与稀硫酸反应 ⑥碳酸钠与盐酸混合 ⑦氧化铜与稀硫酸 ⑨盐酸滴入硝酸银 ⑧氢氧化钠溶液加入稀硫酸 ⑩硫酸滴入氯化钡溶液 9.某未知溶液,其实验程序和实验现象如下: 写出 A、B、C、D的化式:
A, ; B ;
C D . 1.写出下列反应的化学方程式。
⑴氢氧化钾溶液中通入二氧化碳气体
⑵氢氧化钠溶液与硝酸铜溶液反应
⑶硫酸铁溶液中滴入氢氧化钠溶液
⑷SO3气体与NaOH溶液反应 2.现有13.3克已部分变质的NaOH,将该固体加到100克某盐酸溶液中,刚好反应,并产生2.2克气体。求:
⑴原固体中NaOH的质量分数。
⑵反应所用盐酸溶液的质量分数。
(1)Fe(过量)、Cu(OH)2、H2SO4 (2)Zn、AgNO3(过量) 、Cu(NO3)2
(3)Fe(过量)、Cu(NO3)2、AgNO3在各种物质里加水搅拌,待充分反应后,过滤,滤纸上有一种金属的是 ;有两种金属的是 ;有三种金属的是 ;(填序号)2.有失去标签的硝酸钾、碳酸钠、硝酸银、硝酸钙和稀盐酸五瓶溶液。将其任意编号:A、B、C、D、E,进行两两混合,其现象如下表:
(1)试推断并写出五种溶液中溶质的化学式。
A ,B ,C ,D ,E 。
(2)写出有关反应的化学方程式。
A+E . B+E . 3.现有稀盐酸、稀硫酸、氢氧化钡、碳酸钠4瓶失去标签的溶液,分别编号为A、B、C、D。每次取少量溶液两两混合,所观察到的现象记录在下表中(“—”表示无明显现象;“↓”表示有沉淀生成;“↑”表示有气体生成)。由此推断4瓶溶液中的溶质的化学式分别为:
A. ;B. ;C. ;D.
写出上述实验过程的有关反应方程式:
A+B: C+D: . 1、硫在氧气中燃烧,火焰的颜色是 ,在空气中燃烧时火焰的颜色是 向通有CO2气体的蒸馏水中加入几滴石蕊试液,溶液会呈 _色原因是 _____
2、检验酒精中是否含有微量的水,可将 投入酒精中,若 证明酒精里含有水,化学方程式是 。
3、用试管取适量碳酸钠溶液,向试管中滴加酚酞试液,现象: 可见,碳酸钠的水溶液呈 性。
4、写出下列物质的化学式:
纯碱 生石灰 石灰石 甲烷 某化工场排放的污水中,常溶有某些对人体有害的物质。通过目测,初步认为可能含有Fe3+、Ba2+、Na+、OH-、CI-、CO32-、SO42-;为了进一步确认,进行实验检测:
(1)取污水仔细观察,呈无色、透明、均一状态。
(2)向取样的污水中,滴入稀硫酸,有大量白色沉淀产生,再加稀硝酸,白色沉淀不消失。
(3)用pH试纸测定污水的pH值,试纸显深蓝色。由此可知,该污水中,肯定含有离子是 。肯定没有的离子是 ,可能含有的离子是 。有一包白色粉末,可能由氯化银、碳酸钠、氢氧化镁、氯化钡、硫酸钠和硝酸钾中的某几种组成。为了鉴定其成分,实验如下:
(1)将少量粉末放入足量水中,搅拌、静置、过滤、得白色沉淀和无色滤液。
(2)向所得沉淀中加入足量稀硝酸,沉淀全部溶解,但无气体产生。
(3)向滤液中滴加硝酸银溶液,有白色沉淀生成,加入足量稀硝酸,沉淀不溶解。试根据以上现象推断该白色粉末中一定含有 ;一定没有 ;可能含有 .(填化学式)1.18.6克NaOH和Na2CO3的混合物中加入100克稀盐酸刚好反应,产生气体4.4克。求:
⑴18.6克混合物中含Na2CO3多少。
⑵所加盐酸溶液的质量分数是多少。
⑶反应后所得溶液的质量分数又是多少。2、酸碱盐的溶解性的:溶的打“√”不溶的打“╳”
NaOH CuSO4 KNO3 CaCO3
BaSO4 AgNO3 Cu(OH)2 FeCl3 BaCO3 Na2SO4 Na2CO3 MgCl2
KCl Ca(OH)2 Al2(SO4)3 ZnSO4 FeSO4 CuSO4 AgCl Mg(OH)21、各举一例:
化合反应: ; 分解反应: ;
置换反应: ; 复分解反应: ; 2、写出下列能反应的化学方式 ①用盐酸除铁锈 ②铜和稀硫酸酸制氢气 ③用氢氧化铝的药品中和胃酸 ④氢氧化钠放在空气中变质 ⑤铁与稀硫酸反应 ⑥碳酸钠与盐酸混合 ⑦氧化铜与稀硫酸 ⑨盐酸滴入硝酸银 ⑧氢氧化钠溶液加入稀硫酸 ⑩硫酸滴入氯化钡溶液 9.某未知溶液,其实验程序和实验现象如下: 写出 A、B、C、D的化式:
A, ; B ;
C D . 1.写出下列反应的化学方程式。
⑴氢氧化钾溶液中通入二氧化碳气体
⑵氢氧化钠溶液与硝酸铜溶液反应
⑶硫酸铁溶液中滴入氢氧化钠溶液
⑷SO3气体与NaOH溶液反应 2.现有13.3克已部分变质的NaOH,将该固体加到100克某盐酸溶液中,刚好反应,并产生2.2克气体。求:
⑴原固体中NaOH的质量分数。
⑵反应所用盐酸溶液的质量分数。
