第二章复习[下学期]
图片预览










文档简介
课件51张PPT。 第一节
物质的分类和利用------物质分类的方法一、物质的分类方法:
(一)根据纯净物的 物理 性质不同。
如 颜色 、 状态 、 气味 , 硬度 、 密度 、 溶解性 等,对纯净物进行分类。
(二)根据纯净物的 化学 性质不同,如可燃性、氧化性,还原性等,对纯净物进行分类。
(三)根据纯净物的 组成 、 用途 的不同,可将纯净物进行 二、常见物质的分类:
(一)、物质可分为 纯净物 和 混合物 。
1.纯净物:由 一种物质 组成的物质。
2.混合物:由 两种或两种 以上的物质混合而成。
3.纯净物和混合物判断的依据:物质是否由一种物质组成。(绝对纯净的物质是没有的)
(二)、纯净物根据 元素组成 不同,可分为 单质 和 化合物 两大类。
1.单质:由 一种元素 组成的纯净物。如氧气、氮气、铁、硫等。
注意:由同种元素组成的物质,可能是单质,也可能是混合物。
1.单质按性质不同分 金属 和 非金属 :
金属如铁,铜、镁等; 非金属如:氧气、碳、硫等。
注意点:(1)金属一定能导电、导热,但能导电导热
的单质不一定是金属。如非金属石墨也能导电,
也能导热。(2)金属在常温下,除汞是液态外,
一般都是固态。非金属在常温,
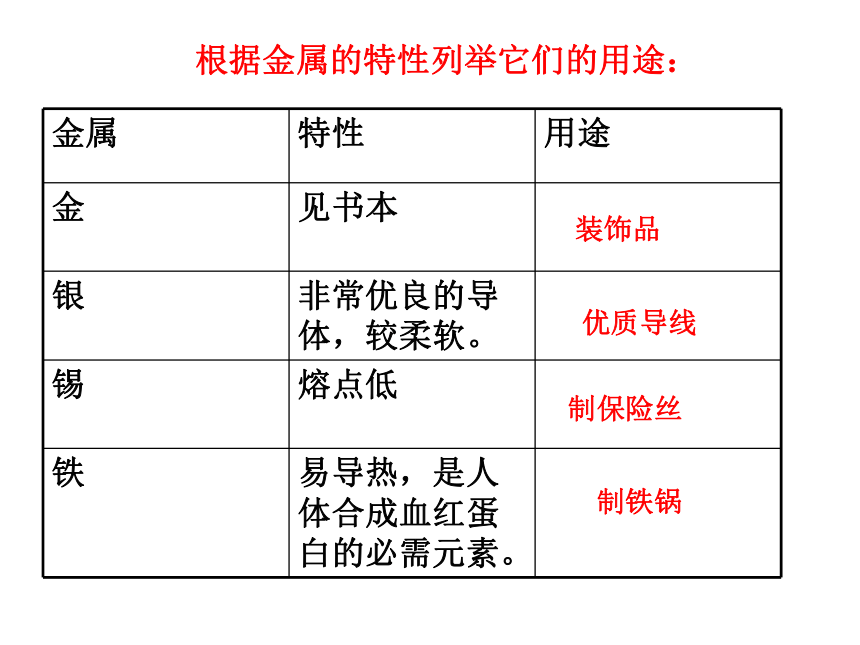
除溴是液态外,一般都是气态或固态 。装饰品优质导线制保险丝制铁锅根据金属的特性列举它们的用途:2.化合物:由 两种或两种以上的元素 组成的纯净物。如水、硫酸、烧碱、食盐等。
化合物可分为: 有机化合物 和 无机化合物 。
2.(1) 有机化合物:含 碳 的化合物,简称有机物。
注意:a.有机化合物一定含有碳元素.但含有碳元素的化合物不一定是有机化合物,例如CO、CO2、H2CO3、Na2CO3 等碳酸盐就属于无机化合物。
b.最简单的有机物是甲烷(CH4)。
2.2 无机化合物:不含碳元素 的化合物。但包括CO、CO2、H2CO3、Na2CO3 等碳酸盐。
?
(三)、无机化合物可分为: 氧化物 、 酸 、 碱 和 盐 。
1.1 氧化物:由 两种元素 组成.其中一种是 氧元素 的化合物。
氧化物可分为:氧化物按元素组成分 金属氧化物 和 非金属氧化物 :
金属氧化物如CuO、Fe2O3、CaO、MgO等。 非金属氧化物如CO、CO2、H2O、SO2等。
1.2 酸:电离出的阳离子 全部是氢离子 的化合物。
1.3 碱:电解质电离出的阴离子 全部是氢氧根离子 的化合物。
1.4 盐:由 金属 (或铵根)阳离子和 酸根 阴离子组成的化合物。
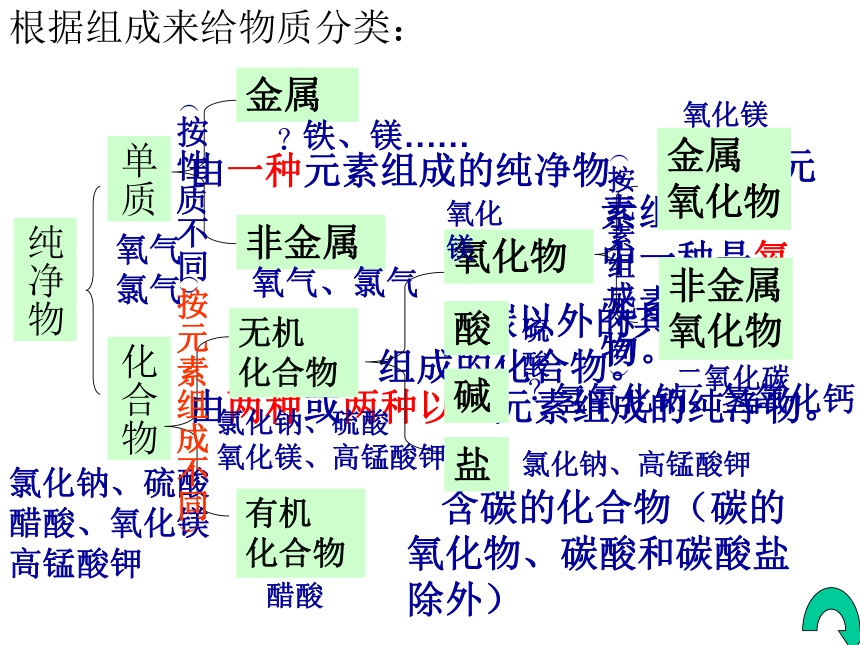
根据组成来给物质分类:纯净物单质化合物金属非金属无机
化合物有机
化合物氧化物酸碱盐 由两种元素组成,其中一种是氧元素的化合物。金属
氧化物非金属
氧化物氧气
氯气氯化钠、硫酸
醋酸、氧化镁
高锰酸钾氧气、氯气?铁、镁……氯化钠、硫酸
氧化镁、高锰酸钾醋酸氧化镁硫酸氯化钠、高锰酸钾?氢氧化钠、氢氧化钙氧化镁二氧化碳(按性质不同)(按元素组成不同)(按元素组成不同)1、下列物质中属于混合物的是( )
A、蒸馏水
B、氯酸钾和二氧化锰混合加热完全反应后试管中剩余物质
C、含铁70%的三氧化二铁样品
D、硫酸氢钠2、下列物质中前者包含后者是的( )
A、纯净物、混合物
B、单质、纯净物
C、化合物、氧化物
D、酸、盐BC3、填表4、下列物质中前者是化合物后者是混合物的是( )
A、蒸馏水、三氧化二铝
B、冰水混合物、空气
C、可口可乐、纯净水 D、石油、海水BNa2CO3Ca(OH)2Ca OCH3PO4NaOH盐碱氧化物单质酸盐碱 5.有一种物质M,经测定是由碳元素组成,则物质M属于( )
A、一定是单质
B、一定是化合物
C、一定是混合物
D、一定不是化合物D6.在下列几种物质中,从物质的组成分析其中和另外三种物质不相同的是( )
A.四氧化三铁 B.河水 C.稀盐酸
D.高锰酸钾制氧气后的剩余物7.有浓盐酸、硫酸铜、氯化铁三种溶液,可以把它们区别开的性质是( )
A.状态 B.气味
C.颜色 D.以上三者都可区别AC8.有下列六种物质:①纯净的空气 ②氮气 ③硫磺 ④矿泉水 ⑤氯酸钾 ⑥黄酒,其中属于混合物的有 ;属于纯净物的有 。 ① ④ ⑥ ② ③ ⑤9.在下列物质或性质中,不可能将CO和CO2区别开的是( )
A.溶解性 B.可燃性
C.石灰水 D.气味 D 第二节
物质的转化规律一、单质、氧化物、酸、碱、盐各类物质的相互关系金属碱CaO+H2O==2Ca(OH)2Ca(OH)2+2HCl==CaCl2+2H2OO2H2O HCl 常见无机物间相互关系一、单质、氧化物、酸、碱、盐各类物质的相互关系两条纵线一、单质、氧化物、酸、碱、盐各类物质的相互关系非金属盐CO2+H2O==H2CO3O2H2OCa(OH)2一、单质、氧化物、酸、碱、盐各类物质的相互关系金属碱非金属盐两条纵线四条横线一、单质、氧化物、酸、碱、盐各类物质的相互关系金属碱非金属盐 无氧酸盐
NaOH+HCl==盐+水含氧酸盐新盐+新盐NaCl+AgNO3==2NaCl
CaSiO3
NaCl+H2O
一、单质、氧化物、酸、碱、盐各类物质的相互关系金属碱非金属盐两条纵线四条横线四条交叉斜线一、单质、氧化物、酸、碱、盐各类物质的相互关系金属碱非金属盐两条纵线四条横线四条交叉斜线两条弯线一、单质、氧化物、酸、碱、盐各类物质的相互关系金属碱非金属盐盐 + 水CuO + H2SO4==盐 + 水CO2 + Ca(OH)2 ==2NaOH+CuSO4==H2SO4 + BaCl2==CuSO4 + H2O新碱 + 新盐
新酸 + 新盐
第三节
常见的材料一、单质、氧化物、酸、碱、盐各类物质的相互关系金属碱非金属盐盐 + 氢气金属+新盐
Zn +2 HCl==Fe + CuSO4=Cu + FeSO4讨论:设计制备ZnSO4 的4种方法。Zn + H2SO4 ===== ZnSO4 + H2↑
ZnO + H2SO4 ===== ZnSO4 + H2O
Zn(OH)2 + H2SO4 ===== ZnSO4 + 2H2O
ZnCO3 + H2SO4 ==== ZnSO4 + CO2↑ + H2O
(一)、常见的材料:金属材料(合金材料)、 无机非金属材料 以及 有机合成材料 。
1.合金是指两种或两种以上的金属(或非金属)熔合在一起具有金属特性的物质,大多数的金属材料实际是合金,钢是最常见、应用较广的一种合金。
(1)铁锈蚀条件:铁与氧气和水等物质相互作用。
(2)防止铁生锈的方法:
①使铁制品隔绝空气或隔绝水,保持铁制品表面干燥和洁净或在铁制品表面涂一层保护膜。如刷油漆,涂油、电镀、烤蓝等。
②改变铁的组成、结构,制成合金钢,如不锈钢。 2.常见的三大无机非金属材料为 水泥 、 玻璃 和 陶瓷 。
(1) 水泥:晋通水泥是由石灰石与黏土混在一起在炉中煅烧成熟料后加石膏磨细而成。
(2) 玻璃:普通玻璃是将石英和石灰石等经过配料、熔化、成型、退火等工序制成的。
(3) 陶瓷:用天然的硅酸盐和其他矿物原料制成,具有耐水、耐酸碱和绝缘性好等优点。
(4) 红色玻璃中加了氧化亚铜(Cu2O),在蓝色玻璃中加的 是氧化钴(Co2O3)。
3.三大有机合成材料为 合成塑料 、 合成纤维 和 合成橡胶 。
材料的发展:
1.根据人类在不同时期的材料发展情况,可将人类的历史分为旧石器时代、新石器时代、铜器时代、青铜器时代、铁器时代、新材料时代。
2.新型材料是指那些新出现或正在发展中的、具有优异特性和功能并能满足技术进步所需要的材料,如光电子信息材料、先进复合材料、超级陶瓷材料、新型金属材料、新型高分子材料、超导材料、纳米材料等。
金属的冶炼
1.金属冶炼主要是指将金属氧化物转化为金属的过程。在金属氧化物中加入还原剂,夺取金属氧化物中的氧,从而使其还原成全属单质。
2.可以作还原剂的物质主要有 碳 、 一氧化碳 和 氢气 。 铜在自然界中主要以孔雀石Cu2(OH)2CO3的形式存在思路①②叙述现象炼铜还
原
剂注意:这个反应要除尾气。
用点燃的方法除尾气金属冶炼的原理:与还原剂共热C、H2、CO1、还原法2、置换法活泼金属比盐中金属活泼实验中的注意问题:装置上:
1、试管口略向下倾斜。
2、导管要伸到试管底部。操作上:
1、实验前,氢气先通,酒精灯后点。
2、实验完毕后,酒精灯先熄,氢气后撤。(口诀:氢、灯、灯、氢)(这个反应是炼铁的原理)注意:这个反应要除尾气。用点燃的方法除尾气炼铁1、指出下列物质中,哪些是混合物,哪些是纯净物?
(1)洁净的空气(2)纯净的盐酸
(3)矿泉水 (4)蒸馏水
(5) 液态空气 (6)液态氧
(7)加热高锰酸钾制取氧气后的剩余物
练习一2、现有(1)氧气(2)氧化镁(3)氮气
(4)二氧化碳(5)铁(6)红磷
(7)氯化钠(8)蓝矾(9)水
(10)氦气 (写出化学式)
其中属于单质的是( )
属于金属单质的是( )
属于非金属单质是( )
属于化合物的是 ( )1、3、5、6、1051、3、6、2、4、7、8、93、下列各组物质中,全都是氧化物的是( )
CO CaO P2O5
SO2 H2SO4 NO2
H2CO3 NaOH H2O
H3PO4 KOH CuSO41、100吨含Fe2O3的质量分数为85%的铁矿石中,可炼出含铁96%的生铁多少吨?2、下列物质的转变,不能由一步反应实现的是 ( )
A、SO3→H2SO4 B、Ca(OH)2 →NaOH
C、CuO →Cu(OH)2 D、CaCl2 →CaCO3练习二4、现有H、O、S、Cu四种元素,请按照下列要求写出相应物质的化学式:
非金属氧化物( )
金属氧化物 ( )
酸( ) 碱( )盐( ) 结晶水合物( )3、煤中含有杂质硫等,燃烧后的产物污染环境。一般将其通过烧碱
溶液吸收而除去,所发生的化学方程式是_____________________。
4. Ba2+有毒,但对胃作X光造影时,BaSO4常用作钡餐而不造成中毒,
这是因为_____________________________; 若用BaCO3代替BaSO4
将发生中毒,这是因为_____________________________________。
5、要除去硝酸钠溶液中含有的少量氯化钠和氯化钡杂质,需依次加入哪一组物质 ( )
A、AgNO3、稀H2SO4 B、稀 H2SO4、 AgNO3
C、K2SO4、 AgNO3 D、Na2SO4、AgNO36、某化学实验室有甲、乙两个药品橱,其中甲橱已存放铜、氢氧化钠溶液。乙橱是空橱。现还有A、碳酸钙;B、稀硫酸;C、锌 D、氧化铜;E、浓盐酸 。 请你指出它们应分别存放入哪个橱中?
(用编号填写)
甲橱:_____________________________________;
乙橱:_____________________________________。
7、上题中,甲、乙两橱中的物质两两反应可以发生的化学反应有( )
A、6个 B、8个 C、10个 D、11个 8、乙醇是以高梁、玉米、薯类等为原料,经发酵、蒸馏而制得,属于可再生能源。在汽油中加入适量乙醇作为汽油燃料,可节省石油资源,减少汽车尾气的污染。2001年4月2日国家技术监督局发布《车用乙醇汽油》国家标准,并于同年4月15日开始实施。乙醇(C2H5OH)完全燃烧时生成CO2和H2O。如果氧气不充足,乙醇燃烧可能还有CO生成。现用以下装置进行实验,确证乙醇燃烧产物中有CO、CO2和H2O。
请回答下列问题:(1)能确证产物中有H2O的现象是 ▲ ;能确证产物中有CO的现象 ▲ _、 ▲ 。(2)实验时,可观察到装置B中石灰水变浑浊,D中石灰水无变化。B装置的作用是 ▲ ;C装置的作用是 ▲ ;D装置的作用是 ▲ 。
(3)1000克乙醇完全燃烧时能产生 ▲ 克的二氧化碳。 无水硫酸铜 澄清石灰水 氢氧化钠 澄清石灰水 澄清石灰水A B C D E F
9、课题式学习是研究性学习的一种方式,其基本学习模式为:
提出问题 → 确定研究方案 → 解决问题 → 总结和评价
某校研究性学习小组的同学在“一氧化碳的化学性质”的学习中,
设计了证明CO具有还原性的实验装置(如图甲),根据其研究过程
请你回答下列问题:
(1)实验过程中,洗气瓶A中的实验现象 。
(2)小余同学认为此装置有待优化,如尾气可先储存在瓶内,然后再处理。如图乙是他设计的贮气瓶,尾气应从 (选a、b填空)口通入。
(3)小徐同学质疑:CO能否使澄清石灰水变浑浊?因此进行设计:在CO通入CuO之前先通过澄清石灰水(即在盛CuO的硬质玻璃管的左端再接入一个盛澄清石灰水的洗气 瓶),来确定CO能否使澄清石灰水变浑浊。请判断小徐的设计是否有必要,并说明理由10、双氧水是过氧化氢(H2O2)的水溶液,常用于消毒、漂白等。实验室也常用它来制取氧气,反应的化学方程式为2H2O2 MnO2 2H2O + O2 。用这种方法制得的氧气中往往含有少量的水蒸气。欲制得干燥的氧气。两位同学分别设计了如图甲、乙所示的实验装置 (A中盛有MnO2、 B中盛有浓H2SO4、 C中盛有无水CuSO4)。
装置B中浓H2SO4的作用是___________。你认为_______(填“甲”或“乙”)装置较为合理。
11、六朝古都南京的地铁建设已经破土动工,考古兴起小组为了研究从地铁建设工地出土的文物,对两件文物的表面物质A和B进行了如图示的实验:
A.请你根据上图实验现象推断下列物质的化学式:B ;E ;F 。
B.写出下列转化的化学方程式:
C→D ;
E→H+1 ;
J+K→L 。
C.在博物馆里很少见到由J制造的完好文物,原因是什么?
物质的分类和利用------物质分类的方法一、物质的分类方法:
(一)根据纯净物的 物理 性质不同。
如 颜色 、 状态 、 气味 , 硬度 、 密度 、 溶解性 等,对纯净物进行分类。
(二)根据纯净物的 化学 性质不同,如可燃性、氧化性,还原性等,对纯净物进行分类。
(三)根据纯净物的 组成 、 用途 的不同,可将纯净物进行 二、常见物质的分类:
(一)、物质可分为 纯净物 和 混合物 。
1.纯净物:由 一种物质 组成的物质。
2.混合物:由 两种或两种 以上的物质混合而成。
3.纯净物和混合物判断的依据:物质是否由一种物质组成。(绝对纯净的物质是没有的)
(二)、纯净物根据 元素组成 不同,可分为 单质 和 化合物 两大类。
1.单质:由 一种元素 组成的纯净物。如氧气、氮气、铁、硫等。
注意:由同种元素组成的物质,可能是单质,也可能是混合物。
1.单质按性质不同分 金属 和 非金属 :
金属如铁,铜、镁等; 非金属如:氧气、碳、硫等。
注意点:(1)金属一定能导电、导热,但能导电导热
的单质不一定是金属。如非金属石墨也能导电,
也能导热。(2)金属在常温下,除汞是液态外,
一般都是固态。非金属在常温,
除溴是液态外,一般都是气态或固态 。装饰品优质导线制保险丝制铁锅根据金属的特性列举它们的用途:2.化合物:由 两种或两种以上的元素 组成的纯净物。如水、硫酸、烧碱、食盐等。
化合物可分为: 有机化合物 和 无机化合物 。
2.(1) 有机化合物:含 碳 的化合物,简称有机物。
注意:a.有机化合物一定含有碳元素.但含有碳元素的化合物不一定是有机化合物,例如CO、CO2、H2CO3、Na2CO3 等碳酸盐就属于无机化合物。
b.最简单的有机物是甲烷(CH4)。
2.2 无机化合物:不含碳元素 的化合物。但包括CO、CO2、H2CO3、Na2CO3 等碳酸盐。
?
(三)、无机化合物可分为: 氧化物 、 酸 、 碱 和 盐 。
1.1 氧化物:由 两种元素 组成.其中一种是 氧元素 的化合物。
氧化物可分为:氧化物按元素组成分 金属氧化物 和 非金属氧化物 :
金属氧化物如CuO、Fe2O3、CaO、MgO等。 非金属氧化物如CO、CO2、H2O、SO2等。
1.2 酸:电离出的阳离子 全部是氢离子 的化合物。
1.3 碱:电解质电离出的阴离子 全部是氢氧根离子 的化合物。
1.4 盐:由 金属 (或铵根)阳离子和 酸根 阴离子组成的化合物。
根据组成来给物质分类:纯净物单质化合物金属非金属无机
化合物有机
化合物氧化物酸碱盐 由两种元素组成,其中一种是氧元素的化合物。金属
氧化物非金属
氧化物氧气
氯气氯化钠、硫酸
醋酸、氧化镁
高锰酸钾氧气、氯气?铁、镁……氯化钠、硫酸
氧化镁、高锰酸钾醋酸氧化镁硫酸氯化钠、高锰酸钾?氢氧化钠、氢氧化钙氧化镁二氧化碳(按性质不同)(按元素组成不同)(按元素组成不同)1、下列物质中属于混合物的是( )
A、蒸馏水
B、氯酸钾和二氧化锰混合加热完全反应后试管中剩余物质
C、含铁70%的三氧化二铁样品
D、硫酸氢钠2、下列物质中前者包含后者是的( )
A、纯净物、混合物
B、单质、纯净物
C、化合物、氧化物
D、酸、盐BC3、填表4、下列物质中前者是化合物后者是混合物的是( )
A、蒸馏水、三氧化二铝
B、冰水混合物、空气
C、可口可乐、纯净水 D、石油、海水BNa2CO3Ca(OH)2Ca OCH3PO4NaOH盐碱氧化物单质酸盐碱 5.有一种物质M,经测定是由碳元素组成,则物质M属于( )
A、一定是单质
B、一定是化合物
C、一定是混合物
D、一定不是化合物D6.在下列几种物质中,从物质的组成分析其中和另外三种物质不相同的是( )
A.四氧化三铁 B.河水 C.稀盐酸
D.高锰酸钾制氧气后的剩余物7.有浓盐酸、硫酸铜、氯化铁三种溶液,可以把它们区别开的性质是( )
A.状态 B.气味
C.颜色 D.以上三者都可区别AC8.有下列六种物质:①纯净的空气 ②氮气 ③硫磺 ④矿泉水 ⑤氯酸钾 ⑥黄酒,其中属于混合物的有 ;属于纯净物的有 。 ① ④ ⑥ ② ③ ⑤9.在下列物质或性质中,不可能将CO和CO2区别开的是( )
A.溶解性 B.可燃性
C.石灰水 D.气味 D 第二节
物质的转化规律一、单质、氧化物、酸、碱、盐各类物质的相互关系金属碱CaO+H2O==2Ca(OH)2Ca(OH)2+2HCl==CaCl2+2H2OO2H2O HCl 常见无机物间相互关系一、单质、氧化物、酸、碱、盐各类物质的相互关系两条纵线一、单质、氧化物、酸、碱、盐各类物质的相互关系非金属盐CO2+H2O==H2CO3O2H2OCa(OH)2一、单质、氧化物、酸、碱、盐各类物质的相互关系金属碱非金属盐两条纵线四条横线一、单质、氧化物、酸、碱、盐各类物质的相互关系金属碱非金属盐 无氧酸盐
NaOH+HCl==盐+水含氧酸盐新盐+新盐NaCl+AgNO3==2NaCl
CaSiO3
NaCl+H2O
一、单质、氧化物、酸、碱、盐各类物质的相互关系金属碱非金属盐两条纵线四条横线四条交叉斜线一、单质、氧化物、酸、碱、盐各类物质的相互关系金属碱非金属盐两条纵线四条横线四条交叉斜线两条弯线一、单质、氧化物、酸、碱、盐各类物质的相互关系金属碱非金属盐盐 + 水CuO + H2SO4==盐 + 水CO2 + Ca(OH)2 ==2NaOH+CuSO4==H2SO4 + BaCl2==CuSO4 + H2O新碱 + 新盐
新酸 + 新盐
第三节
常见的材料一、单质、氧化物、酸、碱、盐各类物质的相互关系金属碱非金属盐盐 + 氢气金属+新盐
Zn +2 HCl==Fe + CuSO4=Cu + FeSO4讨论:设计制备ZnSO4 的4种方法。Zn + H2SO4 ===== ZnSO4 + H2↑
ZnO + H2SO4 ===== ZnSO4 + H2O
Zn(OH)2 + H2SO4 ===== ZnSO4 + 2H2O
ZnCO3 + H2SO4 ==== ZnSO4 + CO2↑ + H2O
(一)、常见的材料:金属材料(合金材料)、 无机非金属材料 以及 有机合成材料 。
1.合金是指两种或两种以上的金属(或非金属)熔合在一起具有金属特性的物质,大多数的金属材料实际是合金,钢是最常见、应用较广的一种合金。
(1)铁锈蚀条件:铁与氧气和水等物质相互作用。
(2)防止铁生锈的方法:
①使铁制品隔绝空气或隔绝水,保持铁制品表面干燥和洁净或在铁制品表面涂一层保护膜。如刷油漆,涂油、电镀、烤蓝等。
②改变铁的组成、结构,制成合金钢,如不锈钢。 2.常见的三大无机非金属材料为 水泥 、 玻璃 和 陶瓷 。
(1) 水泥:晋通水泥是由石灰石与黏土混在一起在炉中煅烧成熟料后加石膏磨细而成。
(2) 玻璃:普通玻璃是将石英和石灰石等经过配料、熔化、成型、退火等工序制成的。
(3) 陶瓷:用天然的硅酸盐和其他矿物原料制成,具有耐水、耐酸碱和绝缘性好等优点。
(4) 红色玻璃中加了氧化亚铜(Cu2O),在蓝色玻璃中加的 是氧化钴(Co2O3)。
3.三大有机合成材料为 合成塑料 、 合成纤维 和 合成橡胶 。
材料的发展:
1.根据人类在不同时期的材料发展情况,可将人类的历史分为旧石器时代、新石器时代、铜器时代、青铜器时代、铁器时代、新材料时代。
2.新型材料是指那些新出现或正在发展中的、具有优异特性和功能并能满足技术进步所需要的材料,如光电子信息材料、先进复合材料、超级陶瓷材料、新型金属材料、新型高分子材料、超导材料、纳米材料等。
金属的冶炼
1.金属冶炼主要是指将金属氧化物转化为金属的过程。在金属氧化物中加入还原剂,夺取金属氧化物中的氧,从而使其还原成全属单质。
2.可以作还原剂的物质主要有 碳 、 一氧化碳 和 氢气 。 铜在自然界中主要以孔雀石Cu2(OH)2CO3的形式存在思路①②叙述现象炼铜还
原
剂注意:这个反应要除尾气。
用点燃的方法除尾气金属冶炼的原理:与还原剂共热C、H2、CO1、还原法2、置换法活泼金属比盐中金属活泼实验中的注意问题:装置上:
1、试管口略向下倾斜。
2、导管要伸到试管底部。操作上:
1、实验前,氢气先通,酒精灯后点。
2、实验完毕后,酒精灯先熄,氢气后撤。(口诀:氢、灯、灯、氢)(这个反应是炼铁的原理)注意:这个反应要除尾气。用点燃的方法除尾气炼铁1、指出下列物质中,哪些是混合物,哪些是纯净物?
(1)洁净的空气(2)纯净的盐酸
(3)矿泉水 (4)蒸馏水
(5) 液态空气 (6)液态氧
(7)加热高锰酸钾制取氧气后的剩余物
练习一2、现有(1)氧气(2)氧化镁(3)氮气
(4)二氧化碳(5)铁(6)红磷
(7)氯化钠(8)蓝矾(9)水
(10)氦气 (写出化学式)
其中属于单质的是( )
属于金属单质的是( )
属于非金属单质是( )
属于化合物的是 ( )1、3、5、6、1051、3、6、2、4、7、8、93、下列各组物质中,全都是氧化物的是( )
CO CaO P2O5
SO2 H2SO4 NO2
H2CO3 NaOH H2O
H3PO4 KOH CuSO41、100吨含Fe2O3的质量分数为85%的铁矿石中,可炼出含铁96%的生铁多少吨?2、下列物质的转变,不能由一步反应实现的是 ( )
A、SO3→H2SO4 B、Ca(OH)2 →NaOH
C、CuO →Cu(OH)2 D、CaCl2 →CaCO3练习二4、现有H、O、S、Cu四种元素,请按照下列要求写出相应物质的化学式:
非金属氧化物( )
金属氧化物 ( )
酸( ) 碱( )盐( ) 结晶水合物( )3、煤中含有杂质硫等,燃烧后的产物污染环境。一般将其通过烧碱
溶液吸收而除去,所发生的化学方程式是_____________________。
4. Ba2+有毒,但对胃作X光造影时,BaSO4常用作钡餐而不造成中毒,
这是因为_____________________________; 若用BaCO3代替BaSO4
将发生中毒,这是因为_____________________________________。
5、要除去硝酸钠溶液中含有的少量氯化钠和氯化钡杂质,需依次加入哪一组物质 ( )
A、AgNO3、稀H2SO4 B、稀 H2SO4、 AgNO3
C、K2SO4、 AgNO3 D、Na2SO4、AgNO36、某化学实验室有甲、乙两个药品橱,其中甲橱已存放铜、氢氧化钠溶液。乙橱是空橱。现还有A、碳酸钙;B、稀硫酸;C、锌 D、氧化铜;E、浓盐酸 。 请你指出它们应分别存放入哪个橱中?
(用编号填写)
甲橱:_____________________________________;
乙橱:_____________________________________。
7、上题中,甲、乙两橱中的物质两两反应可以发生的化学反应有( )
A、6个 B、8个 C、10个 D、11个 8、乙醇是以高梁、玉米、薯类等为原料,经发酵、蒸馏而制得,属于可再生能源。在汽油中加入适量乙醇作为汽油燃料,可节省石油资源,减少汽车尾气的污染。2001年4月2日国家技术监督局发布《车用乙醇汽油》国家标准,并于同年4月15日开始实施。乙醇(C2H5OH)完全燃烧时生成CO2和H2O。如果氧气不充足,乙醇燃烧可能还有CO生成。现用以下装置进行实验,确证乙醇燃烧产物中有CO、CO2和H2O。
请回答下列问题:(1)能确证产物中有H2O的现象是 ▲ ;能确证产物中有CO的现象 ▲ _、 ▲ 。(2)实验时,可观察到装置B中石灰水变浑浊,D中石灰水无变化。B装置的作用是 ▲ ;C装置的作用是 ▲ ;D装置的作用是 ▲ 。
(3)1000克乙醇完全燃烧时能产生 ▲ 克的二氧化碳。 无水硫酸铜 澄清石灰水 氢氧化钠 澄清石灰水 澄清石灰水A B C D E F
9、课题式学习是研究性学习的一种方式,其基本学习模式为:
提出问题 → 确定研究方案 → 解决问题 → 总结和评价
某校研究性学习小组的同学在“一氧化碳的化学性质”的学习中,
设计了证明CO具有还原性的实验装置(如图甲),根据其研究过程
请你回答下列问题:
(1)实验过程中,洗气瓶A中的实验现象 。
(2)小余同学认为此装置有待优化,如尾气可先储存在瓶内,然后再处理。如图乙是他设计的贮气瓶,尾气应从 (选a、b填空)口通入。
(3)小徐同学质疑:CO能否使澄清石灰水变浑浊?因此进行设计:在CO通入CuO之前先通过澄清石灰水(即在盛CuO的硬质玻璃管的左端再接入一个盛澄清石灰水的洗气 瓶),来确定CO能否使澄清石灰水变浑浊。请判断小徐的设计是否有必要,并说明理由10、双氧水是过氧化氢(H2O2)的水溶液,常用于消毒、漂白等。实验室也常用它来制取氧气,反应的化学方程式为2H2O2 MnO2 2H2O + O2 。用这种方法制得的氧气中往往含有少量的水蒸气。欲制得干燥的氧气。两位同学分别设计了如图甲、乙所示的实验装置 (A中盛有MnO2、 B中盛有浓H2SO4、 C中盛有无水CuSO4)。
装置B中浓H2SO4的作用是___________。你认为_______(填“甲”或“乙”)装置较为合理。
11、六朝古都南京的地铁建设已经破土动工,考古兴起小组为了研究从地铁建设工地出土的文物,对两件文物的表面物质A和B进行了如图示的实验:
A.请你根据上图实验现象推断下列物质的化学式:B ;E ;F 。
B.写出下列转化的化学方程式:
C→D ;
E→H+1 ;
J+K→L 。
C.在博物馆里很少见到由J制造的完好文物,原因是什么?
同课章节目录
