2007年 中考复习 科学探究专题 化学实验(广东省深圳市罗湖区)
文档属性
| 名称 | 2007年 中考复习 科学探究专题 化学实验(广东省深圳市罗湖区) |  | |
| 格式 | rar | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2008-04-11 09:14:00 | ||
图片预览









文档简介
课件49张PPT。2007初三科学复习
科学探究专题 实验一、仪器识别和使用二、基本操作三、制备气体、检验、除杂化学实验考点◆注重科学探究能力(实验和实验设计35%)的考查四、几个重要的实验知识框架科学实验常见的仪器:量筒、胶头滴管、酒精灯、试管、
烧杯、集气瓶
基本操作:取药、收集气体、加热、过滤、
蒸发、配溶液、先后顺序检验氧气、二氧化碳检验酸碱性、稀释浓硫酸等等 注意安全制备气体:检验、鉴别、除杂几个重要的实验:设计实验探究原理、装置、步骤、收集、检验区别碱、鉴别CO32--
书写实验报告粗盐提纯本课教学目标 ◇对于知识与技能:梳理知识,提高实验技能和答题能力。 ◇对于过程与方法:培养学生实验和设计实验的科学探究能力,学习科学探究的方法。
◇对于情感态度与价值观:增强安全意识,珍爱生
命;树立环保意识,增强社会责任感;培养学生严谨求
实的科学态度。1、知道防范常见化学物质对人体的危害,如:一氧化碳、甲醇、苯、甲醛。
2、了解强酸、强碱的腐蚀性(使用注意事项)。
3、实验操作规范,确保安全;有污染的实验在
通风橱中进行。(微型实验可有效减少实验污染)
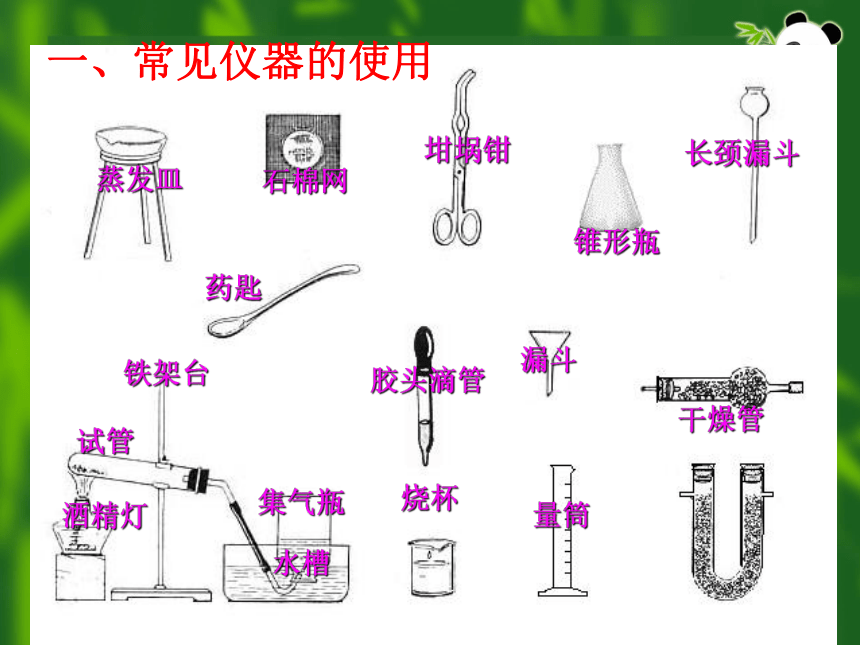
安全第一EX一、1认识图标药匙 石棉网蒸发皿坩埚钳 锥形瓶长颈漏斗干燥管漏斗量筒烧杯 胶头滴管铁架台试管酒精灯水槽集气瓶一、常见仪器的使用1、常用作少量物质的反应容器,或给少量液体或固体加热的仪器是 。
2、搅拌、过滤、蘸取液体时常用 。
3、向NaOH溶液中逐滴滴入盐酸 。
4、收集或贮存少量气体 。
5、取粉末状药品 。
6、溶液蒸发、浓缩和结晶 。
7、量取80mL的盐酸 。选择合适的仪器填空:试管玻璃棒胶头滴管集气瓶药匙或纸槽蒸发皿量筒 8、将锌粒加入试管 。
9、取18克NaCl固体 。
10、往酒精灯里添加酒精 。
11、盛硫磺在集气瓶中燃烧 。
12、拿到热的蒸发皿 。
13、使烧杯、烧瓶均匀受热 。
14、用于装配气体发生器,便于往装置中添加液体 。
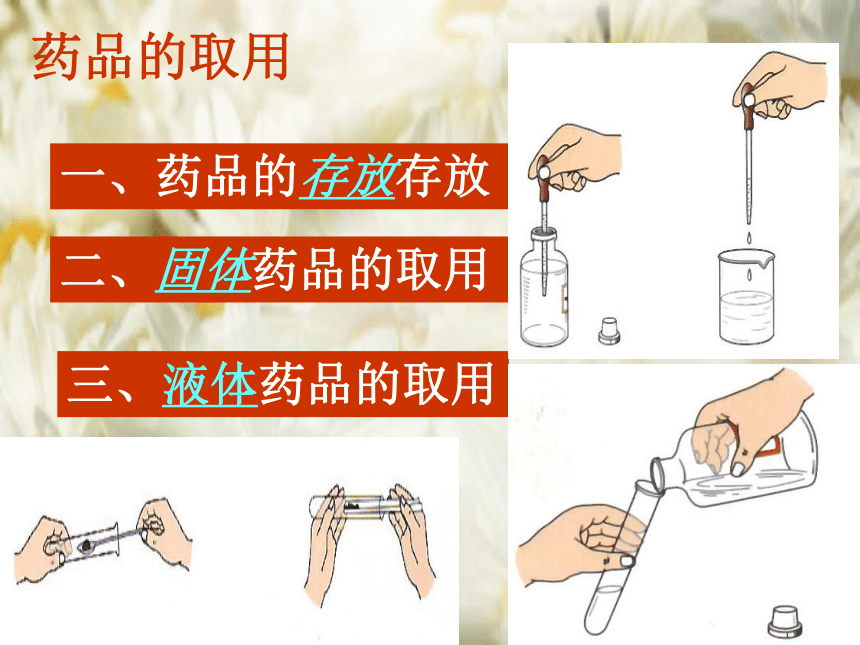
15、给较大量加热,较大量物质反应容器,过滤中用于承接滤液 。镊子天平漏斗燃烧匙坩埚钳石棉网长颈漏斗烧杯药品的取用一、药品的存放存放二、固体药品的取用三、液体药品的取用二、化学实验基本操作——
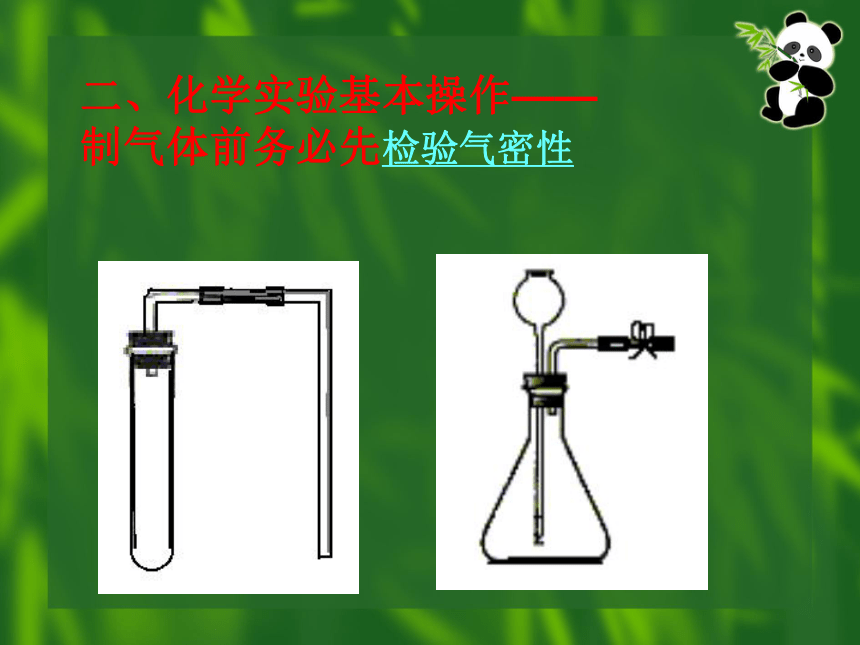
制气体前务必先检验气密性气密性的检查 导管的口端浸入水中,用双手掌紧握试管或烧瓶,内面的气体受热膨胀,导管口有气泡冒出,把手移开,道观内形成一段水柱。物质的加热:1、加热仪器:酒精灯酒精量:大于1/4小于2/3
火焰:外焰2、被加热仪器:直接加热仪器:试管、蒸发皿、燃烧匙间接加热仪器:烧杯、烧瓶3、固体加热:管口略朝下4、液体加热:管口与水平面成45度外焰、内焰、焰心,其中外焰温度最高。 5、使用酒精灯的三禁止:对燃、往燃灯中加酒精、嘴吹灭 化学实验基本操作——指错块状固体用玻璃棒蘸到 试纸上。视线沿水平方向缺棒没靠加热要点:应用内焰;1/3;拿长柄实验基本操作(1)扎实的基础(2)严谨的分析练习1:下图所示的实验操作与方法正确的是( )A【用品】托盘天平、烧杯、玻璃棒、药匙、量筒(10mL、100mL)、氯化钠。
实验步骤:计算称量溶解.
???????????????????????????????????????????????????????????????????????????????????????????
三、配溶液四、两种混合物分离操作
(1)过滤(P27图)
一贴:滤纸紧贴漏斗内壁
二低:①滤纸边缘稍低于漏斗口;②漏斗内液面低于滤纸边缘
三靠:①倾倒液体时烧杯口紧靠玻棒;②玻璃棒紧靠三层过滤纸;
③漏斗下端紧靠烧杯内壁
(2)蒸发:不断用玻璃棒搅拌;出现较多固体时,停止加热。重要实验粗盐提纯的步骤:溶解→过滤→蒸发。取药、加热、检查气密性、
氢气还原氧化铜、收集气体、
稀释浓硫酸、过滤、蒸发过 滤蒸 发熟记几个实验步骤的“先后”顺序:
4、铁丝在氧气中燃烧:先在瓶底装少量水或细沙 1、实验室制气体:先检查气密性 ,再装药。2、点燃可燃性气体:先验纯,再点燃。3、H2还原CuO实验:先通H2,再加热 。 5、用过滤分离混合物:
先溶解,再过滤。 6、稀释浓硫酸:
先装水,后倒酸。 学 会 归 纳 ①凡用固体加热制取气体的都选用高锰酸钾制O2装置(固固加热型); 凡用固体与液体反应且不需加热制气体的都选用双氧水制O2装置(固液不加热型)。 ②凡是给试管固体加热,都要先预热,试管口都应略向下倾斜。 ③凡是生成的气体难溶于水(不与水反应)的,都可用排水法收集。 凡是生成的气体密度比空气大的,都可用向上排空气法收集。 凡是生成的气体密度比空气小的,都可用向下排空气法收集。 实验中的规律:④凡是制气体实验时,先要检查装置的气密性,导管应露出橡皮塞1-2ml,铁夹应夹在距管口1/3处。 ⑤凡是用长颈漏斗制气体实验时,长颈漏斗的末端管口应插入液面下。 ⑥凡是点燃可燃性气体时,一定先要检验它的纯度。 ⑦凡是使用有毒气体做实验时,最后一定要处理尾气。 ⑧凡是使用还原性气体还原金属氧化物时,一定是“一通、二点、三灭、四停”
实验中的规律:实验中的规律:9、用洗气瓶除杂的连接:长进短出 用洗气瓶排水收集气体的连接:短进长出 用洗气瓶排空气收集气体的连接:密小则短进长出,密大则长进短出 10、实验除杂原则:先除其它,后除水蒸气 实验检验原则:先验水,后验其它 思考: 1、若所要收集的气体有毒且能溶于水,应该选择何种装置来收集此气体? 若气体密度大于空气密度,应从___端进;
若气体密度小于空气密度,应从 ___端进。左右医院给病人输氧时用到类似右图所示的装置。关于该装置,你认为:氧气钢瓶的出气口应该连接在a处还是b处?实验室要收集O2时,O2应从 端通入。若要用水将收集在装置的O2排出进行实验时,水应从_端流入。水BAA练习2: 写出下列反应的第一步操作
(1)使用石蕊试纸检验溶液的酸碱性
(2)点燃可燃性气体(如H2、CO等) 重要实验:稀释浓硫酸时,一定要将 沿着 缓慢地注入 中,并用玻璃棒不断 ,使产生的热 。 用洁净的玻璃棒蘸取待测液,滴在
PH试纸上。将试纸显示的颜色与标
准比色卡对照(在半分钟之内),
看与哪种颜色最接近,从而确定被
测试液的PH。根据PH便可判断溶液
的酸碱性强弱。五、1常见气体的检验方法:O2 ——
CO2 ——
H2O ——
CO H2 CH4 ——带火星的木条 复燃澄清的石灰水 浑浊无水硫酸铜 变蓝检验燃烧的产物注意:检验和验满操作不一样操 作现 象常见离子的检验H+
OH-
Cl-
SO42-
CO32-
石蕊、铁
石蕊
AgNO3 HNO3
Ba (NO3 )2 HNO3
HCl Ca(OH)2_
练习1、如何证明一瓶无色气体是CO2 ?
2、如何证明一瓶无色溶液是硫酸?
3、如何证明一瓶无色溶液是碳酸钠溶液?Ca(OH)2Ba (NO3 )2 HNO3HCl Ca(OH)2五、2物质鉴别 鉴别是指已知几种物质,根据物质的不同
特性,区分它们分别是什么。例如:
1)区分氧气、二氧化碳
2)区分盐酸和硫酸
3)区分氢氧化钠和氢氧化钙用带火星的木条用氯化钡用CO2 ( )或碳酸钠( )无色酚酞ABC装入C试管内的
液体是NaOH装入A试管内的 液体是NaCl装入B试管内的液体是H2SO4只用酚酞鉴别NaCl、H2SO4 、 NaOH六、常见气体的制备:反应原理反应装置气体收集气体检验(写化学方程式)(加热?)(密度、溶解性)(特性)实验步骤( ?)查、药、收、验满、放查气密性六、常见气体的制备:1、实验室制取氧气的步骤: “茶(查)、庄(装)、定、点、收、利(离)、息(熄)” “查”检查装置的气密性“装”盛装药品,连好装置 “定”试管固定在铁架台“点”点燃酒精灯进行加热 “收”收集气体“离”导管移离水面 “熄”熄灭酒精灯,停止加热。 2、用CO还原氧化铜的实验步骤: “一通、二点、三灭、四停、五处理” “一通”先通氢气,“二点”后点燃酒精灯进行加热; “三灭”实验完毕后,先熄灭酒精灯,“四停”等到室温时再停止通氢气;“五处理”处理尾气,防止CO污染环境。 比较下列几套装置:气体的制取—— ①发生装置②气体的收集
A装置适宜收集 气体;
B装置适宜收集 气体;
C装置适宜收集 气体;1.反应原理:Zn+H2SO4=ZnSO4+H2↑
CaCO3+2HCl=CaCl2+CO2↑+H2O
2H2O2 == 2H2O + O2 ↑ MnO2分解反应置换反应复分解反应 加热法气体不能收集CO2 只收集H2 2、反应装置:ABCED练习3:改正下列制取氢气装置中的错误。1、长颈漏斗的末端没有液封。
2、气体导出管过长。
3、氢气不能用向上排空气法收集H2指出图中存在的错误之处:实验操作顺序3.改正下列制取气体装置中的错误,说明原因。 制氧气 制氧气 制取CO2 试管口应略向下倾斜,应用酒精灯加热。
伸入试管内的导气管应刚露出胶塞 长颈漏斗应该插入液面以下。伸入反应容器中的导气管不宜过长。常用的气体的净化和干燥装置③气体的净化、转化与检验 [例] 、实验室用锌和盐酸反应来制取的氢气中常常混有少量的HCl气体和水蒸气,现用下面的装置除去HCl气体和水蒸气,装置如何连接? 回顾制取O2、H2、CO2等气体的实验,我们 (1)首先研究生成该气体的化学反应原理; (2)然后根据 和 选择并安装实验装置,而且一定要检查 ; (3)根据 确定气体的收集方法。[小结]实验室制气体的一般思路反应物性质 反应条件 装置的气密性 气体的性质 综合实验(探究、设计)综合实验的主要内容:
①气体的制取、净化、性质的组合;
②混合气体成分的验证;
③定性实验和定量实验的结合;几个重要的探究性实验(理解每个实验的目的和研究的方法。 )
(1)我们吸入的空气和呼出的气体有什么不同探究
(2)酸雨危害的探究
(3)金属活动性的探究
(4)铁生锈的探究
(5)酸、碱化学性质的探究
(6)粗盐提纯的探究
(7)区分盐酸盐、硫酸盐、碳酸盐的探究
(8)金属回收的探究探究1:桌上放了一瓶气体(如图所示),
纯净、无色无毒。请你用学过的知识进行探究:
该气体是什么气体?猜想:
步骤:
现象:
结论: 学会分析该气体是CO2书写实验报告
向瓶中注入石灰水,震荡石灰水变浑浊是CO2 [例] (04年南宁)某探究学习小组在帮助实验员整理化学试剂时, 发现 一个盛有无色溶液的试剂瓶,标签破损(如图所示). 已知它们是氯化钠、氢氧化钠、碳酸钠、 硫酸钠四种溶液中的一种.请你对该试剂作出猜想,并设计实验验证。
⑴猜想:这种试剂可能是 溶液,也可能是 溶液。
⑵实验验证。(要求写出操作、现象、结论)
。
碳酸钠硫酸钠综合性气体制备实验的设计?净化
装置干燥
装置收集
装置尾气处理
装置发生
装置(1)固 ? 气体 (2)固+液——气体(2)“长进短出” : CO2——NaOH溶液;石灰水(可检验)
HCl ——NaOH溶液;Ca(OH)2溶液;AgNO3溶液 (可检验)
H2O—— 浓H2SO4;固体NaOH;生石灰;氯化钙等;
无水CuSO4只检验(1)排水法(O2、H2);(2)向上排空气法(O2、CO2); (3)向下排空气法(H2)(1)点燃法(如CO) (2)吸收法
烧杯、集气瓶
基本操作:取药、收集气体、加热、过滤、
蒸发、配溶液、先后顺序检验氧气、二氧化碳检验酸碱性、稀释浓硫酸等等 注意安全制备气体:检验、鉴别、除杂几个重要的实验:设计实验探究原理、装置、步骤、收集、检验区别碱、鉴别CO32--
书写实验报告粗盐提纯本课教学目标 ◇对于知识与技能:梳理知识,提高实验技能和答题能力。 ◇对于过程与方法:培养学生实验和设计实验的科学探究能力,学习科学探究的方法。
◇对于情感态度与价值观:增强安全意识,珍爱生
命;树立环保意识,增强社会责任感;培养学生严谨求
实的科学态度。1、知道防范常见化学物质对人体的危害,如:一氧化碳、甲醇、苯、甲醛。
2、了解强酸、强碱的腐蚀性(使用注意事项)。
3、实验操作规范,确保安全;有污染的实验在
通风橱中进行。(微型实验可有效减少实验污染)
安全第一EX一、1认识图标药匙 石棉网蒸发皿坩埚钳 锥形瓶长颈漏斗干燥管漏斗量筒烧杯 胶头滴管铁架台试管酒精灯水槽集气瓶一、常见仪器的使用1、常用作少量物质的反应容器,或给少量液体或固体加热的仪器是 。
2、搅拌、过滤、蘸取液体时常用 。
3、向NaOH溶液中逐滴滴入盐酸 。
4、收集或贮存少量气体 。
5、取粉末状药品 。
6、溶液蒸发、浓缩和结晶 。
7、量取80mL的盐酸 。选择合适的仪器填空:试管玻璃棒胶头滴管集气瓶药匙或纸槽蒸发皿量筒 8、将锌粒加入试管 。
9、取18克NaCl固体 。
10、往酒精灯里添加酒精 。
11、盛硫磺在集气瓶中燃烧 。
12、拿到热的蒸发皿 。
13、使烧杯、烧瓶均匀受热 。
14、用于装配气体发生器,便于往装置中添加液体 。
15、给较大量加热,较大量物质反应容器,过滤中用于承接滤液 。镊子天平漏斗燃烧匙坩埚钳石棉网长颈漏斗烧杯药品的取用一、药品的存放存放二、固体药品的取用三、液体药品的取用二、化学实验基本操作——
制气体前务必先检验气密性气密性的检查 导管的口端浸入水中,用双手掌紧握试管或烧瓶,内面的气体受热膨胀,导管口有气泡冒出,把手移开,道观内形成一段水柱。物质的加热:1、加热仪器:酒精灯酒精量:大于1/4小于2/3
火焰:外焰2、被加热仪器:直接加热仪器:试管、蒸发皿、燃烧匙间接加热仪器:烧杯、烧瓶3、固体加热:管口略朝下4、液体加热:管口与水平面成45度外焰、内焰、焰心,其中外焰温度最高。 5、使用酒精灯的三禁止:对燃、往燃灯中加酒精、嘴吹灭 化学实验基本操作——指错块状固体用玻璃棒蘸到 试纸上。视线沿水平方向缺棒没靠加热要点:应用内焰;1/3;拿长柄实验基本操作(1)扎实的基础(2)严谨的分析练习1:下图所示的实验操作与方法正确的是( )A【用品】托盘天平、烧杯、玻璃棒、药匙、量筒(10mL、100mL)、氯化钠。
实验步骤:计算称量溶解.
???????????????????????????????????????????????????????????????????????????????????????????
三、配溶液四、两种混合物分离操作
(1)过滤(P27图)
一贴:滤纸紧贴漏斗内壁
二低:①滤纸边缘稍低于漏斗口;②漏斗内液面低于滤纸边缘
三靠:①倾倒液体时烧杯口紧靠玻棒;②玻璃棒紧靠三层过滤纸;
③漏斗下端紧靠烧杯内壁
(2)蒸发:不断用玻璃棒搅拌;出现较多固体时,停止加热。重要实验粗盐提纯的步骤:溶解→过滤→蒸发。取药、加热、检查气密性、
氢气还原氧化铜、收集气体、
稀释浓硫酸、过滤、蒸发过 滤蒸 发熟记几个实验步骤的“先后”顺序:
4、铁丝在氧气中燃烧:先在瓶底装少量水或细沙 1、实验室制气体:先检查气密性 ,再装药。2、点燃可燃性气体:先验纯,再点燃。3、H2还原CuO实验:先通H2,再加热 。 5、用过滤分离混合物:
先溶解,再过滤。 6、稀释浓硫酸:
先装水,后倒酸。 学 会 归 纳 ①凡用固体加热制取气体的都选用高锰酸钾制O2装置(固固加热型); 凡用固体与液体反应且不需加热制气体的都选用双氧水制O2装置(固液不加热型)。 ②凡是给试管固体加热,都要先预热,试管口都应略向下倾斜。 ③凡是生成的气体难溶于水(不与水反应)的,都可用排水法收集。 凡是生成的气体密度比空气大的,都可用向上排空气法收集。 凡是生成的气体密度比空气小的,都可用向下排空气法收集。 实验中的规律:④凡是制气体实验时,先要检查装置的气密性,导管应露出橡皮塞1-2ml,铁夹应夹在距管口1/3处。 ⑤凡是用长颈漏斗制气体实验时,长颈漏斗的末端管口应插入液面下。 ⑥凡是点燃可燃性气体时,一定先要检验它的纯度。 ⑦凡是使用有毒气体做实验时,最后一定要处理尾气。 ⑧凡是使用还原性气体还原金属氧化物时,一定是“一通、二点、三灭、四停”
实验中的规律:实验中的规律:9、用洗气瓶除杂的连接:长进短出 用洗气瓶排水收集气体的连接:短进长出 用洗气瓶排空气收集气体的连接:密小则短进长出,密大则长进短出 10、实验除杂原则:先除其它,后除水蒸气 实验检验原则:先验水,后验其它 思考: 1、若所要收集的气体有毒且能溶于水,应该选择何种装置来收集此气体? 若气体密度大于空气密度,应从___端进;
若气体密度小于空气密度,应从 ___端进。左右医院给病人输氧时用到类似右图所示的装置。关于该装置,你认为:氧气钢瓶的出气口应该连接在a处还是b处?实验室要收集O2时,O2应从 端通入。若要用水将收集在装置的O2排出进行实验时,水应从_端流入。水BAA练习2: 写出下列反应的第一步操作
(1)使用石蕊试纸检验溶液的酸碱性
(2)点燃可燃性气体(如H2、CO等) 重要实验:稀释浓硫酸时,一定要将 沿着 缓慢地注入 中,并用玻璃棒不断 ,使产生的热 。 用洁净的玻璃棒蘸取待测液,滴在
PH试纸上。将试纸显示的颜色与标
准比色卡对照(在半分钟之内),
看与哪种颜色最接近,从而确定被
测试液的PH。根据PH便可判断溶液
的酸碱性强弱。五、1常见气体的检验方法:O2 ——
CO2 ——
H2O ——
CO H2 CH4 ——带火星的木条 复燃澄清的石灰水 浑浊无水硫酸铜 变蓝检验燃烧的产物注意:检验和验满操作不一样操 作现 象常见离子的检验H+
OH-
Cl-
SO42-
CO32-
石蕊、铁
石蕊
AgNO3 HNO3
Ba (NO3 )2 HNO3
HCl Ca(OH)2_
练习1、如何证明一瓶无色气体是CO2 ?
2、如何证明一瓶无色溶液是硫酸?
3、如何证明一瓶无色溶液是碳酸钠溶液?Ca(OH)2Ba (NO3 )2 HNO3HCl Ca(OH)2五、2物质鉴别 鉴别是指已知几种物质,根据物质的不同
特性,区分它们分别是什么。例如:
1)区分氧气、二氧化碳
2)区分盐酸和硫酸
3)区分氢氧化钠和氢氧化钙用带火星的木条用氯化钡用CO2 ( )或碳酸钠( )无色酚酞ABC装入C试管内的
液体是NaOH装入A试管内的 液体是NaCl装入B试管内的液体是H2SO4只用酚酞鉴别NaCl、H2SO4 、 NaOH六、常见气体的制备:反应原理反应装置气体收集气体检验(写化学方程式)(加热?)(密度、溶解性)(特性)实验步骤( ?)查、药、收、验满、放查气密性六、常见气体的制备:1、实验室制取氧气的步骤: “茶(查)、庄(装)、定、点、收、利(离)、息(熄)” “查”检查装置的气密性“装”盛装药品,连好装置 “定”试管固定在铁架台“点”点燃酒精灯进行加热 “收”收集气体“离”导管移离水面 “熄”熄灭酒精灯,停止加热。 2、用CO还原氧化铜的实验步骤: “一通、二点、三灭、四停、五处理” “一通”先通氢气,“二点”后点燃酒精灯进行加热; “三灭”实验完毕后,先熄灭酒精灯,“四停”等到室温时再停止通氢气;“五处理”处理尾气,防止CO污染环境。 比较下列几套装置:气体的制取—— ①发生装置②气体的收集
A装置适宜收集 气体;
B装置适宜收集 气体;
C装置适宜收集 气体;1.反应原理:Zn+H2SO4=ZnSO4+H2↑
CaCO3+2HCl=CaCl2+CO2↑+H2O
2H2O2 == 2H2O + O2 ↑ MnO2分解反应置换反应复分解反应 加热法气体不能收集CO2 只收集H2 2、反应装置:ABCED练习3:改正下列制取氢气装置中的错误。1、长颈漏斗的末端没有液封。
2、气体导出管过长。
3、氢气不能用向上排空气法收集H2指出图中存在的错误之处:实验操作顺序3.改正下列制取气体装置中的错误,说明原因。 制氧气 制氧气 制取CO2 试管口应略向下倾斜,应用酒精灯加热。
伸入试管内的导气管应刚露出胶塞 长颈漏斗应该插入液面以下。伸入反应容器中的导气管不宜过长。常用的气体的净化和干燥装置③气体的净化、转化与检验 [例] 、实验室用锌和盐酸反应来制取的氢气中常常混有少量的HCl气体和水蒸气,现用下面的装置除去HCl气体和水蒸气,装置如何连接? 回顾制取O2、H2、CO2等气体的实验,我们 (1)首先研究生成该气体的化学反应原理; (2)然后根据 和 选择并安装实验装置,而且一定要检查 ; (3)根据 确定气体的收集方法。[小结]实验室制气体的一般思路反应物性质 反应条件 装置的气密性 气体的性质 综合实验(探究、设计)综合实验的主要内容:
①气体的制取、净化、性质的组合;
②混合气体成分的验证;
③定性实验和定量实验的结合;几个重要的探究性实验(理解每个实验的目的和研究的方法。 )
(1)我们吸入的空气和呼出的气体有什么不同探究
(2)酸雨危害的探究
(3)金属活动性的探究
(4)铁生锈的探究
(5)酸、碱化学性质的探究
(6)粗盐提纯的探究
(7)区分盐酸盐、硫酸盐、碳酸盐的探究
(8)金属回收的探究探究1:桌上放了一瓶气体(如图所示),
纯净、无色无毒。请你用学过的知识进行探究:
该气体是什么气体?猜想:
步骤:
现象:
结论: 学会分析该气体是CO2书写实验报告
向瓶中注入石灰水,震荡石灰水变浑浊是CO2 [例] (04年南宁)某探究学习小组在帮助实验员整理化学试剂时, 发现 一个盛有无色溶液的试剂瓶,标签破损(如图所示). 已知它们是氯化钠、氢氧化钠、碳酸钠、 硫酸钠四种溶液中的一种.请你对该试剂作出猜想,并设计实验验证。
⑴猜想:这种试剂可能是 溶液,也可能是 溶液。
⑵实验验证。(要求写出操作、现象、结论)
。
碳酸钠硫酸钠综合性气体制备实验的设计?净化
装置干燥
装置收集
装置尾气处理
装置发生
装置(1)固 ? 气体 (2)固+液——气体(2)“长进短出” : CO2——NaOH溶液;石灰水(可检验)
HCl ——NaOH溶液;Ca(OH)2溶液;AgNO3溶液 (可检验)
H2O—— 浓H2SO4;固体NaOH;生石灰;氯化钙等;
无水CuSO4只检验(1)排水法(O2、H2);(2)向上排空气法(O2、CO2); (3)向下排空气法(H2)(1)点燃法(如CO) (2)吸收法
