【教师原创】人教版化学九年级下册9.3 溶液的浓度课件(23张ppt)
文档属性
| 名称 | 【教师原创】人教版化学九年级下册9.3 溶液的浓度课件(23张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-02-05 00:00:00 | ||
图片预览







文档简介
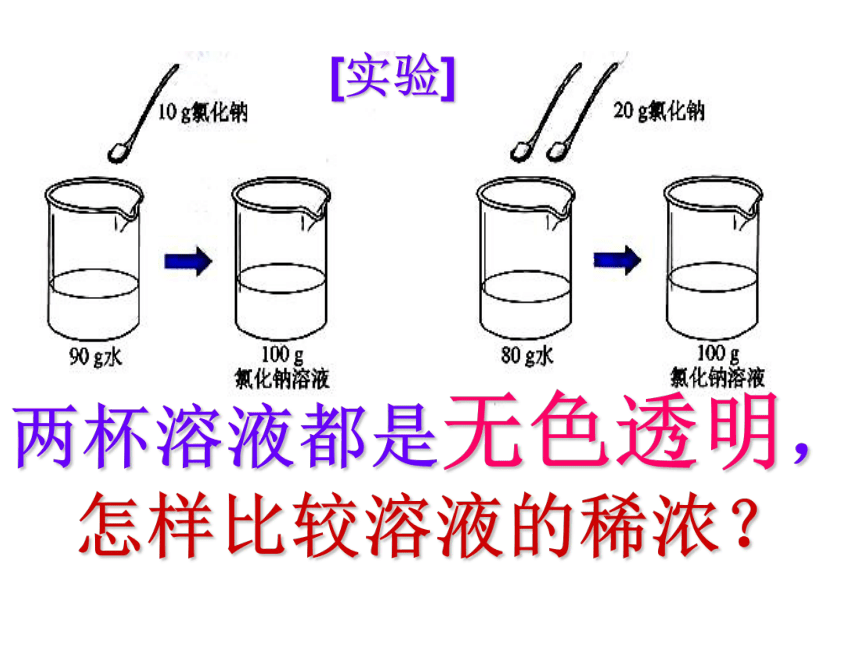
课件23张PPT。课题3溶液的浓度实验颜色:淡蓝 蓝色 深蓝在三支试管中各加入20mL水,然后分别加入约0.5g、1g、2g固体硫酸铜。比较三种溶液的颜色。浅较深深20g20g20g0.1g0.5g2g20.1g20.5g22g溶质质量分数4.8%9.1%16.7%[实验]两杯溶液都是无色透明,
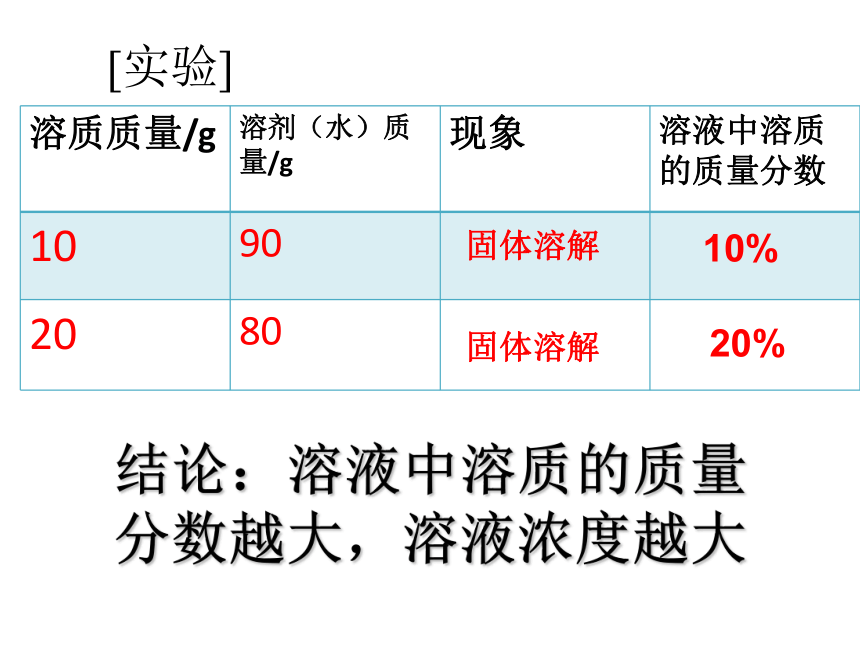
怎样比较溶液的稀浓?飞机喷洒农药喷洒药水药液太稀不能杀死害虫和病菌,但药液太浓又会毒害农作物或树木.结论:溶液中溶质的质量分数越大,溶液浓度越大固体溶解固体溶解10%
20%[实验][讨论]某氯化钠溶液中溶质的质量分数为10%,其含义是什么?
表示100份质量的氯化钠溶液中含有10份质量的氯化钠,90份质量的水。溶质质量:溶剂质量=1:9[题型一] :有关溶质、溶剂和溶液之间的换算 二、有关溶质质量分数的计算溶质质量溶液质量?100% 溶质质量分数=溶液质量 = 溶质质量 + 溶剂质量计算的依据 :溶质的质量分数定义:溶质的质量与溶液的质量之比。(通常以百分数表示) 注意:
①溶质的质量:形成溶液的那部分溶质,无溶入溶液的不计。
②溶液的质量 = 溶质的质量 + 溶剂的质量。
(必须分清溶质、溶剂与溶液)。
③计算时上下质量单位要统一。
④不要忘记X100%,最后得到百分数。
【例题1】在农业生产中,常需要用质量分数为16%的氯
化钠溶液来选种。现要配制150kg这种溶液,
需要氯化钠和水的质量各是多少?【解】答: 配制150kg质量分数为16%的氯化钠溶液
需24 kg氯化钠和126 kg水。 向20%的某浓溶液中加水后溶液、溶质和溶剂的质量如何变化? 如何解决有关溶液稀释的计算? ? [题型三] :有关溶液稀释或浓缩的计算计算的依据 : 稀释前溶质质量 = 稀释后溶质质量 浓缩前溶质质量 = 浓缩后溶质质量例题2:化学实验室现有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液需要多少克水?课本44页解:设稀释后溶液的质量为x50g ?98% = X ?20%答:需要水的质量195g需要水的质量= 245 g– 50g = 195g练习:配制10%硫酸98g,要98%硫酸(密度为1.84g/m L )多少mL ?解:设需要98%硫酸的体积为V V?1.84g/mL ?98% = 98g ?10%V = 答:要98%硫酸5.4mL
练习1、20g 10%的盐水中放入 2g水或2g食盐,求:所得溶液的溶质质量分数。练习2、20g 10%的盐水中倒出一半,求:剩余溶液的溶质的质量分数。剩余溶液的溶质质量分数不变,仍是 10 % 溶质质量分数的 计 算解:20g X10%加水:20g +2g=9.1%加盐:20g X10%+2g20g +2g=18.2%小试牛刀:1、配制100mL密度为1.1g/mL的20%的NaCl溶液
需要多少gNaCl和多少g水?2、配制500m L20%的硫酸溶液(密度为1.14g/mL)
需要98%硫酸溶液(密度为1.84g / mL )多少mL ?解:所需NaCl的质量为:100mL?1.1g/mL?20% = 22g所需水的质量为:100mL? 1.1g/mL – 22g = 88g答:略解:设需要98%硫酸的体积为V500mL? 1.14g/mL?20%= V? 1.84g/mL ?98%答:略 实验室用100g稀硫酸和多少g锌恰好完全反应可制得0.8g氢气。H2SO4 + Zn = ZnSO4 + H2?98 65100g X答:略A解:设所需锌的质量为 XX=66.3gH2SO4 + Zn = ZnSO4 + H2?65 2X 0.8gB解:设所需锌的质量为 XX=26g下面哪种解法正确?注意点:溶液是混合物,溶液的质量不能直接代入
化学方程式中计算,必须换算成溶质的质量。例题4:100g 9.8%硫酸跟多少克锌反应?同时生成多少克氢气?解:100g9.8%硫酸中含纯硫酸的质量为:100g?9.8%=9.8g设参加反应的锌质量为X ,生成氢气的质量为YZn + H2SO4 = ZnSO4 + H2?65 98 2X 9.8g YX=6.5g Y=0.2g答:略[题型四]: 有关化学方程式的计算 练习:实验室用100g稀硫酸和一定量的锌完全反应
在,制得0.8g氢气。求该稀硫酸溶质的质量分数。解:设稀硫酸溶质的质量分数为x%H2SO4 + Zn = ZnSO4 + H2?98 2100g? x% 0.8gX%==39.2%答:略[讨论] :200C时,氯化钠溶解度为36克, (1)若将36克氯化钠溶于100克水里,所得溶液中溶质的质量分数是多少?
(2)若将38克氯化钠溶于100克水里,所得溶液中溶质的质量分数是多少? 从上面例题中你得到什么启示?说明什么问题? 饱和溶液的溶质质量分数= 溶解度100g+溶解度溶质的质量分数36% 是指:
溶质T0C时溶解度36g是指:溶质质量分数与溶解度的比较100g溶液中含有36g溶质。在T0C 时,100g水最多溶解该溶质36g。浓度与溶解度的比较表示溶液中溶质
质量的多少表示物质
溶解性的强弱 不一定一 定 不一定 不一定100克单位为1,省略不写必须饱和质量单位(克)[题型二]:饱和溶液中溶质的质量分数计算 计算的依据 :饱和溶液的溶质质量分数= 溶解度100g+溶解度 例2、已知20℃时食盐的溶解度为36g,求20℃时食盐饱和溶液的溶质质量分数。 解:20℃时食盐饱和溶液的溶质质量分数为=26.5%36g100g+36g答:20℃时食盐饱和溶液的溶质质量分数为26.5%
怎样比较溶液的稀浓?飞机喷洒农药喷洒药水药液太稀不能杀死害虫和病菌,但药液太浓又会毒害农作物或树木.结论:溶液中溶质的质量分数越大,溶液浓度越大固体溶解固体溶解10%
20%[实验][讨论]某氯化钠溶液中溶质的质量分数为10%,其含义是什么?
表示100份质量的氯化钠溶液中含有10份质量的氯化钠,90份质量的水。溶质质量:溶剂质量=1:9[题型一] :有关溶质、溶剂和溶液之间的换算 二、有关溶质质量分数的计算溶质质量溶液质量?100% 溶质质量分数=溶液质量 = 溶质质量 + 溶剂质量计算的依据 :溶质的质量分数定义:溶质的质量与溶液的质量之比。(通常以百分数表示) 注意:
①溶质的质量:形成溶液的那部分溶质,无溶入溶液的不计。
②溶液的质量 = 溶质的质量 + 溶剂的质量。
(必须分清溶质、溶剂与溶液)。
③计算时上下质量单位要统一。
④不要忘记X100%,最后得到百分数。
【例题1】在农业生产中,常需要用质量分数为16%的氯
化钠溶液来选种。现要配制150kg这种溶液,
需要氯化钠和水的质量各是多少?【解】答: 配制150kg质量分数为16%的氯化钠溶液
需24 kg氯化钠和126 kg水。 向20%的某浓溶液中加水后溶液、溶质和溶剂的质量如何变化? 如何解决有关溶液稀释的计算? ? [题型三] :有关溶液稀释或浓缩的计算计算的依据 : 稀释前溶质质量 = 稀释后溶质质量 浓缩前溶质质量 = 浓缩后溶质质量例题2:化学实验室现有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液需要多少克水?课本44页解:设稀释后溶液的质量为x50g ?98% = X ?20%答:需要水的质量195g需要水的质量= 245 g– 50g = 195g练习:配制10%硫酸98g,要98%硫酸(密度为1.84g/m L )多少mL ?解:设需要98%硫酸的体积为V V?1.84g/mL ?98% = 98g ?10%V = 答:要98%硫酸5.4mL
练习1、20g 10%的盐水中放入 2g水或2g食盐,求:所得溶液的溶质质量分数。练习2、20g 10%的盐水中倒出一半,求:剩余溶液的溶质的质量分数。剩余溶液的溶质质量分数不变,仍是 10 % 溶质质量分数的 计 算解:20g X10%加水:20g +2g=9.1%加盐:20g X10%+2g20g +2g=18.2%小试牛刀:1、配制100mL密度为1.1g/mL的20%的NaCl溶液
需要多少gNaCl和多少g水?2、配制500m L20%的硫酸溶液(密度为1.14g/mL)
需要98%硫酸溶液(密度为1.84g / mL )多少mL ?解:所需NaCl的质量为:100mL?1.1g/mL?20% = 22g所需水的质量为:100mL? 1.1g/mL – 22g = 88g答:略解:设需要98%硫酸的体积为V500mL? 1.14g/mL?20%= V? 1.84g/mL ?98%答:略 实验室用100g稀硫酸和多少g锌恰好完全反应可制得0.8g氢气。H2SO4 + Zn = ZnSO4 + H2?98 65100g X答:略A解:设所需锌的质量为 XX=66.3gH2SO4 + Zn = ZnSO4 + H2?65 2X 0.8gB解:设所需锌的质量为 XX=26g下面哪种解法正确?注意点:溶液是混合物,溶液的质量不能直接代入
化学方程式中计算,必须换算成溶质的质量。例题4:100g 9.8%硫酸跟多少克锌反应?同时生成多少克氢气?解:100g9.8%硫酸中含纯硫酸的质量为:100g?9.8%=9.8g设参加反应的锌质量为X ,生成氢气的质量为YZn + H2SO4 = ZnSO4 + H2?65 98 2X 9.8g YX=6.5g Y=0.2g答:略[题型四]: 有关化学方程式的计算 练习:实验室用100g稀硫酸和一定量的锌完全反应
在,制得0.8g氢气。求该稀硫酸溶质的质量分数。解:设稀硫酸溶质的质量分数为x%H2SO4 + Zn = ZnSO4 + H2?98 2100g? x% 0.8gX%==39.2%答:略[讨论] :200C时,氯化钠溶解度为36克, (1)若将36克氯化钠溶于100克水里,所得溶液中溶质的质量分数是多少?
(2)若将38克氯化钠溶于100克水里,所得溶液中溶质的质量分数是多少? 从上面例题中你得到什么启示?说明什么问题? 饱和溶液的溶质质量分数= 溶解度100g+溶解度溶质的质量分数36% 是指:
溶质T0C时溶解度36g是指:溶质质量分数与溶解度的比较100g溶液中含有36g溶质。在T0C 时,100g水最多溶解该溶质36g。浓度与溶解度的比较表示溶液中溶质
质量的多少表示物质
溶解性的强弱 不一定一 定 不一定 不一定100克单位为1,省略不写必须饱和质量单位(克)[题型二]:饱和溶液中溶质的质量分数计算 计算的依据 :饱和溶液的溶质质量分数= 溶解度100g+溶解度 例2、已知20℃时食盐的溶解度为36g,求20℃时食盐饱和溶液的溶质质量分数。 解:20℃时食盐饱和溶液的溶质质量分数为=26.5%36g100g+36g答:20℃时食盐饱和溶液的溶质质量分数为26.5%
同课章节目录
