水是常用的溶剂
图片预览











文档简介
课件78张PPT。海水河水湖水自来水这些澄清透明的天然水,
是不是纯净水? 一滴自来水滴在玻璃片上,水干后有没有东西留下?结论:自来水不是纯净水,
天然水都不是纯净水? 纯净水是一种良好的溶剂。它能溶解各种固、
液和气态的物质。
海水、河水、井水等,都不是纯净的水,而是含有许多溶解性物质和非溶解性物质的极其复杂的混合物。 1.天然水是混合物。
2.纯净物与混合物的区别:
纯净物只有一种物质;
混合物由两种或两种以上物质组成。一、纯净物和混合物 二、固体药品的取用: 块状固体用镊子夹, 粉末状或细晶体用药匙取, (必要时可用纸槽。) 固体药品的取用:活动操作: 把试管横放, 将药品送到试管底部, 再把试管竖起。 把容器横放,把药品或金属颗粒放入
容器口以后,再把容器慢慢地竖立起
来,使药品或金属颗粒缓缓地滑到容
器的底部,以免打破容器。
粉状固体块状固体探究活动一取两个烧杯,各加入20mL的水,然后分别加入半药匙 的蔗糖、高锰酸钾晶体,用玻璃棒搅拌,还能看到固体吗? 1、为什么这些固体会“消失”在水中?
2、观察硫酸铜溶液颜色深浅是否各处相同?
3、形成溶液后,有固体与液体分离吗?
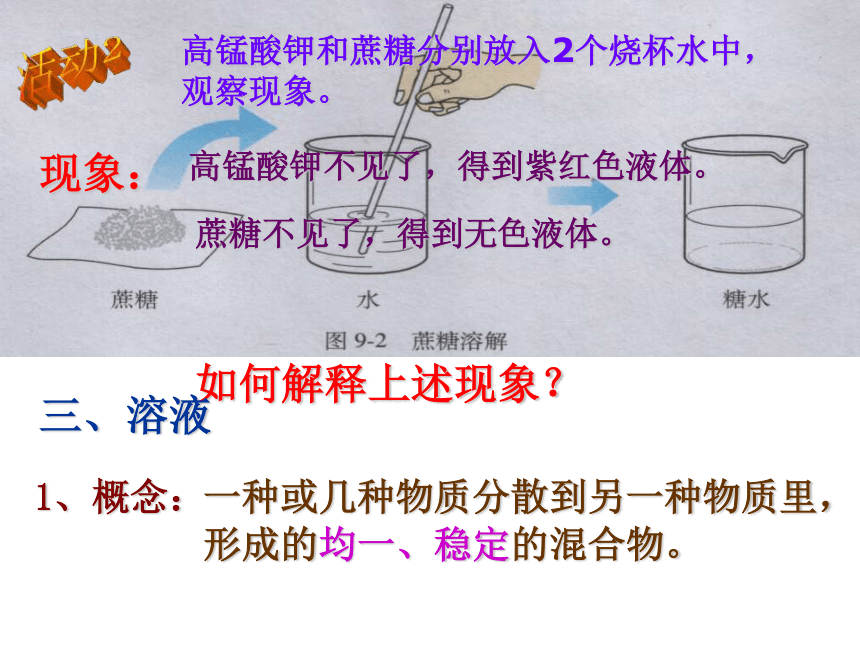
4、此时的溶液是纯净物还是混合物? 同学们思考以下问题 图 一高锰酸钾和蔗糖分别放入2个烧杯水中,观察现象。 现象: 高锰酸钾不见了,得到紫红色液体。 蔗糖不见了,得到无色液体。 如何解释上述现象?一种或几种物质分散到另一种物质里,形成的均一、稳定的混合物。1、概念:三、溶液活动2均一:溶液 各处的浓稀相同
稳定:条件不变时,溶质与溶剂长期不会分离出来 溶液的特征:均一性、稳定性、混合物。
理解溶液定义中所包含的三层意义: 第一,均一和稳定是溶液的特征。
第二,分散两字体现溶液的形成。
第三,溶液是混合物。 即溶液的质量=溶质的质量+溶剂的质量
如食盐水,食盐是溶质,水是溶剂。2、能溶解其他物质的物质叫做溶剂水是常用的溶剂3、被溶解的物质叫做溶质一般固体、液体、气体都可作为溶质4、溶液是由溶质和溶剂组成的【例1】指出汽水、碘酒、36度的白酒这三种溶
液中的溶质、溶剂。在汽水中,二氧化碳是溶质,水是溶剂。
在碘酒中,碘是溶质,酒精是溶剂。
在白酒中,酒精是溶质,水是溶剂。溶质和溶剂是相对而言的,两种液体相互溶解时,
通常把量多的一种叫做溶剂。当溶液中有水时,
习惯上把水叫做溶剂。通常不指明溶剂的溶液,
一般指的是水溶液。 氢氧化钠溶液中,溶质是氢氧化钠,溶剂是水.注:讨论题:溶液中溶质和溶剂是如何确定的?1. 分别指出下列各种溶液里的溶质和溶剂 ⑴. 注射用葡萄糖液
⑵. 医用卫生酒精
⑶. 生理食盐水
⑷. 石灰水课堂练习:⑵溶质是酒精、溶剂 是水⑶溶质是食盐、溶剂 是水⑴溶质是葡萄糖、溶剂是水⑷溶质是氢氧化钙、溶剂 是水2.我们平常所喝的的矿泉水清澈透明,喝起来的一种甘甜的滋味,因此矿泉水是纯净水,这种说法是否正确?这种说法是错误的。因为纯净水是无色无味的,而矿泉水有甘甜的滋味矿泉水中有多种矿物质,是混合物。3.河水中溶解了哪些物质?能否用来养鱼?冷开水能否用来养鱼?河水中溶有矿物质,还溶有氧气等所以可以养鱼,而冷开水中的氧气矿物质很少,不能提供鱼生活所必需的物质。溶液的命名法则1、水作溶剂的溶液,叫做某某的水溶液。例:蔗糖溶于水,叫做蔗糖的水溶液。2、通常不指明溶剂的溶液,一般指的是水溶液。例:高锰酸钾溶液3、当水和其他液体相互溶解时,通常不论液体
的含量多少,都把水看作溶剂,另一种看作溶质。
即:有水的水作溶剂。例:75%的酒精,叫做酒精的水溶液。
表示:100克溶液中,含75克酒精,25克水。4、两种液体相互溶解时,量多的为溶剂,量少
的为溶质。例:5ml汽油中,滴入2滴机油。
叫做:机油的汽油溶液。1、溶液是无色的。
2、无色透明的液体就是溶液。
3、把食盐溶液倒掉一半后,变稀了。
4、在温度不变,水不蒸发的条件下,
蔗糖溶 液中蔗糖会从水中分离出来。
练习一:判断说明 活动指导
(1)在两支试管中各加入2mL-3mL水,分别加入 1-2小粒碘和高锰酸钾;另取两支试管中各加 入2mL-3mL汽油,再分别加入1-2小粒碘和 高锰酸钾
(2)在两支试管中分别加入2mL-3mL水和几滴 植物油,向一支试管中滴入几滴洗涤剂振荡 后静置,2分钟后倒掉并用水冲洗
(3)在实验“1”盛有高锰酸钾溶液的试管中, 用滴管缓慢加入约2mL酒精,先不要振 荡,然后振荡碘几乎不溶于水高锰酸钾溶于水中碘溶解在汽油中高锰酸钾几乎不溶于汽油思考:1、碘和水、碘和汽油,高锰酸钾与水、高锰酸钾 与汽油混合的现象对比会有什么结论?
2、碘跟水、高锰酸钾跟水,碘跟汽油、高锰 酸钾跟汽油混合的现象对比有什么结论?相同的溶质在不同的溶剂中溶解性不同
不同的溶质在相同的溶剂中溶解性不同水和乙醇能够互溶
1、溶剂有多种(水、汽油等),水是一种常用的溶剂。
2、溶质可以是固体,也可以是液体、_________。 但如果其中有一种是水,一般把水叫做溶剂。
综合活动我们可以得出:量少的为溶质3、如果两种液体互相混合时量多的为溶剂气体试物管质内从水 + 植 物 油 混合的 实验可知:
1、不是任何液体互相混合都能溶解的。
2、水与油混合(分层)不均一、不稳定,故不能形成溶液。探究把不同的物质放入水中,都能形成溶液吗?实验:观察泥土、植物油、蔗糖和食盐的状态,
把他们分别加入4支各装有10毫升水的试
管里按下表1、2、3三步操作,认真、细
致地观察变化的全过程,记录并比较产生
的实验现象。1、把四种物质分别放入水中2、充分振荡3、放置一段时间泥土沉到水底植物油漂浮在水面蔗糖沉到水底食盐沉到水底混浊,有泥土小颗粒悬浮在水中
不均一混浊,有小油滴悬浮在水中
不均一透明,蔗糖溶在水中,均一透明,食盐溶在水中,均一不稳定,有泥土沉淀下来不稳定,油与水分上下两层稳定,无蔗糖析出稳定,无食盐析出结论:不同物质放入水中,不是都能形成溶液。一、浊液1、悬浊液:
固体小颗粒悬浮在液体里的混合物。2、乳浊液:
液体小液滴悬浮在液体里的混合物。肥皂水是乳浊液这些是溶液牛奶是乳浊液血液是悬浊液3、溶液、悬浊液、乳浊液的区别:固、液、气固液分子或离子许多分子的集合体许多分子的集合体均一、
稳定不均一、
不稳定不均一、
不稳定食盐水、糖水、碘酒泥浆、豆浆牛奶其他常用的溶剂探究二: 在两个试管中,各加入5毫升的水和
汽油,然后分别滴入两滴植物油,振荡
后观察现象。现象:植物油不溶于水,植物油溶于汽油。结论:汽油可以作为溶剂。溶质对溶剂是有选择性的。其它常用的溶剂[活动与探究]
[实验1]:取2只试管,各加入5ml水和汽油,分别滴入2滴食物油、振荡观察实验现象 。
[实验2]:取2只试管,各加入5ml水和酒精,分别加入少量松香粉,振荡观察实验现象 。不同种物质在同一种溶剂中溶解能力不同。
同一种物质在不同种溶剂中溶解能力不同。[结论]:探究三: 在两个试管中,各加入5毫升的水和
酒精,然后分别加入一块碘晶体和一些
蔗糖,振荡后观察现象。悬浊液悬浊液蔗糖溶液碘酒溶液结论:1、同种物质在不同种溶剂中的溶解能力不同。2、不同种物质在同种溶剂中的溶解能力不同。常用的溶剂还有酒精、汽油、丙酮等如汽油能溶解油脂,酒精能溶解碘等【思考】:衣服沾了油怎么办?[结论]:用汽油擦洗涤剂原理【例】:服装干洗的原理是什么?为什么干洗的衣服不能即日领回? 干洗店使用一些有机溶剂作为干洗液,把油性污渍掉.由于干洗溶剂都是一些致物质或具有中度毒性,对人体人害性.所以,拿干洗衣服要相隔数天才可领回,使残留的干洗溶剂先挥发掉.讨论题:什么是乳浊液?乳浊液和溶液的 区别是什么?乳浊液——小液滴分散到液体里形成的混合物。一种或几种物质另一种物质分散到均一稳定的混合物形成溶 液溶剂被溶解的物质能溶解其它物质的物质溶质固体 液体 气体乳浊液—————乳化剂乳化现象水 是 最 常 用 的 溶剂不同物质溶解过程中的能量转化 [活动与探究] [实验1]:取3只烧杯,各加入50ml水,用温度计测量水的温度。 [实验2]分别将一药匙硝酸铵、氯化钠和氢氧化钠加入上述3只烧杯中,搅拌至固体溶解,测量溶液的温度。 8℃7℃8℃17℃比水温低1℃比水温高9℃无变化[交流与讨论]在许多情况下,人们希望能较快地溶解某些固体物质。怎样才能达到上述目的?请提出建议。
建议1:_______________
建议2:_______________
建议3:_______________[结论]:在物质溶解于水形成溶液的过程中,通常伴有热量的变化。有些物质溶解使溶液的温度升高,有些物质溶解使溶液的温度降低。有些物质溶解温度变化不明显。溶解时不断搅拌溶解时加热把固体研细后溶解 讨论题:
甲、乙两位同学分别取装一定量水的烧杯,放在木板上。甲在烧杯和木板之间放适量固体石蜡,乙在烧杯和木板之间洒少量水。甲向烧杯中加入固体 NaOH,乙向烧杯中加入固体NH4NO3,充分搅拌后,发现两个烧杯均和木板“粘”在一起。请你分析产生上述现象的原因。巩固练习一、选择题
1.下列液体属于溶液的是 ( )
A.牛奶 B.泥水 C.液氧 D. 碘酒
2.一杯溶液中各部分的性质 ( )
A.上面和下面不相同 B.完全相同
C.完全不同 C.不一定相同
3.下列各用途与乳化无关的是( )
A.用洗衣粉洗去衣服上的油脂 B.用盐酸洗去铁块表面的锈 C.农药、医药制剂的合成D.各种日用洗涤剂的配制DBB4.下列小实验不能得到溶液的是( )食盐粉尘植物油蔗糖水水水汽油5.等同条件下,下列物质溶于水后能使水的温度明显降低的是 ( )
A.食盐 B.硝酸铵 C.浓硫酸 D.氢氧化钠6.现有一杯糖水,取出一部分,测其密度为a g/cm3,则剩余糖水的密度是( )
A.小于 a g/cm3 B.等于 a g/cm3
C.大于a g/cm3 D.无法确定BABCDBB7.若要加快某固体物质的溶解速度而又不影响实验效果,则下列方法中不适宜的是( ) A.不断搅拌 B.加热 C.将固体粉碎 D.加溶剂 二、交流与讨论 向右图试管里的水中加入某中物质后,U形管左边支管的红墨水液面下降,右边支管的液面上升的物质可能是 (a.蔗糖 b.生石灰 c.活性炭 d.硝酸铵 e.氢氧化钠 f.浓硫酸)红墨水水b e fD通常把一种物质溶解在另一种物质里的能力叫做溶解性。物质的溶解性
实验:结论:10ml水10ml汽油等量的植物油10ml水10ml水较多的蔗糖较少的熟石灰(1)(2)溶解性的大小跟溶质和溶剂的性质有关。且受温度等外界条件的影响。一.可溶物在一定量的水中能否无限溶解?取两只试管各加10毫升水:固体消失有晶体存在有更多晶体存在固体消失固体消失有晶体存在1.可溶物在一定量的水中不能无限溶解;2.不同物质在水中溶解能力不一样;3.不同温度下,物质的溶解能力不同.二.溶液的分类:饱和溶液和不饱和溶液1、饱和溶液的前提条件是什么?
2.在上面的前提条件下,关键看什么?
3.为什么必须说明是“这种溶质”的饱和溶液?
一定温度、一定量的溶剂。溶质是否能继续溶解二.饱和溶液和不饱和溶液硝酸钾饱和溶液说明:1.硝酸钾的饱和溶液能
继续溶解高锰酸钾2.此液为硝酸钾饱和溶液高锰酸钾不饱和溶液[练习] 20度时,将33克食盐放入100克水中,食盐全部溶解,此时溶液质量为 克,再向此溶液加入3克食盐又恰好全部溶解,则溶质为 克,现在溶液恰好饱和,此时溶液的质量为 克,再向此溶液加入3克食盐,溶液的质量是 克。 13336136136再加硝酸钾 指出下列各题的错误之处,并加以改正:
1.不能再溶解某种溶质的溶液叫饱和溶液;
2.装有饱和溶液的瓶的瓶底,一定有这种溶质的固体;
3.使一接近饱和的溶液变成饱和溶液,可将其中的溶
剂倒出一些;
4. 在同一温度下,同体积的某物质的饱和溶液,一定
会比另一物质的不饱和溶液含有的溶质多;
5.浓溶液一定是饱和溶液,稀溶液一定是不饱和溶液。
在一定温度.一定量的溶剂中,不能…….不一定,有可能刚好达到饱和.依然是不饱和溶液.不一定,这两种物质的溶解能力有可能不同.浓溶液不一定是饱和溶液动 动 手10毫升水 + 2克食盐:振荡,
现象:
溶液类型:
10毫升水 + 0.2克熟石灰 :振荡,
现象:
溶液类型: 食盐溶解 食盐的不饱和溶液 熟石灰不完全溶解 熟石灰的饱和溶液浓度大浓度小[总结一] 浓溶液不一定是饱和溶液,稀溶液不
一定是不饱和溶液。
[总结二] 同一物质,相同温度,饱和溶液比不
饱和溶液要浓。
[练习] 1、在一定温度下,某物质的饱和溶液一定是:
1)非常浓的溶液;
2)增加该溶质,能继续溶解的溶液;
3)非常稀的溶液;
4)增加该溶质,不能继续溶解的溶液。 二.浓稀溶液与饱和溶液的关系:浓溶液 稀溶液加溶质;蒸发溶剂饱和溶液 不饱和溶液升温降温 在其它条件不变的情况下,要使接近饱和溶液的硝酸钾溶液达到饱和溶液,下列措施达不到目的的是:
1)降低溶液温度; 2)加入溶质硝酸钾;
3)升高溶液的温度; 4)蒸发溶液中的溶剂。
三. 溶液的相互转化:P41:5.为什么汗水带咸味?被汗水浸湿的衣服晾
干后,为什么常出现白色的斑痕?6.有一瓶蒸馏水和一瓶稀氯化钾溶液,用什么简单的方法
把它们区分开?讨 论答:人分泌的汗水,是氯化钠溶液.因为溶有氯化钠,
所以带咸味.凉干,是将水分蒸发,所以有氯化钠析出。蒸发.通电讨 论1.在一定温度下,某物质的饱和溶液一定是
A.很浓的溶液
B.很稀的溶液
C.不能继续溶解该物质的溶液
D.不能溶解任何物质的溶液.2.某物质的饱和溶液中,加入一些该溶质的固体,
则下列说法正确的是
A.溶质质量减少;
B.溶液质量增大;
C.固体质量不变;
D.溶质质量增加.3.一定温度下,从500克的饱和溶液中倒出100克
溶液,剩余的溶液里,下列数值比原溶液减少的是①溶质的质量; ②溶剂的质量;
③溶液的密度; ④溶液的质量;
⑤溶质的质量分数(即:浓度);
①②③④ B. ②③④⑤
C ①② ④. D.①②③④⑤讨 论[课堂小结]
1、饱和溶液和不饱和溶液的定义、区别、判断方法
和 相互转化;2、饱和溶液和浓溶液,不饱和溶液与稀溶液的关系。
饱和溶液 不饱和溶液讨论:如何比较蔗糖和食盐在水中的溶解性大小?条件
控制
相同温度相同质量的溶剂达到饱和状态室温时,蔗糖比食盐更易溶于水定量比较固体溶解能力大小的要素:一定温度100g溶剂饱和状态单位(克)
讨论:设计实验——怎样比较食盐和蔗糖哪一个更易溶于水?达到饱和固体
溶解度
(S)在一定温度下在100g溶剂
(通常是水)中物质所溶解的克数
(单位g/100g水) 1.固体的溶解度定义: 在一定温度下,某固态物质的在100克溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。一定温度100克溶剂(一般指水)饱和状态质量(克)固体的溶解度的四要素:例:蔗糖在20℃是的溶解度是203.9g。在20℃时,100g水中最多可溶解203.9g蔗糖。在20℃时,100g水中溶解203.9g蔗糖,溶液达到饱和。表示在某一温度时,某固体物质在100克溶剂(通常是水)中最多溶解的质量(克)
表示在某一温度时,某固体溶质的饱和溶液的组成情况 固体物质溶解度数据的含义练习:1、在20℃时,100g水中溶解36g氯化钠溶液达到饱和,则20 ℃时氯化钠溶解度是____g。362、在0℃时,100g水中最多可溶解13.3g硝酸钾,则0℃时硝酸钾溶解度是____g。
13.33、20℃时硝酸钾的溶解度是31.6g,这句话的含义是什么?将其关系代入下表: 20℃31.6g100g131.6g易溶 可溶 微溶 难(不)溶 练习: 1、不溶物就是绝对不溶于水的物质。此话是否正确? 2、20℃时碳酸钙的溶解度是0.0013g,所以碳酸钙是___溶物质。 3、20℃时氯化钠的溶解度是36g,则氯化钠属于( ) A.易溶 物质 B.可溶物质 C.微溶物质 D.难溶物质 难>10g>1g<1g<0.01g A 2、溶解度与溶解性的关系难溶微溶可溶易溶溶解性与溶解度的关系物质在20℃时溶解度曲线”,
________,_________,_________是易溶物质;
_________是可溶物质; _________是微溶物质,_________是难溶物质。氯化钠硝酸钠硝酸银氯酸钾氢氧化钙氯化银50
10
20
30
40
0
60
70
808
90
100
50
10
20
30
40
80
60
70
8 0
90
100
110
180
170
160
150
140
130
120
190
200
硝酸铵
硝酸钾
硝酸钠
氯化铵
氯化钾
氯化钠
硼酸
硝酸钾在不同温度时的溶解度:13.331.620.945.863.985.5110138168202246(1)列表法: 3.不同温度下物质溶解度表示的方法温度/℃.....硝酸钾....(2)溶解度曲线0.050.100.150.2090704001020506080100300.050.100.150.209070400102050608010030温度/℃熟石灰的溶解度曲线:讨论:
固体物质溶解度受温度变化影响情况: 大多数固体物质溶解度随温度升高而增大, 例如 硝酸钠、氯化铵等。 少数固体物质溶解度受温度影响不大, 例如食盐。 极少数固体物质溶解度随温度升高反而减小, 例如熟石灰。大多数物质的溶解度
随温度上升而变大少数物质(氯化钠)
的溶解度
受温度影响不大少数物质(氢氧化钙)
的溶解度
随温度上升而变小固体物质的溶解度受温度影响的一般规律
50
10
20
30
40
0
60
70
808
90
100
50
10
20
30
40
80
60
70
8 0
90
100
110
180
170
160
150
140
130
120
190
200
硝酸铵
硝酸钾
硝酸钠
氯化铵
氯化钾
氯化钠
硼酸
100硼酸硝酸铵硝酸钠硝酸钾氯化铵氯化钾氯化钠6070501020304080901001101801701601501401301201902005010203040090607080温度/℃固体的溶解度曲线:1、横坐标60,纵坐标110 的交点表示什么意义? 练习:2、40℃时氯化铵的溶解度为______, 70℃时氯化铵的溶解度为______。 70℃时氯化钾的溶解度为____。46g44g60gA.60
70
808
50
10
20
100硼酸硝酸铵硝酸钠硝酸钾氯化铵氯化钾氯化钠6070501020304080901001101801701601501401301201902005010203040090607080温度/℃固体的溶解度曲线:68134g小于B.氯化铵、氯化钾、氯化钠、硼酸溶解度同种溶质在不同的溶 剂中的溶解能力不同不同的溶质在同种溶 剂中的溶解能力不同溶解性物质的溶解度易溶 、可溶 、 微溶 、 难(不)溶 固体的溶解度气体的溶解度影响因素(温度) 影响因素 (温度、压强)表示方法表示方法小结:判断下列说法是否正确(2) 20℃时,20克氯化钠可溶解在100克水中,所以20℃时氯化钠的溶解度是20g/100g水。(3) 硝酸钾的溶解度是31 .6g/100g水。(1) 40℃时,11克硝酸铵溶解在水中达到饱和,所以40℃时硝酸铵的溶解度是11g/100g水。(4) t ℃时,把10克某物质溶解在100克水里恰好制成饱和溶液,t ℃时,这种物质的溶解度就是10。错误错误错误错误请同学们回答下列问题: 1、什么叫溶解度?理解这个概念时要把握哪四个要素(关键)? 2、20℃时,氯化钠的溶解度是36g。则20℃时,氯化钠饱和溶液中溶质、溶剂、饱和溶液的质量比是_________________。 3、在20℃时,50g水最多能溶解7.4g某物质,则这种物质属于( ) A、易溶物质
B、可溶物质 C、微溶物质 D、难溶物质36:100:136A一、根据溶解度曲线回答 ;
1、 ℃时硝酸钠的溶解度为80克;
2、10 ℃时硝酸铵的溶解度为 ;
3、 ℃时硝酸钠与硝酸钾的溶解度相等,为 克。
4、20 ℃时硝酸钠 、氯化铵、氯化钠 硝酸钾四种物质的溶解度由高到低的顺序排列为 。
5、10 ℃时150克硝酸铵投入100克水中充分搅拌所得溶液
为 溶液(填“饱和或不饱和”);温度升高到20 ℃,所得溶液为 溶液。10140克70135硝酸钠 氯化铵 氯化钠 硝酸钾 饱和不饱和读图:
1、大多数固体的溶解度与温度的关是 ;
2、温度对溶解度影响最大的物质是 ,影响最小的物质是 ;
3、极少数固体的溶解度(如 )随温度的升高而 。随温度的升高而增大硝酸钾熟石灰减少氯化钠氢氧化钙的溶解度曲线甲乙丙B温度(℃)溶解度
(g)T1 T2(1)T2时,溶解度最大的是________;(2)B点代表的含义是
_______________________
_______________;(3)T1时的甲溶液升温到T2,甲溶液变成
_______________. 甲T1℃时,甲、丙两种物质
的溶解度相等不饱和溶液4.某物质的溶解度如图所示。在一个大烧杯中装着该物质的饱和溶液,而且杯中还有少量该物质固体存在,现将温度由60℃降到20℃,下列说法正确的是( )
A.杯中固体减少
B.杯中固体增多
C.杯中固体不变B60℃20℃
是不是纯净水? 一滴自来水滴在玻璃片上,水干后有没有东西留下?结论:自来水不是纯净水,
天然水都不是纯净水? 纯净水是一种良好的溶剂。它能溶解各种固、
液和气态的物质。
海水、河水、井水等,都不是纯净的水,而是含有许多溶解性物质和非溶解性物质的极其复杂的混合物。 1.天然水是混合物。
2.纯净物与混合物的区别:
纯净物只有一种物质;
混合物由两种或两种以上物质组成。一、纯净物和混合物 二、固体药品的取用: 块状固体用镊子夹, 粉末状或细晶体用药匙取, (必要时可用纸槽。) 固体药品的取用:活动操作: 把试管横放, 将药品送到试管底部, 再把试管竖起。 把容器横放,把药品或金属颗粒放入
容器口以后,再把容器慢慢地竖立起
来,使药品或金属颗粒缓缓地滑到容
器的底部,以免打破容器。
粉状固体块状固体探究活动一取两个烧杯,各加入20mL的水,然后分别加入半药匙 的蔗糖、高锰酸钾晶体,用玻璃棒搅拌,还能看到固体吗? 1、为什么这些固体会“消失”在水中?
2、观察硫酸铜溶液颜色深浅是否各处相同?
3、形成溶液后,有固体与液体分离吗?
4、此时的溶液是纯净物还是混合物? 同学们思考以下问题 图 一高锰酸钾和蔗糖分别放入2个烧杯水中,观察现象。 现象: 高锰酸钾不见了,得到紫红色液体。 蔗糖不见了,得到无色液体。 如何解释上述现象?一种或几种物质分散到另一种物质里,形成的均一、稳定的混合物。1、概念:三、溶液活动2均一:溶液 各处的浓稀相同
稳定:条件不变时,溶质与溶剂长期不会分离出来 溶液的特征:均一性、稳定性、混合物。
理解溶液定义中所包含的三层意义: 第一,均一和稳定是溶液的特征。
第二,分散两字体现溶液的形成。
第三,溶液是混合物。 即溶液的质量=溶质的质量+溶剂的质量
如食盐水,食盐是溶质,水是溶剂。2、能溶解其他物质的物质叫做溶剂水是常用的溶剂3、被溶解的物质叫做溶质一般固体、液体、气体都可作为溶质4、溶液是由溶质和溶剂组成的【例1】指出汽水、碘酒、36度的白酒这三种溶
液中的溶质、溶剂。在汽水中,二氧化碳是溶质,水是溶剂。
在碘酒中,碘是溶质,酒精是溶剂。
在白酒中,酒精是溶质,水是溶剂。溶质和溶剂是相对而言的,两种液体相互溶解时,
通常把量多的一种叫做溶剂。当溶液中有水时,
习惯上把水叫做溶剂。通常不指明溶剂的溶液,
一般指的是水溶液。 氢氧化钠溶液中,溶质是氢氧化钠,溶剂是水.注:讨论题:溶液中溶质和溶剂是如何确定的?1. 分别指出下列各种溶液里的溶质和溶剂 ⑴. 注射用葡萄糖液
⑵. 医用卫生酒精
⑶. 生理食盐水
⑷. 石灰水课堂练习:⑵溶质是酒精、溶剂 是水⑶溶质是食盐、溶剂 是水⑴溶质是葡萄糖、溶剂是水⑷溶质是氢氧化钙、溶剂 是水2.我们平常所喝的的矿泉水清澈透明,喝起来的一种甘甜的滋味,因此矿泉水是纯净水,这种说法是否正确?这种说法是错误的。因为纯净水是无色无味的,而矿泉水有甘甜的滋味矿泉水中有多种矿物质,是混合物。3.河水中溶解了哪些物质?能否用来养鱼?冷开水能否用来养鱼?河水中溶有矿物质,还溶有氧气等所以可以养鱼,而冷开水中的氧气矿物质很少,不能提供鱼生活所必需的物质。溶液的命名法则1、水作溶剂的溶液,叫做某某的水溶液。例:蔗糖溶于水,叫做蔗糖的水溶液。2、通常不指明溶剂的溶液,一般指的是水溶液。例:高锰酸钾溶液3、当水和其他液体相互溶解时,通常不论液体
的含量多少,都把水看作溶剂,另一种看作溶质。
即:有水的水作溶剂。例:75%的酒精,叫做酒精的水溶液。
表示:100克溶液中,含75克酒精,25克水。4、两种液体相互溶解时,量多的为溶剂,量少
的为溶质。例:5ml汽油中,滴入2滴机油。
叫做:机油的汽油溶液。1、溶液是无色的。
2、无色透明的液体就是溶液。
3、把食盐溶液倒掉一半后,变稀了。
4、在温度不变,水不蒸发的条件下,
蔗糖溶 液中蔗糖会从水中分离出来。
练习一:判断说明 活动指导
(1)在两支试管中各加入2mL-3mL水,分别加入 1-2小粒碘和高锰酸钾;另取两支试管中各加 入2mL-3mL汽油,再分别加入1-2小粒碘和 高锰酸钾
(2)在两支试管中分别加入2mL-3mL水和几滴 植物油,向一支试管中滴入几滴洗涤剂振荡 后静置,2分钟后倒掉并用水冲洗
(3)在实验“1”盛有高锰酸钾溶液的试管中, 用滴管缓慢加入约2mL酒精,先不要振 荡,然后振荡碘几乎不溶于水高锰酸钾溶于水中碘溶解在汽油中高锰酸钾几乎不溶于汽油思考:1、碘和水、碘和汽油,高锰酸钾与水、高锰酸钾 与汽油混合的现象对比会有什么结论?
2、碘跟水、高锰酸钾跟水,碘跟汽油、高锰 酸钾跟汽油混合的现象对比有什么结论?相同的溶质在不同的溶剂中溶解性不同
不同的溶质在相同的溶剂中溶解性不同水和乙醇能够互溶
1、溶剂有多种(水、汽油等),水是一种常用的溶剂。
2、溶质可以是固体,也可以是液体、_________。 但如果其中有一种是水,一般把水叫做溶剂。
综合活动我们可以得出:量少的为溶质3、如果两种液体互相混合时量多的为溶剂气体试物管质内从水 + 植 物 油 混合的 实验可知:
1、不是任何液体互相混合都能溶解的。
2、水与油混合(分层)不均一、不稳定,故不能形成溶液。探究把不同的物质放入水中,都能形成溶液吗?实验:观察泥土、植物油、蔗糖和食盐的状态,
把他们分别加入4支各装有10毫升水的试
管里按下表1、2、3三步操作,认真、细
致地观察变化的全过程,记录并比较产生
的实验现象。1、把四种物质分别放入水中2、充分振荡3、放置一段时间泥土沉到水底植物油漂浮在水面蔗糖沉到水底食盐沉到水底混浊,有泥土小颗粒悬浮在水中
不均一混浊,有小油滴悬浮在水中
不均一透明,蔗糖溶在水中,均一透明,食盐溶在水中,均一不稳定,有泥土沉淀下来不稳定,油与水分上下两层稳定,无蔗糖析出稳定,无食盐析出结论:不同物质放入水中,不是都能形成溶液。一、浊液1、悬浊液:
固体小颗粒悬浮在液体里的混合物。2、乳浊液:
液体小液滴悬浮在液体里的混合物。肥皂水是乳浊液这些是溶液牛奶是乳浊液血液是悬浊液3、溶液、悬浊液、乳浊液的区别:固、液、气固液分子或离子许多分子的集合体许多分子的集合体均一、
稳定不均一、
不稳定不均一、
不稳定食盐水、糖水、碘酒泥浆、豆浆牛奶其他常用的溶剂探究二: 在两个试管中,各加入5毫升的水和
汽油,然后分别滴入两滴植物油,振荡
后观察现象。现象:植物油不溶于水,植物油溶于汽油。结论:汽油可以作为溶剂。溶质对溶剂是有选择性的。其它常用的溶剂[活动与探究]
[实验1]:取2只试管,各加入5ml水和汽油,分别滴入2滴食物油、振荡观察实验现象 。
[实验2]:取2只试管,各加入5ml水和酒精,分别加入少量松香粉,振荡观察实验现象 。不同种物质在同一种溶剂中溶解能力不同。
同一种物质在不同种溶剂中溶解能力不同。[结论]:探究三: 在两个试管中,各加入5毫升的水和
酒精,然后分别加入一块碘晶体和一些
蔗糖,振荡后观察现象。悬浊液悬浊液蔗糖溶液碘酒溶液结论:1、同种物质在不同种溶剂中的溶解能力不同。2、不同种物质在同种溶剂中的溶解能力不同。常用的溶剂还有酒精、汽油、丙酮等如汽油能溶解油脂,酒精能溶解碘等【思考】:衣服沾了油怎么办?[结论]:用汽油擦洗涤剂原理【例】:服装干洗的原理是什么?为什么干洗的衣服不能即日领回? 干洗店使用一些有机溶剂作为干洗液,把油性污渍掉.由于干洗溶剂都是一些致物质或具有中度毒性,对人体人害性.所以,拿干洗衣服要相隔数天才可领回,使残留的干洗溶剂先挥发掉.讨论题:什么是乳浊液?乳浊液和溶液的 区别是什么?乳浊液——小液滴分散到液体里形成的混合物。一种或几种物质另一种物质分散到均一稳定的混合物形成溶 液溶剂被溶解的物质能溶解其它物质的物质溶质固体 液体 气体乳浊液—————乳化剂乳化现象水 是 最 常 用 的 溶剂不同物质溶解过程中的能量转化 [活动与探究] [实验1]:取3只烧杯,各加入50ml水,用温度计测量水的温度。 [实验2]分别将一药匙硝酸铵、氯化钠和氢氧化钠加入上述3只烧杯中,搅拌至固体溶解,测量溶液的温度。 8℃7℃8℃17℃比水温低1℃比水温高9℃无变化[交流与讨论]在许多情况下,人们希望能较快地溶解某些固体物质。怎样才能达到上述目的?请提出建议。
建议1:_______________
建议2:_______________
建议3:_______________[结论]:在物质溶解于水形成溶液的过程中,通常伴有热量的变化。有些物质溶解使溶液的温度升高,有些物质溶解使溶液的温度降低。有些物质溶解温度变化不明显。溶解时不断搅拌溶解时加热把固体研细后溶解 讨论题:
甲、乙两位同学分别取装一定量水的烧杯,放在木板上。甲在烧杯和木板之间放适量固体石蜡,乙在烧杯和木板之间洒少量水。甲向烧杯中加入固体 NaOH,乙向烧杯中加入固体NH4NO3,充分搅拌后,发现两个烧杯均和木板“粘”在一起。请你分析产生上述现象的原因。巩固练习一、选择题
1.下列液体属于溶液的是 ( )
A.牛奶 B.泥水 C.液氧 D. 碘酒
2.一杯溶液中各部分的性质 ( )
A.上面和下面不相同 B.完全相同
C.完全不同 C.不一定相同
3.下列各用途与乳化无关的是( )
A.用洗衣粉洗去衣服上的油脂 B.用盐酸洗去铁块表面的锈 C.农药、医药制剂的合成D.各种日用洗涤剂的配制DBB4.下列小实验不能得到溶液的是( )食盐粉尘植物油蔗糖水水水汽油5.等同条件下,下列物质溶于水后能使水的温度明显降低的是 ( )
A.食盐 B.硝酸铵 C.浓硫酸 D.氢氧化钠6.现有一杯糖水,取出一部分,测其密度为a g/cm3,则剩余糖水的密度是( )
A.小于 a g/cm3 B.等于 a g/cm3
C.大于a g/cm3 D.无法确定BABCDBB7.若要加快某固体物质的溶解速度而又不影响实验效果,则下列方法中不适宜的是( ) A.不断搅拌 B.加热 C.将固体粉碎 D.加溶剂 二、交流与讨论 向右图试管里的水中加入某中物质后,U形管左边支管的红墨水液面下降,右边支管的液面上升的物质可能是 (a.蔗糖 b.生石灰 c.活性炭 d.硝酸铵 e.氢氧化钠 f.浓硫酸)红墨水水b e fD通常把一种物质溶解在另一种物质里的能力叫做溶解性。物质的溶解性
实验:结论:10ml水10ml汽油等量的植物油10ml水10ml水较多的蔗糖较少的熟石灰(1)(2)溶解性的大小跟溶质和溶剂的性质有关。且受温度等外界条件的影响。一.可溶物在一定量的水中能否无限溶解?取两只试管各加10毫升水:固体消失有晶体存在有更多晶体存在固体消失固体消失有晶体存在1.可溶物在一定量的水中不能无限溶解;2.不同物质在水中溶解能力不一样;3.不同温度下,物质的溶解能力不同.二.溶液的分类:饱和溶液和不饱和溶液1、饱和溶液的前提条件是什么?
2.在上面的前提条件下,关键看什么?
3.为什么必须说明是“这种溶质”的饱和溶液?
一定温度、一定量的溶剂。溶质是否能继续溶解二.饱和溶液和不饱和溶液硝酸钾饱和溶液说明:1.硝酸钾的饱和溶液能
继续溶解高锰酸钾2.此液为硝酸钾饱和溶液高锰酸钾不饱和溶液[练习] 20度时,将33克食盐放入100克水中,食盐全部溶解,此时溶液质量为 克,再向此溶液加入3克食盐又恰好全部溶解,则溶质为 克,现在溶液恰好饱和,此时溶液的质量为 克,再向此溶液加入3克食盐,溶液的质量是 克。 13336136136再加硝酸钾 指出下列各题的错误之处,并加以改正:
1.不能再溶解某种溶质的溶液叫饱和溶液;
2.装有饱和溶液的瓶的瓶底,一定有这种溶质的固体;
3.使一接近饱和的溶液变成饱和溶液,可将其中的溶
剂倒出一些;
4. 在同一温度下,同体积的某物质的饱和溶液,一定
会比另一物质的不饱和溶液含有的溶质多;
5.浓溶液一定是饱和溶液,稀溶液一定是不饱和溶液。
在一定温度.一定量的溶剂中,不能…….不一定,有可能刚好达到饱和.依然是不饱和溶液.不一定,这两种物质的溶解能力有可能不同.浓溶液不一定是饱和溶液动 动 手10毫升水 + 2克食盐:振荡,
现象:
溶液类型:
10毫升水 + 0.2克熟石灰 :振荡,
现象:
溶液类型: 食盐溶解 食盐的不饱和溶液 熟石灰不完全溶解 熟石灰的饱和溶液浓度大浓度小[总结一] 浓溶液不一定是饱和溶液,稀溶液不
一定是不饱和溶液。
[总结二] 同一物质,相同温度,饱和溶液比不
饱和溶液要浓。
[练习] 1、在一定温度下,某物质的饱和溶液一定是:
1)非常浓的溶液;
2)增加该溶质,能继续溶解的溶液;
3)非常稀的溶液;
4)增加该溶质,不能继续溶解的溶液。 二.浓稀溶液与饱和溶液的关系:浓溶液 稀溶液加溶质;蒸发溶剂饱和溶液 不饱和溶液升温降温 在其它条件不变的情况下,要使接近饱和溶液的硝酸钾溶液达到饱和溶液,下列措施达不到目的的是:
1)降低溶液温度; 2)加入溶质硝酸钾;
3)升高溶液的温度; 4)蒸发溶液中的溶剂。
三. 溶液的相互转化:P41:5.为什么汗水带咸味?被汗水浸湿的衣服晾
干后,为什么常出现白色的斑痕?6.有一瓶蒸馏水和一瓶稀氯化钾溶液,用什么简单的方法
把它们区分开?讨 论答:人分泌的汗水,是氯化钠溶液.因为溶有氯化钠,
所以带咸味.凉干,是将水分蒸发,所以有氯化钠析出。蒸发.通电讨 论1.在一定温度下,某物质的饱和溶液一定是
A.很浓的溶液
B.很稀的溶液
C.不能继续溶解该物质的溶液
D.不能溶解任何物质的溶液.2.某物质的饱和溶液中,加入一些该溶质的固体,
则下列说法正确的是
A.溶质质量减少;
B.溶液质量增大;
C.固体质量不变;
D.溶质质量增加.3.一定温度下,从500克的饱和溶液中倒出100克
溶液,剩余的溶液里,下列数值比原溶液减少的是①溶质的质量; ②溶剂的质量;
③溶液的密度; ④溶液的质量;
⑤溶质的质量分数(即:浓度);
①②③④ B. ②③④⑤
C ①② ④. D.①②③④⑤讨 论[课堂小结]
1、饱和溶液和不饱和溶液的定义、区别、判断方法
和 相互转化;2、饱和溶液和浓溶液,不饱和溶液与稀溶液的关系。
饱和溶液 不饱和溶液讨论:如何比较蔗糖和食盐在水中的溶解性大小?条件
控制
相同温度相同质量的溶剂达到饱和状态室温时,蔗糖比食盐更易溶于水定量比较固体溶解能力大小的要素:一定温度100g溶剂饱和状态单位(克)
讨论:设计实验——怎样比较食盐和蔗糖哪一个更易溶于水?达到饱和固体
溶解度
(S)在一定温度下在100g溶剂
(通常是水)中物质所溶解的克数
(单位g/100g水) 1.固体的溶解度定义: 在一定温度下,某固态物质的在100克溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。一定温度100克溶剂(一般指水)饱和状态质量(克)固体的溶解度的四要素:例:蔗糖在20℃是的溶解度是203.9g。在20℃时,100g水中最多可溶解203.9g蔗糖。在20℃时,100g水中溶解203.9g蔗糖,溶液达到饱和。表示在某一温度时,某固体物质在100克溶剂(通常是水)中最多溶解的质量(克)
表示在某一温度时,某固体溶质的饱和溶液的组成情况 固体物质溶解度数据的含义练习:1、在20℃时,100g水中溶解36g氯化钠溶液达到饱和,则20 ℃时氯化钠溶解度是____g。362、在0℃时,100g水中最多可溶解13.3g硝酸钾,则0℃时硝酸钾溶解度是____g。
13.33、20℃时硝酸钾的溶解度是31.6g,这句话的含义是什么?将其关系代入下表: 20℃31.6g100g131.6g易溶 可溶 微溶 难(不)溶 练习: 1、不溶物就是绝对不溶于水的物质。此话是否正确? 2、20℃时碳酸钙的溶解度是0.0013g,所以碳酸钙是___溶物质。 3、20℃时氯化钠的溶解度是36g,则氯化钠属于( ) A.易溶 物质 B.可溶物质 C.微溶物质 D.难溶物质 难>10g>1g<1g<0.01g A 2、溶解度与溶解性的关系难溶微溶可溶易溶溶解性与溶解度的关系物质在20℃时溶解度曲线”,
________,_________,_________是易溶物质;
_________是可溶物质; _________是微溶物质,_________是难溶物质。氯化钠硝酸钠硝酸银氯酸钾氢氧化钙氯化银50
10
20
30
40
0
60
70
808
90
100
50
10
20
30
40
80
60
70
8 0
90
100
110
180
170
160
150
140
130
120
190
200
硝酸铵
硝酸钾
硝酸钠
氯化铵
氯化钾
氯化钠
硼酸
硝酸钾在不同温度时的溶解度:13.331.620.945.863.985.5110138168202246(1)列表法: 3.不同温度下物质溶解度表示的方法温度/℃.....硝酸钾....(2)溶解度曲线0.050.100.150.2090704001020506080100300.050.100.150.209070400102050608010030温度/℃熟石灰的溶解度曲线:讨论:
固体物质溶解度受温度变化影响情况: 大多数固体物质溶解度随温度升高而增大, 例如 硝酸钠、氯化铵等。 少数固体物质溶解度受温度影响不大, 例如食盐。 极少数固体物质溶解度随温度升高反而减小, 例如熟石灰。大多数物质的溶解度
随温度上升而变大少数物质(氯化钠)
的溶解度
受温度影响不大少数物质(氢氧化钙)
的溶解度
随温度上升而变小固体物质的溶解度受温度影响的一般规律
50
10
20
30
40
0
60
70
808
90
100
50
10
20
30
40
80
60
70
8 0
90
100
110
180
170
160
150
140
130
120
190
200
硝酸铵
硝酸钾
硝酸钠
氯化铵
氯化钾
氯化钠
硼酸
100硼酸硝酸铵硝酸钠硝酸钾氯化铵氯化钾氯化钠6070501020304080901001101801701601501401301201902005010203040090607080温度/℃固体的溶解度曲线:1、横坐标60,纵坐标110 的交点表示什么意义? 练习:2、40℃时氯化铵的溶解度为______, 70℃时氯化铵的溶解度为______。 70℃时氯化钾的溶解度为____。46g44g60gA.60
70
808
50
10
20
100硼酸硝酸铵硝酸钠硝酸钾氯化铵氯化钾氯化钠6070501020304080901001101801701601501401301201902005010203040090607080温度/℃固体的溶解度曲线:68134g小于B.氯化铵、氯化钾、氯化钠、硼酸溶解度同种溶质在不同的溶 剂中的溶解能力不同不同的溶质在同种溶 剂中的溶解能力不同溶解性物质的溶解度易溶 、可溶 、 微溶 、 难(不)溶 固体的溶解度气体的溶解度影响因素(温度) 影响因素 (温度、压强)表示方法表示方法小结:判断下列说法是否正确(2) 20℃时,20克氯化钠可溶解在100克水中,所以20℃时氯化钠的溶解度是20g/100g水。(3) 硝酸钾的溶解度是31 .6g/100g水。(1) 40℃时,11克硝酸铵溶解在水中达到饱和,所以40℃时硝酸铵的溶解度是11g/100g水。(4) t ℃时,把10克某物质溶解在100克水里恰好制成饱和溶液,t ℃时,这种物质的溶解度就是10。错误错误错误错误请同学们回答下列问题: 1、什么叫溶解度?理解这个概念时要把握哪四个要素(关键)? 2、20℃时,氯化钠的溶解度是36g。则20℃时,氯化钠饱和溶液中溶质、溶剂、饱和溶液的质量比是_________________。 3、在20℃时,50g水最多能溶解7.4g某物质,则这种物质属于( ) A、易溶物质
B、可溶物质 C、微溶物质 D、难溶物质36:100:136A一、根据溶解度曲线回答 ;
1、 ℃时硝酸钠的溶解度为80克;
2、10 ℃时硝酸铵的溶解度为 ;
3、 ℃时硝酸钠与硝酸钾的溶解度相等,为 克。
4、20 ℃时硝酸钠 、氯化铵、氯化钠 硝酸钾四种物质的溶解度由高到低的顺序排列为 。
5、10 ℃时150克硝酸铵投入100克水中充分搅拌所得溶液
为 溶液(填“饱和或不饱和”);温度升高到20 ℃,所得溶液为 溶液。10140克70135硝酸钠 氯化铵 氯化钠 硝酸钾 饱和不饱和读图:
1、大多数固体的溶解度与温度的关是 ;
2、温度对溶解度影响最大的物质是 ,影响最小的物质是 ;
3、极少数固体的溶解度(如 )随温度的升高而 。随温度的升高而增大硝酸钾熟石灰减少氯化钠氢氧化钙的溶解度曲线甲乙丙B温度(℃)溶解度
(g)T1 T2(1)T2时,溶解度最大的是________;(2)B点代表的含义是
_______________________
_______________;(3)T1时的甲溶液升温到T2,甲溶液变成
_______________. 甲T1℃时,甲、丙两种物质
的溶解度相等不饱和溶液4.某物质的溶解度如图所示。在一个大烧杯中装着该物质的饱和溶液,而且杯中还有少量该物质固体存在,现将温度由60℃降到20℃,下列说法正确的是( )
A.杯中固体减少
B.杯中固体增多
C.杯中固体不变B60℃20℃
同课章节目录
- 第1章 水
- 1 地球上的水
- 2 水的三态变化
- 3 水是常用的溶剂
- 4 配制溶液
- 5 水的组成
- 6 水资源的利用和保护
- 第2章 空气
- 1 空气的存在
- 2 空气的成分
- 3 氧气
- 4 二氧化碳
- 5 保护大气圈
- 第3章 阳光
- 1 太阳辐射能
- 2 阳光的传播
- 3 阳光的组成
- 第4章 土壤
- 1 土壤的组成和性状
- 2 土壤与植物
- 3 人类活动与土壤
- 第5章 生态系统
- 1 种群和群落
- 2 生态系统
- 3 生物圈
- 第6章 动物和人的生殖与发育
- 1 动物的生殖与发育
- 2 人的生殖与发育
- 第7章 植物和微生物的生殖与发育
- 1 绿色开花植物的有性生殖和发育
- 2 种子的萌发和幼苗形成
- 3 植物的无性生殖
- 4 细菌和真菌的繁殖
