常见的盐(浙江省宁波市海曙区)
图片预览






文档简介
课件17张PPT。第五节 常见的盐——盐的性质常见的盐
1、物理性质盐的性质
(1)大多数盐在常温下都是晶体
(2)盐在水中的溶解性盐的溶解性规律 钾钠铵盐硝酸盐,
都能溶于水中间。
盐酸不溶氯化银,
硫酸难溶有钡铅。
碳酸磷酸多不溶,
溶者只有钾钠铵。判断下列物质是否溶于水写出下列反应的化学方程式1.铁和硫酸铜溶液反应;
2.碳酸钠和稀盐酸反应;
3.碳酸钠溶液和澄清石灰水反应;
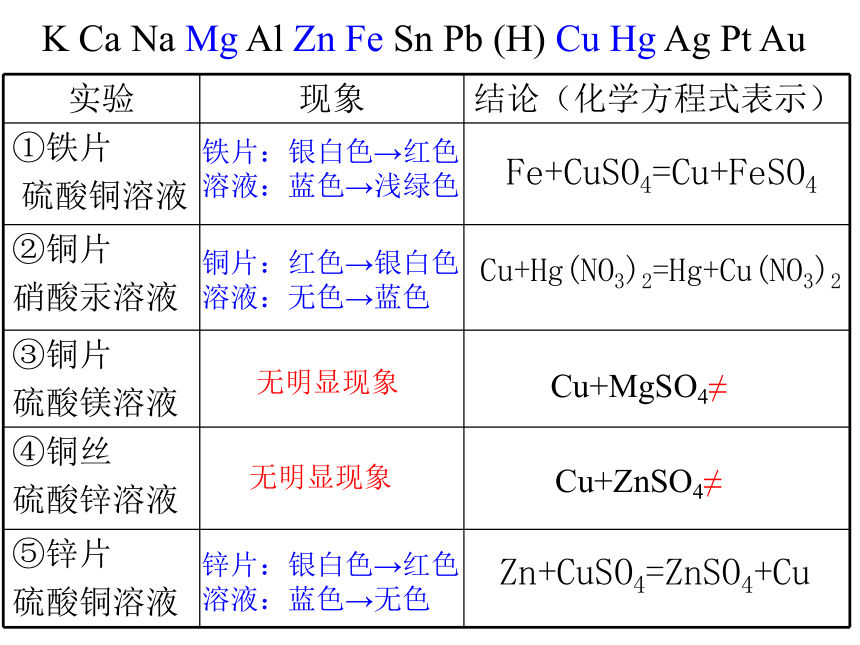
4.氯化钠溶液和硝酸银溶液反应。Fe+CuSO4=Cu+FeSO4Cu+Hg(NO3)2=Hg+Cu(NO3)2Cu+MgSO4≠K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au 铜片:红色→银白色
溶液:无色→蓝色无明显现象铁片:银白色→红色
溶液:蓝色→浅绿色2、化学性质置换反应发生的条件:
1.必须是盐溶液;
2.在金属活动性顺序中,只有前面的金属可把后面的金属从它的盐溶液中置换出来。K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au 练习:快速判断下列反应能否进行
Cu投入AgNO3溶液中
Al投入NaNO3溶液中
Zn投入FeSO4溶液中
Fe和AgCl的反应Cu+2AgNO3=2Ag+Cu(NO3)2Zn+FeSO4=Fe+ZnSO4(2) 盐+酸 练习:新盐+新酸 (3)盐(可溶)+碱(可溶) 练习 CuCl2 + KOH
新盐+新碱CuSO4+2NaOH=Na2SO4+Cu(OH)2↓FeCl3+3NaOH=3NaCl+Fe(OH)3↓= BaSO4↓+2NaOHBa(OH)2 + Na2SO4(4)盐(可溶)+盐(可溶) 实验
1.硝酸银溶液和氯化钠溶液混合
2. 硫酸钠溶液与氯化钡溶液混合
新盐+新盐Na2SO4 +BaCl2 =2NaCl +BaSO4↓AgNO3 +NaCl=AgCl ↓ + NaNO3小结:盐的化学性质 酸、碱、盐等物质之间发生复分解反应的条件是什么?
???沉淀气体水三、复分解反应发生的条件生成物有沉淀、气体、水 之一AgCl,BaSO4 ,
CaCO3等
CO2等
练习题:1、跟盐酸不反应,但能和硝酸银溶液反应的物是( )
A、铜片 B、铁丝 C、碳酸钠溶液 D、氢氧化铜
2、下列物质中滴加硝酸银溶液或硫酸钾溶液都有白色沉淀生成的是( )
A、氯化镁溶液 B、氯化钡溶液
C、碳酸钾溶液 D、硝酸钡溶液
AB
3、下列物质既能和盐酸反应,又能与碳酸钠反应的是( )
A、 硫酸 B、氢氧化钙 C、氢氧化钠 D、氯化钙
4、X、Y、Z三种金属,将Y、Z分别放入稀硫酸中,Y溶
解,Z不溶解;将Z放入X的盐溶液里,Z表面有X析出。 则这三种金属的活动性由强到弱的顺序是( )
A、X>Y>Z B、 Y>Z>X
C、 Y>X>Z D、Z>Y>X
BB练习题:
(2)盐在水中的溶解性盐的溶解性规律 钾钠铵盐硝酸盐,
都能溶于水中间。
盐酸不溶氯化银,
硫酸难溶有钡铅。
碳酸磷酸多不溶,
溶者只有钾钠铵。判断下列物质是否溶于水写出下列反应的化学方程式1.铁和硫酸铜溶液反应;
2.碳酸钠和稀盐酸反应;
3.碳酸钠溶液和澄清石灰水反应;
4.氯化钠溶液和硝酸银溶液反应。Fe+CuSO4=Cu+FeSO4Cu+Hg(NO3)2=Hg+Cu(NO3)2Cu+MgSO4≠K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au 铜片:红色→银白色
溶液:无色→蓝色无明显现象铁片:银白色→红色
溶液:蓝色→浅绿色2、化学性质置换反应发生的条件:
1.必须是盐溶液;
2.在金属活动性顺序中,只有前面的金属可把后面的金属从它的盐溶液中置换出来。K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au 练习:快速判断下列反应能否进行
Cu投入AgNO3溶液中
Al投入NaNO3溶液中
Zn投入FeSO4溶液中
Fe和AgCl的反应Cu+2AgNO3=2Ag+Cu(NO3)2Zn+FeSO4=Fe+ZnSO4(2) 盐+酸 练习:新盐+新酸 (3)盐(可溶)+碱(可溶) 练习 CuCl2 + KOH
新盐+新碱CuSO4+2NaOH=Na2SO4+Cu(OH)2↓FeCl3+3NaOH=3NaCl+Fe(OH)3↓= BaSO4↓+2NaOHBa(OH)2 + Na2SO4(4)盐(可溶)+盐(可溶) 实验
1.硝酸银溶液和氯化钠溶液混合
2. 硫酸钠溶液与氯化钡溶液混合
新盐+新盐Na2SO4 +BaCl2 =2NaCl +BaSO4↓AgNO3 +NaCl=AgCl ↓ + NaNO3小结:盐的化学性质 酸、碱、盐等物质之间发生复分解反应的条件是什么?
???沉淀气体水三、复分解反应发生的条件生成物有沉淀、气体、水 之一AgCl,BaSO4 ,
CaCO3等
CO2等
练习题:1、跟盐酸不反应,但能和硝酸银溶液反应的物是( )
A、铜片 B、铁丝 C、碳酸钠溶液 D、氢氧化铜
2、下列物质中滴加硝酸银溶液或硫酸钾溶液都有白色沉淀生成的是( )
A、氯化镁溶液 B、氯化钡溶液
C、碳酸钾溶液 D、硝酸钡溶液
AB
3、下列物质既能和盐酸反应,又能与碳酸钠反应的是( )
A、 硫酸 B、氢氧化钙 C、氢氧化钠 D、氯化钙
4、X、Y、Z三种金属,将Y、Z分别放入稀硫酸中,Y溶
解,Z不溶解;将Z放入X的盐溶液里,Z表面有X析出。 则这三种金属的活动性由强到弱的顺序是( )
A、X>Y>Z B、 Y>Z>X
C、 Y>X>Z D、Z>Y>X
BB练习题:
